镁基合金PMMA复合制备及其结构与储氢性能
毛奇峰,韩会会,吉 祥,朱云峰,李李泉
(南京工业大学材料科学与工程学院,江苏南京210009)
镁基合金PMMA复合制备及其结构与储氢性能
毛奇峰,韩会会,吉 祥,朱云峰,李李泉
(南京工业大学材料科学与工程学院,江苏南京210009)
利用球磨及喷雾成膜法制备了聚甲基丙烯酸甲酯(PMMA)纳米限域的氢化燃烧合成(HCS)镁基氢化物(MgH2)。利用场发射扫描电镜(FESEM)、X射线粉末衍射(XRD)、透射电镜(TEM)等测试对样品进行了成分及结构分析。压力-组成-温度(PCT)测试表明样品在温度250℃、3.0 MPa H2下,60 min内吸氢容量能到达3.24%(质量分数),同时样品放氢的起始温度由原来的250℃降到60℃,在温度250℃、0.005 MPa H2下,120 min内放氢容量为2.08%(质量分数)。
镁基储氢合金;纳米限域结构;机械球磨;PMMA
氢能作为理想的二次清洁能源,能够有效地缓解化石能源消耗带来的环境问题[1]。镁作为储氢材料,资源丰富,价格低廉,理论储氢容量高达7.6%(质量分数),是国内外储氢材料研究同行长期关注的重点[2]。但是,随着研究的深入,镁基储氢材料在应用上的问题也越来越明显,例如吸放氢温度高(>573 K),吸放氢动力学低,耐氧性能差,循环稳定性差等[3]。目前,有四种比较常用的方法对镁基储氢材料进行改性,即复合化,纳米化,合金化和催化剂[4-6]。
纳米化是一种比较常规的方法,泛函理论研究表明,当Mg/MgH2纳米线直径接近1 nm时,其吸放氢焓变可降至块体的近一半 (<40 kJ/mol),直径0.85 nm纳米线的脱附焓仅为34.54 kJ/mol,理论脱氢温度仅为264.25 K[7]。余学斌课题组制备的直径为4 nm的Li2Mg(NH)2@C在130℃具有良好的吸放氢循环性能,105℃达到理论储氢量5.3%(质量分数),并循环20次[8]。纳米化的手段有许多,球磨是其中一项最常用也是最方便的手段,在球磨过程中添加的球磨过程控制剂不仅有利于降低颗粒尺寸,同时也可以作为催化剂提高镁基储氢材料的吸放氢性能[9]。
通过镁与其它金属元素的合金化形成AB5、AB3等合金也可有效降低其吸放氢温度。催化剂是常用的降低活化能的方法,镁基储氢材料使用的催化剂也比较多样,例如贵金属Pd、NbF5以及众多碳材料[10-12]。
复合化就是针对镁基储氢材料存在的问题,选择特定的材料进行复合,利用该材料的性能改善镁基储氢材料在应用上的不足。Jeon等将镁基金属材料纳米限域在聚甲基丙烯酸甲酯(PMMA)中能够有效提高其吸放氢性能,采用二茂镁原位还原制备PMMA纳米限域镁基储氢材料,在200℃,30 min吸氢量达6%(质量分数)(相对于Mg而言)[13]。但是,由于采用聚合物的量比较多,总体上吸氢含量较少。
本文基于氢化燃烧合成(HCS)制备的镁基储氢材料通过机械球磨及喷雾成膜制备聚合物PMMA限域镁基储氢材料,并进行结构表征和性能测试。
1 实验
1.1 样品制备
MgH2样品通过氢化燃烧合成制备[1]。根据HCS工艺,将市售雾化镁粉 [纯度≥99.7%(质量分数),325目]和镍粉 (纯度≥99.9%,粒度 2~3 μm)按原子比 95∶5称量配料,在丙酮中超声混匀1 h,干燥箱中53℃干燥4 h,置入氢化燃烧合成炉,抽真空后通入Ar气洗涤,再抽真空,反复3次,最后通入2.0 MPa高纯H2。将反应器从室温加热到580℃,保温1 h,然后降温至340℃,保温10 h,关闭电源,自然冷却至室温。
将HCS产物进行球磨,球磨速度为400 r/min,球磨时间为10 h,球料比为40∶1(质量比),以Ar气氛保护。将球磨后的MgH2放入50 mL烧杯中,加入10 mL N,N-二甲基甲酰胺(DMF)溶剂和相应比例的PMMA,以保鲜膜封口,将烧杯在室温下超声1 h。以0.2~0.4 MPa的N2压力进行喷雾成膜,最后在真空干燥箱中60℃干燥样品一夜,得到样品。
1.2 结构表征与性能测试
X射线衍射(XRD)使用Cu靶(Cu靶Kα谱线,40 kV×35 mA)。将样品与KBr粉末混合压片并进行傅里叶红外测试(FTIR,NEXU670)。样品结构表征采用场发射扫描电镜(FESEM,S4800)和透射电镜(TEM,JEM-2010 UHR)。材料吸放氢性能测试在美国AMC公司的GRC仪器上完成。
2 结果与讨论
2.1 样品相成分分析
图1分别给出了质量分数为5%和10%的PMMA通过喷雾成膜纳米限域镁基储氢合金的XRD图,HCS后的镁基储氢合金的XRD图和纯PMMA的XRD图。不同质量分数PMMA限域的镁基合金的XRD特征峰与HCS后的镁基合金能够吻合且主峰没有发生变化,说明限域样品中成分没有发生改变。同时,通过谢勒公式式(1)计算平均晶粒尺寸(K为基于颗粒模型的常数,0.89;λ为X射线波长,0.154 096 nm;B为半高宽,单位为弧度;θ为衍射角),HCS后的镁基合金的晶粒尺寸为60 nm,而限域后的样品平均晶粒尺寸在22 nm左右。


图1 PMMA纳米限域镁基储氢合金及HCS后Mg95Ni5、纯PMMA的XRD图
这是由于球磨的纳米化效应造成的。球磨作为纳米化手段中最常用同时也是最简单的方法能够快速使颗粒细化。聚合物PMMA与镁基储氢合金混合采用球磨工艺,因为球磨不仅工艺简单,同时也能够满足实验纳米化的要求,也表明了该方法的有效性。
为了证明聚合物限域样品中聚合物结构是否发生变化,将样品进行傅里叶红外测试。图2为质量分数为5%和10%的PMMA纳米限域镁基储氢合金以及HCS后的Mg95Ni5、纯PMMA的红外谱图,限域样品和HCS后的镁基合金在特征峰上完全吻合(波数 3 500~3 250 cm-1,2 375 cm-1),其中 Mg-H的伸缩振动峰(900~1 300 cm-1)在限域样品中有部分变化,这是由于聚合物的存在导致的。同时,限域样品在波数为1 735 cm-1处的酯基伸缩振动峰明显,这说明样品中的聚合物没有改变其结构,也说明在球磨过程中聚合物能够保持结构的稳定性。
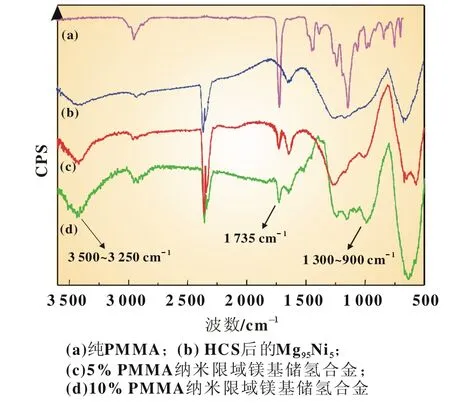
图2 纳米限域镁基储氢合金及HCS后Mg95Ni5、纯PMMA的红外谱图
2.2 样品微观结构表征
图3给出了质量分数为5%和10%的PMMA纳米限域镁基储氢合金在不同放大倍率下的FESEM图,两个样品的颗粒尺寸大概在100 nm到1 μm不等,但与之前的颗粒尺寸10 μm相比[14],颗粒尺寸明显下降。同时,10%PMMA限域的样品与5%限域的样品在颗粒尺寸上没有明显区别,但在颗粒形状[图3(a)和3(c)]上,10%的样品更加分散,颗粒更加圆滑。不同质量分数PMMA限域镁基储氢合金的样品均具有结块现象,这是由于样品中聚合物的粘滞性造成的。

图3 纳米限域镁基储氢合金在不同放大倍率下的FESEM图
为了进一步表征其限域结构,将10%PMMA限域镁基储氢合金样品进行TEM测试。图4为10%(质量分数)的PMMA纳米限域镁基储氢合金的TEM图。图4(a)中颗粒大小为100 nm左右,而图4(c)中晶粒尺寸为20 nm左右,这一结果与XRD和FESEM测试结果相同。图4(b)为图4(a)的高倍率图,图中1为合金区,1中晶格条纹并不明显,进一步放大,如图4(c)[对应于图4(b)中白色矩形框区域],晶格条纹十分明显,其晶面间距d=0.223 7 nm,对应MgH2的(110)晶面。图4(b)中2为聚合物区,图4(d)将该区域进一步放大[图4(b)中圆形区域],可以看出上半部存在晶格条纹,而中间无晶格条纹,同时选区电子衍射也证明该区域的非晶性,符合聚合物的TEM测试特征,其宽度在8 nm左右。这说明聚合物限域镁基储氢合金结构已经成功制得,且制备的样品聚合物厚度为8 nm。

图4 10%的PMMA纳米限域镁基储氢合金的TEM图
2.3 样品储氢性能测试
10%(质量分数)纳米限域镁基储氢合金及HCS后的Mg95Ni5的热脱附曲线如图5所示,10%纳米限域镁基储氢合金的热脱附曲线表明限域后的样品起始脱氢温度为60℃,脱氢量为3.5%(质量分数);而HCS后的Mg95Ni5的起始脱氢温度为250℃,脱氢量为4.0%(质量分数)。两者相比,限域样品的起始脱氢温度明显降低,这是由于通过球磨及喷雾成膜后,样品颗粒变小,其热力学性能改善。但是由于在球磨过程中,部分MgH2分解为Mg,导致放氢量下降,由图1也可知,HCS后Mg95Ni5的主峰MgH2高于限域后的样品。
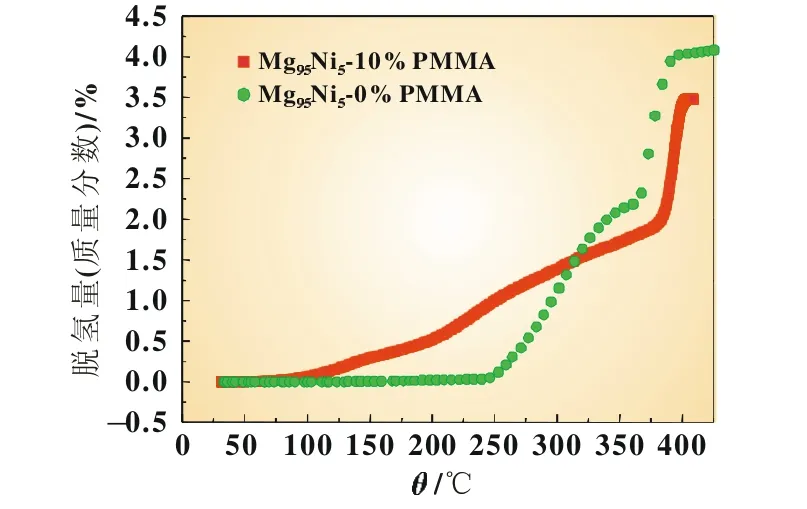
图5 10%纳米限域镁基储氢合金及HCS后的Mg95Ni5热脱附曲线
进一步测试样品的储氢性能,如图6所示。图6(a)为10%(质量分数)PMMA限域镁基储氢合金在200、250℃及 3.0 MPa下的吸氢曲线,样品在200℃,60 min内吸氢量达到2.95%(质量分数),提高吸氢温度至250℃,相同时间内,吸氢量3.24%(质量分数),与HCS后的Mg95Ni5相比,吸氢容量明显提高。这是由于镁基储氢合金经过球磨后,颗粒尺寸下降,同时,聚合物作为球磨添加剂,有利于进一步降低颗粒尺寸。如图6(b)和 6(d)所示,在相同条件(200、250℃,0.005 MPa H2)下的放氢测试,聚合物限域镁基储氢合金的样品明显优于HCS 后的 Mg95Ni5,在 250 ℃、0.005 MPa H2下,120 min 内10%PMMA限域镁基储氢合金的样品放氢容量为2.08%(质量分数),而HCS后的Mg95Ni5在250℃、0.005 MPa H2下,120 min内基本没有放氢,这说明聚合物的添加及球磨有利于提高HCS后镁基合金的放氢性能。

图6 10%纳米限域镁基储氢合金及HCS后Mg95Ni5的吸放氢曲线
3 结论
本文通过球磨法及喷雾成膜成功制备了聚合物纳米限域HCS镁基储氢合金。TEM测试表明聚合物PMMA的厚度大概在8 nm左右,同时FESEM表明限域样品的颗粒尺寸在1 μm到100 nm之间。聚合物限域镁基储氢合金的吸放氢性能:在250℃、3.0 MPa H2下,60 min内吸氢容量能到达3.24%(质量分数),放氢的起始温度由原来的250℃降到60℃,在250℃、0.005 MPa H2下,120 min内放氢容量为2.08%(质量分数)。
[1]YUAN J G,ZHU Y F,LI L Q.Highly efficient bimetal synergetic catalysis by a multi-wall carbon nanotube supported palladium and nickel catalyst for the hydrogen storage of magnesium hydride[J].Chem Commun,2014,50:6641-6644.
[2]刘春娜.氢能——绿色能源的未来[J].电源技术,2010,34(6):535-538.
[3]陈军,朱敏.高容量储氢材料的研究进展[J].中国材料进展,2009,28:2-10.
[4]LIU T,CHEN C G,WANG F,et al.Enhanced hydrogen storage properties of magnesium by the synergic catalytic effect of TiH1.971and TiH1.5nanoparticles at room temperature[J].J Power Sources,2014,267:69-77.
[5]ZHANG Y H,ZHAI T T,YANG T,et al.Electrochemical hydrogen-storage performance of Mg20-xYxNi10(x=0-4)alloys prepared by mechanical milling[J].J Appl Electrochem,2015,45:931-941.
[6]RUMINSKI A M,BARDHAN R,URBAN J J,et al.Synergistic enhancement of hydrogen storage and air stability via Mg nanocrystal-polymer interfacial interactions[J].Energy Environ Sci,2013,6:3267-3271.
[7]LI L L,PENG B,CHEN J,et al.A quantum chemical study on magnesium(Mg)/magnesium-hydrogen(Mg-H) nanowires[J].Journal of Alloys and compounds,2009,484(1/2):308-313.
[8]XIA G L,TAN Y B,YU X B,et al.Hierarchical porous Li2Mg(NH)2@C nanowires with long cycle life towards stable hydrogen storage[J].Scientific Reports,2014,4:6599.
[9]FLORIANO R,LEIVA D R,DELEDDA S,et al.MgH2-based nanocomposites prepared by short-time high energy ball milling followed by cold rolling:A new processing route[J].J Hydrogen Energy,2014,39:4404-4413.
[10]XIE W Y,WEST D J,SUN Y Y,et al.Role of nano in catalysis:palladium catalyzed hydrogen desorption from nanosized magnesium hydride[J].Nano Energy,2013,2:742-748.
[11]LUO Y,WANG P,MA L P,et al.Hydrogen sorption kinetics of MgH2catalyzed with NbF5[J].J Alloys and Compounds,2008,453:138-142.
[12]LOTOTSKYYA M,SIBANYONIA J M,DENYS R V,et al.Magnesium-carbon hydrogen storage hybrid materials produced by reactive ball milling in hydrogen[J].Carbon,2013,57:146-160.
[13]JEON K J,MOON H R,RUMINSKI A M,et al.Air-stable magnesium nanocomposites provide rapid and high-capacity hydrogen storage without using heavy-metal catalysts[J]. Nature Mater,2011,10:286-290.
[14]刘虎,朱云峰,李李泉,等.氯化盐溶液中氢化燃烧合成MgH2的水解制氢性能[J].电源技术,2015,39(3):488-490.
Preparation,microstructure and hydrogen storage property of composite of PMMA+Mg-based alloy
MAO Qi-feng,HAN Hui-hui,JI Xiang,ZHU Yun-feng,LI Li-quan
(College of Materials Sciences and Engineering,Nanjing Tech University,Nanjing Jiangsu 210009,China)
Mg-based hydrides obtained from hydriding combustion synthesis (HCS) nano-confined by polymer polymethyl methacrylate(PMMA)were successfully prepared by mechanical milling(MM)and spray drying process.The surface morphology and crystal structure were characterized by using FESEM,XRD,TEM,et al.The absorption hydrogen amount was 3.24%within 60 min at the temperature of 250℃under the 3.0 MPa H2.Simultaneously,the on-set temperature of hydrogen desorption of the Mg-based hydrides nano-comfined by PMMA was reduced from 250℃to 60℃and the amount of hydrogen desorption was 2.08%within 120 min at the temperature of 250℃under the 0.005 MPa H2.
Mg-based hydrogen storage alloy;nano-confined structure;mechanical milling;polymethyl methacrylate
TM 91
A
1002-087 X(2017)10-1427-04
2017-03-13
国家自然科学基金(51571112,51471087);江苏高校优势学科建设工程资助
毛奇峰(1990—),男,江苏省人,硕士研究生,主要研究方向为镁基材料储氢技术。

