超高效液相色谱-串联质谱法测定犬血浆中利培酮和帕潘立酮及药代动力学研究
王 璐, 刘成雁, 王志嘉, 李 红, 任雪冬, 田福林
(1.辽宁省分析科学研究院,辽宁沈阳 110015;2.吉林大学生命科学学院,吉林长春 130021)
利培酮(Risperidone,Ris)是苯丙异恶唑类药物,通过阻断5-HT和多巴胺D受体发挥抗精神病作用[1]。帕潘立酮(Paliperdone,Pal)为利培酮的活性代谢产物,为新型抗精神病药物[2]。因此,同时监测Ris和Pal能更准确反映血药浓度与治疗效果和毒性效应的关系。为提高病人用药依从性,增加药物的治疗效果,杨森制药公司研发的注射用利培酮微球一次给药可以持续释放药物达数日[3]。因此,筛选专一性强、灵敏度高的血药浓度测定方法,对于制定个体剂量方案,评价临床疗效及安全性具有重要意义。
目前,检测Ris和Pal的方法主要有放射免疫法(RIA)[4]、气相色谱法(GC)[5]和高效液相色谱法(HPLC)[6 - 8]等。近年来,高效液相色谱-串联质谱法(LC - MS/MS)[9 - 11]也有报道。但未见报道利培酮缓释微球剂型药动力学方面的研究。本文建立了测定血浆中Ris和Pal浓度的超高效液相色谱(UPLC)-MS/MS分析方法,同时对利培酮缓释微球进行药代动力学研究,为临床用药提供参考。
1 实验部分
1.1 主要仪器、试剂与材料
Agilent 1200 UPLC/6410 B MS/MS 液相色谱-串联四极杆质谱联用仪(安捷伦科技有限公司)。
标准品:利培酮(含量>99.1%)、帕潘立酮(含量>99.5%)、盐酸曲马多(内标:IS,含量>99.4%),均购自中国药品生物制品检定所。标准品、内标储备液(1.0 mg/mL):分别精密称取25 mg Ris、Pal和曲马多标准品于25 mL容量瓶中,加乙腈-水(80∶20,V/V)溶解,并稀释至刻度,配制成1.0 mg/mL储备液。使用时曲马多储备液用乙腈-水(80∶20,V/V)稀释至10 ng/mL,4 ℃保存;Ris和Pal混合储备液,分别用乙腈-水(80∶20,V/V)逐级稀释,Ris溶液的浓度分别为0.05、0.10、0.30、1.00、3.00、10.0和30.0 ng/mL,Pal溶液的浓度分别为0.10、0.30、1.00、3.00、10和30.0 ng/mL。分别取适量母液,用乙腈-水(80∶20,V/V)稀释至质控样本所需的浓度,低、中、高分别为0.10、1.00、和10.0 ng/mL(Ris);0.3、3.0和10.0 ng/mL(Pal)。乙腈、甲醇(色谱纯,美国Fisher Scientific公司);甲酸(分析纯,美国Tedia公司);实验用水为Milli-Q纯水系统(Millipole公司)。
恒德利培酮微球注射液(25 mg,美国 Alkermes,Inc.)。
1.2 血浆样品处理
取100 μL血浆样品,分别加入100 μL内标溶液,100 μL乙腈-水(80∶20,V/V)溶液,再加入500 μL乙腈,涡流混合30 s,振荡10 min,离心10 min,取上清液于30 ℃下氮气吹干,残余物加100 μL流动相溶解,取20 μL进行UPLC-MS/MS分析。
1.3 色谱-质谱条件
色谱条件:色谱柱:Zorbax SB-C18柱(150×4.6 mm i.d.,5 μm);流动相:乙腈-10 mmol/L 乙酸铵(65∶35,V/V);流速:1.2 mL/min(分流);柱温:35 ℃;进样量:20 μL。
质谱条件:电喷雾离子源(ESI),正离子方式检测;干燥气(N2)温度350 ℃,干燥气流量 9.0 L/min;雾化气(N2)压力295.4 kPa;电喷雾电压4 000 V;扫描方式为多反应监测(MRM)模式。Ris、Pal和IS的解簇电压:50、53、29 V;碰撞能量:35、35、41 eV;用于定量分析的离子对分别为:m/z411.2→m/z191.1(Ris),m/z427.2→m/z207.1(Pal)和m/z264.1→m/z58.0(IS)。
2 结果与讨论
2.1 色谱及质谱条件的选择
Ris和Pal在酸性条件下可被质子化,故采用正离子检测,扫描方式为多反应监测(MRM)。在一级全扫描质谱图中获得Ris和Pal的准分子离子峰为m/z411.2和m/z427.2,选择性地对[M+H]+进行二级质谱分析(图1)。Ris主要碎片离子有m/z191.1、163.5、110.1,选择信号最强的碎片离子m/z191.1作为定量离子。Pal主要碎片离子为m/z207.1。研究发现有机相含有乙腈较甲醇色谱峰形更好,重现性更佳。在本实验的色谱条件下,每个样品的分析时间仅为2 min。
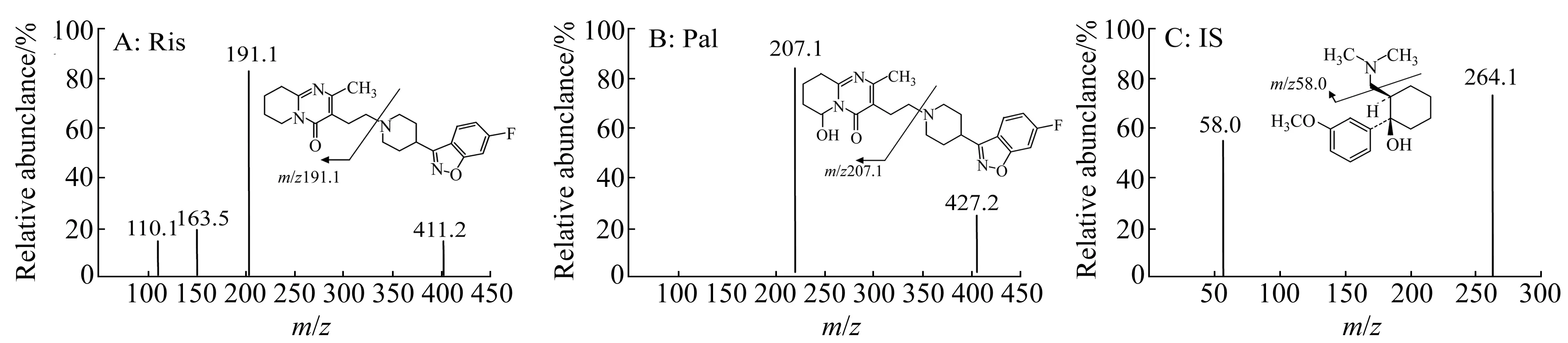
图1 全扫描质谱图及二级质谱图 Fig.1 Full-scan mass spectra and tandem mass spectra
2.2 方法的选择性
取犬的空白血浆100 μL操作,进样20 μL,得色谱图2A;将一定浓度的Ris、Pal和内标标准溶液加入空白血浆中,依同法操作,得色谱图2B;取受试犬给药后收集的血浆样品,依同法操作,得色谱图2C。结果表明,空白血浆中的内源性物质不干扰Ris、Pal和内标的测定。
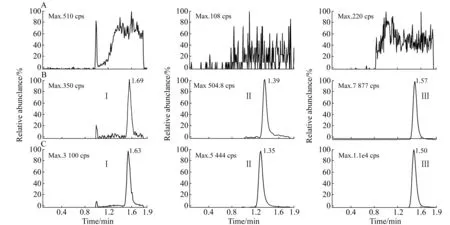
图2 血浆中Ris、Pal和IS的典型MRM色谱图Fig.2 MRM chromatograms of Ris,Pal and internal standard in plasma(A) a blank plasma sample;(B) a blank plasma sample spiked with Ris(0.05 ng/mL),Pal(1.00 ng/mL),and IS(10.0 ng/mL);(C) Beagle plasma sample at 30 d after injection risperidone microspheres(I:Ris;Ⅱ:Pal;Ⅲ:IS).
2.3 基质效应的考察
取空白犬血浆100 μL,按1.2操作,制备低、中、高3个浓度的样品,每浓度6样本;同时另一组分别用100 μL水代替空白血浆,按1.2操作,取20 μL进行UPLC-MS/MS分析,获得相应峰面积,以每一浓度两种处理方法的峰面积比值计算基质效应,低、中、高3个浓度的基质效应分别为99.9%、95.9%和97.2%(Ris),91.2%、93.9%和94.2%(Pal),表明基质不影响样品中Ris和Pal的测定。
2.4 线性范围和定量限
以待测物浓度(x)为横坐标,待测物与内标物的峰面积比值(y)为纵坐标,用加权(W=1/x2)最小二乘法进行回归运算。回归方程为:yRis=0.244x+0.0019(r2=0.9993);yPal=0.136x+0.0061(r2=0.9995)。结果表明,两种化合物分别在0.05~30.0 ng/mL和0.10~30.0 ng/mL范围内的线性关系良好(r2>0.999),定量限分别为0.05 ng/mL和0.10 ng/mL。
2.5 回收率及精密度
取空白血浆100 μL,配制低、中、高3 个质量浓度控制样品,每一浓度进行6样本分析,连续测定3 d,根据当日的标准曲线,计算精密度和回收率,结果见表1。结果表明:本实验分析方法符合相关要求[12]。

表1 Ris与Pal的精密度和回收率
2.6 方法稳定性
已有文献报道[13],Ris和Pal血浆样品在-20 ℃长期冷冻放置2个月及室温放置24 h稳定,经历3次冷冻-解冻循环后稳定性良好。本实验重点考察了采用沉淀蛋白处理后的血浆样品室温放置8 h的稳定性。Ris与Pal低、中、高三浓度的血浆样品进行3样本分析,相对标准偏差分别为5.4%、6.5%、5.5%(Ris)和3.4%、2.1%、3.7%(Pal)。表明沉淀蛋白处理后的血浆样品室温放置8 h内稳定。
2.7 血浆样品测定及利培酮缓释微球药代动力学研究
取健康Beagle犬10只,雌雄各半,体重平均12.0 kg,用5%葡萄糖注射液稀释按2.08 mg/kg的剂量经犬后肢肌肉注射给药。给药前(0 h)和给药后0.25、 0.5、 1、 1.5、 2、 3、 4、 8、 24 h,采血2 mL,24 h后每隔2 d采血1次,连续采血40 d。图3和图4分别为Ris和Pal在10只Beagle犬体内不同时刻的平均血药浓度-时间曲线。根据测得的Ris和Pal血药浓度数据,利用Topfit2.0计算Ris和Pal药代动力学参数:达峰时间tmax分别为492.1±189.2、658±189.2 h(均值±标准差,下同);半衰期t1/2分别为36.1±7.7、30.1±2.9 h;cmax分别为4.2±1.3、14.3±2.6 ng/mL; AUC:药时曲线下面积分别为1058±752.1、4058±642.1 ng·h/mL。利培酮缓释微球可以稳定释放20 d。
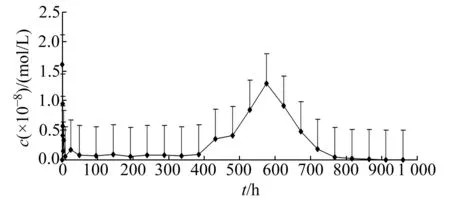
图3 Ris平均血药浓度-时间曲线Fig.3 Average plasma concentration vs time curves for Ris
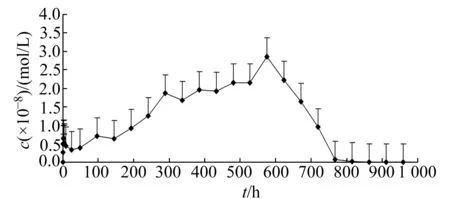
图4 Pal平均血药浓度-时间曲线Fig.4 Average plasma concentration vs time curves for Pal
3 结论
建立了一种快速、高效、灵敏测定血浆中Ris、Pal含量的UPLC-MS/MS法,该方法样品处理简捷,分析检测时间短,专属性强,可用于利培酮缓释微球药动学的研究。

