腐殖酸在泥灰岩中的吸附与降解特征研究*
王甜甜 王心义,2,3# 刘小满 杨 光
(1.河南理工大学资源环境学院,河南 焦作 454000;2.中原经济区煤层(页岩)气河南协同创新中心,河南 焦作 454000;3.中国平煤神马集团研究院,河南 平顶山 467000)
腐殖酸在泥灰岩中的吸附与降解特征研究*
王甜甜1王心义1,2,3#刘小满1杨 光1
(1.河南理工大学资源环境学院,河南 焦作 454000;2.中原经济区煤层(页岩)气河南协同创新中心,河南 焦作 454000;3.中国平煤神马集团研究院,河南 平顶山 467000)
为研究腐殖酸在泥灰岩中的吸附与降解特性,借助三维荧光技术,采用静态吸附和动态淋滤实验模拟了腐殖酸在平顶山矿区泥灰岩中运移的过程。结果表明:(1)随着腐殖酸初始浓度的增加,泥灰岩对腐殖酸的吸附呈现出线性增加的趋势。(2)泥灰岩对腐殖酸的吸附符合原始质量吸附方程,斜率为0.008 7,截距为0.073 1,R2=0.986 2,拟合度很好,泥灰岩对于腐殖酸有着很强的亲和力。(3)腐殖酸在泥灰岩中发生了微生物降解,这是一个先吸附后降解的动力过程,泥灰岩中的微生物将腐殖酸(Ⅴ区)降解为溶解性微生物代谢产物(Ⅳ区)。
腐殖酸 吸附 降解 三维荧光光谱

表1 泥灰岩理化性质
1 材料与方法
1.1 供试材料
1.1.1 泥灰岩介质
选择新近系泥灰岩扰动土为供试岩样,除去其中的石块、植物枝叶等杂物,自然风干后,用研钵捣碎研细,过2 mm筛子备用。泥灰岩的取样深度及基本性质见表1,矿物分析见表2。
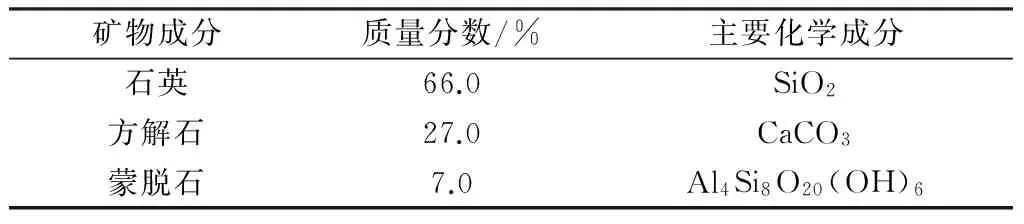
表2 泥灰岩矿物分析
1.1.2 腐殖酸溶液
已有研究表明,地下水中DOM的3DEEM可粗略地分为5个区域[17]:(1)Ⅰ区,EX(发射波长)≤250 nm、EM(激发波长)<330 nm,代表酪氨酸;(2)Ⅱ区,EX≤250 nm、330 nm≤EM≤380 nm,代表色氨酸;(3)Ⅲ区,EX≤250 nm、EM>380 nm,代表富里酸;(4)Ⅳ区,EX>250 nm、EM≤380 nm,代表溶解性微生物代谢产物;(5)Ⅴ区,EX>250 nm、EM>380 nm,代表腐殖酸类物质。70.9 mg/L的腐殖酸溶液的3DEEM特征的荧光峰落在Ⅴ区(见图1),基本理化性质指标见表3。
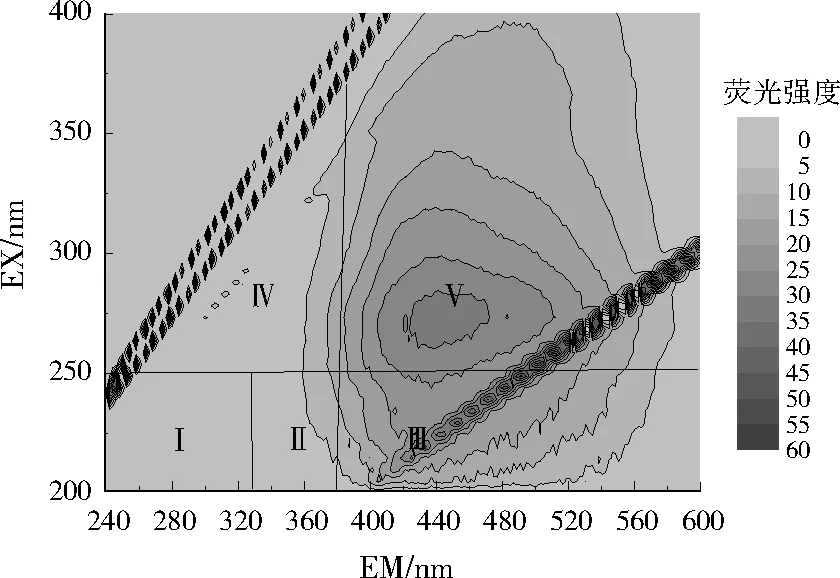
注:左上角和右下角斜线均为贝平分线。图4同。图1 腐殖酸的3DEEM特征Fig.1 3DEEM feature of humic acid
1.2 实验装置与检测仪器
实验装置如图2所示。有机玻璃柱为高50 cm、内径7 cm,柱体顶端和底端分别开孔,柱体内均匀分层填装处理好的泥灰岩,上下两端填装粒径为1~3 cm的粗粒石英砂,以使液体分布均匀。用胶管连接上下两端孔口,作为进样口和出样口。泥灰岩装填容重约1.47 g/cm3,有效孔隙度为0.23。实验中将高位水桶和蠕动泵(BT100-2J)作为供水装置,提供稳定流场。
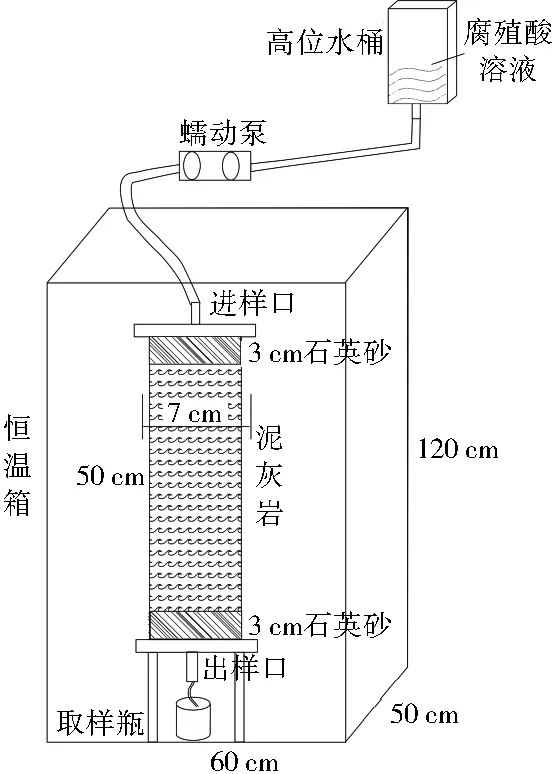
图2 实验装置Fig.2 Experimental device

表3 腐殖酸溶液基本理化性质指标
水中腐殖酸浓度以COD表征。3DEEM采用HITACHI F-7000型荧光分光光度计检测,光电倍增管(PMT)电压为400 V,激发和发射狭缝宽度均为10 nm,扫描速度为12 000 nm/min。EM、EX分别为240~600、200~400 nm,分别以5、2 nm步长递增。拉曼散射的空白校正使用去离子水,数据采用Origin软件处理,以等高线图表征。实验所用真空抽滤装置为GM-0.5A型真空泵及500 mL玻璃砂芯过滤装置。水样理化指标测定使用SX751型数显测量仪。
1.3 实验方法
1.3.1 静态吸附
配置34.6、47.5、70.9、97.0、129.8、160.7 mg/L的腐殖酸溶液。称取7份制备好的泥灰岩,每份均为5 g左右,置于7个250 mL的容量瓶中,向其中6个容量瓶分别依次加入50 mL不同浓度的腐殖酸溶液,最后1个容量瓶中加入50 mL去离子水溶液作为空白样对照。将容量瓶置于SHA-C型水浴振荡器中进行振荡,温度设置为25 ℃,转速调至150 r/min,达到吸附平衡后取出,离心后用0.45 μm滤膜抽滤测定上清液中腐殖酸浓度,并计算岩样吸附量,绘制吸附曲线。
1.3.2 动态淋滤
在培养目标体系中旅游管理实践能力按照学生个体对自身目标的需求分为景区规划与管理方向和酒店经营与管理方向,分别培养学生旅游景区规划、旅游产品开发、项目策划、资源环境保护管理能力与酒店实务操作能力。有针对性的教学符合学生个人目标的实现,能更好地适应市场的需求。
模拟地下水入渗淋滤泥灰岩介质情况,将70.9 mg/L的腐殖酸溶液(具体理化性质见表3)作为入渗水,自顶端进入模拟土柱中,在底端出样口流出,每日进行取样以供分析。实验过程中温度为25 ℃,流速为20 mL/min。每日取样测量腐殖酸浓度及理化指标,并测定3DEEM。
2 结果与讨论
2.1 静态吸附实验
由表4可见,腐殖酸初始质量浓度从34.6 mg/L增加至160.7 mg/L时,泥灰岩的吸附量从0.38 mg/g增加到1.52 mg/g。随着初始浓度的增加,腐殖酸溶液在泥灰岩中的吸附状况可采用原始质量吸附方程(见式(1))来描述[18]。
R=mX-b
(1)
式中:R为孔隙介质吸持的COD,mg/L;m为回归系数(介质对腐殖酸的亲和力);X为腐殖酸初始质量浓度,mg/L;b为在无腐殖酸加入时孔隙介质本身释放的COD,mg/L。
泥灰岩对腐殖酸具有很强的吸附性,随着腐殖酸初始浓度的增加,泥灰岩对腐殖酸的吸附呈现出线性增加的趋势,并且泥灰岩对腐殖酸的吸附符合原始质量吸附方程,斜率为0.008 7,截距为0.073 1,R2=0.986 2,拟合度很好,泥灰岩对于腐殖酸有很强的亲和力。其原因与泥灰岩中含有一定量的蒙脱石(见表2)有关,蒙脱石为铝的氢氧化物,对腐殖酸具有较强的吸附能力。此外,蒙脱石是伊利石进一步风化的产物,颗粒很小,直径一般约1 μm,比表面积约为6×106m2/g,巨大的比表面积增加了蒙脱石的吸附能力,从而使泥灰岩具有较强的吸附性。
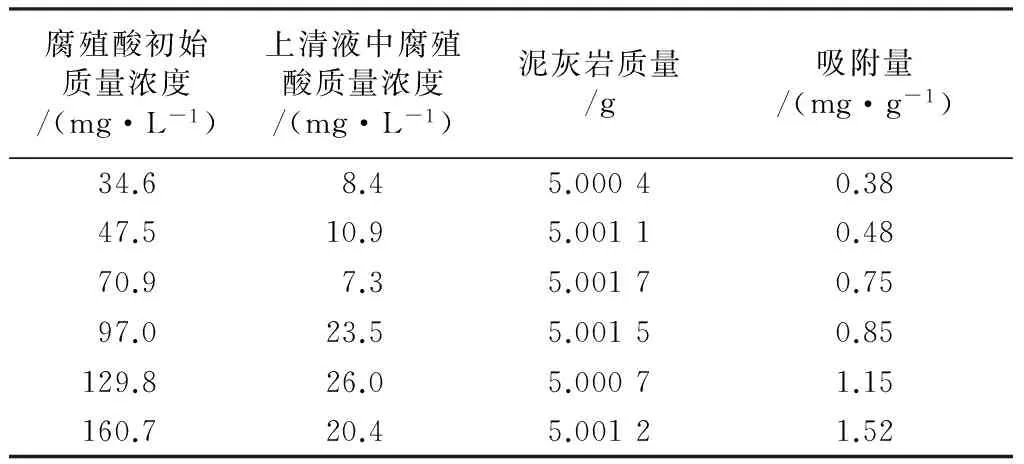
表4 泥灰岩静态吸附结果1)
注:1)空白样上清液中腐殖酸质量浓度为11.6 mg/L。
2.2 动态淋滤实验
2.2.1 淋出液中腐殖酸浓度变化
淋滤实验持续378 h,基本达到稳定。由图3可见,在土柱淋滤液浓度和流量稳定的条件下,淋出液腐殖酸浓度经历了5个阶段:(1)0~36 h为第1阶段,浓度无明显变化;(2)36~59 h为第2阶段,浓度迅速上升;(3)59~80 h为第3阶段,浓度迅速下降;(4)80~165 h为第4阶段,浓度缓慢下降;(5)165~378 h为第5阶段,浓度基本稳定不变。
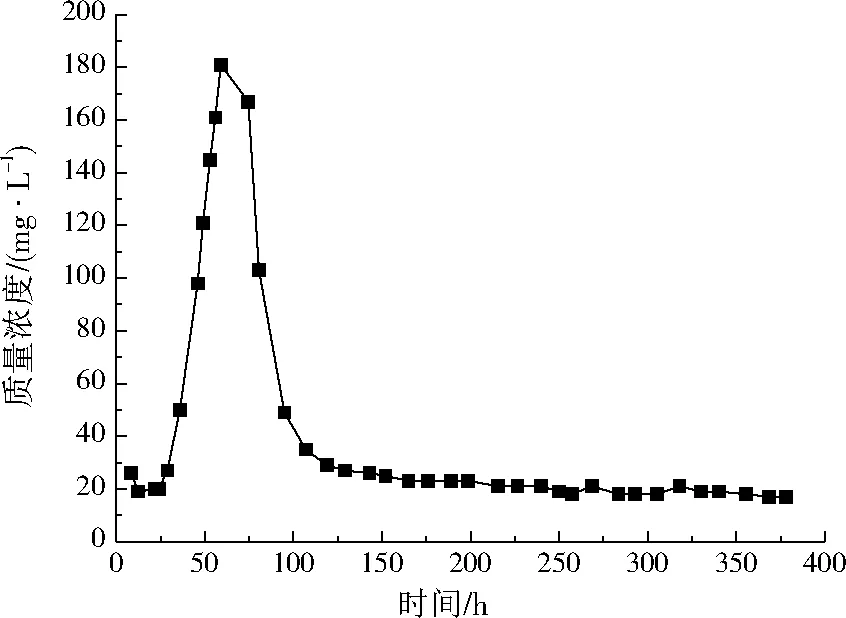
图3 淋出液中腐殖酸质量浓度变化曲线Fig.3 Concentration change curve of humic acid in leachate
第1阶段:实验初期的淋出液以土柱里原有的饱和孔隙水为主,淋出液中腐殖酸浓度很小且基本无变化。第2阶段:腐殖酸溶液逐步驱替饱和孔隙水,淋出液中腐殖酸浓度不断上升,直到59 h时达到最大值。淋出液中腐殖酸浓度最大值远高于淋滤液腐殖酸初始浓度,这是因为泥灰岩中也含有一定的DOM,随着淋滤时间的推移,泥灰岩本身的DOM不断被淋滤出来,增加了淋出液腐殖酸浓度。第3阶段:随着淋滤时间的推移,腐殖酸浓度迅速下降,这是因为泥灰岩对腐殖酸具有很强的亲和力,腐殖酸被泥灰岩吸附,淋出液中腐殖酸浓度明显降低。这个阶段进水流速维持在20 mL/min,经历了21 h,2.12 kg左右的泥灰岩柱子吸附量为0.84 mg/g(大于静态吸附量的0.75 mg/g),说明整个泥灰岩柱子达到了吸附平衡。第4阶段:80 h后腐殖酸浓度逐渐降低,变化幅度减少,随着淋滤液的不断注入,泥灰岩对腐殖酸的吸附达到吸附平衡,不再吸附新的腐殖酸。然而,原来泥灰岩吸附的腐殖酸逐渐发生降解,腐殖酸浓度不断下降。第5阶段:腐殖酸浓度基本维持不变,吸附与降解均达到了平衡。
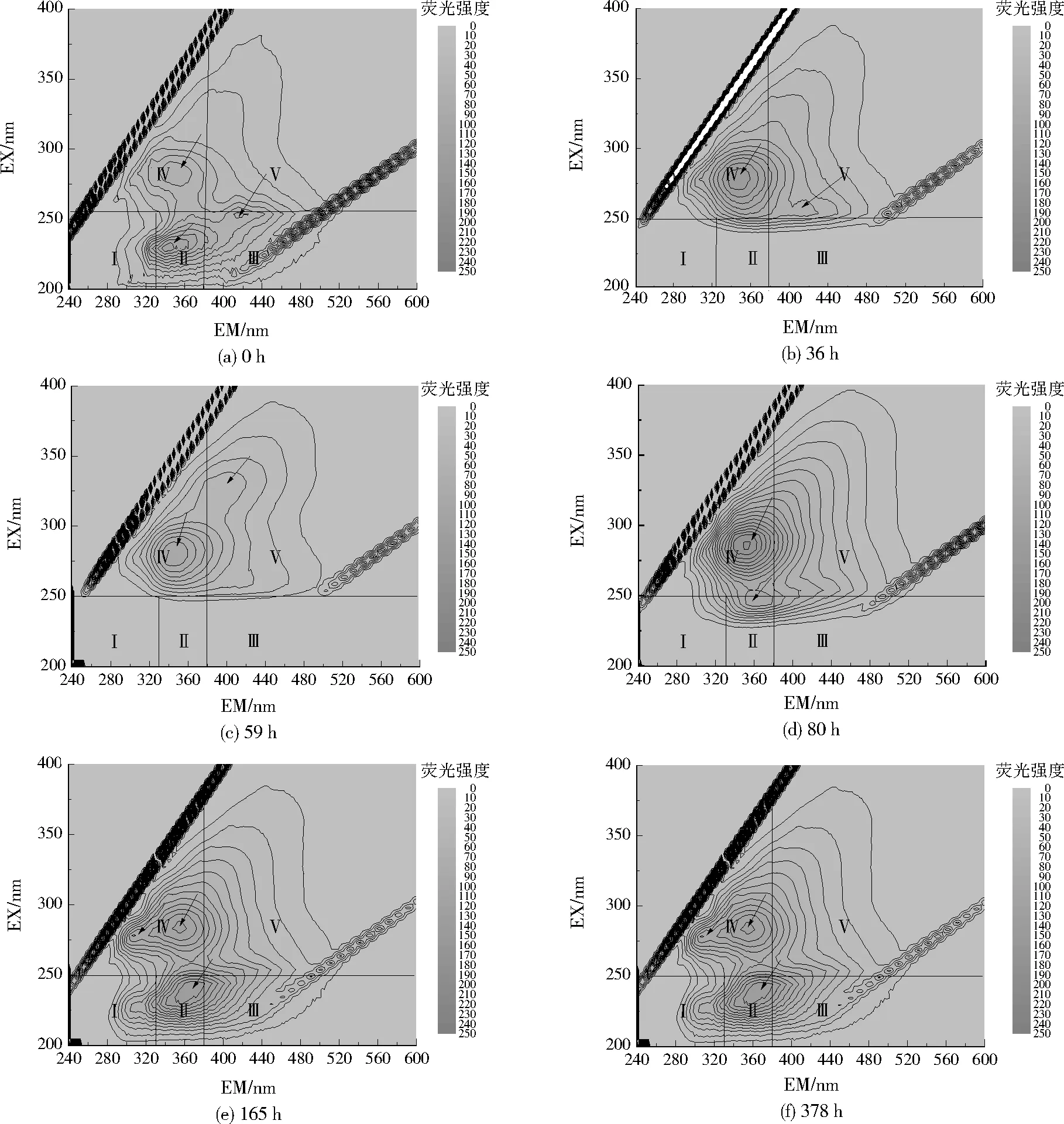
图4 不同时间淋出液的3DEEM特征Fig.4 3DEEM feature of leachate at different times
2.2.2 淋出液3DEEM特征
不同时间淋出液的3DEEM特征见图4。随着腐殖酸在泥灰岩中的迁移与转化,荧光峰位置发生了明显的变化。0 h时淋出液中主要有3个荧光峰,分别落在Ⅱ区、Ⅲ区、Ⅳ区。随着腐殖酸驱替泥灰岩中的空隙水,36 h时淋出液中有一个荧光峰初次出现在Ⅴ区,并且随着时间推移持续到59 h。80 h时淋出液中荧光峰只落在Ⅱ区、Ⅳ区,Ⅴ区消失,因为59~80 h时腐殖酸逐渐被被泥灰岩吸附,而Ⅲ区消失是因为其他荧光峰的荧光强度过高,屏蔽了Ⅲ区荧光峰。165 h时,Ⅲ区荧光峰仍然处于屏蔽状态;Ⅳ区存在2个荧光峰(Ⅳ1区、Ⅳ2区),出现了新的荧光峰(Ⅳ2区);Ⅱ区荧光峰位置基本不变。378 h时荧光峰和165 h保持一致,165~378 h这个阶段处于平衡稳定状态,未发生变化。3DEEM的变化与腐殖酸浓度变化完全吻合。
由图5可以看出,Ⅱ区和Ⅳ1区的荧光峰荧光强度基本保持不变,而Ⅳ2区荧光峰荧光强度从100逐渐上升到180,呈现出不断上升的趋势。说明Ⅴ区荧光峰消失后,转化为Ⅳ2区荧光峰,由此可以推断腐殖酸在与泥灰岩作用的过程中发生了生物降解,微生物将腐殖酸降解为溶解性微生物代谢产物,使得腐殖酸浓度降低。腐殖酸与泥灰岩的作用过程实质上是先吸附后降解的过程,这是因为泥灰岩中含有一定的微生物,当泥灰岩吸附腐殖酸后,泥灰岩中的微生物将腐殖酸(Ⅴ区)降解为溶解性微生物代谢产物(Ⅳ区)。
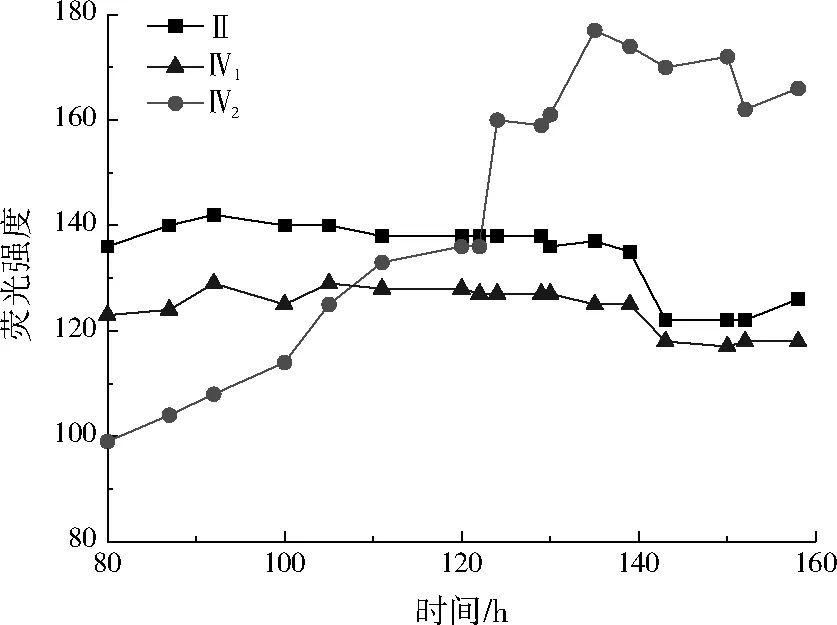
图5 80~165 h时主要荧光峰荧光强度变化Fig.5 Intensity change of main fluorescence peak during 80-165 h
3 结 论
(1) 腐殖酸在泥灰岩的运移表现为吸附作用与降解作用,随着腐殖酸初始浓度的增加,泥灰岩对腐殖酸的吸附呈现出线性增加的趋势。
(2) 泥灰岩对腐殖酸的吸附符合原始质量吸附方程,斜率为0.008 7,截距为0.073 1,R2=0.986 2,拟合度很好,泥灰岩对于腐殖酸有着很强的亲和力。
(3) 腐殖酸在泥灰岩中发生了微生物降解,这是一个先吸附后降解的动力过程,泥灰岩中的微生物将腐殖酸(Ⅴ区)降解为溶解性微生物代谢产物(Ⅳ区)。
[1] 宋海燕,尹友谊,宋建中.不同来源腐殖酸的化学组成与结构研究[J].华南师范大学学报(自然科学版),2009(1):61-66.
[2] 杨策,钟宁宁,师玉雷,等.煤矿区水体溶解有机质三维荧光光谱特征[J].光谱学与光谱分析,2008,28(1):174-177.
[3] MAXIMILIANO B,GRACIELA Z,MARCELO A.Effect of pH,anions and cations on the dissolution kinetics of humic acid particles[J].Colloids and Surfaces,2009,347(1):180-186.
[4] 凌婉婷,徐建民,高彦征,等.溶解性有机质对土壤中有机污染物环境行为的影响[J].应用生态学报,2004,15(2):326-330.
[5] 周岩梅,张琼,汤鸿霄.多环芳烃类有机物在腐殖酸上的吸附行为研究[J].腐植酸,2010,30(8):1564-1571.
[7] 李春越,党廷辉,王万忠,等.腐殖酸对农田土壤磷素吸附行为的影响研究[J].水土保持学报,2011,25(3):77-82.
[8] 余贵芬,青长乐,牟树森,等.汞在腐殖酸上的吸附与解吸特征[J].腐植酸,2001,21(5):601-606.
[9] 杨毅,王晓昌,金鹏康,等.水环境中腐殖酸与镉离子结合作用的影响因素[J].环境工程学报,2013,12(7):4603-4606.
[10] PI Kunfu,WANG Yanxin,XIE Xianjun,et al.Geochemical effects of dissolved organic matter biodegradation on arsenic transport in groundwater systems[J].Journal of Geochemical Exploration,2015,148(3):8-21.
[11] 贺倩,颜丽,杨凯,等.不同来源腐殖酸的组成和性质研究[J].土壤通报,2003,34(4):343-345.
[12] HAMBLY A C,ARVIN E,PEDERSEN L F,et al.Characterising organic matter in recirculating aquaculture systems with fluorescence EEM spectroscopy[J].Water Research,2015,83(11):112-120.
[13] WANG Xinyi,ZHEN Xiaoge,LI Renzheng,et al.Migration and transformation characteristics of DOM in fine sand and marl rock[J].Water Science & Technology,2016,74(1):157-164.
[14] 李任政,王心义,刘小满,等.温度及渗透流速影响下的溶解性有机质运移特征[J].环境工程学报,2015,11(9):5193-5198.
[15] 杨建.桌子山矿区地下水中溶解性有机质荧光特征分析[J].煤矿安全,2014,45(2):131-137.
[16] 刘小满,杨建,王心义,等.平顶山十矿地下水中天然有机质垂向分布特征[J].安全与环境学报,2014,14(4):53-56.
[17] CHEN Wen,WESTERHOFF P,LEENHEER J A.Flourescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J].Environmental Science and Technology,2003,37(24):5701-5710.
[18] NODVIN S C,DRISCOLL C T,LIKENS G E.Simple partitioning of anions andissolved organic carbon in a forest soil[J].Soil Science,1986,143(1):27-35.
Researchontheadsorptionanddegradationcharacteristicsofhumicacidinmarlstone
WANGTiantian1,WANGXinyi1,2,3,LIUXiaoman1,YANGGuang1.
(1.InstituteofResources&Environment,HenanPolytechnicUniversity,JiaozuoHenan454000;2.CollaborativeInnovationCenterofCoalbedMethaneandShaleGasforCentralPlainsEconomicRegion,JiaozuoHenan454000;3.InstituteofChinaPingmeiShenmaGroup,PingdingshanHenan467000)
The adsorption and degradation characteristics of humic acid were studied in marlstone. Static adsorption tests and dynamic column experiments were performed. At the same time,three dimensional excitation emission matrix (3DEEM) in the leaching solution were tested. The results showed that:(1) adsorption of humic acid was increased with concentration of humic acid linearly. (2) Marlstone adsorption of humic acid was in line with the original quality adsorption equation. Slope of equation was 0.008 7,intercept was 0.073 1 andR2was 0.986 2. This showed that marlstone could adsorb humic acid strongly. (3) The humic acid was absorbed by marlstone,and then absorbed humic acid was degraded by microorganism. In one word, it was a complex dynamic process. Humic acid (Ⅴ zone) in marlstone was degraded into soluble microbial products (Ⅳ zone) by microorganism.
humic acid; adsorption; degradation; 3DEEM
王甜甜,女,1991年生,硕士研究生,研究方向为环境地质与水文地质。#
。
*国家自然科学基金资助项目(No.41272250、No.41302214、No.41402220);河南省高校科技创新团队支持计划资助项目(No.15IRTSTHN027)。
10.15985/j.cnki.1001-3865.2017.06.011
2016-04-12)

