CYP2C19基因检测指导我国急性冠脉综合征患者抗血小板治疗方案的药物经济学评价
曹爱霖,钱 皎,王 卓(上海长海医院药学部,上海 200433)
CYP2C19基因检测指导我国急性冠脉综合征患者抗血小板治疗方案的药物经济学评价
曹爱霖*,钱 皎,王 卓#(上海长海医院药学部,上海 200433)
目的:从药物经济学角度评价我国拟行介入手术的急性冠脉综合征(ACS)患者依据CYP2C19基因指导抗血小板药物应用的可行性。方法:基于全球范围内的PLATO试验数据,依据治疗策略将患者分为3组(氯吡格雷组、替格瑞洛组、基因检测组)。通过运用Treeage Pro 2011软件构建短期决策树模型及长期Markov模型,导入我国相关数据,评价不同治疗策略的成本-效果。结果与结论:针对ACS患者,根据我国国内生产总值水平,常规应用替格瑞洛对自费患者及上海市的医保患者更具药物经济学优势,而CYP2C19基因检测指导抗血小板药物应用在全国范围的医保患者中更具有药物经济学优势。
替格瑞洛;氯吡格雷;基因检测;药物经济学;成本-效果分析;CYP2C19基因
冠状动脉粥样硬化性心脏病(Coronary atherosclerotic heart disease,CAHD)简称冠心病,是指冠状动脉粥样硬化使血管腔狭窄或阻塞,或(和)因冠状动脉功能性改变(痉挛)导致心肌缺血缺氧或坏死而引起的心脏病,临床上分为急性冠脉综合征(Acute coronary syndrome,ACS)和慢性冠脉病(Chronic coronary artery disease,CAD)。据《中国统计年鉴2015》所示,2014年我国城市居民主要疾病死亡率及死因构成中,心脏病均排在第2位[1]。又据《2013中国卫生统计年鉴》中对2012年30种疾病人均住院医药费用的统计,急性心肌梗死(下文简称“心梗”)已成为内科疾病序列中人均住院费用最高的病种[2]。可见,心脏疾病不仅严重威胁我国居民的身体健康,而且带来了沉重的经济负担。
根据国内外最新指南对ACS的治疗推荐,双联抗血小板药物仍是ACS患者介入术后的首选[3-5]。然而,近几年研究显示,即使行双联抗血小板治疗,仍有患者发生心血管事件,其部分原因为氯吡格雷抵抗[6]。氯吡格雷抵抗尚缺乏公认的定义且影响因素众多,用药依从性、细胞色素P450(Cytochrome P450,CYP)基因的多态性、体质量等均可能影响其治疗效果[6]。氯吡格雷是前药,需要经过小肠的吸收和CYP的代谢才能转化为有活性的代谢产物,这些代谢产物不可逆地抑制由P2Y12基因编码的二磷酸腺苷受体,进而抑制血小板的聚集[7]。据文献报道显示,影响氯吡格雷药物功能的主要因素是其代谢酶的基因多态性,其中CYP2C19*2、CYP2C19*3与之关系最密切;有别于欧裔人种,亚裔人种CYP2C19*2和CYP2C19*3的突变率高[7],故基因检测有利于指导临床用药。继2012年12月替格瑞洛上市,ACS双联抗血小板治疗方案有了新的选择。由2009年的PLATO试验可知,替格瑞洛在临床疗效方面有着不受基因影响、起效迅速等优势[8],但也存在着价格昂贵、未纳入我国医保等缺点。基于此,对替格瑞洛、氯吡格雷以及CYP2C19基因检测进行药物经济学评价可以为临床ACS的治疗决策提供依据。
1 资料与方法
1.1 资料来源与临床试验设计
本研究基于全球范围内的PLATO试验[8]——一项采用多中心、双盲、以氯吡格雷为对照的随机对照试验(Randomized controlled trial,RCT),纳入了18 624例ACS患者(后因各种因素脱落5 388例),分为替格瑞洛组(6 651例)和氯吡格雷组(6 585例),在同时口服阿司匹林治疗的基础上,替格瑞洛组患者给予180 mg替格瑞洛负荷剂量后再予以90 mg维持治疗1年,氯吡格雷组患者给予300~600 mg氯吡格雷负荷剂量后再予以75 mg维持治疗1年。试验的主要终点为心血管死亡、心梗或卒中组成的复合终点。此外,试验还分别针对基因、经济学和介入治疗等进行了亚组研究。
1.2 药物经济学评价
1.2.1 模型设计 参照PLATO试验经济学亚组研究的设计思路[9],从患者的角度出发,模拟ACS患者应用替格瑞洛、氯吡格雷以及CYP2C19基因检测的治疗策略。选用成本-效果分析模型,依据ACS指南中的治疗策略[3-5],参考Nikolic E等[10]发表的PLATO试验成本-效果分析模型,将本研究中的成本-效果分析模型结构分为两部分:前半部分为基于PLATO 1年期研究的决策树模型,后半部分为用于长期外推的Markov模型,详见图1(图中的转换概率说明:①为ACS患者1年后出现非致死性心梗的概率;②为ACS患者1年后出现非致死性卒中的概率;③为ACS患者1年后出现死亡的概率;④为非致死性心梗患者1年内死亡的概率;⑤为非致死性卒中患者1年内死亡的概率;⑥为非致死性心梗患者第2年死亡的概率;⑦为非致死性卒中患者第2年死亡的概率)。

图1 成本-效果分析的模型结构Fig 1 Model structure of cost-effectiveness analysis
基于我国人群和PLATO试验主要研究人群CYP2C19的基因型分布不同,有别于PLATO试验经济学亚组研究,本研究加入了对基因检测的决策判定,增加了基因检测组作为研究对象。依据检测结果,携带CYP2C19*2、CYP2C19*3基因的慢代谢(Poor metabolizer,PM)患者给予替格瑞洛治疗,而携带CYP2C19*1/ CYP2C19*1基因的快代谢(Extensive metabolizer,EM)患者继续给予氯吡格雷治疗。具体模型见图2(图中,*表示我国人群的EM基因型,#表示我国人群的PM基因型)。
1.2.2 数据来源 本研究中,决策树模型及Markov模型中的转换概率均源于已发表的中、英文文献,通过检索PubMed、Medline、万方期刊全文数据库及维普中文科技期刊数据库,英文检索词为“Ticagrelor”“Clopidogrel”“Cost-effectiveness”“Gene”“Genotype”“Economic analysis”,中文检索词为“替格瑞洛”“氯吡格雷”“经济学”“成本效果”“基因型”“药物经济学”等,各检索词以“and”连接,按需要组合,检索时限截至2015年12月31日,详见表1。
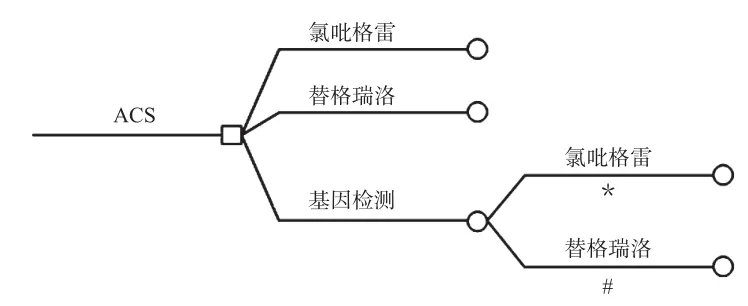
图2 决策树模型(主干部分)Fig 2 Decision tree model(main part)

表1 模型中相关转换概率参数来源Tab 1 Source of related transition probability parameters in model
1.2.3 成本确定 本研究从患者的角度出发,以《上海市医疗机构医疗服务项目和价格汇编(2014年)》[17]为参考,对患者住院及出院后费用进行计算,成本详见表2(表中医保部分成本依据2015年上海市城镇职工基本医疗保险报销比例进行计算,因我国ACS患者患病年龄区间较大,表中数据以门诊起付标准700元、报销比例80%,住院起付标准1 200元、报销比例92%计算)。以上海多家医院的平均价格(截至2015年10月31日)为参考,替格瑞洛为183元/盒(14粒*90 mg/盒,自费),氯吡格雷为137元/盒(7粒*75 mg/盒,医保)。
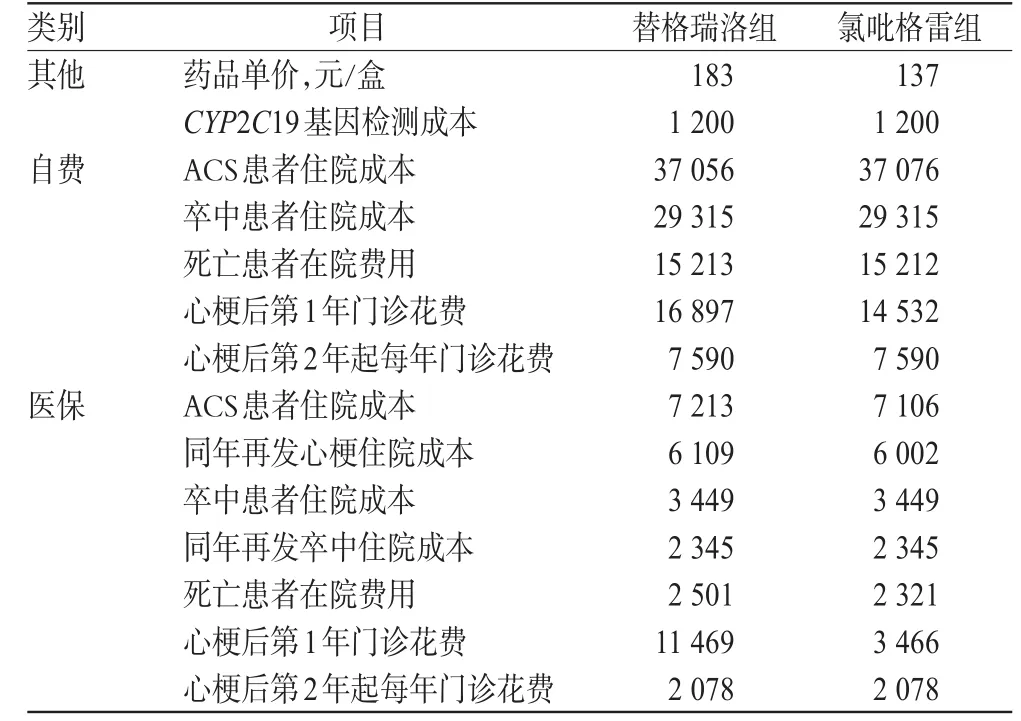
表2 患者医疗成本(元)Tab 2 Medical cost of patients(yuan)
1.2.4 效果指标 本研究以质量调整生命年(Quality adjusted life years,QALYs)为效果指标,测量工具为欧洲五维健康量表(EuroQol-5 dimensions,EQ-5D)。通过PLATO试验过程中对来自52个国家ACS患者进行EQ-5D问卷调查的结果,计算各治疗节点的平均18 624例QALYs[18],详见表3。
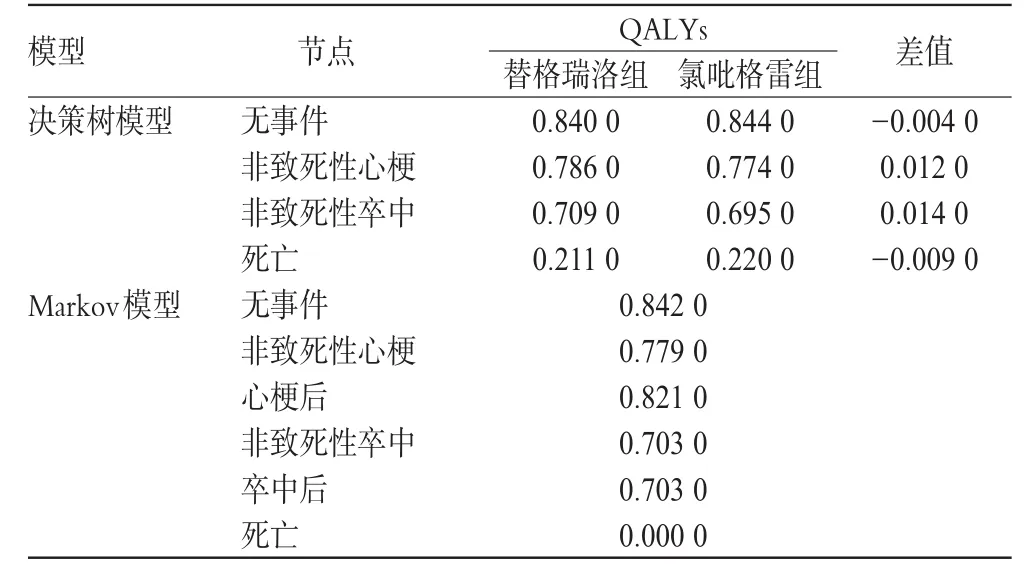
表3 成本-效果分析中各节点的QALYsTab 3 QALY of each part in the cost-effectiveness model
1.2.5 成本-效果分析 根据收集的数据建模,进行成本-效果分析,计算增量成本-效果比(Incremental cost effectiveness ratio,ICER),比较各方案改善单位效果所需的成本。
1.2.6 敏感度分析 依据成本-效果分析结果,对模型中的转换概率、主要成本参数、Markov模型中的QALYs值以及贴现率进行敏感度分析。
1.3 数据整理与统计分析
依据图1、图2模型结构,运用Treeage Pro 2011软件建立决策树联合Markov的模型,将各转换概率、成本及效果指标导入模型进行运算,随后进行数据整理和统计分析。
2 结果
2.1 模型运行
在导入各项数据后,依据患者是否有医保、基因检测是否纳入医保范畴分组,运用Treeage Pro 2011软件对决策树联合Markov的模型进行运算,模拟计算ACS患者应用替格瑞洛或氯吡格雷1年,及其后40年的成本及效果情况[19];并依据《中国药物经济学评价指南(2011版)》[20]对成本进行贴现,贴现率定为5%。
2.2 成本-效果分析结果
2.2.1 自费患者的成本-效果分析结果 与氯吡格雷组相比,替格瑞洛组的ICER为8 833.86,小于基因检测组的11 513.88,详见表4。
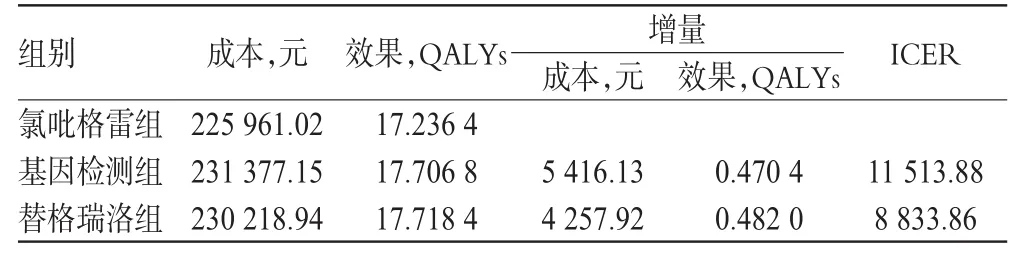
表4 自费患者的成本-效果分析结果Tab 4 Results of cost-effectiveness analysis for uninsured inpatients
按照世界卫生组织(WHO)关于药物评价的推荐意见:ICER<人均国内生产总值(Gross domestic product,GDP),增加的成本完全值得;人均GDP<ICER<3倍人均GDP,增加的成本可以接受;ICER>3倍人均GDP,增加的成本不值得[20]。依据国家统计局2016年1月19号公布的2015年GDP,计算得2015年人均GDP约为4.92万元[21]。结合表4可知,相比氯吡格雷组,替格瑞洛组的ICER不仅小于基因检测组,而且远小于人均GDP,因此可得,自费的ACS患者直接应用替格瑞洛具有药物经济学优势,增加的成本完全值得。
2.2.2 医保(基因检测项目自费)患者的成本-效果分析结果 与氯吡格雷组相比,基因检测组的ICER为17 323.24,小于替格瑞洛组的21 729.11,详见表5。
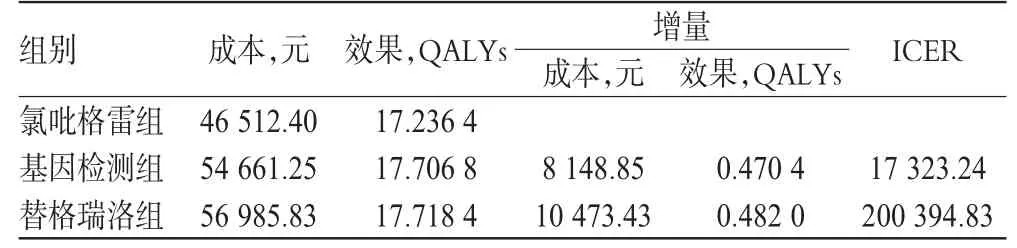
表5 医保(基因检测自费)患者的成本-效果分析结果Tab 5 Results of cost-effectiveness analysis for insured patients(gene detection at their own expense)
与基因检测组相比,替格瑞洛组的ICER为200 394.83,远大于3倍人均GDP,增加的成本不值得。但是,因本研究主要基于上海市2014年的成本信息,故同时选取上海市2015年人均GDP(10.31万元)[22]作为参照,可得替格瑞洛组对于上海居民而言,增加的成本可以接受。
2.2.3 医保(基因检测项目纳入医保范畴)患者的成本-效果分析结果 与氯吡格雷组相比,基因检测组的ICER为14 976.30,小于替格瑞洛组的21 729.11,详见表6。
与基因检测组相比,替格瑞洛组的ICER为295 567.24,远大于3倍人均GDP,增加的成本不值得。而对于上海市居民而言,增加的成本在可以接受范围内。
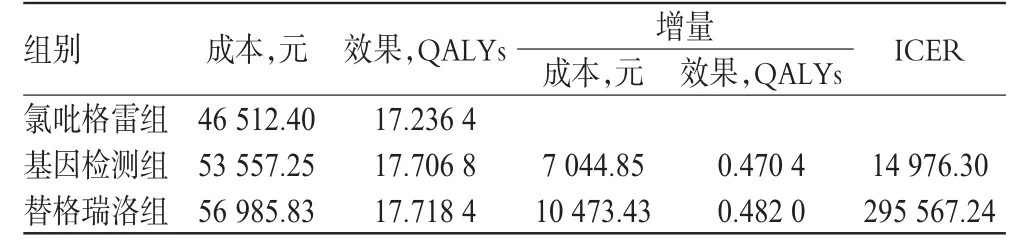
表6 医保(基因检测纳入医保)患者的成本-效果分析结果Tab 6 Results of cost-effectiveness analysis for insured patients(gene detection included in medical insurance)
2.3 敏感度分析
2.3.1 一维敏感度分析 对患者携带功能缺失基因概率进行一维敏感度分析,结果显示,基因概率在0.3~0.5范围之间转换时,对成本-效果分析结果无影响。
2.3.2 概率敏感度分析 基于模型设计的药物经济学评价,由于缺乏患者成本和效果方面的样本数据,故不能采用标准的统计学方法处理不确定性,单因素敏感度分析和极端分析法也不适用[23]。目前,在参数较多和模型设计的情况下进行不确定性分析时,多采用蒙特卡洛模拟(Monte Carlo simulation)进行概率敏感度分析,条件允许时可使用成本-效果可接受曲线(Cost-effectiveness acceptability curve,CEAC)表示不确定性分析的结果[20]。
本研究定义成本为正态分布,效果服从三角分布,概率服从β分布。模拟10 000个样本,对模型进行蒙特卡洛模拟。按照《中国药物经济学评价指南(2011版)》,把支付意愿(Willingness to pay,WTP)定义为人均GDP的3倍[20]。依据2015年全国人均GDP及上海市人均GDP,将WTP定为15万元/QALYs(全国)和30万元/QALYs(上海)。
结果可得:①对于纯自费患者,WTP>3万元时,近100%的人群愿意接受替格瑞洛治疗。②在基因检测未纳入医保的前提下,WTP为15万元时,约5.1%的人群愿意接受替格瑞洛治疗,约94.9%的人群愿意接受基因检测来指导药物应用;当WTP为30万元时,约90.2%的人群愿意接受替格瑞洛治疗,约9.8%的人群愿意接受基因检测来指导药物应用,详见图3。③在基因检测纳入医保的前提下,当WTP为15万元时,近100%的人群愿意接受基因检测来指导药物应用;而当WTP为30万元时,约51.3%的人群愿意接受替格瑞洛治疗,约48.7%的人群愿意接受基因检测来指导药物应用,详见图4。
3 讨论
2012年底,替格瑞洛获得了原国家食品药品监督管理局(State Food and Drug Administration,SFDA)颁发的进口药品许可证(Import drug license,IDL),获准在我国正式上市。2015年,欧美及我国ACS指南[3-5]均将替格瑞洛作为Ⅰ类推荐用药,提到了与氯吡格雷相同的高度。本研究从药物经济学角度进行分析,为替格瑞洛、氯吡格雷及CYP2C19基因检测在我国ACS患者药物治疗决策方面提供了参考依据。

图3 医保(基因检测自费)患者的蒙特卡洛可接受曲线Fig 3 Monte Carlo acceptability curve of insured patients(gene detection at their own expense)

图4 医保(纳入基因检测)患者的蒙特卡洛可接受曲线Fig 4 Monte Carlo acceptability curve of insured patients(including gene detection)
本研究结合ACS疾病及药物治疗特点,使用决策树联合Markov模型进行循证药物经济学评价,外推性良好。模型采用的是PLATO卫生经济学亚洲成本-效果分析长期Markov模型,数据也多来源于PLATO试验;为保证数据更加贴近我国实际情况,部分转换概率选用我国亚组试验结果。此外,除成本核算基于最新临床实际情况外,就近几年氯吡格雷基因型检测陆续开展这一实际情况,增加了以基因型结果指导临床用药这一治疗策略,国内尚无此类相关文献报道。因2015年全国人均GDP(约为4.92万元)远小于2015年上海人均GDP(约为10.31万元),故从药物经济学角度出发,不同地区的患者选择的治疗策略应不同:对于自费患者,推荐使用替格瑞洛治疗;对于医保患者,无论基因检测是否纳入医保范畴,均推荐基因检测来指导用药;而就上海地区患者而言,替格瑞洛更具经济学优势。
本研究尚存在一定的局限性:(1)氯吡格雷抵抗尚无公认金标准,基因型的检测仅可作为预测氯吡格雷抵抗的证据之一;(2)本研究部分数据取自PLATO试验,并不能完全代表我国患者的实际情况,但随着替格瑞洛在我国Ⅳ期临床“大禹研究”[7]结果的公布,将会收集到更为精准的数据;(3)因ACS患者多为老年低收入人群,WTP应考虑患者的实际情况。
[1] 国家统计局.中国统计年鉴2015[EB/OL].(2015-12-10)[2016-04-01].http://www.stats.gov.cn/tjsj/ndsj/2015/indexch.htm.
[2] 国家卫生计生委统计信息中心.2013中国卫生统计年鉴[EB/OL].(2015-04-26)[2016-04-01].http://www.nhfpc.gov.cn/htmlfiles/zwgkzt/ptjnj/year2013/index2013.html.
[3] 中华医学会心血管病学分会.急性ST段抬高型心肌梗死诊断和治疗指南[J].中华心血管病杂志,2015,43(5):380-393.
[4] Roffi M,Patrono C,Collet JP,et al.2015 ESC guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation:task force for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation of the European Society of Cardiology(ESC)[J].Eur Heart J,2016,37(3):267-315.
[5] Amsterdam EA,Wenger NK,Brindis RG,et al.2014 AHA/ ACC guideline for the management of patients with non-ST-elevation acute coronary syndromes:a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines[J].J Am Coll Cardiol,2014,64(24):e139-e228.
[6] 王淑宏,王燕慧.氯吡格雷抵抗机制的研究进展[J].国际检验医学杂志,2013,34(7):843-846.
[7] 祝锦,刘丽宏.氯吡格雷药物基因组学研究进展[J].中国新药杂志,2013,22(15):1774-1778.
[8] Wallentin L,Becker RC,Budaj A.For the PLATO investigators.Ticagrelor versus clopidogrel in patients with acute coronary syndromes[J].N Engl J Med,2009,361(11):1045-1057.
[9] 何江江,张崖冰,高润霖,等.替格瑞洛与氯吡格雷治疗急性冠脉综合征的药物经济学分析[J].中国药物经济学,2013,8(3):27-32.
[10] Nikolic E,Janzon M,Hauch O,et al.Cost-effectiveness of treating acute coronary syndrome patients with ticagrelor for 12 months:results from the PLATO study[J].Eur Heart J,2013,34(3):220-228.
[11] 吴永健.替格瑞洛:给中国ACS患者更有力的拯救[EB/ OL].(2013-10-30)[2016-04-01].http://www.medsci. cn/article/show_article.do?id=1a112595676.
[12] Cannon CP,Harrington RA,James S,et al.Comparison of ticagrelor with clopidogrel in patients with a planned invasive strategy for acute coronary syndromes(PLATO):a randomised double-blind study[J].Lancet,2010,375(9711):283-293.
[13] Wallentin L,James S,Storey RF,et al.Effect of CYP2C19 and ABCB1 single nucleotide polymorphisms on outcomes of treatment with ticagrelor versus clopidogrel for acute coronary syndromes:a genetic substudy of the PLATO trial[J].Lancet,2010,376(9749):1320-1328.
[14] 张爱玲,杨莉萍,胡欣.亚洲健康人群CYP2C19等位基因发生率的合并分析[J].中国循证医学杂志,2013,13(12):1431-1439.
[15] 梁岩,朱俊,谭慧琼,等.中国地区非ST抬高急性冠脉综合征患者生存时间的影响因素分析[J].中华医学杂志,2005,85(13):873-878.
[16] 武海滨,龚巍巍,潘劲,等.首次脑卒中患者生存率和死亡影响因素的研究[J].中华流行病学杂志,2014,35(7):812-816.
[17] 上海市物价局.上海市医疗机构医疗服务项目和价格汇编:2014年[EB/OL].(2014-11-24)[2016-04-01].http:// www.shdrc.gov.cn/wcm.files/upload/CMSshfgw/201512/ 201512291106055.pdf.
[18] Liverpool Reviews and Implementation Group.Ticagrelor for acute coronarysyndromes[EB/OL].(2011-02-04)[2016-04-01].http://www.nets.nihr.ac.uk/__data/assets/pdf_file/ 0011/82568/ERGReport-08-240-01.pdf.
[19] Sorich MJ,Horowitz JD,Sorich W,et al.Cost-effectiveness of using CYP2C19 genotype to guide selection of clopidogrel or ticagrelor in Australia[J].Pharmacogenomics,2013,14(16):2013-2021.
[20]《中国药物经济学评价指南》课题组.中国药物经济学评价指南:2011版[J].中国药物经济学,2011,6(3):6-48.
[21] 国家统计局.2015年国民经济运行稳中有进、稳中有好[EB/OL].(2016-01-19)[2016-04-01].http://www.stats. gov.cn/tjsj/zxfb/201601/t20160119_1306083.html.
[22] 上海市统计局.2015年上海市国民经济和社会发展统计公报[EB/OL].(2016-02-29)[2016-04-01].http://www. stats-sh.gov.cn/sjfb/201602/287258.html.
[23] 杨莉,胡善联.药物经济学评价中处理不确定性的方法[J].中国药物经济学,2007,2(5):11-15.
(编辑:胡晓霖)
Pharmacoeconomics Evaluation of CYP2C19 Genetic Test Guiding Antiplatelet Therapy for Acute Coronary Syndrome Patients in China
CAO Ailin,QIAN Jiao,WANG Zhuo(Dept.of Pharmacy,Shanghai Changhai Hospital,Shanghai 200433,China)
OBJECTIVE:To evaluate the feasibility of using CYP2C19 gene to guide the use of antiplatelet agents in acute coronary syndrome(ACS)patients undergoing interventional operation in China from the viewpoint of pharmacoeconomics.METHODS:Based on global PLATO trial data,the patients were divided into 3 groups according to treatment strategies(clopidogrel group,ticagrelor group,genetic test group).By applying Treeage Pro 2011 software,short-term decision tree model and long-term Markov model were established,and related data were imported to evaluate cost-effectiveness of different treatment strategies.RESULTS&CONCLUSIONS:For ACS patients,according to the level of GDP in China,conventional use of ticagrelor is of pharmacoeconomic advantage for in Shanghai and uninsured patients insured patients;the use of antiplatelet agents guided by CYP2C19 gene test is of pharmacoeconomic advantage among nationwide insured patients.
Ticagrelor;Clopidogrel;Genetic test;Pharmacoeconomics;Cost-effectiveness analysis;CYP2C19 gene
R956;R349+.55
A
1001-0408(2017)23-3183-05
2016-09-01
2016-11-10)
*药师。研究方向:临床药学。电话:021-31162331。E-mail:601905411@qq.com
#通信作者:副主任药师,博士。研究方向:临床药学。电话:021-31162299。E-mail:wangzhuo088@163.com
DOI10.6039/j.issn.1001-0408.2017.23.04

