活性维生素D及其类似物治疗血液透析患者继发性甲状旁腺功能亢进相关指南推荐
王 蔚 综述 李贵森 王 莉 审校
·血液净化·
活性维生素D及其类似物治疗血液透析患者继发性甲状旁腺功能亢进相关指南推荐
王 蔚 综述 李贵森 王 莉 审校
维生素D是钙、磷及骨代谢的重要调节激素,在血液透析患者中使用维生素D可上调维生素D受体,控制继发性甲状旁腺功能亢进(SHPT),纠正钙磷失衡。各国指南都推荐使用维生素D作为SHPT的重要治疗手段。但是,不合理的使用维生素D治疗,尤其是活性维生素D及类似物的过早或过量使用,可能增加体内钙磷负荷,心血管系统钙化及心血管事件的发病风险。因此,本文整理各国慢性肾脏病-矿物质和骨异常(CKD-MBD)指南中有关活性维生素D及其类似物治疗SHPT的内容,希望从发挥其有益的治疗作用,减少不良反应的角度,为临床医生治疗SHPT提供更多的参考。
血液透析 继发性甲状旁腺功能亢进 维生素D 指南
维生素D(VD)是钙、磷及骨代谢的重要调节激素。维生素D受体(VDR)在体内广泛分布,还具有影响机体的代谢、免疫及调节细胞生命周期等多方面的功能[1]。活性维生素D及其类似物是目前治疗血透患者继发性甲状旁腺功能亢进的常用药物,近年来已有多项研究表明使用活性维生素D及其类似物治疗能改善慢性肾脏病(CKD)患者维生素D缺乏、纠正继发性甲状旁腺功能亢进(SHPT),并能降低患者死亡率、改善患者预后。系统性的激活全身各处的VDR,可能为CKD 患者带来多种有利于心血管系统并降低死亡风险的效果。这些效果可能包括:延缓血管钙化的进程,阻断动脉粥样硬化的发生及发展;通过对肾素-血管紧张素-醛固酮系统(RAAS)与内皮素系统抑制及纠正SHPT从而减轻心脏负荷,心肌纤维化,瓣膜钙化与心脏肥大[2-3]。
但是,活性维生素D又会增加血钙、血磷水平,从而增加体内钙磷负荷,心血管系统钙化及心血管事件的发病风险。因此,了解各国有关VD治疗SHPT的规范或指南推荐,尤其是掌握适当的干预时机,避免过度使用,对合理地使用VD治疗SHPT有很好的参考意义。
西班牙,日本,韩国指南提供了较为系统的推荐意见
西班牙的慢性肾脏病矿物质与骨异常(CKD-MBD)指南发表于2011年[4],对血液透析患者,建议将全段甲状旁腺激素(iPTH)水平维持在150~300 pg/ml范围内,避免低于100 pg/ml或高于500 pg/ml。这与KDIGO指南中显示的“极端值”(<2倍或>9倍的iPTH正常值上限)几乎一致。为使更多的患者达到目标值,工作组推荐使用活性VD及类似物(骨化三醇或阿法骨化醇)控制PTH水平,但如果观测到钙和/或磷的水平较高或PTH<100 pg/ml(<2倍正常上限值),则应减少VD剂量或暂停给药。选择性维生素D受体激动剂(sVDRA,帕立骨化醇)对钙磷的影响更小,且回顾性研究的结果显示患者的远期预后更好[5],因此推荐在血液透析患者中使用sVDRA。同样,如果发现钙和(或)磷的水平较高或PTH<100 pg/ml(<2倍正常上限值),则应减少sVDRA的剂量或停药。在具体临床实践中,帕立骨化醇的剂量可参照血清iPTH水平(pg/ml),以iPTH/80或iPTH/120作为单次起始剂量,例如,iPTH为480,那么帕立骨化醇的单次初始计量为4 μg或6 μg。在维持治疗阶段,每周最低1~5 μg的使用,并可考虑与拟钙剂合用。
日本的CKD-MBD指南发表于2013年[6]。该指南在确定PTH目标范围时,主要考虑到iPTH水平对血液透析患者远期生存的影响:2006年以前,日本按照KDOQI设定的目标值,即考虑到血液透析患者维持正常骨代谢的需求,认为iPTH目标设为150~300 pg/ml之间较为合理[7]。2006年以后,基于日本透析治疗协会自身调研数据的分析,发现在日本血液透析患者中,iPTH<180 pg/ml的患者1年和3年预后更好[8],因此,2006年的指南将iPTH目标设定为60~180 pg/ml。但是,临床应用中反映目标范围较窄,且欧洲[9]和南美[10]新报道的研究数据支持维持略高的iPTH水平,日本在新版指南中最终建议将血液透析患者的iPTH目标范围设定为60~240 pg/ml。当iPTH水平持续高于管理目标范围的上限时,建议在纠正可调节因素的基础上,通过药物治疗降低iPTH水平,这些手段包括对血清磷、钙进行管理以及给予VDRA和(或)拟钙剂。具体的用药推荐:当iPTH水平较高且血清磷、钙水平正常或较高时,可考虑给予拟钙剂;当血清磷或钙水平正常或较低时,可考虑给予VDRA(图1)[6]。日本指南强调了磷、钙管理的优先性,但只要血清磷、钙水平无显著偏差,则可给予VDRA,无需考虑iPTH水平。我们认为这个建议是在维持钙磷平衡稳定的前提下,考虑了激活VDR的积极意义。

图1 VDRA或拟钙剂治疗继发性甲状旁腺功能亢进的九宫格分区图[6]VDRA:维生素D受体激动剂;↑:启动或增加治疗;↓:减少或暂停治疗;*:血清PTH水平高;**:血清甲状旁腺激素水平低
韩国的CKD-MBD指南推荐发表于2015年[11]。该指南首先参考了KDOQI和日本的指南推荐,日本血液透析患者iPTH水平为180 pg/ml左右时研究发现,生存率更好。其次,韩国2014年完成的多中心研究提示多数韩国患者的iPTH水平处于较低水平[12],因此韩国工作组将血液透析患者的血清iPTH水平设定为100~300 pg/ml范围内。为了达到目标范围,当血液透析患者的iPTH>200~300 pg/ml时,即可开始药物治疗。如果iPTH<150 pg/ml,则应降低当前药物治疗的剂量。对于iPTH<100 pg/ml的血液透析患者,则应停止抑制PTH的治疗手段。对已给予合理治疗而iPTH仍持续>500 pg/ml的患者,则考虑甲状旁腺切除术。
在VDRA的应用方面,韩国明确区分了骨化三醇和帕立骨化醇两种药物(图2)[11]:对于iPTH>200 pg/ml或口服骨化三醇疗效不好的血液透析患者,可使用静脉用骨化三醇(0.5~1.5 μg,1~3次/周,最高不超过5 μg/周);如果iPTH>300 pg/ml,则考虑给予帕立骨化醇。帕立骨化醇的起始剂量通常为每次透析2~5 μg,在维持期内,可每次减少剂量1~2 μg(剂量的1/3或1/4),同时监测iPTH和钙、磷的水平。对长期维持治疗以及减、停药方面,韩国指南的推荐意见:如iPTH<150 pg/ml,则降低药物剂量或者暂停给药。如果iPTH<100 pg/ml,则应考虑停用VDRAs。在暂停治疗之后,如果iPTH水平升高至>100 pg/ml,给药剂量为停药前的1/2。如果在暂停治疗之前的给药剂量已经达到最低剂量,则可以将给药时间调整为每2次透析给药1次。此外,韩国指南推荐,VDRA与拟钙剂合用可以作为控制PTH的有效手段,而手术治疗则仅适用于通过各种药物治疗后仍然无法控制SHPT的患者。
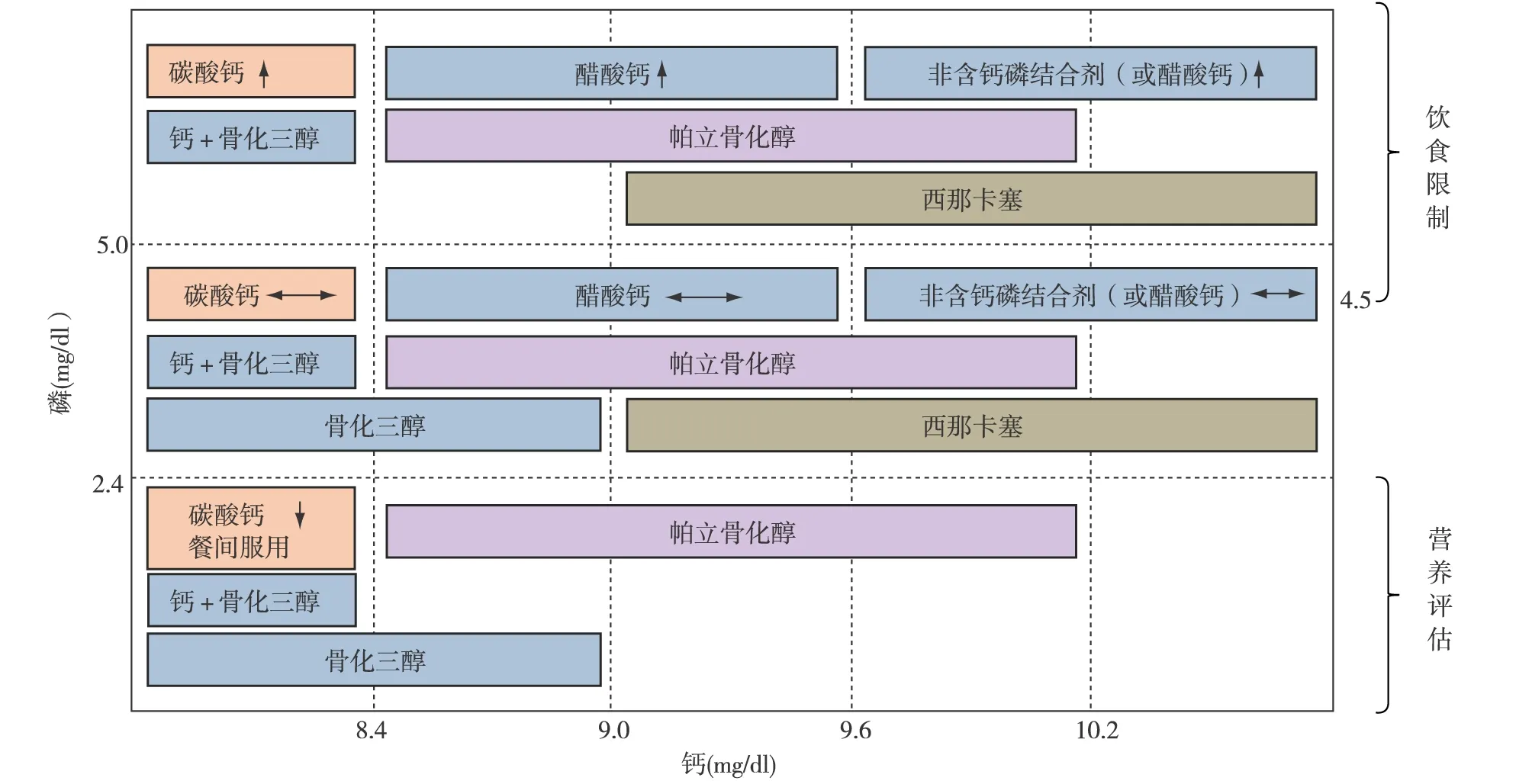
图2 根据钙磷水平选择治疗方案[11]
英国,加拿大,澳大利亚及KDIGO指南未明确提供药物选择和剂量的具体方案
英国2010年首次发布CKD-MBD指南[13],在2015年进行了更新[14]。对血液透析患者,应维持iPTH水平在正常值上限的2~9倍。iPTH在目标范围内的患者,应动态监测iPTH水平,如果iPTH水平进行性升高或始终高于参考范围的,则推荐使用活性维生素D治疗。此外,在2010年欧洲最佳肾脏实践组织(European Renal Best Practice,ERBP)针对2009年版KDIGO指南的注解中[15],对于高iPTH或iPTH持续升高的患者,建议使用骨化三醇或其他维生素D类似物治疗,如果iPTH水平下降未达到目标范围或患者出现药物不耐受、并发高钙血症或高磷血症,则可改用拟钙剂,或小剂量维生素D和拟钙剂联合使用。
加拿大的CKD-MBD指南(2008)[16 ]没有明确规定iPTH的目标范围,可能和指南发布时间较早有关,。该指南仅指出如果血清iPTH水平高于53 pmol/L,可考虑使用VD类似物。如果出现高钙血症或高磷血症,或甲状旁腺激素水平低于10.6 pmol/L,则停止治疗,对sVDRA,拟钙剂等未做任何建议。
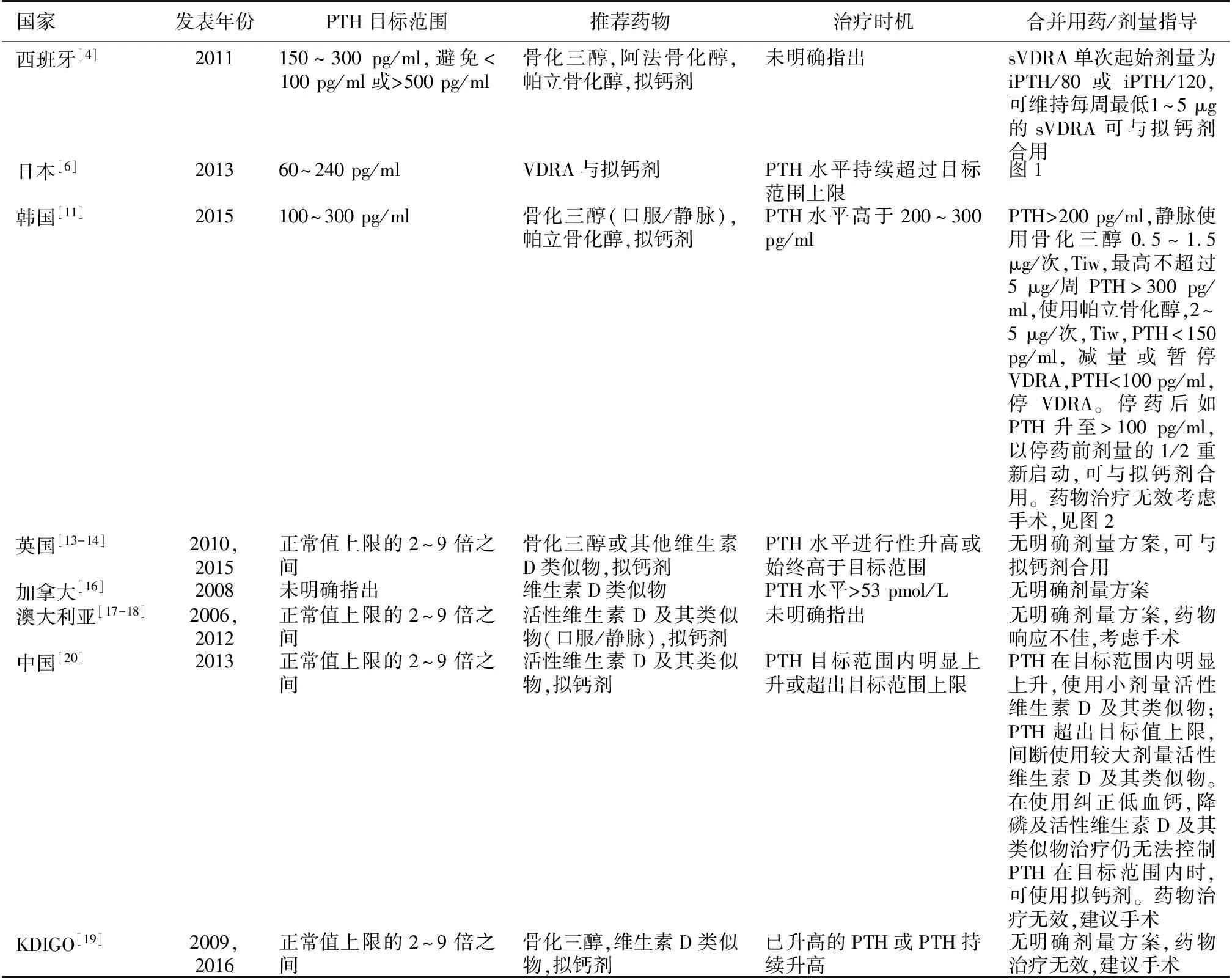
表1 各国指南推荐对比
sVDRA:维生素D受体激动剂;PTH:甲状旁腺激素
澳大利亚的CKD-MBD指南发布于2006年[17],明确提出VD及其类似物不论是每日口服、间断性口服还是静脉内给药均可有效降低血液透析患者的iPTH水平。口服骨化三醇无效的患者,或口服骨化三醇依从性较差的患者,可静脉使用骨化三醇。由于血液透析患者有静脉血管通路,应优先选择静脉维生素D和静脉维生素D类似物治疗,静脉治疗可在每次透析结束时给药,以提高患者依从性。2012年澳大利亚更新指南[18 ],提出血液透析患者的iPTH水平为正常值上限的2~9倍,且避免在目标范围内的大幅波动。药物方面,可使用活性维生素D3和拟钙剂控制SHPT,当药物响应不佳时,可考虑甲状旁腺切除。
2016年,KDIGO发布了新版指南[19],强调对CKD 3a~5D期患者的磷、钙及PTH进行综合管理。尤其在血钙管理方面,从过去“维持血钙在正常范围”调整为“避免高钙血症”。基于此,对CKD 3a~5D期患者,不再常规推荐活性VD及类似物,而仅在PTH“重度”升高或“持续进展”的患者中使用。对血液透析患者,PTH目标范围仍然维持为正常值上限2~9倍的推荐。在SHPT治疗方面,同时推荐拟钙剂、骨化三醇,或维生素D类似物,或拟钙剂与骨化三醇或维生素D类似物合并使用。工作组将上述治疗方法作为血液透析患者的临床一线治疗选择,并未指出优先推荐顺序。
中华医学会肾脏病学分会CKD-MBD诊治指导
在上述各国指南的基础上, 中国于2013年9月发表了CKD-MBD诊治指导[20],建议将血液透析患者的iPTH水平维持于正常值上限的2~9倍。在积极控制可调节因素如高血磷、低血钙和维生素D缺乏的基础上,如果iPTH在目标范围内出现明显上升趋势时,建议使用小剂量活性维生素D及其类似物,如果超出目标值上限,建议间断使用较大剂量的活性维生素D及其类似物治疗。在使用包括纠正低血钙,控制高血磷和使用活性维生素D及其类似物治疗等传统治疗方法仍无法将iPTH控制在目标范围时,建议血液透析患者选择性使用拟钙剂。血液透析患者合并药物治疗无效的严重甲状旁腺功能亢进,建议行甲状旁腺切除术。
综上所述,各国在2005年以后的指南都推荐活性维生素D及其类似物治疗SHPT。与SHPT有关的各项生化指标,如PTH、钙、磷的治疗目标范围在各国指南有细微的差别,但其长期的管理目标是一致的,包括稳定维持iPTH在目标范围内并避免大幅度的上下波动;避免患者进展为低转运/无动力性骨病;维持VDR的激活以发挥其多效性作用;避免钙磷负荷过重及钙磷水平反复波动;避免心血管钙化及减少心血管事件的发生风险;改善患者的生活质量及远期预后等。在上述宏观原则的指导下,日本和韩国进一步给出了更为细致的治疗路径和用药选择,尤其是韩国指南在达标后减量这一环节给出了细致的表述,值得参考。同时各国指南,尤其KDIGO指南提出,避免在CKD患者早期过早使用活性维生素D及其类似物,以避免高钙血症及异位钙化的风险。最后,表1总结各国指南推荐的PTH目标值、药物及治疗方案,希望给临床医师在治疗SHPT患者选择个体化治疗方案时提供更多的参考依据。
1 Bover J,Egido J,Fernández-Giráldez E,et al.Vitamin D,vitamin D receptor and the importance of its activation in patients with chronic kidney disease.Nefrologia,2015,35(1):28-41.
2 Cozzolino M,Ketteler M,Zehnder D.The vitamin D system:a crosstalk between the heart and kidney.Eur J Heart Fail,2010,12(10):1031-1041.
3 Kovesdy CP,Kalantar-Zadeh K.Vitamin D receptor activation and survival in chronic kidney disease.Kidney Int,2008,73(12):1355-1363.
4 Torregrosa JV,Bover J,Cannata Andía J,et al.Spanish Society of Nephrology recommendations for controlling mineral and bone disorder in chronic kidney disease patients (S.E.N.-M.B.D.).Nefrologia,2011,31(Suppl.1):3-32.
5 Teng M,Wolf M,Lowrie E,et al.Survival of Patients Undergoing Hemodialysis with Paricalcitol or Calcitriol Therapy.N Engl J Med,2003,349(5):446-456.
6 Fukagawa M,Yokoyama K,Koiwa F,et al.Clinical practice guideline for the management of chronic kidney disease-mineral and bone disorder.Ther Apher Dial,2013,17(3):247-288.
7 Qi Q,Monier-Faugere MC,Geng Zet al.Predictive value of serum parathyroid hormone levels for bone turnoverin patients on chronic maintenance dialysis.Am J Kidney Dis,1995,26(4):622-631.
8 Nakai S,Akiba T,Kazama J,et al.Effects of serum calcium,phosphorous,and intact parathyroid hormone levels on survival in chronic hemodialysis patients in Japan.Ther Apher Dial,2008,12(1):49-54.
9 Floege J,Kim J,Ireland E,et al.Serum iPTH,calcium and phosphate,and the risk of mortality in a European haemodialysis population.Nephrol Dial Transplant,2011,26(6):1948-1955.
10 Naves-Díaz M,Passlick-Deetjen J,Guinsburg A,et al.Calcium,phosphorus,PTH and death rates in a large sampleof dialysis patients from Latin America.The CORES Study.Nephrol Dial Transplant,2011,26(6):1938-1947.
11 Hwang E,Choi BS,Oh KH,et al.Management of chronic kidney disease-mineral and bone disorder:Korean working group recommendations.Kidney Res Clin Pract,2015,34(1):4-12.
12 Kim GH,Choi BS,Cha DR,et al.Serum calcium and phosphorus levels in patients undergoing maintenance hemodialysis:A multicentre study in Korea.Kidney Res Clin Pract,2014,33(1):52-57.
13 Simon Steddon,Ed Sharples.Clinical practice guideline CKD-mineral and bone disorders (CKD-MBD).UK Renal Association,2010.
14 Clinical practice guideline CKD-mineral and bone disorders (CKD-MBD) Final Version (01/03/2015)
15 Goldsmith DJ,Covic A,Fouque D,et al.Endorsement of the kidney disease improving global outcomes(KDIGO) chronic kidney disease-mineral and bone disorder(CKD-MBD) guidelines:a european renal best practice (ERBP)commentary statement.Nephrol Dial Transplant,2010,25(12):3823-3831.
16 Levin A,Hemmelgarn B,Culleton B,et al.Guidelines for the management of chronic kidney disease.CMAJ,2008,179(11):1154-1162.
17 Grahame Elder,Randall Fanll,et al.The CARI Guidelines-Caring for Australasians with Renal Impairment.Bone Disease.Calcium,Phosphate and Parathyroid Hormone.
18 Chronic Kidney Disease (CKD) Management in General Practice (2nd edition).Kidney Health Australia,Melbourne,2012.
19 KDIGO 2016 clinical practice guideline updateon diagnosis,valuation,prevention andtreatment of CKD-mbdpublic review draft.AUGUST 2016.
20 王莉, 李贵森,刘志红.中华医学会肾脏病学分会《慢性肾脏病矿物质与骨异常诊治指导》.肾脏病与透析肾移植杂志,2013,22(6):554-559.
(本文编辑 律 舟 书 实)
Treatment of secondary hyperparathyroidism in hemodialysis patients with active vitamin D and its analogue—guidelines review
WANGWei,LIGuisen,WANGLi
DepartmentofNephrology&InstituteofNephrology,RenalDepartment,SichuanProvincialPeople’sHospital&MedicalSchoolofUESTC,Chengdu610072,China
Vitamin D (VD) is an essential hormone which is functional in adjustment of calcium and phosphorus homeostasis and bone metabolism. Treat hemodialysis patients with VD could exert meaningful effect on upregulating expressing of VD receptor, secondary hyperparathyroidism control and reversion of calcium and phosphorus homeostasis. But inappropriate VD treatment, especially early use and over-dose treatment of active VD or its analogue also increases internal load of calcium and phosphorus, and the risk of cardiovascular calcification. So this review is trying to summarize detail recommendations and descriptions of VD treatment in CKD-MBD guidelines from multiple countries, standing on angle of benefit against side effect, wish to offer a handy reference to Chinese real clinical practice.
hemodialysis secondary hyperparathyroidism vitamin D guideline
10.3969/j.issn.1006-298X.2017.04.018
电子科技大学医学院·四川省人民医院肾内科(成都,610072)
2017-04-24

