心脏再同步化治疗逆转合并左心室收缩功能不全的三度房室传导阻滞患者左心室重构的预测因素分析
谢翠平,陈康玉,严激,徐健,苏浩,宇霏,朱红军,沈伟,安春生,杨冬妹
心脏再同步化治疗逆转合并左心室收缩功能不全的三度房室传导阻滞患者左心室重构的预测因素分析
谢翠平,陈康玉,严激,徐健,苏浩,宇霏,朱红军,沈伟,安春生,杨冬妹
目的:分析合并左心室收缩功能不全的三度房室传导阻滞(AVB)患者应用心脏再同步化治疗(CRT)后发生左心室重构逆转的预测因素。
方法:选取2009-01至2015-05在安徽省立医院植入CRT的三度AVB患者65例,收集术前临床资料及术后随访资料,术后12个月左心室收缩末期容积(LVESV)较术前下降≥15%或左心室射血分数(LVEF)增加≥5%定义为左心室重构逆转。将患者分为逆转组(n=36)和无逆转组(n=29),比较两组患者的临床资料,并采用二分类Logisitic回归模型分析CRT逆转左心室重构的预测因素。
结果:共入选患者65例,平均年龄(62 ± 14)岁,随访12个月,发生心室重构逆转的患者为36例(55.4%),逆转组女性(P=0.011)、基线QRS时限>120 ms(P=0.001)、心室间激动延迟(IVMD)≥40 ms(P=0.027)、心率校正后的心电图Q波起始点距离左心室16节段最小容积点时间间隔的标准差[Tmsv16-SD(%R-R)]≥8.3%(P=0.001)的比例高于无逆转组,二元Logisitic回归分析显示,女性(OR=6.228,95%CI:1.561~24.842,P=0.01)、QRS时限>120 ms(OR=7.778,95%CI 1.996~30.769,P=0.003)与Tmsv16-SD(%R-R)≥8.3%(OR=8.134,95%CI:2.064~32.057,P=0.003)是心室重构发生逆转的独立预测因素。
结论:对于合并左心室收缩功能不全的三度AVB患者,女性、QRS时限>120 ms及Tmsv16-SD(%R-R)≥8.3%或可作为CRT逆转左心室重构的预测因素。
心脏再同步治疗;房室传导阻滞;心室重构
(Chinese Circulation Journal, 2017,32:766)
长期以来,以右心室起搏为基础的单腔或双腔起搏器是三度房室传导阻滞(AVB)患者的主要治疗方法,但越来越多的证据表明右心室起搏会损害心功能,在合并左心室收缩功能不全的患者中更为明显[1],其机制尚不明确,目前多认为是由于右心室起搏可引起类似左束支传导阻滞的医源性电传导异常,使心脏机械运动不同步,致心室腔逐渐扩大,心功能受损,最终导致患者心力衰竭发生率及住院率增加[2,3],心脏再同步化治疗(CRT)已被证实能纠正心脏的不同步情况,显著改善慢性心力衰竭患者的心功能,降低心力衰竭住院率及死亡率[4],而随着BLOCK HF研究结果的公布,CRT在房室传导阻滞患者中的应用日益受到关注[5],我们的研究亦发现CRT可逆转合并左心室收缩功能不全的三度AVB患者的心室重构,但并非所有患者均会发生逆转,本研究旨在探讨合并左心室收缩功能不全的三度AVB患者应用CRT后发生左心室重构逆转的相关预测因素。
1 资料与方法
病例选择:选取我院2009-01至2015-05成功植入CRT装置的三度AVB患者65例;入选标准:左心室舒张末期内径(LVEDD)≥55 mm,左心室射血分数(LVEF)≤50%,纽约心脏协会(NYHA)心功能分级 Ⅰ~Ⅲ级;排除标准:曾接受心脏电器械装置植入(无论后期保留或移除),不稳定性心绞痛,急性心肌梗死,入选前3个月内有冠状动脉搭桥或介入手术史,存在具修复指征的瓣膜病,预期寿命小于1年。
超声心动图指标及测量方法:(1)仪器:应用Philips iE33彩色超声诊断仪,采用S5-1探头,频率为1~5 MHz,常规检查,X3-1探头,频率1~3 MHz,实时三维显像。应用Qlab7.0定量分析软件,对三维数据图像进行定量分析。(2)心脏结构及功能指标:测量LVEF、左心室收缩末期容积(LVESV)、左心室舒张末期容积(LVEDV)、LVEDD、左心室收缩末期内径(LVESD)、二尖瓣反流(MR)分级,MR分级定义为:1级(轻度反流):二尖瓣反流面积/左心房面积<20%,2级(中度反流):20%≤二尖瓣反流面积/左心房面积≤45%,3级(重度反流):二尖瓣反流面积/左心房面积>45%。(3)心脏不同步指标:①心室间激动延迟(IVMD):定义为左心室与右心室射血前间期差值,正常值<40 ms,≥40 ms为室间不同步;②左心室内不同步:a:左心室间隔至后壁运动延迟(SPWMD):使用M型超声测量从前间隔运动方向改变的点到后壁运动方向改变的点的间期,正常值<130 ms,≥130 ms为左心室内不同步;b:左心室12节段收缩速度达峰时间标准差(12-SD):使用组织多普勒超声,测量左心室壁12节段(心尖四腔、二腔和三腔观的基底段和中间段)的收缩达峰时间的最大差异,正常值<30 ms,≥33 ms为左心室内不同步;c:心率校正后的心电图Q波起始点距离左心室16节段最小容积点时间间隔的标准差[(Tmsv16-SD(%R-R)]:使用实时三维超声心动图,将左心室分为16个节段(基底部6个节段+中间部6个节段+心尖部4个节段),测量从心动周期的起始点(定义为R波的起始处)至每个节段最小收缩容积时间,然后计算标准差,再计算该数值占RR间期的百分比,以排除心率差异的影响,正常值<5%,≥8.3%为左心室内不同步[6,7]。
12导联心电图检查:测量QRS波时限及形态(左束支传导阻滞,非左束支传导阻滞)。
CRT植入:采用Seldinger技术穿刺左侧锁骨下静脉,送入三根J型导丝,透视下至下腔静脉,在锁骨下切开皮肤,层层分离至肌筋膜,并做一囊袋备用,逆行造影显示冠状静脉各分支走形,将左心室导线送至靶静脉(首选侧静脉或侧后静脉),常规测试和10 V高压起搏测试满意后固定,将右心室导线植入心尖部或间隔部,右心房导线置于右心耳处,测试后,连接脉冲发生器,缝合囊袋。
随访及结果比较:随访过程中,主要观察超声心动图相关指标变化,结合相关研究[8],以术后12个月LVESV较术前下降≥15%或LVEF增加≥5%定义为左心室重构逆转,将患者分为逆转组(n=36)和无逆转组(n=29),比较两组间各项指标差异是否存在统计学意义,评价CRT逆转心室重构的预测因素。
统计学处理:采用SPSS 16.0统计分析软件,计量资料经正态分布检验,符合正态分布的资料以均数±标准差表示,采用t检验比较,不符合正态分布的资料以中位数(四分位间距)表示,非正态分布或方差不齐时,采用秩和检验;计数资料以例数(n)或百分比表示,采用卡方检验比较,理论频数<5时采用Fisher确切概率法。采用二分类Logisitic回归模型分析CRT逆转心室重构的预测因素,P<0.05为差异有统计学意义。
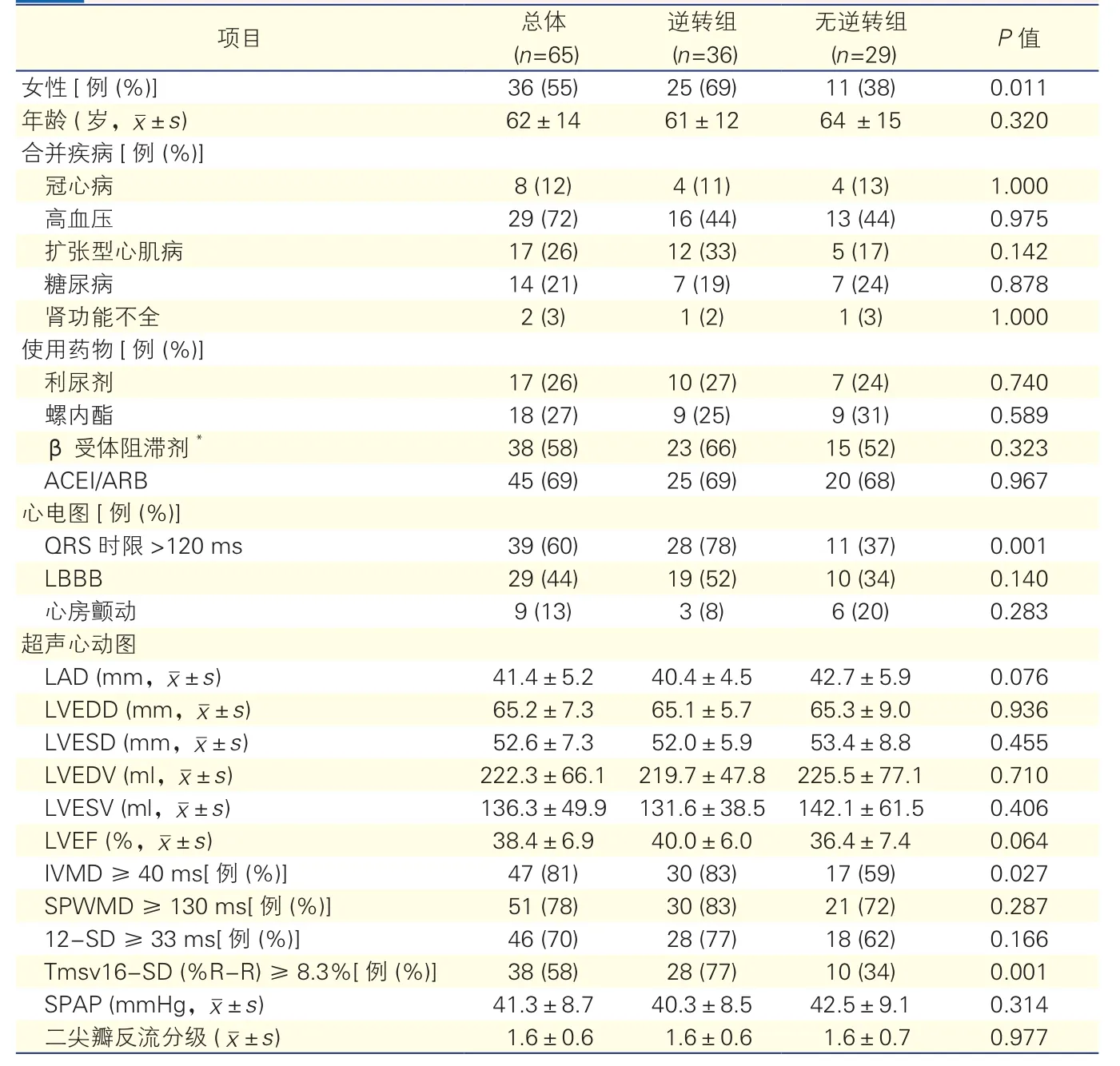
表1 65例患者基线资料比较
2 结果
共入选患者65例,平均年龄(62±14)岁,随访12个月,合并高血压病29例(72%),冠心病8例(12%),糖尿病14例(21%),扩张型心肌病17例(26%),发生心室重构逆转的患者为36例(55.4%),逆转组患者女性(P=0.011)、基线QRS时限>120 ms(P= 0.001)、心室间激动延迟(IVMD)≥40 ms(P=0.027)、Tmsv16-SD(% R-R)≥8.3%(P=0.001)的比例高于无逆转组(表1),二分类Logisitic回归分析显示(表2),女性[OR=6.228,95%可信区间(CI) :1.561~24.842,P=0.01]、QRS时限>120 ms(OR=7.778,95%CI:1.996~30.769,P=0.003)与Tmsv16-SD(%R-R)≥8.3%(OR=8.134,95%CI:2.064~32.057,P=0.003)是左心室重构发生逆转的独立预测因素。
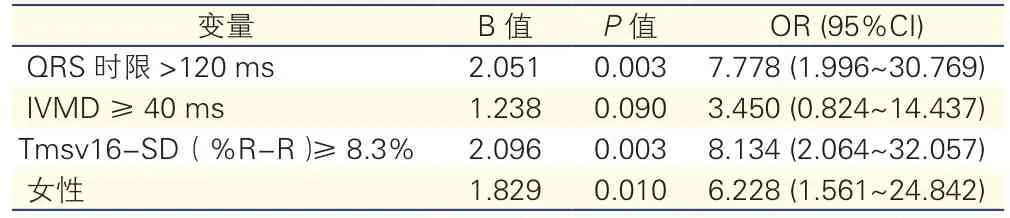
表2 二分类 Logistic回归模型分析CRT逆转心室重构的预测因素
3 讨论
正常心脏电活动通过特殊传导系统以3~4 m/s的速度迅速传导,可使心肌即刻同步收缩或舒张,而右心室心尖部起搏期间,电活动以正常速度的1/4沿心肌缓慢传导,主要从肌细胞传至肌细胞,这导致心室电活动不同步,表现为室间隔单向运动及左心室后下基底部最迟激动,这与在左束支传导阻滞患者中观察到的异常活动相似[9]。近1/3右心室起搏患者在起搏即刻出现异常的机械活动[10],这一比例在长期起搏时增至50%[11],长时间、高比率的右心室起搏可使左心室发生重构,进而损害心功能,研究发现右心室起搏比率每增加10%,心力衰竭住院风险增加20%[12];起搏治疗的患者中约50%为房室传导功能异常,近1/3存在左心室收缩功能损害[3],其中三度AVB患者常常需要高比率起搏,80%以上患者起搏比率>80%[13],是右心室起搏时出现心功能损害的高危人群。
目前已有多项研究发现对于左心室收缩功能不全、需起搏治疗的患者,双心室起搏可逆转心室重构,改善心功能,优于右心室起搏。我们的研究有相似结果,但我们也发现,此类患者应用CRT后并非均能发生心室重构逆转及心功能改善,为此,本研究针对CRT逆转该类患者心室重构的预测因素进行了探讨。
目前心室重构逆转的定义主要包括CRT有反应和超反应,多数研究以LVESV下降≥15%或LVEF增加≥5%作为CRT有反应标准,这也是本研究中选取左心室重构逆转标准的重要参考。
与传统适应人群相似,CRT通过纠正AVB患者的心脏运动不同步而起到改善心功能的作用,而后者的不同步目前认为主要是右心室起搏所致的电传导延迟,而本研究发现,对于合并左心室收缩功能不全的三度AVB患者,QRS时限>120 ms,Tmsv16-SD(%R-R)≥8.3%可作为CRT逆转左心室重构的预测因素,这一发现提示对于AVB患者,CRT或许并非仅仅通过避免右心室起搏引起的不同步起作用,当患者存在基线电、机械不同步时,更有可能从CRT中获益。
QRS时限延长是电不同步的有效指标,是预测CRT效果的重要因素。REVERSE研究入选了610例QRS时限>120ms的轻度心力衰竭患者,依据QRS时限将患者分为<134 ms、134~152 ms、152~167 ms、168~219 ms组,以临床复合评分为终点事件,随访发现当QRS时限>120 ms时,CRT获益与QRS时限呈正相关,而当QRS时限<120 ms时,不能观察到CRT获益[14]。目前研究认为QRS时限越宽,从CRT获益的可能性越大,CARE-HF研究以死亡率和非计划心血管事件住院作为主要终点事件,入选813例QRS时限≥120ms的心力衰竭患者,分为QRS时限≥160 ms及<160 ms组,对比其接受CRT-P或药物治疗的效果差异,发现各QRS组患者CRT效果均优于药物治疗,而在QRS时限≥160 ms时获益尤为明显[15]。另一些研究则认为只有当QRS时限>150 ms时,患者方能从CRT中获益[16,17]。而对于存在左心室收缩功能不全的三度AVB患者,我们的研究发现QRS时限>120 ms对CRT逆转其心室重构具有预测意义。
以电不同步指标筛选CRT患者时,约有30%被认为不适合的患者可从CRT中获益,可能因为机械不同步并非总与电传导异常存在联系[18],然而目前二维超声、组织多普勒等超声指标未能在CRT患者的选择方面起到有利作用[6]。三维超声可能优于上述传统方法,本研究显示Tmsv16-SD(%R-R)≥8.3%可作为三度AVB患者接受CRT治疗后左心室重构逆转的预测因素。Padeletti等[19]纳入了73项研究,进行Meta分析显示使用三维超声心动图测量的左心室收缩不同步指数(SDI)评价CRT治疗反应具有良好的准确性,以9.8%为截点预测CRT有反应的敏感性和特异性分别为93%和75%,另一项研究也发现以SDI>10%预测CRT反应性的敏感性为96%,特异性为88%[20]。
本研究认为对于合并左心室收缩功能不全的三度AVB患者,需进一步结合预测因素筛选可能从CRT获益的人群,基线电、机械运动不同步的存在或能提高患者获益的可能性,但本研究存在一定局限性:为回顾性研究,主要基线资料来源于收集患者住院及门诊的相关材料,未能评价患者的生活质量、住院率、生存率情况;此外样本量较小,结论尚需更多研究证实。
[1] Fang F, Sanderson JE, Yu CM. Should all patients with heart block receive biventricular pacing? All heart block patients with a pacemaker indication should receive biventricular pacing: one move, double the gains? Circ Arrhythm Electrophysiol, 2015, 8: 722-729.
[2] Ahmed M, Gorcsan J, Marek J, et al. Right ventricular apical pacinginduced left ventricular dyssynchrony is associated with a subsequent decline in ejection fraction. Heart Rhythm , 2014, 11: 602-608.
[3] 常龙, 程中伟, 方全. 减少不必要右心室起搏的方法. 中国循环杂志, 2015, 30: 1244-1247.
[4] Linde C, Curtis AB, Fonarow GC, et al. Cardiac resynchronization therapy in chronic heart failure with moderately reduced left ventricular ejection fraction: Lessons from the Multicenter InSync Randomized Clinical Evaluation MIRACLE EF study. Int J Cardiol, 2016, 202: 349-355.
[5] Ponikowski P, Voors AA, Anker SD, et al. The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure: The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Developed withthe special contribution of the Heart Failure Association (HFA) of the ESC. Eur J Heart Fail, 2016, 18: 891-975.
[6] Chung ES, Leon AR, Tavazzi L, et al. Results of the Predictors of Response to CRT (PROSPECT) trial. Circulation, 2008, 117: 2608-2616.
[7] El Missiri AM. Echocardiographic assessment of left ventricular mechanical dyssynchrony - A practical approach. The Egyptian Heart Journal, 2014, 66: 217-225.
[8] Ypenburg C, van Bommel RJ, Borleffs CJ, , et, al. Long-term prognosis after cardiac resynchronization therapy is related to the extent of left ventricular reverse remodeling at midterm follow-up. J Am Coll Cardiol, 2009, 53: 483-490.
[9] 李岚, 吴忠东, 赵勤英, 等. 长期右心室起搏出现心力衰竭的患者升级三腔起搏对心功能影响的探讨. 中国循环杂志, 2013, 28: 338-341.
[10] Martinelli Filho M, de Siqueira SF, Costa R, et al. Conventional versus biventricular pacing in heart failure and bradyarrhythmia: the COMBAT study. J Card Fail, 2010, 16: 293-300.
[11] Tops LF, Suffoletto MS, Bleeker GB, et al. Speckle-tracking radial strain reveals left ventricular dyssynchrony in patients with permanent right ventricular pacing . J Am Coll Cardiol, 2007, 50: 1180-1188.
[12] Curtis AB, Worley SJ, Adamson PB, et al. Biventricular pacing for atrioventricular block and systolic dysfunction. N Engl J Med, 2013, 368: 1585-1593.
[13] Gierula J, Cubbon RM, Jamil HA, et al. Patients with long-term permanent pacemakers have a high prevalence of left ventricular dysfunction. J Cardio Med, 2015, 16: 743-750.
[14] Gold MR, Thebault C, Linde C, et al. Effect of QRS duration and morphology on cardiac resynchronization therapy outcomes in mild heart failure: results from the Resynchronization Reverses Remodeling in Systolic Left Ventricular Dysfunction (REVERSE) study. Circulation, 2012, 126: 822-829.
[15] Cleland JG, Daubert JC, Erdmann E, et al. The effect of cardiac resynchronization on morbidity and mortality in heart failure. N Engl J Med, 2005, 352: 1539-1549.
[16] Tang AS, Wells GA, Talajic M, et al. Cardiac resynchronization therapy for mild-to moderate heart failure. N Engl J Med, 2010, 363: 2385-2395.
[17] Zareba W, Klein H, Cygankiewicz I, et al. Effectiveness of cardiac resynchronization therapy by QRS Morphology in the Multicenter Automatic Defibrillator Implantation Trial-Cardiac Resynchronization Therapy (MADIT-CRT). Circulation, 2011, 123: 1061-1072.
[18] Cai Q, Ahmad M. Left ventricular dyssynchrony by three-dimensional echocardiography: Current understanding and potential future clinical applications. Echocardiography, 2015, 32: 1299-1306.
[19] Padeletti L, Paoletti Perini A, Gronda E. Cardiac resynchronization therapy: the issue of non-response. Heart Fail Rev, 2012, 17: 97-105. [20] Kleijn SA, Aly MF, Knol DL, et al. A meta-analysis of left ventricular dyssynchrony assessment and prediction of response to cardiac resynchronization therapy by threedimensional echocardiography. Eur Heart J Cardiovasc Imaging, 2012, 13: 763-775.
Predictor Analysis of Left Ventricular Reverse Remodeling in Patients With III° Atrio-ventricular Block Combining Left Ventricular Systolic Dysfunction After Cardiac Resynchronization Therapy
XIE Cui-ping, CHEN Kang-yu, YAN Ji, XU Jian, SU Hao, YU Fei, ZHU Hong-jun, SHEN Wei, AN Chun-sheng, YANG Dong-mei.
Department of Cardiology, Anhui Provincial Hospital Affiliated to Anhui Medical University, Hefei (230001), Anhui, China
YAN Ji, Email: yanjillllll@126.com
Objective: To analyze the predictors of left ventricular reverse remodeling in patients with III˚ atrio-ventricular block (AVB) combining left ventricular systolic dysfunction after cardiac re-synchronization therapy (CRT).
��A total of 65 III˚ AVB patients
CRT in our hospital from 2009-01 to 2015-05 were enrolled. Clinical information before and after the operation were recorded. Left ventricular reverse remodeling was defined by left ventricular end systolic volume (LVESV) decreased 15% or left ventricular ejection fraction (LVEF) increased≥5% at 12 months after CRT. The patients were divided into 2 groups: Reversal group, n=36 and No reversal group, n=29. Clinical condition was compared between 2 groups, predictors for CRT reversing left ventricular remodeling were evaluated by two classification Logistic regression analysis.
Results: The patients’ average age was (62±14) years and 36/65 (55.4%) with reverse remodeling. In Reversal group, the ratios of female (P=0.011), baseline QRS width>120ms (P=0.001), inter-ventricular mechanical delay (IVMD)≥40 ms (P=0.027) and standard deviation of time-to-minimum systolic volume of 16 segments [Tmsv16-SD (%R-R)≥8.3%, (P=0.001)] werehigher than those in No reversal group. Two classification Logisitic regression analysis indicated that female (OR=6.228, 95%CI 1.561-24.842, P=0.01), QRS duration>120 ms (OR=7.778, 95% CI 1.996-30.769, P=0.003) and Tmsv16-SD (%RR)≥8.3% (OR=8.134, 95% CI 2.064-32.057, P=0.003) were the independent predictors for ventricular reverse remodeling .
Conclusion: Female, QRS>120ms and Tmsv16-SD (%R-R)≥8.3% could be used as the predictors for CRT reversing left ventricular remodeling in III˚ AVB patients combining left ventricular systolic dysfunction.
Cardiac resynchronization threapy; Atrio-ventricular block; Ventricular remodeling
book=766,ebook=42
2016-10-26)
(编辑:汪碧蓉)
2013年安徽省科技攻关计划项目(1301042210);安徽省第八批 “115”产业创新团队
230001 安徽省合肥市,安徽医科大学附属省立医院 心血管内科
谢翠平 硕士研究生 主要从事心脏起博及电生理研究 Email:710256873@qq.com 通讯作者:严激 Email: yanji111111@126.com
R541
A
1000-3614(2017)08-0766-05
10.3969/j.issn.1000-3614.2017.08.009

