rhG-CSF包含体处理工艺改进
刘建飞+匡瑾瑾+傅晖
摘 要 通过使用管式离心机替代转子离心机对rhG-CSF(赛格力)包含体处理工艺进行改进,使4个亚批次处理的包含体合并为1个批次进行处理,操作时间缩短4倍。通过改进前后的质量对比研究发现,本工序变性蛋白的纯度、内毒素及残余DNA与原工艺相比均无明显差异,且符合企业质量要求,而人工和动力成本下降了75%。
关键词 包含体 rhG-CSF 变性蛋白
中图分类号:TQ464.7 文献标识码:A 文章编号:1006-1533(2017)15-0075-04
Process improvement of inclusion-body of rhG-CSF
LIU Jianfei*, KUANG Jinjin, FU Hui
(Shanghai Sunway Biotech Co., Ltd., Shanghai 201206, China)
ABSTRACT An improved process for the treatment of rhG-CSF inclusion body was established by using tubular centrifuge instead of rotor centrifuge, which could make 4 sub-batches treatment of inclusion bodies in the original process into only one and total operation time be reduced to one fourth. It was found that the purity of denatured protein and the contaimination of endotoxin and residual DNA in the improved process was comparable to those in the original process and the quality could meet the requirements of enterprises while the costs of labor and power could be reduced by 75%.
KEY WORDS inclusion body; rhG-CSF; denatured protein
人粒细胞集落刺激因子是一个小的弱酸性蛋白,分子量为18.8 kD。重组人粒细胞集落刺激因子(rhG-CSF)为利用基因重组技术通过工程菌的发酵生产的,与天然产品相比,生物活性在体内、外基本一致。rhG-CSF是调节骨髓中粒系造血的主要细胞因子之一,选择性作用于粒系造血祖细胞,促进其增殖、分化,并可增加粒系终末分化细胞的功能[1]。它对于治疗由肿瘤放化疗、骨髓移植所引起的粒细胞减少症具有显著疗效[2-4]
赛格力(SunGran)为我们公司生产的重组人粒细胞集落刺激因子注射液的商品名,是以大肠埃希氏菌为表达载体,表达的rhG-CSF以包含体[5]形式存在与大肠埃希氏菌细胞质中,须经细胞破碎后收集包含体,再经包含体处理、复性、纯化,制备成赛格力原液[5-7]。
包含体处理一般采用多种缓冲液对其进行洗涤,最后用高浓度变性剂(6 mol/L盐酸胍或8 mol/L尿素)对其进行溶解。由于包含体难溶解和密度的特异性,缓冲液洗涤后,都用离心机来进行固液分离,重新收集包含体[8-11]。目前广泛运用的转子离心机由于处理量小,效率较低。管式离心机利用连续离心的原理,可以在短时间内一次离心大量的液体。本研究利用管式离心机代替传统的转子离心机,对包含体处理工艺进行改进,实践证明工艺改进后的产量和质量无明显变化,而工作效率大大提高了。
1 材料与方法
1.1 材料
基因工程大肠埃希氏菌在发酵罐中进行高密度发酵[12-13],最终获得50 L发酵液,离心收集到2 800 g菌体,收集的大肠埃希氏菌经超声破碎、离心后获得的固体物质约600 g。
脱氧胆酸钠、十二烷基肌氨酸钠、Acrylamide/bisacrylamide,30% solution(分析纯,Sigma公司);二巯苏糖醇、Tris(分析纯,Promega公司);低分子量标准蛋白(marker,中国科学院上海生物化学研究所,分子量依次为97.4、66.2、43.0、31.0、20.1和14.4 kD);细菌内毒素工作标准品(10 EU/ml及1 000 EU/ml)、鲎试剂(湛江安度斯生物有限公司);盐酸胍(分析纯,英潍捷基上海贸易有限公司);DIG High Prime DNA Labeling and Detection Starter KIT(Roche公司);其他常用化學试剂为市售分析纯或药用辅料。
1.2 设备
GQ76管式离心机、GL-21M高速冷冻离心机(上海离心机研究所);PowerPac HV电泳仪、GelDocXR凝胶成像仪(Bio-Rad公司)。J98-Ⅲ DN型超声仪(宁波新芝生物科技有限公司)。
1.3 方法
1.3.1 溶液制备
破菌缓冲液:20 mmol/L pH 8.0 Tris-EDTA-2Na盐酸缓冲液;水溶性洗涤液(A液):1 mmol/L乙二胺四乙酸二钠、0.1 mol/L氯化钠;脂溶性洗涤液(B液):含1%脱氧胆酸钠、5 mmol/L二巯苏糖醇、5 mmol/L乙二胺四乙酸二钠的50 mmol/L Tris-HCl缓冲液(pH 9.0);蛋白溶解液(C液):含2%十二烷基肌氨酸钠、20 mmol/L硫酸铜的50 mmol/L Tris-HCl缓冲液(pH 8.0);变性液(D液):含6 mol/L盐酸胍的40 mmol/L的HAc-NaAc缓冲液(pH 4.0)。
1.3.2 原工艺和改进后工艺
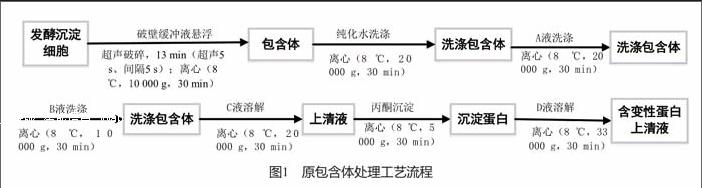
赛格力一批发酵所获得的包含体分成4个亚批进行处理。首先,包含体分别经纯化水、A液、B液洗涤,每次洗涤后均离心收集沉淀。B液洗涤后收集的沉淀,用C液溶解后,收集上清液,然后在上清液中加入冷冻后的丙酮(在冰浴条件下)进行搅拌离心,收集沉淀,最后用变性剂D液溶解,离心获得含变性蛋白的上清液(图1)。
改进后工艺流程和改进前一样,只是前5步用管式离心机代替转子离心机,但是考虑到安全原因,丙酮沉淀后的步骤还是保留使用转子离心机。
1.4 检测方法
内毒素检测:按照《中国药典》2015年版通则1143方法1 凝胶法进行检测。
残余DNA测定:按照《中国药典》2015年版通则3407第一法 DNA探针杂交法进行检测。
电泳方法:按照《中国药典》2015年版通则0541第五法SDS-聚丙烯酰胺凝胶电泳法进行检测。
2 结果与讨论
2.1 产量比较
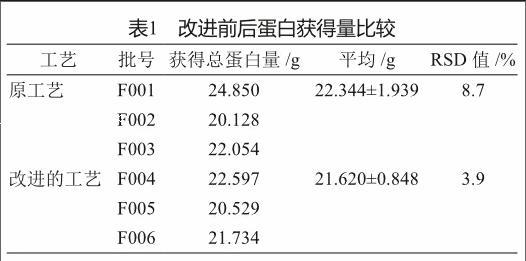
采用管式离心机劳动效率得到了大大提高,但是两者所采用的离心模式以及离心力还是有所不同的。管式离心机是否能够把洗涤液中的包含体全部离心收集起来,将是影响其产量的关键因素。分别选取了工艺改进前和后连续的3批包含体处理后所得到的蛋白量进行比较(表1)。结果表明,改进前后产量无明显差异。同时改进后3批RSD为3.9%较改进前的8.7%有着更好的稳定性和重现性。
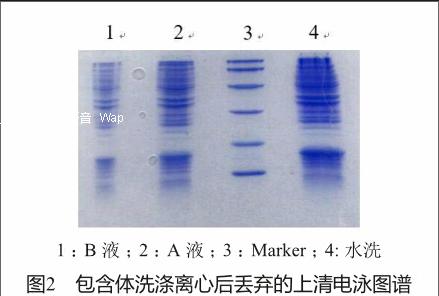
对采用改进工艺的F004处理时的纯化水、A液、B液丢弃上清取样,进行电泳检测(图2)。丢弃的上清中含有大量的杂质蛋白。对照rhG-CSF分子量为18.8 kD,在电泳的相应分子量位置未见有大量目标蛋白存在。经电泳图谱扫描,损失蛋白大约在10%以下,与原有工艺基本持平。
2.2 质量对比
2.2.1 纯度
包含体内除了含有目标蛋白外,还含有大量的宿主蛋白。利用包含体的不易溶解的特性,分别用不同的缓冲液来溶解大肠埃希氏菌本身的蛋白质,从而达到分离宿主蛋白的目的。图3是工艺改进前后各1批处理后获得变性蛋白的电泳图谱。工艺改进前后的图谱基本一致,改进后未见有新的杂蛋白产生。同时对电泳图谱进行扫描,图形基本一致(图4)。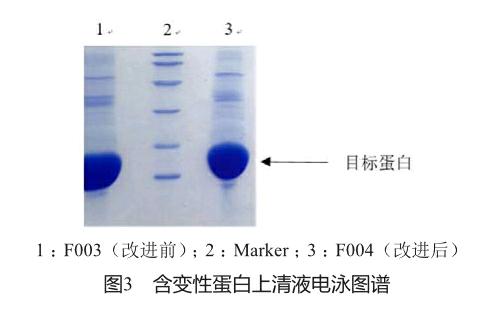
表3对工艺改进前后连续各3批变性蛋白的纯度进行了统计与比较。工艺改进后纯度均在80%以上,达到变性蛋白质量标准要求,并且RSD值为1.80%,说明改进工艺具有相当稳定的重现性。
2.2.2 内毒素
工程菌大肠埃希氏菌属革兰阴性菌,超声破壁后收集包含体时,裂解液中也含有大量的细菌内毒素,须尽可能地去除掉。经我们检测,未经处理的包含体,其细菌内毒素含量大于1 000万EU/ml。检测连续3批包含体处理后样品的内毒素含量,值均在100~1 000 EU/ml之间,达到要求。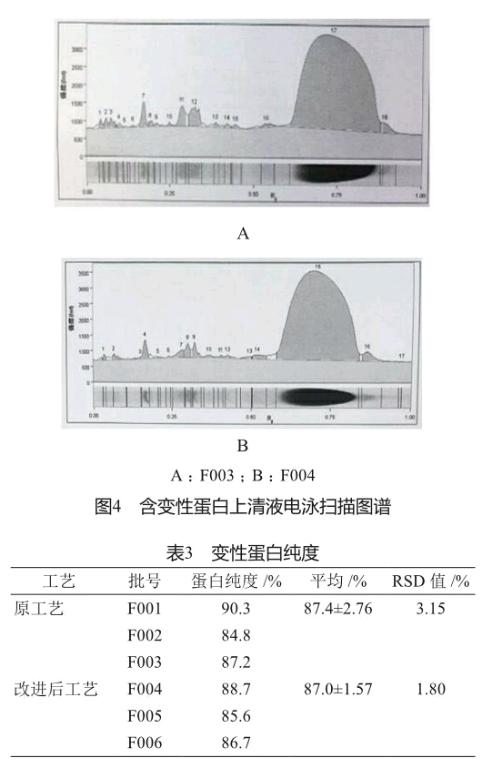
2.2.3 残余DNA
随着超声破碎,大肠埃希氏菌的宿主DNA也与包含体粘连在一起。由于微生物来源的基因组DNA富含CpG和非甲基化序列,故残余DNA增加了重组蛋白药物在体内的免疫源性风险[14-15],一直是国内外药品监管机构关注的重点。目前检测的方法为半定量法,通过样品与标准品颜色深浅的比较,来确定残余宿主DNA含量的范围。从图5可以看出,工艺改进前后2批次的样品F001和F004颜色深浅几乎一样,介于标准品100 ng和10 ng之间,满足变性蛋白质量标准中残余DNA≤100 ng/ml的要求。表4统计了连续3批工艺改进处理后最终样品的残余DNA含量,均小于100 ng/ml,达到要求。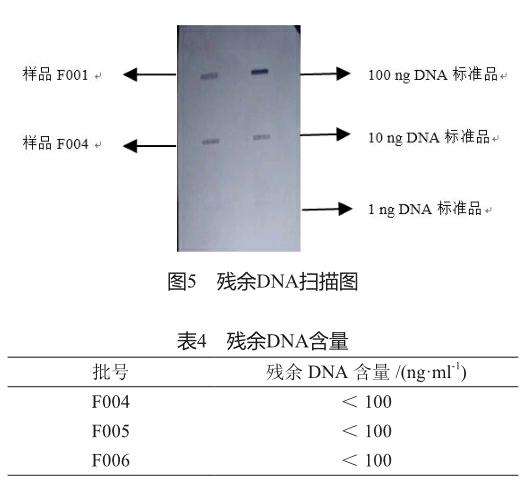
2.3 生产效率
用转子离心机处理一批高密度发酵所获得的包含体,必须分成4个亚批次进行处理。每个亚批次的时间为2个工作日,也就是处理完1批完整的包含体需要8个工作日。用管式离心代替转子离心机可以一次性處理完整的一批包含体,并且只需要2个工作日。生产效率提高了4倍。节约了6 d操作时间。劳动效率的提升,带来了生产成本的降低。1批发酵按照上海市人2017年人均工资计算,改进后节省人工成本1 740元,同时动力消耗也节省9 000元。
1批发酵获得的包含体通过处理,一般可以获得22 g蛋白。原工艺的人工和动力成本为14 320元,而改进后的成本为3 580元。获得的粗蛋白的成本从651元/g下降到163元/g,成本下降了75%。
3 讨论
从产量、蛋白纯度、内毒素和残余DNA几个方面对赛格力包含体洗涤改进工艺与原工艺进行了比较,改进工艺在产量和质量上与原工艺基本持平,具有相当好的稳定性和重现性,同时大大提高了劳动效率,降低了生产成本,表明改进工艺在实际生产上是可行的。
参考文献
[1] 李迎新. rhG-CSF粒细胞集落因子药理学研究[D]. 哈尔滨:哈尔滨医科大学, 1998.
[2] 张力, 李龙芸, 林宏英, 等. 重组人粒细胞集落刺激因子对肿瘤患者白细胞的影响[J]. 中国临床药学杂志, 2001, 10(4): 207-210.
[3] 候梅, 鄢希, 石晶, 等. 国产重组人粒细胞集落刺激因子Ⅱ期临床试验[J]. 中国新药杂志, 2001, 10(4): 279-281.
[4] 茅伟, 邱慧敏, 许德凤. 赛格力和惠尔血防治肿瘤化疗所致白细胞减少的观察[J]. 同济大学学报(医学版), 2001, 22(3): 89-90.
[5] Palmer I, Wingfield PT. Preparation and extraction of insoluble(inclusion body) proteins from Escherichia coli[J/ OL]. Curr Protoc Protein Sci, 2012 [2017-05-31]. https:// www.ncbi.nlm.nih.gov/pmc/articles/PMC3809847/.
[6] 宋爽, 蒋文宏, 蒋永平. 新一代重组人粒细胞集落刺激因子的工业化发酵、复性和纯化[J]. 中国生物医学工程学报, 2012, 31(4): 552-557.
[7] 张兵, 邹文艺, 戎隆富, 等. 重组人粒细胞集落刺激因子的表达、纯化以及PEG修饰[J]. 生物学杂志, 2008, 25(2): 36-39.
[8] 邝爱丽, 陈圆圆, 彭志峰, 等. 包涵体的形成原因及其处理方法[J]. 上海畜牧兽医通讯, 2009(1): 62-63.
[9] 高永贵, 关怡新, 姚善泾. 包涵体蛋白的变复性研究[J].科技通报, 2003, 19(1): 10-15.
[10] 张婷婷, 叶波平. 包涵体蛋白质的复性研究进展[J]. 药物生物技术, 2007, 14(4): 306-309.
[11] 罗惠霞, 李敏, 王玉炯. 包涵体蛋白复性的几种方法[J].生物技术通讯, 2007(5): 96-98.
[12] 高丽华. rhG-CSF基因工程菌高密度发酵的研究[D]. 上海:华东理工大学, 2011.
[13] 岑仡, 童涌,杨峰. 溶氧浓度对rhG-CSF工程菌高密度发酵的影响[J]. 药学实践杂志, 2011, 29(3): 197-199.
[14] 王兰, 王军志. 关于生物制品残余DNA质量控制问题[J].中国新药杂志, 2011, 20(8): 678-683.
[15] 张昀, 陈兴. 生物制剂中残余DNA的潜在危害性及其检测方法的研究進展[J]. 中国生物制品学杂志, 2014, 27(10): 1348-1353.

