一种检测水合肼荧光探针的合成与应用
张 琪,高 潮,梁焕如,侯 鹏
(齐齐哈尔医学院 药学院,黑龙江 齐齐哈尔 161006)
一种检测水合肼荧光探针的合成与应用
张 琪,高 潮,梁焕如,侯 鹏*
(齐齐哈尔医学院 药学院,黑龙江 齐齐哈尔 161006)
基于香豆素类染料,设计合成了一种具有较高选择性和灵敏度,可在生理条件(pH 7.4)下检测水合肼的荧光探针,同时利用核磁共振和高分辨质谱对探针的分子结构进行了表征。基于水合肼进攻探针分子结构中的4-丁酸酯,生成酚氧负离子,同时发生分子内环化反应后生成具有强烈荧光的亚胺香豆素,实现了探针分子对水合肼的检测。光谱学研究表明,当向探针溶液加入水合肼(0~100 μmol/L)后,探针溶液在绿色光谱区域(502 nm)呈现一个显著的荧光增强响应(增强至55倍)。并且,探针可以检测相对较低浓度的水合肼,检出限为1.7×10-7mol/L。此外,相对于其他阴离子和亲核试剂,探针对水合肼的识别显示出较高的选择性和灵敏度。探针成功实现了细胞内水合肼的荧光成像,证明其在细胞成像中具有潜在的应用能力。
荧光成像;合成;香豆素;荧光探针;水合肼
肼(NH2NH2)是无色易燃液体,具有较强的毒性且不稳定。临床研究表明,暴露的肼会对人类的肝脏、肾脏和中枢神经系统造成严重损伤[1]。为此,美国环境保护局(EPA)已将肼归类为可能的人类致癌物,其暴露的阈限值为10 ppb[2]。肼作为一种重要的精细化工原料,被广泛用于化学、制药、农业和航空航天工业等领域。据报道,一些固氮菌能够产生作为副产物的肼[3]。因此,开发用于快速、简单、灵敏和选择性检测肼的方法在环境和生物科学中非常重要。目前,检测肼的分析方法有分光光度法、色谱法和电化学方法等[4-6]。然而,这些方法需繁琐的样品和试剂制备过程,或需复杂仪器,因此不适于现场分析。相对于其它方法,荧光分析法操作简便、灵敏度高,适用于细胞内检测,已成为目前研究生物体内水合肼的理想方法[7-8]。
目前,关于水合肼探针的报道主要基于以下几种反应机理:水合肼将乙酰丙酸基团脱保护,水合肼对丙二腈基团的取代反应,水合肼将邻苯二甲酰亚胺脱保护以及水合肼将4-位的丁酰酯脱保护等。这些反应机理大大促进了肼的荧光探针的开发[9-15]。其中,水合肼将4-位的丁酰酯脱保护,由于合成简便而被广泛采用。但是,基于该机理的绝大多数探针需使用高含量的有机溶剂,有的甚至超过90%,这极大地限制了其在实际检测中的灵敏度和选择性,并且不适于细胞内成像。因此,开发具有高灵敏度、高选择性以及能用于细胞成像的水合肼探针具有重要意义。
香豆素类染料又名1,2-苯并吡喃酮,是一类具有芳香气味的荧光染料。由于香豆素类荧光染料分子具有高度的刚性和优良的光物理化学性能(较大的Stokes位移、较高的荧光量子产率以及发射光谱位移蓝绿色区域),被广泛应用于非线性光学材料、增白剂和荧光分析领域[16]。本文合成了以香豆素染料为信号表达基团,4-丁酰酯部分作为潜在反应位点的选择性水合肼荧光探针,并将其用于细胞内水合肼的荧光成像检测。在缓冲溶液中,由于探针分子1结构的自由度较大,能量会通过非辐射方式消耗,因此探针分子1几乎不产生荧光。当加入水合肼后,水合肼进攻探针分子中的4-丁酰酯,生成酚氧负离子,同时发生分子内环化反应,生成具有强烈绿色荧光的亚胺香豆素2(图1)。本文利用水合肼和探针1反应前后荧光强度的变化,建立了一种荧光增强识别水合肼的分析方法。
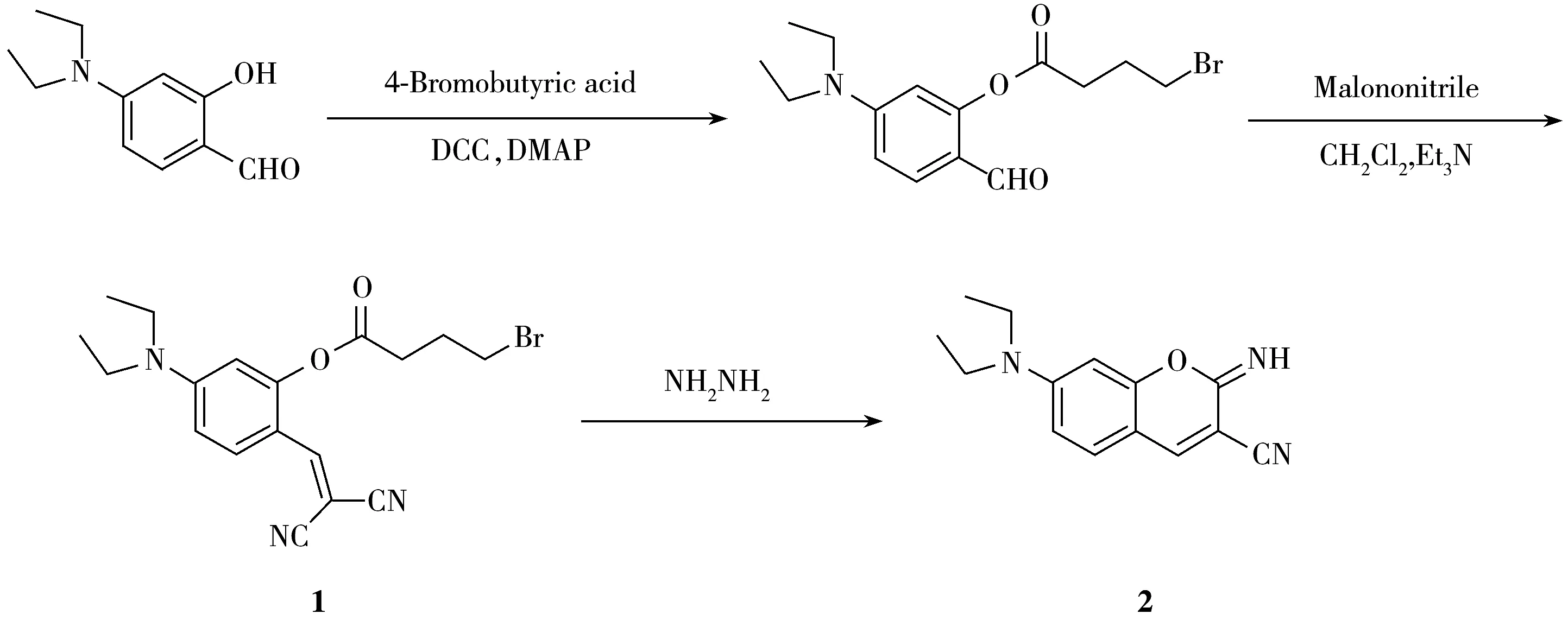
图1 探针1的合成及水合肼可能的识别机理Fig.1 Synthesis of probe 1 for hydrazine and possible hydrazine-selective signaling mechanism
1 实验部分
1.1 试剂与仪器
4-溴丁酸(TCI化学试剂有限公司),7-二烷基水杨醛(安耐吉化学试剂有限公司),丙二腈(玛雅化学试剂),石油醚、乙酸乙酯(天津市东丽区天大化学试剂厂),二氯甲烷(天津市凯通化学试剂有限公司),测试所用离子均购于上海国药试剂有限公司。
Bruker ultraflexⅡ基质辅助时间飞行质谱、Bruker AV400 光谱仪(美国Bruker公司),F4600-荧光分光光度计(日本日立公司),荧光倒置显微镜(日本Nikon Eclipse TE300)。
1.2 探针1的合成与表征
氩气保护下,将7-二乙胺基水杨醛(97 mg,0.5 mmol)、4-溴丁酸(125 mg,0.75 mmol)、DMAP(4-二甲氨基吡啶,37 mg,0.3 mmol)和 DCC(二环己基碳二亚胺,155 mg,0.75 mmol)溶于30 mL无水二氯甲烷中,将反应液加热至回流,反应4 h。反应完成后,旋去溶剂直接用于下一步反应。将上一步所得化合物溶于8 mL二氯甲烷中,加入丙二腈28.3 mg和三乙胺15 mg,室温搅拌5 h。反应结束后,将反应液倒入水中,二氯甲烷萃取,无水硫酸钠干燥,柱层析分离(石油醚-二氯甲烷=3∶1)得到产品(收率 56%),即为探针分子1。1H NMR(400 MHz,DMSO)δ8.17(d,J=9.3 Hz,1H),7.98(s,1H),6.85(d,J=9.3 Hz,1H),6.62(d,J=1.7 Hz,1H),3.65(t,J=6.5 Hz,2H),3.48 (q,J=6.8 Hz,4H),2.88(t,J=7.3 Hz,2H),2.27-2.04(m,2H),1.13(t,J=6.9 Hz,6H);HRMS(EI)m/zcalcd for[C18H20BrN3O2+H]+:390.080 9,Found:390.081 6。
1.3 光谱测试
称取适量的探针分子1经无水乙腈溶解,于容量瓶定容,配成1.0×10-3mol/L 的探针母液,低温保存备用。称取适量待测离子盐和中性小分子(NaCl,KCl,CaCl2,MgCl2,ZnCl2,AlCl3,NaF,NaI,NaBr,NaAcO,Cys,GSH,尿素,苯胺,羟胺,乙二胺和乙酰肼)溶于蒸馏水中,配成1.0×10-3mol/L的溶液,低温保存备用。测试体系的配制:用移液枪量取0.003 mL 上述探针的母液、1.8 mL PBS缓冲液(20.0 mmol/L,pH 7.4)、0.897 mL无水乙腈和 0.3 mL 各检测物质于比色皿中,充分混合均匀后,在室温下测试。
1.4 细胞培养与成像
将人乳腺癌231细胞接种于十二孔板中,加入含10% 胎牛血清的DMEM培养液中,置于培养箱中在37 ℃,5% CO2的条件下培养24 h。待细胞贴壁后,换液,用PBS缓冲液洗涤3次,然后加入探针溶液(5 μmol/L)继续培养 30 min。成像前再用PBS缓冲液洗涤3次,用荧光倒置显微镜成像。
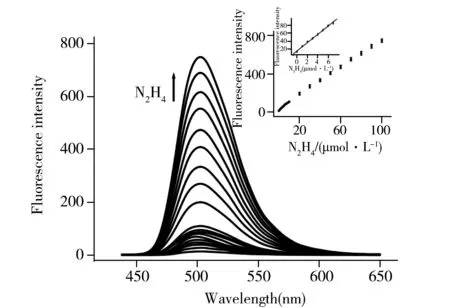
图2 探针1与不同浓度N2H4反应的荧光响应及探针1和N2H4反应的荧光强度与浓度的线性关系Fig.2 Fluorescence spectra of probe 1(10 μmol/L) reacted with different concentrations of N2H4concentration of N2H4 (from bottom to top):0-100 μmol/L;inset:linear relationship of fluorescence intensity of probe 1 with gradual addition of N2H4
2 结果与讨论
2.1 荧光光谱研究
在含有30%乙腈探针1的PBS缓冲溶液(pH 7.4)中加入水合肼,水合肼可以诱导丁酰酯基脱去保护,同时发生环化反应,从而释放出染料2使其荧光增强。如图2所示,随着加入水合肼浓度的增大,探针在502 nm处的荧光发射峰不断增强,最高可增强为探针本底荧光的55倍。同时,在紫外灯的照射下,加入100 μmol/L水合肼的探针溶液会呈现出强烈的绿色荧光。值得注意的是,探针1对水合肼的响应非常灵敏,即使向探针1溶液中加入1 μmol/L水合肼溶液也会引起探针溶液超过2倍的荧光增强。此外,当加入水合肼的浓度为1,2,3,4,5,6,7 μmol/L时,水合肼的浓度x和探针1在502 nm处的荧光强度y之间存在着很好的线性关系(y=16.316+10.347x),相关系数为0.995 2(图2插图),检出限(S/N=3)为1.7×10-7mol/L。美国环境保护局(EPA)将肼的暴露阈限值设定为10 ppb,因此,探针1的灵敏度符合实际应用中水合肼检测的定量要求。
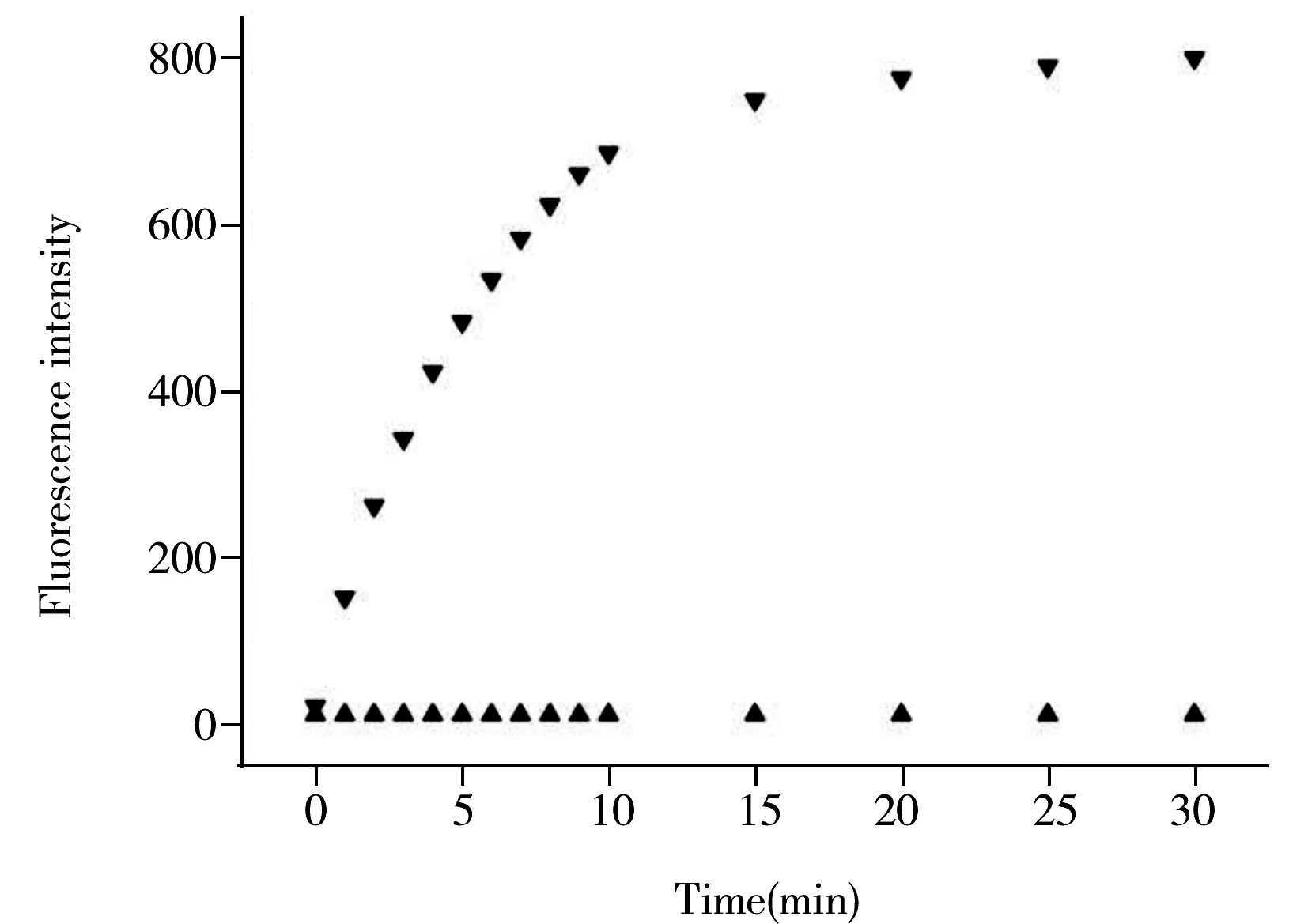
图3 探针1(▲)及探针1与N2H4(▼)反应的荧光强度随时间变化情况Fig.3 Time-depent fluorescence intensity of probe 1(▲) and probe 1 with N2H4(▼)
2.2 选择性与干扰实验
性能优良的荧光探针应具有良好的选择性和抗干扰能力。为了评价探针1的选择性能,本文测试了探针1对常见阴、阳离子和生物小分子的荧光响应情况。结果显示,在探针溶液中加入常见的阴、阳离子和生物小分子(如Na+,K+,Ca2+,Mg2+,Zn2+,Al3+,F-,Cl-,I-,Br-,AcO-,Cys,GSH)后,荧光光谱未呈现明显的荧光响应信号(F/F0=0.96~1.08)。同时,向探针分子1的溶液中加入高浓度的亲核试剂(尿素,苯胺,羟胺,乙二胺和乙酰肼(100.0 μmol/L),光谱数据显示,加入的亲核试剂未引起探针溶液的荧光发生显著增强(F/F0=0.97~1.04)。由此证明,探针1对水合肼具有很好的选择性。为进一步评估探针1对水合肼的高度选择性,在Na+,K+,Ca2+,Mg2+,Zn2+,Al3+,F-,Cl-,I-,Br-,AcO-,Cys,GSH存在的条件下进行干扰性试验。结果表明,其他测试物均不影响探针1对水合肼的检测(F1+N2H4+other analyte/F1+N2H4=0.94~1.07)。以上研究表明,探针1在生理pH值下对水合肼显示了极高的选择性,并能够有效抵抗其他阴离子和亲核试剂的干扰。
2.3 反应时间
本文对探针1与水合肼的反应动力学进行了研究。如图3所示,在整个测试时间内,单独的探针1溶液在502 nm处的荧光强度无明显变化(F=13.62~14.83),说明探针1在测试体系中具有很好的稳定性。然而,加入100 μmol/L水合肼之后,探针1溶液在502 nm处的荧光强度发生显著变化,随着反应时间的延长,荧光强度不断增大,反应进行到20 min时,荧光强度基本恒定。以上研究表明,探针1具有较好的稳定性并且可以快速识别测试体系中的水合肼。

图4 细胞成像实验Fig.4 Experiment of cell imagingA.bright field image of 231cells pretreated with N2H4,followed by incubation with probe 1(231细胞预先加入N2H4培养后,再加入探针1培养的明场成像);B.fluorescence image of 231cells pretreated with N2H4,followed by incubation with probe 1(231细胞预先加入N2H4培养后,再加入探针1培养的荧光成像);C.bright field image of 231cells incubated with probe 1(231细胞加入探针1的明场成像);D.fluorescence image of 231cells incubated with probe 1(31细胞加入探针1的荧光成像)
2.4 荧光成像
肼作为一种神经毒素,容易通过皮肤接触或呼吸吸入,从而损害人体的脏器及中枢神经系统。为了实现探针对细胞内水合肼的检测,选取人乳腺癌231细胞进行荧光成像实验。将细胞预先加入50 μmol/L 水合肼培养30 min后,再加入5 μmol/L探针1培养30 min,置于荧光倒置显微镜下,首先在明场下,照射细胞,细胞形态良好(图4A),再调至荧光场下,此时细胞呈现非常强烈的绿色荧光(图4B)。将探针1直接加入到载有细胞的培养皿内作为对照试验,培养30 min后,置于明场下,观察细胞状态良好(图4C),再置于荧光场下成像,观察到细胞仅呈现出较微弱的绿色荧光(图4D)。以上实验证明探针1不仅具有较好的细胞穿透能力,而且能够实现对细胞内的水合肼进行荧光成像。
3 结 论
本文利用4-丁酸酯作为识别基团成功地开发了一种具有较好光稳定性,发射波长处于绿光区域的新型水合肼荧光探针。该探针对水合肼的响应非常灵敏,其检出限低至1.7×10-7mol/L,同时具有较高的选择性,能够高选择性地对水合肼进行响应而不受阴、阳离子和亲核试剂的干扰。此外,该探针还具有很好的细胞穿透能力,能够对细胞内的水合肼进行荧光成像,通过细胞内的原位荧光成像,为监测环境及体内水合肼的存在和含量提供了便捷的检测手段。
[1] Garrod S,Bollard M E,Nicholls A W,Connor S C,Gonnelly J,Nicholson J K,Holmes E.Chem.Res.Toxicol.,2005,18:115-122.
[2] Chen S,Hou P,Wang J,Liu L,Zhang Q.Spectrochim.ActaA,2017,173:170-174.
[3] Liu B,Liu Q,Shah M,Wang J F,Zhang G,Pang Y.Sens.ActuatorsB,2014,202:194-200.
[4] Batchelor-McAuley C,Banks C E,Simm A O,Jones T G J,Compton R G.Analyst,2006,131:106-110.
[5] Elder D P,Snodin D,Teasdale A.J.Pharm.Biomed.Anal.,2011,54:900-910.
[6] Qu D Y,Chen J L,Di B.Anal.Methods,2014,6:4705-4709.
[7] Chen S,Wang J,Hou P,Liu L,Wang X.J.Instrum.Anal.(陈颂,王静,侯鹏,刘磊,王鑫.分析测试学报),2016,25(8):1046-1049.
[8] Yuan X Y,Wang T L,Guan T T,Wang J L,Huang H W,Yi S J,Tang C R,Zeng Y L.J.Instrum.Anal.(元晓云,王天伦,关婷婷,王金龙,黄昊文,易守军,唐春然,曾云龙.分析测试学报),2015,34(4):463-467.[9] Xiao L L,Tu J,Sun S Q,Pei Z C,Pei Y X,Pang Y,Xu Y Q.RSCAdv.,2014,4:41807-41811.
[10] Zhou J,Shi R Y,Liu J X,Wang R,Xu Y F,Qian X H.Org.Biomol.Chem.,2015,13:5344-5348.
[11] Yu S L,Wang S X,Yu H Z,Feng Y,Zhang S T,Zhu M Z,Yin H,Meng X M.Sens.ActuatorsB,2015,220:1338-1345.
[12] Reja S I,Gupta N,Bhalla V,Kaur D,Arora S,Kumar M.Sens.ActuatorsB,2016,222:923-929.
[13] Cui L,Ji C F,Peng Z X,Zhong L,Zhou C H,Yan L L,Qu S,Zhang S P,Huang C S,Qian X H,Xu Y F.Anal.Chem.,2014,86:4611-4617.
[14] Xiao Y H,Xi G,Zhao X X,Zhou S,Zhou Z Q,Zhao B X.J.Fluoresc.,2015,25:1023-1029.
[15] Zhou D Y,Wang Y Y,Jia J,Yu W Z,Qu B F,Li X,Sun X.Chem.Commun.,2015,51:10656-10659.
[16] Lee D N,Kim G J,Kim H J.TetrahedronLett.,2009,50(33):4766-4768.
Synthesis and Application of a Fluorescent Probe for Hydrazine Determination
ZHANG Qi,GAO Chao,LIANG Huan-ru,HOU Peng*
(College of Pharmacy,Qiqihar Medical University,Qiqihar 161006,China)
A fluorescent probe with high selectivity and sensitivity was synthesized for hydrazine determination in physioligical condition(pH 7.4) based on coumarin dyes.Structure of the probe was characterized by nuclear magnetic resonnce and high resolution mass spectrometry.A strong fluorescence imine coumarin was generated by using hydrazine attacking 4-butyrate to release phenolic oxygen anion and produce molecular inner reaction.With the addition of hydrazine(0-100 μmol/L),the fluorescence intensity of the probe displayed a remarked enhancement(55 fold) in green spectral region(502 nm).The probe could be used to detect low concentration of hydrazine,with a detection limit of 1.7×10-7mol/L.Compared with the other anions and nuclear reagents,this probe showed higher selectivity and sensitivity to recognize hydrazine.More importantly,the probe was successfully implemented to detect hydrazine in living cells,which proved that the hydrazine fluorescent probe has a potential capability in cell imaging.
fluorescence imaging;synthesis;coumarin;fluorescence probe;hydrazine
2017-02-24;
2017-03-29
黑龙江省大学生创新创业训练计划项目(201611230068)
10.3969/j.issn.1004-4957.2017.07.019
O657.3;O623.752
A
1004-4957(2017)07-0937-04
*通讯作者:侯 鹏,博士,研究方向:有机小分子荧光探针的光学性能研究,Tel:0452-2663152,E-mail:houpeng1982@163.com

