纳米Fe2O3修饰涂碳型硫酸沙丁胺醇选择电极的研制与应用
张 静,窦 月,岳京立
(锦州医科大学 药学院,辽宁 锦州 121000)
纳米Fe2O3修饰涂碳型硫酸沙丁胺醇选择电极的研制与应用
张 静,窦 月,岳京立*
(锦州医科大学 药学院,辽宁 锦州 121000)
制备了以纳米Fe2O3为修饰剂的涂碳型硫酸沙丁胺醇选择电极,采用电位分析方法对其各项性能进行测定。结果表明,该纳米Fe2O3修饰电极有很好的能斯特响应,其线性范围为1.0×10-6~ 0.1 mol/L,级差电位为59 mV/pC,与普通电极相比,响应时间较短(10 s),检出限更低(2.8×10-7mol/L)。将修饰电极应用于猪肉样品中硫酸沙丁胺醇含量的测定,结果与标准方法结果相符。
纳米Fe2O3;硫酸沙丁胺醇;测定;电极;猪肉
硫酸沙丁胺醇属于β2肾上腺素受体激动剂,临床上具有扩张支气管作用,用于治疗支气管哮喘等疾病。当其用量超过推荐治疗剂量的5~10倍时,即可促进动物生长,刺激体内蛋白质合成,使脂肪分解代谢增强,增加猪瘦肉比例[1]。硫酸沙丁胺醇在现代猪肉养殖中被用作饲料添加剂,以提高猪的瘦肉产量,进而在动物组织和肌肉中有不同程度的残留。人类食用含有该药物残留的动物源性食品会产生潜在的危害,如中枢神经疾病、心血管疾病以及心脏疾病,甚至可能出现急性食用后死亡[2]。因此,动物性食品中硫酸沙丁胺醇残留的检测成为一项重要任务。目前,对硫酸沙丁胺醇的检测方法主要有高效液相色谱法[3]、液相色谱-质谱联用法[4]、气相色谱-质谱联用法[5]以及酶联免疫法[6]。但以上检测方法存在仪器昂贵,操作繁琐,成本较高等局限性。而电化学分析方法因具有操作简单、价格低廉和携带方便等优点在生物医学和分析化学领域[7-9]有着广阔的前景。
近年来,纳米材料因其比表面积较大、化学反应活性高、吸附能力强等独特的理化特性,引起越来越多的关注[10-12]。其中,纳米Fe2O3是一种性能优良的新型材料,因具有化学性质稳定,催化活性高,耐光性良好等特性,在生物医药、催化和分析领域中得到广泛应用[13-14]。而其作为修饰剂制备电极以改善电极的电化学性能,已成为电化学分析研究领域中引人瞩目的前沿问题[15-16]。
本文以纳米Fe2O3为修饰剂制备了涂碳型硫酸沙丁胺醇选择电极,建立了电位分析方法对猪肉样品中硫酸沙丁胺醇的含量进行测定,结果与标准方法[17]相符。纳米Fe2O3的修饰提高了电极的检测范围,降低了检出限,为电化学方法测定猪肉样品中硫酸沙丁胺醇的含量提供了参考。
1 实验部分
1.1 仪器与试剂
KH-100SP型双频数控超声波清洗器(昆山禾创超声仪器有限公司);雷磁PHS-25型pH计、PHS-10C数字酸度/离子计(上海精密科学仪器有限公司)。硫酸沙丁胺醇(纯度99.9%)、FeCl3·6H2O均购于上海晶纯生化科技股份有限公司;邻苯二甲酸二丁酯(分析纯,天津市光复精细化工研究所);所用试剂均为分析纯,实验用水为去离子水。
1.2 实验方法
1.2.1 纳米Fe2O3的制备 按照文献[18]制备Fe2O3纳米颗粒:配制一定浓度的FeCl3·6H2O溶液,缓慢加入0.1 mol/L的KOH溶液,调至pH 13.0,得到红褐色的Fe(OH)3,将该悬浮液转移至高压釜中,于180 ℃下高压12 h后,得到的沉淀物用水和乙醇洗涤数次,干燥后得到纳米Fe2O3。
1.2.2 电活性物的制备 称取硫酸沙丁胺醇适量,加水溶解,配成50 mL 0.01 mol/L的硫酸沙丁胺醇溶液,将此溶液缓慢加入0.01 mol/L四苯硼钠溶液中,并不断搅拌,即生成白色沉淀。待沉淀完全,静置1 h后,用3号砂芯漏斗抽滤,将沉淀置于烘箱中50 ℃恒温烘干,得到硫酸沙丁胺醇-四苯硼钠电活性物质。
1.2.3 纳米Fe2O3修饰电极的制备 分别称取纳米Fe2O32.5 mg和电活性物5 mg,混合均匀后,加入200 mg聚氯乙烯粉、5 mL四氢呋喃和0.6 mL邻苯二甲酸二丁酯,超声溶解至溶液均匀透明。将此溶液均匀涂于预先处理好的碳电极表面,待挥发干燥后重复涂3~4次,放入干燥箱中干燥2 d,即得纳米Fe2O3修饰涂碳型硫酸沙丁胺醇选择电极。按上述方法不加入纳米Fe2O3即制得普通涂碳型硫酸沙丁胺醇电极。
1.2.4 电位分析法的建立 将纳米Fe2O3修饰涂碳型硫酸沙丁胺醇选择电极和普通电极分别与饱和甘汞电极(SCE)组成电池:纳米Fe2O3修饰涂碳型硫酸沙丁胺醇选择电极|硫酸沙丁胺醇待测液SCE,普通电极|硫酸沙丁胺醇待测液SCE,并分别测定硫酸沙丁胺醇溶液的电位值。
2 结果与讨论
2.1 纳米Fe2O3的表征
图1A为纳米Fe2O3的扫描电子显微镜图(SEM),图1B为纳米Fe2O3的X射线衍射图(XRD),由图可见,制备的纳米Fe2O3粒径大小均匀,颗粒较小约为50 nm,且纳米Fe2O3的主要衍射峰与参考文献[18]一致,表明实验制得的Fe2O3纯度较高。

2.2 纳米Fe2O3修饰电极的电化学行为研究
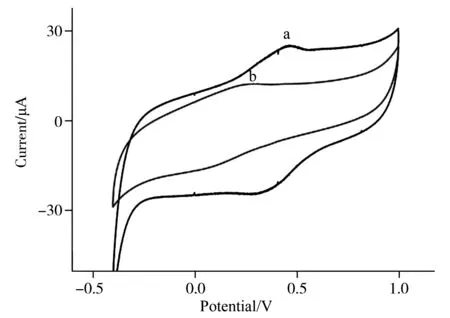
图2 纳米Fe2O3修饰电极(a)和普通电极(b)的循环伏安图 Fig.2 Cyclic voltammograms of nano-Fe2O3 modified electrode(a) and unmodified electrode(b) c(salbutamol sulfate):1.0×10-3 mol/L ; scan rate:100 mV/s

图3 纳米Fe2O3修饰电极(a)和普通电极(b)的响应曲线 Fig.3 Response curves of nano-Fe2O3 modified electrode (a) and unmodified electrode(b)
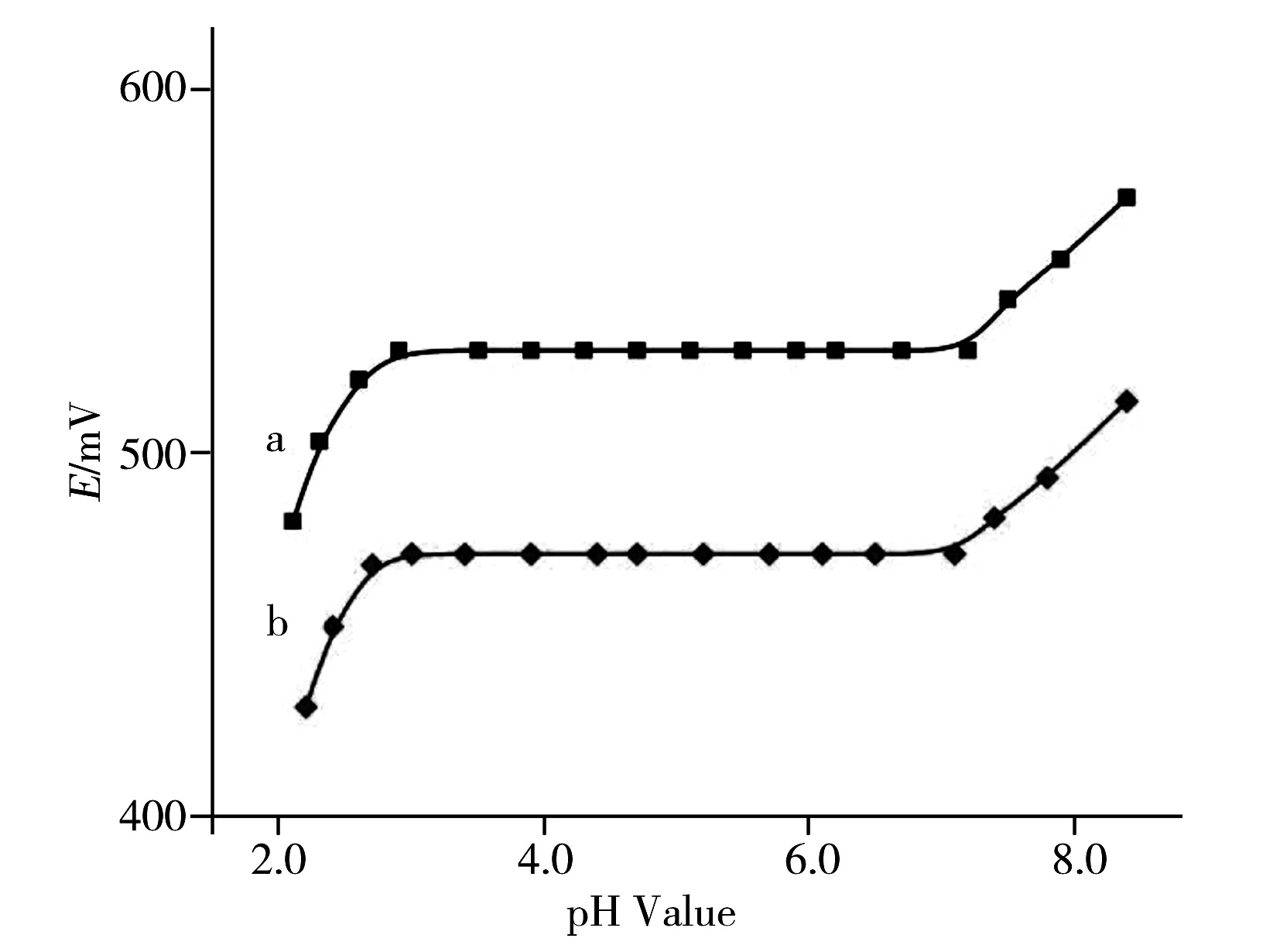
图4 pH值对电极的影响Fig.4 Effect of pH value on the modified electrode
采用循环伏安法对电极的电化学行为进行研究,图2为纳米Fe2O3修饰电极(曲线a)和普通电极(曲线b)在1.0×10-3mol/L硫酸沙丁胺醇溶液中的循环伏安图。由图可见,在0.4~1.0 V电位扫描范围内,与普通电极相比,纳米Fe2O3修饰电极的氧化还原峰电流明显增强。这可能因为采用纳米Fe2O3作为修饰剂,增加了电极的比表面积,提高了电极表面的电子转移速率,从而增强了电极在硫酸沙丁胺醇溶液中的响应。
2.3 响应曲线与检出限
离子选择电极的响应范围是标准曲线的线性部分,在线性响应范围内,离子选择电极符合能斯特响应方程。按试验方法测定系列浓度的硫酸沙丁胺醇标准溶液的电位,以电位(E)为纵坐标,相应溶液浓度的负对数(pC)为横坐标作图。分别采用纳米Fe2O3修饰涂碳型电极和普通电极测定系列浓度的硫酸沙丁胺醇溶液(1.0×10-8~0.1 mol/L)的响应曲线(图3)。由图可知,纳米Fe2O3修饰电极(曲线a)的线性响应范围为1.0×10-6~0.1 mol/L,其线性方程为E=-58.7pC+707.9,相关系数为0.999 6,级差电位为59 mV/pC,根据IUPAC推荐的方法,计算检出限为2.8×10-7mol/L。而普通电极(曲线b)在1.0×10-5~1.0×10-2mol/L范围内呈线性响应,线性方程为E=-31.8pC+587.3,相关系数为0.999 4,级差电位为32 mV/pC,检出限为1.9×10-6mol/L。此结果表明,纳米Fe2O3修饰电极比普通电极的检测范围更宽,检出限更低。这可能是因为Fe2O3纳米颗粒修饰于电极表面后,使得电极的比表面积增加,具有较高的比表面能,增加了电极表面反应活性,使得级差电位增大,线性响应范围增加。
2.4 pH值的影响
实验考察了pH值对测定的影响,用0.1 mol/L的HCl和NaOH溶液调节HAc-NaAc缓冲溶液的pH值,并用纳米Fe2O3修饰电极分别测定1.0×10-3mol/L和1.0×10-4mol/L的硫酸沙丁胺醇溶液的电位值,电位与pH值的关系曲线见图4。从图4可知,电极对不同浓度的硫酸沙丁胺醇溶液的测定结果相差不大,pH值在3.0 ~ 7.1范围内,电极电位基本不变。因此,实验选择pH 5.0的HAc-NaAc缓冲溶液控制pH值。
2.5 电极的响应时间与使用寿命
电极的响应时间是离子选择电极的一个重要性能,是指工作电极和参比电极同时浸入待测溶液中,到电极电位变为稳定数值的某一瞬时所经过的时间。本实验中,纳米Fe2O3修饰电极的响应时间为10 s,普通电极的响应时间为30 s。因此纳米Fe2O3修饰电极比普通电极响应迅速。电极每次使用后,用去离子水洗至电极电位保持稳定,并保存于遮光干燥箱中,电极的使用寿命大约为3个月,此后电极的性能略有下降,其检出限略有升高。表1为纳米Fe2O3修饰电极和普通电极的使用寿命对比,结果表明,纳米Fe2O3修饰电极和普通电极在正常使用约3个月后,其检出限均增大。
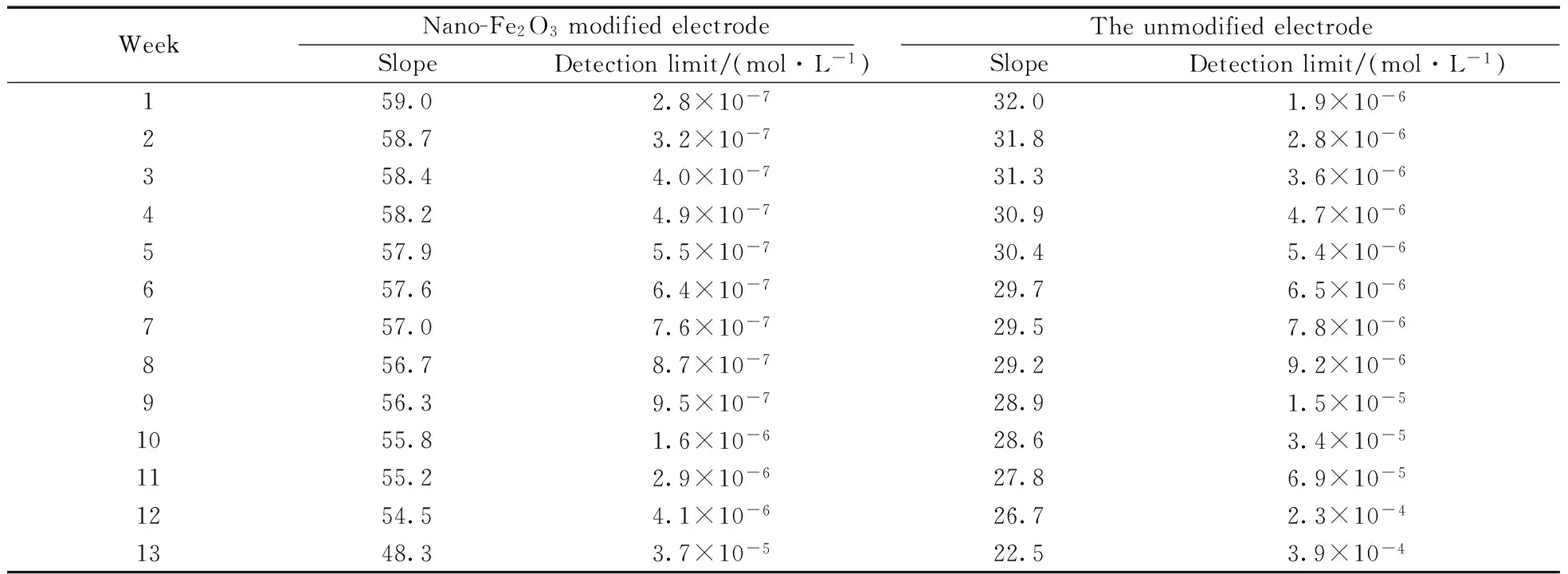
表1 电极的使用寿命Table 1 The life-time of the electrode
2.6 干扰试验
考察了一些常见的阴阳离子对硫酸沙丁胺醇溶液测定的影响,分别测定了Cu2+,Cd2+,NH4+,Zn2+,Cl-,Ca2+,Fe3+,K+,Na+,I-,Fe2+,Mg2+,Al3+,SO42-,CH3COO-,NO3-等离子的选择性系数。结果表明,上述离子的选择性系数均较小,对测定基本无影响。同时测定了其他β-受体激动剂(如盐酸克伦特罗、盐酸莱克多巴胺、盐酸多巴胺和盐酸氯丙那林)的选择性系数,其值分别为1.86×10-4,2.47×10-4,5.48×10-3和6.79×10-4,表明以上β-受体激动剂均不干扰硫酸沙丁胺醇的测定。
2.7 电极的稳定性与重现性
将修饰电极置于1.0×10-3mol/L硫酸沙丁胺醇溶液中,每隔2 h测定其电位,连续测定12 h,结果显示电位值无明显变化,表明该电极的稳定性良好。同时反复5次测定1.0×10-4mol/L硫酸沙丁胺醇溶液的电位,其相对标准偏差(RSD)为2.8%,表明电极具有良好的重现性。
2.8 回收率试验
配制一定浓度的硫酸沙丁胺醇溶液,按实验方法对其进行测定分析,做加标回收实验,测定结果如表2所示。数据表明,采用纳米Fe2O3修饰的硫酸沙丁胺醇电极测定时的回收率为96.8%~102.6%。

表2 回收率的测定Table 2 Determination of the recovery
2.9 实际样品分析
取市售新鲜猪肉适量,对其进行处理,并用标准方法[17]测定,未检出硫酸沙丁胺醇。分别移取上述处理后所得溶液3份,加入硫酸沙丁胺醇标准品后,用本方法和标准方法分别进行测定,每个样品测定5次,结果见表3。由以下数据可知,本方法与标准方法之间无显著性差异。
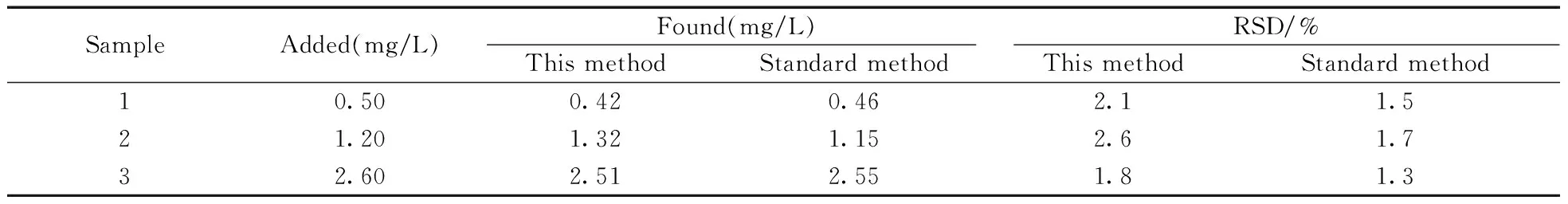
表3 猪肉样品中硫酸沙丁胺醇的测定结果(n=5)Table 3 Determination results of salbutamol sulfate in pork sample(n=5)
3 结 论
本文制备了Fe2O3纳米颗粒,并以其为修饰剂制备涂碳型硫酸沙丁胺醇选择电极,建立了测定硫酸沙丁胺醇含量的电位分析方法。与普通电极相比,纳米Fe2O3修饰电极的响应时间较短,检出限更低,对硫酸沙丁胺醇的测定不受其他干扰物质的影响。将建立的方法应用于猪肉样品中硫酸沙丁胺醇的测定,结果与标准方法相符。该方法检测快捷方便,结果准确,研究结果可为猪肉组织中硫酸沙丁胺醇的电化学分析提供参考。
[1] Carter W J,Lynch M E.Metabolism,1994,43(9): 1119-1125.
[2] Liu X B,Pang Y F,Hou Y Z,Cai H X,Li B B,Ren S J.ShanghaiJ.AnimalHusbandryVeter.Med.(刘宣兵,庞玉芳,侯玉泽,彩鸿翔,李彬彬,任守金.上海畜牧兽医通讯),2008,(4):83-85.
[3] Vichapong J,Burakham R,Srijaranai S.Anal.Lett.,2016,49(2): 208-216.
[4] Shi A.J.Instrum.Anal.(石奥.分析测试学报),2016,35(1): 74-78.
[5] Tian M.J.Instrum.Anal.(田苗.分析测试学报),2010,29(7): 712-716.
[6] Sheu S Y,Lei Y C,Tai Y T,Chang T H,Kuo T F.Anal.Chim.Acta,2009,654(2): 148-153.
[7] Zhou Y L,Zhang H Q,Chang Z,Ye B X,Xu M.Int.J.Electrochem.Sci.,2016,11(6):5154-5164.
[8] Sun K,Sun D M.Chin.J.Anal.Chem.(孙凯,孙登明.分析化学),2014,42(7): 991-996.
[9] Hajiaghababaei L,Abutalebyar B,Darvich M R,Shekoftefar S.Sens.Lett.,2013,11(12): 2315-2321.
[10] Wang S H,Niu H Y,Cai Y Q.J.Instrum.Anal.(王赛花,牛红云,蔡亚岐.分析测试学报),2015,34(2): 127-133.
[11] Johnston H,Brown D,Kermanizadeh A,Gubbins E,Stone V.J.ControlledRelease,2012,164(3): 307-313.
[12] Mu M,Zhang Y T,Qi G C,Liu Z Y.J.Instrum.Anal.(慕苗,张琰图,齐广才,刘珍叶.分析测试学报),2015,34(8): 958-961.
[13] Fan G,Wang Y,Hu M,Luo Z Y,Zhang K H,Li G.Sensors,2012,12(4): 4594-4604.
[14] Liu G Y.Chem.Res.Appl.(刘广友.化学研究与应用),2014,26(11): 1746-1750.
[15] Zhu X,Song X Y,Ma X L,Ning G Q.ACS.Appl.Mater.Int.,2014,6(10): 7189-7197.
[16] Liu F,Guo Z H,Zheng X W.FoodSci.(刘芳,郭志慧,郑行望.食品科学),2011,32(6): 311-313.
[17] GB/T 22286-2008.Determination ofβ-Agonists Residues in Foodstuff of Animal Origin-Liquid Chromatography with Tandem-Mass Spectrometric Method.National Standards of the People′s Republic of China(动物源性食品中多种β-受体激动剂残留量的测定 液相色谱-串联质谱法.中华人民共和国国家标准).
[18] Bazrafshan H,Tesieh Z A,Dabirnia S,Touba R S,Manghabati H,Nasernejad B.PowderTechnol.,2017,308: 266-272.
Preparation and Application of Carbon Coated Polyvinyl Chloride Membrane Salbutamol Sulfate Selective Electrode Modified with Nano-Fe2O3
ZHANG Jing,DOU Yue,YUE Jing-li*
(College of Pharmacy,Jinzhou Medical University,Jinzhou 121000,China)
A potentiometric method was developed for the determination of salbutamol sulfate by using a novel carbon coated polyvinyl chloride membrane salbutamol sulfate selective electrode modified with nano-Fe2O3.The prepared electrode showed a good Nernst response in the linear range of 1.0×10-6-0.1 mol/L with a slope of 59 mV/pC.Compared to the unmodified electrode,the electrode modified with nano-Fe2O3exhibited a faster response time(10 s) and a lower detection limit(2.8×10-7mol/L).The modified electrode was applied in the determination of salbutamol sulfate in pork samples, and the results were in agreement with those obtained by the standard method.
nano-Fe2O3; salbutamol sulfate; determination; electrode; pork
2017-02-17;
2017-04-18
辽宁省大学生科技创新项目(201510160000059);锦州医科大学大学生科技创新项目(2014D17)
10.3969/j.issn.1004-4957.2017.07.008
O657.1; TQ460.72
A
1004-4957(2017)07-0887-05
*通讯作者:岳京立,博士,教授,研究方向:电化学分析,Tel: 0416-4673404,E-mail:huaxue618@163.com
研究简报

