天芪降糖胶囊联合二甲双胍治疗老年2型糖尿病伴脑微血管病变的临床观察
柴 红,路一芳,肖红珍,李 颖,崔 坤,张援月#(.唐山市工人医院内分泌科,河北唐山 06000;.唐山市工人医院危重症内科,河北唐山 06000;.唐山市工人医院呼吸危重症内科,河北唐山 06000)
天芪降糖胶囊联合二甲双胍治疗老年2型糖尿病伴脑微血管病变的临床观察
柴 红1*,路一芳1,肖红珍1,李 颖2,崔 坤3,张援月2#(1.唐山市工人医院内分泌科,河北唐山 063000;2.唐山市工人医院危重症内科,河北唐山 063000;3.唐山市工人医院呼吸危重症内科,河北唐山 063000)
目的:观察天芪降糖胶囊联合二甲双胍治疗老年2型糖尿病伴脑微血管病变的疗效和安全性。方法:96例老年2型糖尿病伴脑微血管病变患者随机分为对照组(48例)和观察组(48例)。对照组患者给予盐酸二甲双胍片0.5 g,口服,每日3次;观察组患者在对照组治疗的基础上给予天芪降糖胶囊1.6 g,口服,每日3次。两组均用药4周。观察两组患者的临床疗效,治疗前后中医证候总积分、血糖水平[空腹血糖(FPG)、餐后2 h血糖(2 hPG)、糖化血红蛋白(HbA1c)]、血脂水平[总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)]、超敏C反应蛋白(hs-CRP)和内皮素-1(ET-1)水平、血液流变学指标、氧化应激指标[丙二醛(MDA)、超氧化物歧化酶(SOD)]及不良反应发生情况。结果:观察组患者总有效率显著高于对照组(89.58%vs.70.83%),差异有统计学意义(P<0.05)。治疗后,两组患者中医证候总积分和血糖、hs-CRP、ET-1、TC、TG、LDLC、血液流变学指标、MDA水平均显著低于同组治疗前,且观察组中医证候总积分、FPG、2 hPG、hs-CRP、ET-1、TC、TG、LDL-C、血液流变学指标、MDA水平均显著低于对照组;两组患者SOD水平均显著高于同组治疗前,且观察组显著高于对照组,同时观察组HDL-C水平显著高于同组治疗前及对照组,差异均有统计学意义(P<0.05)。两组患者治疗期间均未见明显不良反应发生。结论:天芪降糖胶囊联合二甲双胍治疗老年2型糖尿病伴脑微血管病变的疗效显著,可降低血糖、血脂水平,改善机体血液流变学状态及氧化应激反应,且安全性较好。
2型糖尿病;脑微血管病变;天芪降糖胶囊;二甲双胍;疗效;安全性
脑微血管病变作为2型糖尿病的一种严重并发症,其发病机制复杂,多与机体糖脂代谢紊乱、血液流变学异常、氧化应激反应等有关[1-2],若不及时诊治可能会引起动脉粥样硬化,加重脑微血管病变,最终导致患者死亡。为此,防治或延缓2型糖尿病患者脑微血管病变就显得至关重要。中医认为,2型糖尿病属于“消渴病”范畴,发病根源在于“气阴两虚”。近年来,中医药在糖尿病的治疗中发挥了重要作用[3]。天芪降糖胶囊具有益气养阴、清热生津之功效,是治疗2型糖尿病的常见中药制剂。二甲双胍可降低血糖及心血管疾病发病率。为此,在本研究中笔者观察了天芪降糖胶囊联合二甲双胍治疗老年2型糖尿病伴脑微血管病变的疗效和安全性,旨在为临床提供参考。
1 资料与方法
1.1 研究对象
选择2014年3月-2016年3月我院收治的老年2型糖尿病伴脑微血管病变患者96例,按随机数字表法将所有患者分为观察组(48例)和对照组(48例)。观察组男性30例、女性18例;年龄(65.47±4.13)岁;体质量指数(BM I)(24.57±2.64)kg/m2;糖尿病病程(6.59±2.41)年;脑微血管病变病程(3.12±2.00)年。对照组男性28例、女性20例;年龄(66.00±4.25)岁;BM I(24.82±1.95)kg/m2;糖尿病病程(6.60±2.36)年;脑微血管病变病程(3.10±2.02)年。两组患者性别、年龄、BM I、病程等基本资料比较,差异均无统计学意义(P>0.05),具有可比性。本研究方案经医院医学伦理委员会审核通过,所有患者均签署了知情同意书。
1.2 纳入/排除/剔除标准
纳入标准:①符合2型糖尿病的相关诊断标准[4];②年龄60~78岁;③2型糖尿病中医辨证为“气阴两虚证”,主症为喉干口燥、乏力,次症为五心烦热、便秘或心悸等,舌红苔薄,脉细数;④餐后2 h血糖(2 hPG)≥11.1 mmol/L,空腹血糖(FPG)≥7.0 mmol/L;⑤相关资料完整。排除标准:①其他疾病引发脑微血管病变;②老年痴呆、抑郁症、精神异常者;③肝肾功能不全、严重感染、凝血机制障碍者;④相关药物禁忌者;⑤有影响认知功能药物使用史;⑥近期有糖皮质激素相关药物使用史,或正参与其他药物干预试验者。剔除标准:①入组后发现与纳入标准不符;②自然脱落;③与研究方案用药不符。
1.3 治疗方法
对照组患者给予盐酸二甲双胍片(中美上海施贵宝制药有限公司,规格:0.5 g/片,批准文号:国药准字H20023370)0.5 g,口服,每日3次;观察组患者在对照组治疗的基础上给予天芪降糖胶囊(黑龙江未名天人制药有限公司,规格:0.32 g/粒,批准文号:国药准字Z20063799)1.6 g,口服,每日3次。两组均用药4周。用药期间两组患者均接受心理疏导、健康教育、运动指导等护理干预。
1.4 观察指标
1.4.1 治疗前后中医证候总积分 主症包括喉干口燥、乏力,次症包括五心烦热、便秘或心悸。主症:0分(无症状)、2分(轻度)、4分(中度)、6分(重度);次症:0分(无症状)、1分(轻度)、2分(中度)、3分(重度)。分数越高表明症状越严重。
1.4.2 治疗前后血糖水平 血糖指标包括FPG、2 hPG、糖化血红蛋白(HbA1c)。采用日立7600型全自动生化仪(日本株式会社日立高新技术公司提供)以葡萄糖氧化酶法测定FPG、2 hPG(试剂盒由北京利德曼生化技术有限公司提供)。采用LC-10AD VP型高效液相色谱仪(杭州科晓化工仪器设备有限公司提供)测定HbA1c。
1.4.3 治疗前后血脂水平 血脂指标包括总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)。
1.4.4 治疗前后超敏C反应蛋白(hs-CRP)和内皮素-1(ET-1)水平 采用酶联免疫吸附法(ELISA)测定hs-CRP;采用放射免疫法测定ET-1(试剂盒均由南京森贝伽生物科技有限公司提供)。
1.4.5 治疗前后血液流变学指标 血液流变学指标包括全血高切黏度、全血低切黏度、血浆黏度、血细胞比容。采用LB-2A型血流变分析仪(天津市唐宇医疗器械科技发展有限公司提供)测定血液流变学指标。
1.4.6 治疗前后氧化应激指标 氧化应激指标包括丙二醛(MDA)、超氧化物歧化酶(SOD)。采用硫代巴比妥酸显色法测定MDA;采用黄嘌呤氧化酶法测定SOD(试剂盒均由南京碧波生物科技有限公司提供)。
1.4.7 不良反应 观察两组患者治疗期间的不良反应发生情况。
1.5 疗效判定标准
显效:治疗后FPG≤7.2mmol/L,临床症状基本消失;好转:治疗后FPG≤8.25 mmol/L,临床症状明显缓解;无效:未达上述标准。总有效率=(显效例数+好转例数)/总例数×100%。
1.6 统计学方法
采用SPSS 19.0统计软件对数据进行分析。计量资料以±s表示,采用t检验;计数资料以率表示,采用χ2检验。P<0.05为差异有统计学意义。
2 结果
2.1 两组患者临床疗效比较
观察组患者总有效率显著高于对照组,差异有统计学意义(P<0.05),详见表1。
2.2 两组患者治疗前后中医证候总积分比较
治疗前,两组患者中医证候总积分比较,差异均无统计学意义(P>0.05)。治疗后,两组患者中医证候总积分均显著低于同组治疗前,且观察组显著低于对照组,差异均有统计学意义(P<0.05),详见表2。

表1 两组患者临床疗效比较[例(%)]Tab 1 Comparison of clinical efficacies between 2 groups[case(%)]
表2 两组患者治疗前后中医证候总积分比较(±s,分)Tab 2 Comparison of the total scoresof TCM symptoms between 2 groups before and after treatment(x± s,score)

表2 两组患者治疗前后中医证候总积分比较(±s,分)Tab 2 Comparison of the total scoresof TCM symptoms between 2 groups before and after treatment(x± s,score)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05Note:vs.before treatment,*P<0.05;vs.controlgroup,#P<0.05
组别观察组对照组治疗后5.67±2.21*#10.16±2.34*n 48 48治疗前18.10±4.13 18.06±3.98
表3 两组患者治疗前后血糖、hs-CRP、ET-1水平比较(±s)Tab 3 Comparison ofblood glucose,hs-CRP and ET-1 levelsbetween 2 groupsbefore and after treatment(±s)

表3 两组患者治疗前后血糖、hs-CRP、ET-1水平比较(±s)Tab 3 Comparison ofblood glucose,hs-CRP and ET-1 levelsbetween 2 groupsbefore and after treatment(±s)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05Note:vs.before treatment,*P<0.05;vs.controlgroup,#P<0.05
组别观察组48 n对照组ET-1,mg/L 140.76±23.38 112.34±23.15*#138.65±24.79 123.69±26.00*48时段治疗前治疗后治疗前治疗后FPG,mmol/L 10.13±2.52 6.91±1.48*#10.00±3.05 7.56±1.12*2hPG,mmol/L 12.01±2.86 8.43±1.11*#12.36±3.24 9.48±2.03*HbA1c,% 7.56±0.75 6.81±0.53*7.60±0.92 7.08±0.73*hs-CRP,mg/L 6.46±1.21 4.10±1.13*#6.48±1.24 5.25±1.23*
表4 两组患者治疗前后血脂水平比较(±s,mmol/L)Tab 4 Comparison of blood lipid levels between 2 groupsbefore and after treatment(±s,mmol/L)
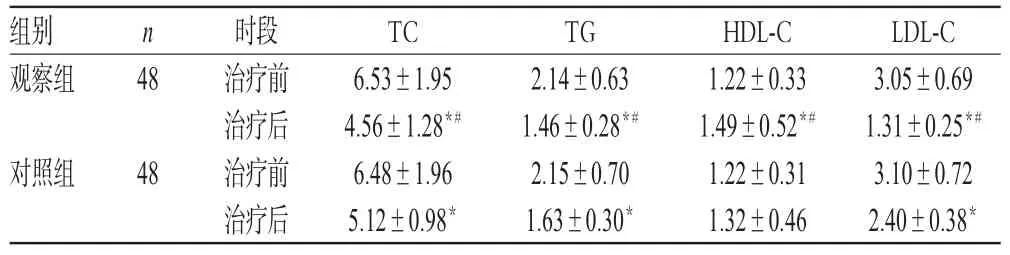
表4 两组患者治疗前后血脂水平比较(±s,mmol/L)Tab 4 Comparison of blood lipid levels between 2 groupsbefore and after treatment(±s,mmol/L)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05Note:vs.before treatment,*P<0.05;vs.controlgroup,#P<0.05
组别观察组48 n对照组LDL-C 3.05±0.69 1.31±0.25*#3.10±0.72 2.40±0.38*48时段治疗前治疗后治疗前治疗后TC 6.53±1.95 4.56±1.28*#6.48±1.96 5.12±0.98*TG 2.14±0.63 1.46±0.28*#2.15±0.70 1.63±0.30*HDL-C 1.22±0.33 1.49±0.52*#1.22±0.31 1.32±0.46
治疗前,两组患者血液流变学指标比较,差异均无统计学意义(P>0.05)。治疗后,两组患者血液流变学指标均显著低于同组治疗前,且观察组显著低于对照组,差异均有统计学意义(P<0.05),详见表5。
表5 两组患者治疗前后血液流变学指标比较(±s)Tab 5 Comparison of rheological indexes between 2 groupsbefore and after treatment(±s)
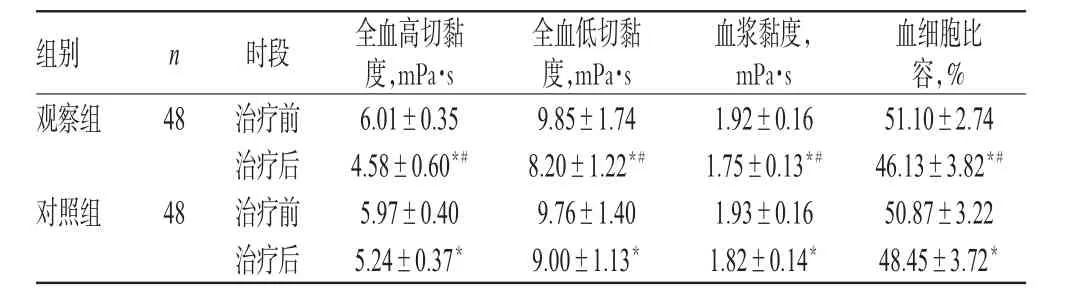
表5 两组患者治疗前后血液流变学指标比较(±s)Tab 5 Comparison of rheological indexes between 2 groupsbefore and after treatment(±s)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05Note:vs.before treatment,*P<0.05;vs.controlgroup,#P<0.05
组别n血细胞比容,%时段全血高切黏度,mPa·s全血低切黏度,mPa·s血浆黏度,mPa·s
2.3 两组患者治疗前后血糖、hs-CRP、ET-1水平比较
治疗前,两组患者血糖、hs-CRP、ET-1水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者血糖、hs-CRP、ET-1水平均显著低于同组治疗前,且观察组FPG、2 hPG、hs-CRP、ET-1水平显著低于对照组,差异均有统计学意义(P<0.05);但两组间HbA1c水平比较,差异无统计学意义(P>0.05),详见表3。
2.4 两组患者治疗前后血脂水平比较
治疗前,两组患者血脂水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者TC、TG、LDL-C水平均显著低于同组治疗前,且观察组显著低于对照组;观察组患者HDL-C水平显著高于同组治疗前及对照组,差异均有统计学意义(P<0.05)。对照组患者治疗前后HDL-C水平比较,差异无统计学意义(P>0.05),详见表4。
2.5 两组患者治疗前后血液流变学指标比较
2.6 两组患者治疗前后MDA、SOD水平比较
治疗前,两组患者MDA、SOD水平比较,差异均无统计学意义(P>0.05)。治疗后,两组患者MDA水平均显著低于同组治疗前,且观察组显著低于对照组;SOD水平均显著高于同组治疗前,且观察组显著高于对照组,差异均有统计学意义(P<0.05),详见表6。
表6 两组患者治疗前后MDA、SOD水平比较(±s)Tab 6 Comparison of MDA and SOD between 2 groups before and after treatment(±s)

表6 两组患者治疗前后MDA、SOD水平比较(±s)Tab 6 Comparison of MDA and SOD between 2 groups before and after treatment(±s)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05Note:vs.before treatment,*P<0.05;vs.controlgroup,#P<0.05
48观察组68.27±4.52 121.10±6.15*#67.78±4.83 75.13±5.34*对照组48治疗前治疗后治疗前治疗后12.32±1.15 4.76±0.64*#12.39±1.20 9.00±1.06*
2.7 不良反应
两组患者治疗期间均未见明显不良反应发生。
3 讨论
糖尿病微血管病变主要特征为微血管基底膜增厚,可在脑、视网膜、神经系统、肾脏等部位发生,其发病机制复杂,可能包括:(1)血糖控制不当可加快基底膜增厚速度,部分或全部微细血管堵塞,致使组织缺氧,加重病变。(2)血管内皮细胞损伤被认为是糖尿病微血管病变发生、发展的基础,易引发血流不畅,血流阻滞,影响相关组织供氧[5]。(3)血流动力学异常。大部分2型糖尿病患者血液高凝,从而增加了血栓形成几率,而血液黏度在很大程度上取决于血浆黏度、红细胞计数及其性状,一旦糖代谢异常,红细胞聚集能力增强,同时血小板高黏附会造成全血黏度上升,血流减缓或阻滞,致使微循环障碍,最终导致微血管病变发生[6]。(4)炎症反应。炎症因子除了可以引发胰岛素抵抗,促使糖耐量下降,加重炎症反应外,还会对胰岛B细胞结构及其功能产生影响[7],加快糖尿病及其并发症发生。(5)氧化应激反应。动物实验表明,2型糖尿病模型鼠脑微血管病变与血液、脑组织中氧化及抗氧化物质异常改变有关,其中SOD活性下降发挥主导作用[8]。
祖国医学认为,糖尿病属于“消渴病”范畴,其病机为本虚标实,阴虚为本,燥热为标。《医学心悟·三消》中记载,“三消之症,皆燥热结聚也”,其治疗在于标本兼治。《素问·五常政要大论》提到,“形不足者,温之以气,精不足者,补之以味”,认为益气能有效改善脏腑功能及元气不足状态。天芪降糖胶囊含有黄芪、天花粉、女贞子、山茱萸、五倍子、人参、旱莲草等成分,方中黄芪、人参补气,女贞子、旱莲草滋阴,天花粉清虚热,山茱萸补益肝肾,五倍子可固精,临床常用于“气阴两虚证”型糖尿病。
二甲双胍为2型糖尿病治疗一线用药,降血糖作用良好,能有效改善机体胰岛素抵抗。hs-CRP为临床典型炎症指标之一,其水平与脑微血管病变密切相关,可直接损伤血管内皮功能,激活单核巨噬细胞,引发或加重炎症反应,损伤血管内皮功能,增加脑微血管病变率。ET-1主要由血管内皮细胞分泌,是糖尿病脑微血管病变的敏感指标。糖尿病患者内皮细胞损伤可使ET分泌增加,促进血管收缩,从而引发局部脑组织微循环障碍。
本研究结果显示,观察组患者总有效率显著高于对照组;治疗后,两组患者血糖、hs-CRP、ET-1水平均显著低于同组治疗前,且观察组FPG、2 hPG、hs-CRP、ET-1水平显著低于对照组,差异均有统计学意义。这表明,天芪降糖胶囊联合二甲双胍降血糖作用更为显著,而二甲双胍具有一定的抗炎作用,这可能与其可减少脂质过氧化产物,提高机体抗氧化能力有关。治疗后,两组患者HbA1c水平比较,差异无统计学意义。这可能与本研究纳入的样本量较小有关。治疗后,两组患者TC、TG、LDL-C水平均显著低于同组治疗前,且观察组显著低于对照组;观察组患者HDL-C水平显著高于同组治疗前及对照组,差异均有统计学意义。对照组患者治疗前后HDL-C水平比较,差异无统计学意义。这提示,天芪降糖胶囊联合二甲双胍对老年2型糖尿病患者血脂调节作用更加明显,而这与天芪降糖胶囊具有调节血脂、降低血液黏度、刺激B细胞释放胰岛素等作用有关。有文献报道,天芪降糖胶囊能通过下调炎症因子来改善胰岛素抵抗作用,而其血脂调节作用可能与过氧化物酶增殖体激活受体α上调相关[9]。本研究结果还显示,治疗后两组患者中医证候总积分、血液流变学指标均显著低于同组治疗前,且观察组显著低于对照组,差异均有统计学意义。这说明,天芪降糖胶囊联合二甲双胍能明显改善患者的中医临床症状;并能明显降低全血黏度、血浆黏度及血细胞比容,抑制血小板聚集,减轻机体高凝状态,缓解脑微血管病变相关症状[10]。有研究表明,氧化应激反应会引发血糖波动,参与糖尿病患者脑微血管病变发生、发展过程[11]。SOD可反映心肌细胞内抗脂质过氧化能力,MDA主要反映脂质过氧化程度。本研究结果显示,治疗后,两组患者SOD水平均显著高于同组治疗前,且观察组显著高于对照组;MDA水平均显著低于同组治疗前,且观察组显著低于对照组,差异均有统计学意义。这表明,天芪降糖胶囊联合二甲双胍能有效减轻机体氧化应激反应。安全性方面,两组患者治疗期间均未见明显不良反应发生。这提示,天芪降糖胶囊联合二甲双胍并未增加不良反应的发生。
综上所述,天芪降糖胶囊联合二甲双胍治疗老年2型糖尿病伴脑微血管病变的疗效显著,可降低血糖、血脂水平,改善机体血液流变学状态及氧化应激反应,且安全性较好。由于本研究纳入的样本量较小,观察时间较短,故此结论有待大样本、多中心研究进一步证实。
[1] 陈彬,张星光,程千鹏,等.艾塞那肽联合二甲双胍对初诊成人2型糖尿病患者血糖控制效果观察[J].解放军医药杂志,2016,28(5):66-69.
[2] 仇江辉.降糖舒片联合二甲双胍治疗2型糖尿病患者的疗效及对血清IL-2、IL-6水平的影响[J].医学临床研究,2015,32(2):370-371.
[3] 中华医学会糖尿病学分会.中国2型糖尿病防治指南:2013年版[J].中华糖尿病杂志,2014,6(7):448.
[4] 唐瑛,李劲松.六味地黄丸加减联合二甲双胍辨治阴虚内热证2型糖尿病的临床研究[J].湖南师范大学学报(医学版),2015,12(4):28-31.
[5] 林垦,郭羿辰.中西医结合治疗对老年2型糖尿病患者微血管病变的影响[J].中国老年学杂志,2014,34(8):2028-2030.
[6] 邹德学.2型糖尿病患者血浆纤维蛋白原含量、抗凝血酶活性、血小板聚集及血液动力学的检测[J].血栓与止血学,2011,17(5):219-220.
[7] 陈鼎,翁雪燕.瑞格列奈联合珍芪降糖胶囊对老年2型糖尿病患者β细胞功能的影响研究[J].中国生化药物杂志,2015,35(8):136-139.
[8] 杨红英,李树清,王卓,等.实验性糖尿病鼠脑微血管病变与氧化应激反应的研究[J].中国微循环,2009,13(4):250-253.
[9] 张茜,肖欣华,王彤,等.应用基因芯片探讨天茂降糖胶囊降糖调脂的机制[J].中国糖尿病杂志,2009,17(3):174-177.
[10] 曹永,王宏宇,徐春,等.天芪降糖胶囊联合二甲双胍对2型糖尿病患者白介素6、肿瘤坏死因子α和C反应蛋白的影响[J].中国糖尿病杂志,2015,23(8):739-741.
[11] 龙艳,苏珂,彭鹰,等.血糖波动与氧化应激对2型糖尿病微血管病变的影响[J].中华老年心脑血管病杂志,2014,16(2):147-150.
(编辑:陈 宏)
Clinical Observation of Tianqi Jiangtang Capsules Combined w ith Metform in in the Treatment of Elderly Patients w ith Type 2 DiabetesMellitusComplicated w ith CerebralM icrovascular Lesions
CHAIHong1,LU Yifang1,XIAO Hongzhen1,LIYing2,CUIKun3,ZHANG Yuanyue2(1.Dept.of Endocrinology,Tangshan W orkers’Hospital,Hebei Tangshan 063000,China;2.ICU of Internal Medicine,Tangshan W orkers’Hospital,Hebei Tangshan 063000,China;3.ICU of Respiratory M edicine,Tangshan W orkers’Hospital,Hebei Tangshan 063000,China)
OBJECTIVE:To observe clinical efficacy and safety of Tianqi jiangtang capsules combined w ith metformin in the treatment of elderly patients w ith type 2 diabetesmellitus complicated w ith cerebralm icrovascular lesions.METHODS:A total of 96 elderly patients w ith type 2 diabetesmellitus complicated w ith cerebralm icrovascular lesions were random ly divided into control group(48 cases)and observation group(48 cases).Control group was given Metform in hydrochloride tablets 0.5 g orally,3 times a day.Observation group was additionally given Tianqi jiangtang capsules 1.6 g orally,3 times a day,on the basis of control group.Both groups
treatment for 4 weeks.Clinical efficacies of 2 groups were observed as well as total score of TCM symptoms,the levels of blood glucose(FPG,2 hPG,HbA1c),blood lipid(TC,TG,HDL-C,LDL-C),hs-CRP,ET-1,blood rheology and oxidative stress indexes(MDA,SOD),the occurrence of ADR.RESULTS:The total response rate of observation group was significantly higher than that of control group(89.58%vs.70.83%),w ith statistical significance(P<0.05).A fter treatment,total score of TCM symptoms,the levels of blood glucose,hs-CRP,ET-1,TC,TG,LDL-C,blood rheology indexes and MDA in 2 groups were significantly lower than before;total score of TCM symptoms,the levels of FPG,2 hPG,hs-CRP,ET-1,TC,TG,LDL-C,blood rheology indexes and MDA in observation group were significantly lower than control group;the level of SOD in 2 groups were significantly higher than before,and the observation group was significantly higher than control group,and the level of HDL-C in observation group was significantly higher than before treatment and control group,w ith statistical significance(P<0.05).No obvious ADR was found in 2 groups during treatment.CONCLUSIONS:Tianqi jiangtang capsules combined w ith metformin show significant therapeutic efficacy in the treatment of elderly patients w ith type 2 diabetesmellitus,and can reduce the levels of blood glucose and lipid,improve blood rheology and oxidative stress reaction,w ith goud safety.
Type 2 diabetesmellitus;Cerebralmicrovascular lesions;Tianqi jiangtang capsules;Metform in;Efficacy;Safety
R587.1
A
1001-0408(2017)15-2053-05
2016-11-04
2017-03-13)
*副主任护师。研究方向:糖尿病健康教育。E-mail:Chai hong868@163.com
#通信作者:主任医师。研究方向:危重症内科。E-mail:3159881538@qq.com
DOI 10.6039/j.issn.1001-0408.2017.15.11

