调强放疗联合同步替吉奥化疗对复发直肠癌的疗效观察
李金伟,肖海,曾红学
(1.赣州市肿瘤医院,江西 赣州 341000;2.赣南医学院病理教研室,江西 赣州 341000)
调强放疗联合同步替吉奥化疗对复发直肠癌的疗效观察
李金伟1,肖海2,曾红学1
(1.赣州市肿瘤医院,江西 赣州 341000;2.赣南医学院病理教研室,江西 赣州 341000)
目的 观察调强放疗联合同步替吉奥治疗复发直肠癌的近期疗效及并发症。方法对39例术后复发直肠癌患者,采用调强放疗,1.8~2.0 Gy/次,5次/周,预防剂量45~48 Gy后肿瘤推量至60~66 Gy。同步口服替吉奥胶囊化疗[80 mg/(m2·d),分2次餐后1小时口服,服2周,停1周]。结果有36例完成治疗,依从性好。放疗结束后3个月时CR 7例,PR 27例,SD 5例,有效率(RR)为87.2%,疾病控制率(DCR)为100%。主要不良反应为消化道反应、血液学毒性、肛周皮肤反应,多为1、2级。结论调强放疗联合替吉奥对复发直肠癌的近期疗效好,显著改善患者生活质量,急性并发症可耐受。
直肠肿瘤/肿瘤复发;放射疗法,同步化疗;替吉奥
我国结直肠癌患者每年新发约15万人,死亡率超过7/10万,且病死率仍有逐年上升趋势[1]。直肠癌主要治疗手段为手术治疗,术后复发是治疗失败的主要模式,局部复发率15%~65%[2]。主要复发部位为骶前及髂内[3]。复发直肠癌的治疗较为棘手,除吻合口复发并发现早可以有再次手术的机会,多数已无手术机会,治疗以同步放化疗+化疗为主。目前尚无较一致的规范治疗方案。本研究对术后复发直肠癌的39例患者,进行调强放疗联合替吉奥口服化疗。现将结果报告如下。
1 资料与方法
1.1 临床资料 共39例符合条件患者,其中男23例,女16例;男女比例为1.44∶1;年龄28~58岁,平均年龄47岁,中位年龄46岁;骶前复发16例,髂内复发13例、吻合口复发10例;复发时间为术后10~32个月,平均19个月;复发前治疗历史:单纯手术例19例,手术+化疗16例,手术+放化疗4例。入选标准:(1)术前经直肠病理组织学证实为腺癌;(2)复发灶经病理学确诊为腺癌(如无法病理确诊需有CEA持续升高并结合CT/MRI/PET临床诊断);(3)预计生存期>6个月;(4)卡氏评分均≥70;(5)血常规、肝肾功能正常、无严重心肺疾患、严重糖尿病;(6)无远处转移;(7)无肠梗阻及肠梗阻倾向;(8)近期未用抗真菌药等其他氟胞嘧啶类药物。
1.2 治疗方法 放疗均采用Varian clinac-IX直线加速器 6MV-X线适形调强放疗,采用Pinical V9.2计划系统,GTV为临床影像可见肿瘤(包括复发灶和/或淋巴结),CTV1:在GTV基础上外扩1 cm;CTV2包括复发灶、直肠周围系膜区、骶前区、髂内及骶3上缘以上的髂外和部分髂总血管周围的淋巴引流区。外放6 mm为各自PTV,照射剂量要求:95%的等剂量线包绕95%的靶体积。1.8~2 Gy/次,5次/周,45~48 Gy后CTV1推量至56~60 Gy,GTV推量至60~66 Gy(既往已行盆腔放疗的4例未行预防照射,直接GTV外扩6 mm给量至60Gy)。在放疗第1天起同时联合服用替吉奥胶囊(山东鲁南制药集团新时代药业有限公司生产,商品名:维康达),按说明书规范用药:80 mg/(m2·d),分2次餐后1小时口服,服2周,停1周。
1.3 观察指标 同步放化疗前及放疗结束3个月后影像学MR结合CEA生化指标为疗效评价值,由2名以上临床肿瘤医师和影像诊断医师共同评价。每周行全血细胞分析,第1、4周、6周行血生化、CEA检查。疗效及不良反应评价标准按《抗肿瘤药对实体肿瘤客观疗效评价标准》评价疗效:分为完全缓解(CR),部分缓解(PR),病情稳定(SD)和疾病进展(PD),CR+PR统计有效率(RR),CR+PR+SD计算疾病控制率(DCR)。放疗急性损伤按RTOG放射损伤标准评定,化疗不良反应按CTCAE V3.0标准评价。
2 结果
2.1 近期疗效 1例患者因Ⅲ°骨髓抑制在第5周时停服替吉奥,2例因Ⅲ°胃肠道反应重停服替吉奥,7例因肛周皮肤Ⅲ°湿性反应及肠炎延迟放疗4~7 d,余均按时足量完成上述治疗,放疗结束3个月时CR7例,PR27例,SD5例,有效率为87.2%,疾病控制率为100%。症状缓解(包括疼痛缓解、出血及黏液排泄物消失、肛门下坠感缓解、排尿困难改善)评价:消失及改善32例、稳定及加重7例。
2.2 放化疗不良反应 主要不良反应为骨髓抑制、胃肠道反应及放射性肠炎,皮肤反应,以Ⅰ~Ⅱ°为主,无Ⅳ°严重不良反应。反应最重多出现在第4周。见表1。
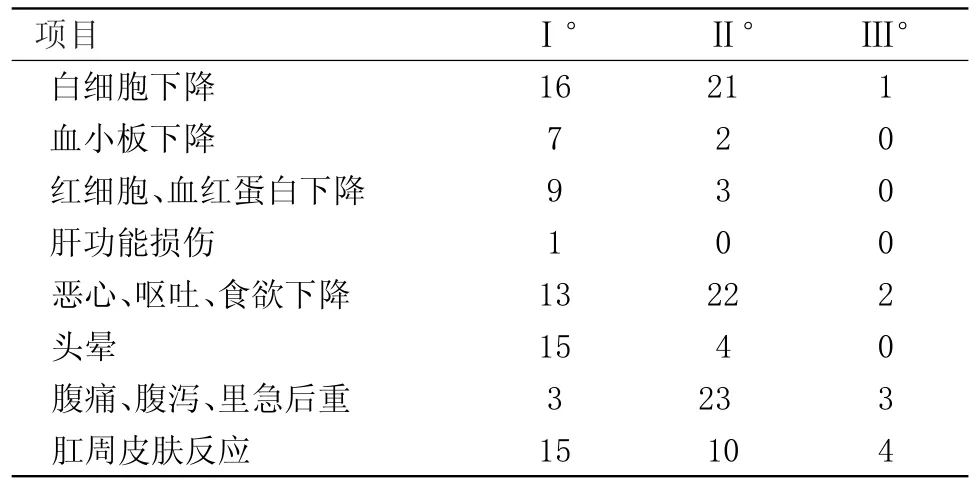
表1 39例直肠癌患者放化疗不良反应情况
3 讨论
直肠癌术后复发率的文献报道30%[4]。直肠癌术后复发多已失去再次手术机会,手术使复发病灶内肿瘤乏氧细胞增多,会使放疗对复发病灶的治疗作用降低。因此,采取积极的放化综合治疗模式,才有可能取得更满意的效果[5]。自5-Fu的临床应用以来,一直被公认为直肠癌药物治疗的基石,使晚期直肠癌患者的中位生存期从最佳支持治疗的6个月增加到14个月[6]。氟尿嘧啶与放射治疗联合应用有增效、增敏作用[7]。
常规放疗由于照射体积大,由于小肠、结直肠,股骨头等器官剂量限制,很难给到根治剂量,疗效较差[8-9]。调强放射治疗剂量曲线与靶区高度一致,在保证局部病灶区域高剂量的同时,又能使上述器官的照剂量显著下降,可给至根治剂量,疗效明显好于三维适形放疗及常规放疗,而使治愈目标成为可能[10-12]。
复发患者既往多常经历多次静脉联合化疗,往往对静脉化疗恐惧,口服化疗多数患者较易接受,愿意口服低毒性化疗药物[13-14]如FT-207、替吉奥胶囊、VP-16等。替吉奥是一种新型口服化疗药,用于治疗晚期胃肠道肿瘤[15-16]。替吉奥是第三代5-Fu类抗肿瘤药,共有3种成分:主要是具有细胞毒性的替加氟及另外两种生化修饰剂:吉美嘧啶及奥替拉西钾按摩尔比1∶0.4∶1组成,其中,替加氟是5-Fu的前体药物,主要在肝微粒体细胞色素P450代谢酶系作用下转变为5-Fu起抗肿瘤作用,具有优良的口服生物利用度,半衰期长达12小时,每天服用2次,符合其时间依赖性的药理特点,是替代持续静滴5-Fu的理想药物[17]。吉美嘧啶为二氢嘧啶脱氢酶抑制剂,减慢5-Fu分解速度,可延长血液和肿瘤组织中5-Fu的药效时间。奥替拉西经口服吸收后主要分布在消化道组织,可在胃肠道内特异性抑制肠道黏膜细胞内乳清酸核糖转移酶,阻断5-Fu磷酸化,而5-Fu的磷酸化产物是造成胃肠道不良反应的主要原因,故而减轻5-Fu引起的胃肠道毒副作用。替吉奥胶囊其12小时服用1次可达恒定血药浓度,口服化疗方便,与5-Fu相比,能维持较高的血药浓度、较高的抗癌活性,明显降低药物的毒性,而且口服使用方便,避免中心静脉穿刺带来的血栓、感染风险,减少胃肠道黏膜反应,耐受性提高。
本研究中,近期疗效较显著,放疗后3个月时CR7例,PR27例,SD5例,有效率(RR)为87.2%,疾病控制率(DCR)为100%。复发患者常有骶丛神经刺激症状,如会阴区下坠感、会阴部疼痛、下肢痛、便血、肛门排出黏液脓血分泌物等。39例患者中症状缓解(包括疼痛缓解、出血及黏液排泄物消失、肛门下坠感缓解、排尿困难改善)较显著:消失及改善32例、稳定及加重7例。症状缓解率82.1%,近期不良反应绝对多数为轻度,表现在:白细胞下降恶心、呕吐、食欲下降、头晕、腹痛、腹泻、里急后重、肛周皮肤反应。Ⅲ、Ⅳ度不良反应主要为胃肠道反应及肛周皮肤粘膜反应。与类似研究文献报道中相似或更高[18-20]。
综上所述,调强放疗同步替吉奥化疗可作为术后局部复发直肠癌的理想治疗手段,其疗效肯定,可明显改善患者的生活质量,且方便实施,治疗依从性高,大部分患者在门诊即可完成,值得临床推广应用,要取得更为准确的结论,需扩大样本量,设计前瞻性随机研究,并长期随访,进一步观察远期疗效及并发症。
[1]Chan CC,Fan CW,Kuo YB,et a1.Multiple serological biomarkers for colorectal cancer detection[J].Int J Cancer,2009,126(7):1683-1690.
[2]殷蔚伯,余子豪,徐国镇.肿瘤放射治疗学[M].北京:中国协和医科大学出版社,2008:859.
[3]宋永文,钱立庭,刘新帆.直肠癌的预后因素和治疗失败原因分析[J].中国肿瘤,2006(7):484-487.
[4]Sejin Park,Yun Sik Lee.Analysis of the prognostic efectiveness of amultivisceral resection for locally advanced colorecta1[J].J Korean Soc Coloproctol,2011,27(1):21-26.
[5]程方芳,张和平,昊君心.调强放疗联合化疗治疗直肠癌术后复发的临床观察[J].实用癌症杂志,2011,26(4):383-386.
[6]葛均波,徐永健.内科学[M].北京:人民卫生出版社,2013:143.
[7]Taher AN,El-Baradie MM,Nasr AM,et a1.Locally advanced rectal carcinoma:preoperativeradiotherapy versus postoperate chemoradiation,10-year folowedup results of arandomized clinical study[J].EgypNatl Canc Inst,2006,18(3):233-243.
[8]李莎,田种泽,岳养军,等.术后复发直肠癌同期放化疗与单纯放疗的随机临床研究[J].中华临床医师杂志,2012,6(6):1421-1424.
[9]高献书,李洪振.局部复发直肠癌放射治疗[J].中国实用外科杂志,2011,31(4):393-296.
[10]龚伟,廖洪,庞晓琳,等.调强适形放疗联合化疗治疗直肠癌术后复发的疗效观察[J].浙江临床医学2014,16(8):1252-1254.
[11]Adkison JB,McHaffie DR,Bentzen SM,et a1.Phase I trial of pelvic noda l dose escalation with hypofractionated IMRT for high-risk prostate cancer[J]. Int J Radiat Oncol Biol Phys,2012,82(1):184-190.
[12]Arbeal L,Ramos LI,Martinez-Monge R,et a1.Intensitymodulated radiation therapy Vs.3D conformal radiotherapy in locally advanced rectal cancer:dosimetric comparison and clinical implications.Radiat Oncol,2010,26(5):17-24.
[13]邹卉瑜,陈笑艳.替吉奥胶囊(S-1)在中国癌症患者体内的药代动力学和生物等效性[J].中国药理学杂志,2010,5(26):349-353.
[14]Koizumi W,Takiuchi H,Yamada Y,et al.PhaseⅡ study of oxaliplatin plus S-1 as first-line treatment for advanced gastric cancer(G-SOX study)[J].Ann Oncol, 2010,21(5):1001-1005.
[15]Emi M,Yamaguchi Y,Hihara J,et al.PhaseⅠtrial of oxaliplatin plus S-1 chemotherapy in patients with metastatic coloectal cancer[J].Oncol lett,2010,1(1): 95-98.
[16]Muro K,Boku N,Shimada Y,et al.Irinotecan plus S-1 (IRIS)versus fluorouracil and folinic acid plus irnotecan(FOLFIRI)as second-line chemotherapy for metastatic colorectal cancer:a randomised phase 2/3 non-inferiority study(FIRIS study)[J].Lancet Oncol, 2010,11(9):853-860.
[17]Ikeda K,Yoshisue K,Matsushima E,et al.Bioactivation of tegafur to 5-fluorouracil is catalyzed by cytochrome P-450 2A6 in human liver microsomes in vitro[J].Clin Cancer Res,2000,6:4409-4415.
[18]田彬.替吉奥化疗同步三维适形放疗治疗复发性结直肠癌的疗效与安全性的回顾性分析[J].中国临床药理学杂志,2013, 29(11):812-814.
[19]贾青青,顾扬.替吉奥化疗同步调强适形放疗治疗老年局部晚期直肠癌的疗效观察[J].中国老年保健医学,2012,10(3):36-37.
[20]翁成荫,刘国龙,关明媚,等.三维适形放疗联合替吉奥治疗42例局部复发直肠癌的临床观察[J].中国实用医药,2012,7 (8):6-8.
ObjectiveTo observe the recent curative effect and complications for the treatment of recurrent colorectal cancer for Intensity Modulated Radiationtherapy combined synchronization chemotherapy for Gimeracil and Oteracil Porassium.Methods39 cases of postoperative recurrence of rectal cancer patients,used of intensity modulated radiation therapy,1.8-2.0 Gy per fraction,five fractions per week,after prevention dose of 45-48 Gy,push the tumor amount to 60-66 Gy.Synchronous oral chemotherapy for Gimeracil and Oteracil Porassium capsule[80 mg/(m2·d),1 hour after the meal points 2 times of oral,takes 2weeks,stop 1 week].Results36 patients underwent treatment,compliance is good.3 months after the radiation,CR7,PR27,SD5 cases respectively,efficient(RR)was 87.2%,the disease control rates(DCR)was 100%.Major adverse events of the digestive tract,hematology toxicity,anus periderm skin reaction,more than 1,level 2.ConclusionCombined Intensity Modulated Radiotherapy with Gimeracil and Oteracil Porassium for recurrence of rectal cancer,The recent curative effect is good,improve patient quality of life,acute complications can be tolerated.
Colorectal cancer/cancer recurrent;Radiotherapy;Synchronization chemotherapy;Gimeracil and Oteracil Porassium
10.3969/j.issn.1009-4393.2017.07.045
曾红学,E-mail:372664031@qq.com

