4,5-二(1H-5-四唑基)-1,2,3-三唑及其含能盐的合成与表征
张艳芳,熊华林,林秋汉,程广斌,杨红伟
(南京理工大学化工学院,江苏 南京 210094)
4,5-二(1H-5-四唑基)-1,2,3-三唑及其含能盐的合成与表征
张艳芳,熊华林,林秋汉,程广斌,杨红伟
(南京理工大学化工学院,江苏 南京 210094)
以4,5-二氰基-1,2,3-三唑为原料,经过重氮化偶联反应和[2+3]偶氮环加成反应合成了4,5-二(1H-5-四唑基)-1,2,3-三唑,并经过复分解反应合成了7种高氮含能盐。采用IR、1H NMR、13C NMR对化合物的结构进行了表征;采用DSC法研究了它们的热行为;基于B3LYP/6-311G**方法计算了各化合物的理论密度、标准生成焓,并通过EXPLO5预估了各化合物的爆速和爆压。结果表明,8种化合物均具有较好的热稳定性;生成焓为647.4~1579.4kJ/mol;爆速为7652~8389m/s;爆压除化合物2外均高于20 GPa;除化合物1、7、8外,其他化合物标准状况下的气体产生量均大于800 L/kg,是潜在的气体发生剂。
有机化学;高氮化合物;四唑;三唑;含能离子盐
引 言
高氮含能化合物作为一种新型含能材料受到世界各国的关注[1-4],具有良好的应用前景[5-6]。高氮含能化合物具有高的生成焓,爆炸产生大量的N2和H2O,不会对环境造成污染。唑类化合物由于氮含量高、热稳定性好等优点已在高氮含能化合物合成领域得到广泛研究[7]。唑类高氮含能离子盐是一类独特的高氮含量的含能材料,含能离子盐与非离子分子相比具有较低的蒸汽压而更具有优势[8]。Thomas M. Klapötke等[9]首先合成1,5-联四唑,由于氮含量高被认为是推进剂的潜在组分;翟连杰、樊学忠等[10]报道了多种合成4,5-二(1H-5-四唑基)-1,2,3-三唑的方法;随后Thomas M. Klapötke等[11]报道了4,5-二(1H-5-四唑基)-1,2,3-三唑及其铵盐、羟胺盐、氨基胍盐的合成,并预估了各化合物的爆轰性能。其爆速介于7785~9022m/s,各化合物还具有较高的生成焓(591~846kJ/mol)和热分解温度(160~301°C)。任晓雪[12]研究表明高氮化合物是具有良好应用前景的烟火型气体发生剂原料。由于四唑类衍生物氮含量和能量均高、毒性低,因而成为高氮化合物的典型代表。
为了进一步扩展唑类化合物作为气体发生剂的应用潜力,本研究在前人工作的基础上合成了4,5-二(1H-5-四唑基)-1,2,3-三唑的一系列高氮含能盐。该系列化合物氮含量高、生成焓高、气体产生量大且不对环境造成污染,符合当代气体发生剂、低特征信号推进剂、低烟或无烟烟火剂等所追求的高性能、绿色环保的特点。
1 实 验
1.1 试剂与仪器
盐酸,上海凌峰化学试剂有限公司;氯化锌,天津市瑞金特化学品有限公司;亚硝酸钠、乙醚,国药集团化学试剂有限公司;硝酸银,上海麦克林生化科技有限公司;水合肼(质量分数80%),上海展云化工有限公司;3-氨基-1,2,4-三氮唑,上海晶纯生化科技股份有限公司;叠氮化钠,山东西亚化学股份有限公司;乙醇、氨水,上海泰坦科技股份有限公司;2,3-二氨基-2-丁烯二腈、羟胺(质量分数50%)、碳酸二酰肼、1,2,4-三氮唑,萨恩化学技术(上海)有限公司。以上试剂均为分析纯。
BOMEM MB系列154S系列傅里叶变换红外光谱仪,加拿大Abb Bomem公司;Bruker Avance 300M数字化核磁共振谱仪,瑞士Bruker公司;TGA/ADTA851e型热重分析仪、DSC823e型差示扫描量热仪,Mettler-Toledo国际贸易有限公司;ZF-1型三用紫外分析仪,上海市安亭电子仪器厂。
1.2 实验过程
1.2.1 8种高氮含能化合物的合成路线如图1所示。
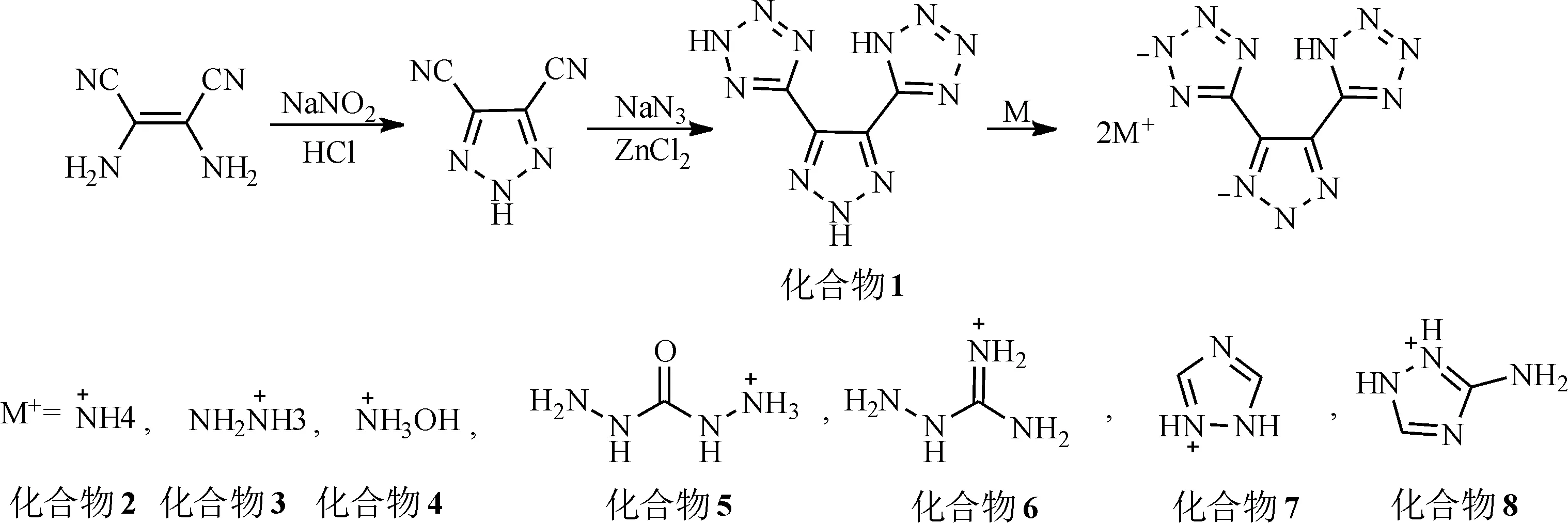
图1 化合物1~8的合成路线Fig.1 Synthetic route of compounds 1-8
1.2.2 4,5-二氰基-1,2,3-三唑的合成[13]
将10.81 g(0.10mol)2,3-二氨基-2-丁烯二腈加入到100mL浓度为1mol/L的盐酸溶液中。将6.89g(0.10mol)亚硝酸钠溶于125mL水中,充分搅拌至完全溶解。在低温条件下,将上述亚硝酸钠的水溶液缓慢滴入反应液中,滴加过程中保持反应液温度介于0~5℃。加料完毕后在该温度下反应0.5h,常温反应1h。经抽滤、乙醚萃取、干燥并旋干乙醚溶液得到10.20g橘色粉末状固体,收率85.61%。
1.2.3 4,5-二(1H-5-四唑基)-1,2,3-三唑(化合物1)的合成[14]
向250mL单口瓶中加入2.38g(37mmol)叠氮化钠、5.00g(37mmol)氯化锌、100mL乙醇,充分搅拌。缓慢加入2.00g(17mmol) 4,5-二氰基-1,2,3-三唑回流24h,TLC监测反应终点。反应结束后,将反应液倒入等体积的冰水中,浓盐酸调节pH值为1。搅拌2h ,经过滤、洗涤、干燥,得到3.01g白色块状固体,收率86.49%。
1H NMR ( DMSO-d6,300 M ),δ:4.27 (s);13C NMR (DMSO-d6,75 M ),δ: 148.37,132.01;IR(KBr), ν(cm-1):3343,3088,2469,1909,1620,1027,980, 886;Tdonset=296.14℃。元素分析(C4H3N11,%):计算值,C 23.42,H 1.47,N 75.11;实测值, C 23.37,H 1.50,N 75.13。
1.2.4 4,5-二(1H-5-四唑基)-1,2,3-三唑盐的合成
(1) 4,5-二(1H-5-四唑基)-1,2,3-三唑铵盐(化合物2)
向25mL 的单口瓶中加入0.20g(0.99mmol) 4,5-二(1H-5-四唑基)-1,2,3-三唑,少量水,升温至50 ℃,缓慢加入0.27mL(1.96mmol)氨水,搅拌2h,过滤、洗涤、干燥得到0.21g白色粉末状固体,收率90.05%。
13C NMR (DMSO-d6,75M),δ:152.92,133.15;IR(KBr),ν(cm-1):3175,3055,2832,1882,1445,1412,994,576;Td,onset=297.75℃。元素分析(C4H9N13,%):计算值,C 20.08,H 3.77,N 76.15;实测值,C 20.12,H 3.81,N 76.07。
(2) 4,5-二(1H-5-四唑基)-1,2,3-三唑肼盐(化合物3)
向25mL 的单口瓶中加入0.20g(0.99mmol) 4,5-二(1H-5-四唑基)-1,2,3-三唑和少量乙醇。缓慢滴入0.13mL(2.14mmol) 质量分数80%的水合肼溶液,常温搅拌2h,抽滤、洗涤、干燥得到0.23g白色粉末状固体,收率88.47%。
1H NMR ( DMSO-d6,300M ),δ:5.62 (s);13C NMR (DMSO-d6,75M),δ:153.35,132.36;IR(KBr),ν(cm-1):3343,2952,2644,1533,1135,927,765,442;Td,onset=301.14℃。元素分析(C4H11N15,%):计算值,C 17.84,H 4.09,N 70.07;实测值,C 17.90,H 4.16,N 77.94。
(3) 4,5-二(1H-5-四唑基)-1,2,3-三唑羟胺盐(化合物4)
向25mL的单口瓶中加入0.20g(0.99mmol) 4,5-二(1H-5-四唑基)-1,2,3-三唑和少量乙醇。缓慢滴入0.14mL(2.19mmol) 质量分数50%的羟胺水溶液,常温搅拌2h,抽滤、洗涤、干燥得到0.23g白色粉末状固体,收率87.71%。
1H NMR ( DMSO-d6,300M ),δ:9.42 (s),3.14 (s);13C NMR (DMSO-d6,75M),δ:150.43, 130.57;IR(KBr),ν(cm-1):3074,2832,2664,1405,994,887,576,489;Td,onset=287.85℃。元素分析(C4H9N13O2,%):计算值,C 1.48,H 3.32,N 67.16,;实测值, C 1.52,H 3.36,N 67.25。
(4) 4,5-二(1H-5-四唑基)-1,2,3-三唑碳酸二酰肼盐(化合物5)
向25mL的单口瓶中加入0.20g(0.99mmol)4,5-二(1H-5-四唑基)-1,2,3-三唑和少量乙醇。将0.20g(2.22mmol)碳酸二酰肼溶于少量水,缓慢滴入到反应液中,常温搅拌2h,过滤、洗涤、干燥得到0.32g白色粉末状固体,收率85.01%。
1H NMR ( DMSO-d6,300 M ),δ:5.01 (s),3.41 (s);13C NMR ( DMSO-d6,75 M ),δ:159.77,150.03,130.60;IR(KBr),ν(cm-1) :3337,3000,2832,2677,1587,1439,987,576;Td,onset=278.22℃。元素分析(C6H15N19O2,%):计算值,C 18.70,H 3.90,N 69.09;实测值,C 18.72,H 3.95,N 68.98。
(5) 4,5-二(1H-5-四唑基)-1,2,3-三唑氨基胍盐(化合物6)
向25mL的单口瓶中加入0.20g(0.84mmol) 4,5-二(1H-5-四唑基)-1,2,3-三唑铵盐和少量水,加热至50 ℃,铵盐逐渐溶解。将0.40g(2.35mmol)硝酸银溶于水,缓慢滴入反应液中搅拌2h,抽滤、洗涤、干燥得到0.34g白色固体,收率84.23%。
向25mL 的单口瓶中加入0.20g(0.48mmol) 4,5-二(1H-5-四唑基)-1,2,3-三唑银盐和少量水,加热至回流。0.10g(1.05mmol)盐酸胍溶于适量水中,缓慢滴入反应液,回流、抽滤、洗涤、干燥得到0.15g白色固体,收率88.93%。
1H NMR ( DMSO-d6,300 M ),δ:8.23 (br),4.76 (s),3.19 (s);13C NMR ( DMSO-d6,75 M ),δ:159.48,156.44,133.79;IR(KBr),ν(cm-1) :3357,3182,3013,1680,1621,1128,980,698;Td,onset=274.41℃。元素分析(C6H15N19,%):计算值,C 20.40,H 4.28,N 75.32;实测值, C 20.42,H 4.30,N 75.28。
(6) 4,5-二(1H-5-四唑基)-1,2,3-三唑1,2,4-三氮唑盐(化合物7)
向25mL 的单口瓶中加入0.20g(0.99mmol) 4,5-二(1H-5-四唑基)-1,2,3-三唑和10mL甲醇。缓慢加入0.15g(2.17mmol) 1,2,4-三氮唑回流,过滤、洗涤、干燥得到 0.29g白色粉末状固体,收率86.65%。
1H NMR ( DMSO-d6,300 M ),δ:9.41 (s),8.86 (s),8.16 (s);13C NMR ( DMSO-d6,75 M ),δ:148.33,143.10,132.07;IR(KBr),ν(cm-1):3512,3243,3082,2462,1903,1028,960,900;Td,onset=300.05℃。元素分析(C8H9N17,%):计算值,C 28.07,H 2.62,N 69.39;实测值, C 28.07,H 2.55,N 69.38。
(7) 4,5-二(1H-5-四唑基)-1,2,3-三唑3-氨基-1,2,4-三氮唑盐(化合物8)
向25mL的单口瓶中加入0.20g(0.99mmol) 4,5-二(1H-5-四唑基)-1,2,3-三唑和10mL甲醇。缓慢加入0.17g(2.02mmol) 3-氨基-1,2,4-三氮唑回流,过滤、洗涤、干燥得到0.27g白色粉末状固体,收率74.19%。
1H NMR ( DMSO-d6,300 M ),δ:9.64 (tr),7.91 (s),3.14 (s);13C NMR ( DMSO-d6, 75 M ),δ:154.52, 149.87, 143.61, 130.69; IR(KBr),ν(cm-1) :3472,3108,2759,1680,1250,953,725,583;Td,onset=309.06℃。元素分析(C8H11N19,%):计算值,C 25.74,H 2.97,N 71.29;实测值, C 25.80,H 2.89,N 71.31。
2 结果与讨论
2.1 热力学性能分析
在氮气流量30mL/min、升温速率10℃/min的条件下,对4,5-二(1H-5-四唑基)-1,2,3-三唑及其含能盐进行DSC分析,结果见图2。

图2 化合物1~8的DSC曲线Fig.2 DSC curves of compounds 1-8
由图2可知,化合物1~8的热分解温度介于274.41~309.06℃,均高于RDX(210℃),表明化合物具有良好的热稳定性。其中化合物3、化合物7、化合物8的热分解温度均高于300℃,优于TNT(295℃)。该系列化合物热稳定性较高是由于这类高氮化合物所含的氮原子电负性高,氮杂环体系形成类似苯环结构的大π键体系,而大π键体系的存在通常使热稳定性较高。化合物1在109.48℃时开始吸热,到126.44℃出现一个峰值,为其吸热峰。从296.14℃开始,经历一个缓慢的放热过程,在301.83℃时放热速率达到最大。化合物2从297.75℃开始放热,在316.20℃放热速率达到最大。化合物3没有经过熔化吸热的过程,而是直接发生剧烈的分解反应释放大量的热,分解峰呈尖锐状。从301.14℃开始放热,在304.60℃放热速率达到最大。化合物4~7均有一个很小的吸收峰。分别从287.85、278.22、274.41、300.05℃开始放热,分别在304.03、288.94、317.97、306.97℃放热速率达到最大。化合物8在257.63℃时开始吸热,到271.57℃出现吸热峰的峰值。从309.06℃开始放热,在319.95℃时放热速率达到最大。
2.2 生成热和爆轰性能的理论计算
运用Gaussian09程序,在B3LYP/6-311+G**水平下对化合物结构进行优化,得到其在势能面上的稳定结构,经振动分析无虚频,并对各化合物的性质进行计算。所有化合物的生成热均基于设计等键反应和运用B3LYP/6-311+G**方法计算,所设计的等键反应如图3所示。各化合物总能量(E0)、零点能(ZPE)、温度校正系数(ΔHT)以及生成热(ΔfHm)见表1。

(a) 化合物1

(b) 化合物2~8阴离子图3 化合物1和化合物2~8阴离子的等键方程Fig.3 Isodesmic reaction for compound 1 and anions of compounds 2-8
表1 各化合物的总能量、零点能、温度校正系数以及生成热
Table 1E0,ZPE,HTand ΔfHmof different compound

化合物E0/(a.u.)ZPE/(kJ·mol-1)ΔHT/(kJ·mol-1)ΔfHm/(kJ·mol-1)1-755.43219.1129.10774.862-56.92124.719.98636.743-112.24166.0212.04789.464-132.09137.0611.20694.985-336.31269.1919.25790.496-261.14255.6117.03745.977-242.59179.3912.861020.998-298.01223.8916.17937.07
各化合物的理论密度是通过分子摩尔质量(M)除以平均摩尔体积(V)的方法计算。对各分子的0.001e/bohr3等电子密度面所包围的体积空间,用Monte-Carlo方法求V,进而求得各分子的密度(ρ)。根据各化合物理论计算所得的生成焓和密度,利用EXPLO5程序[15-16]对关键爆轰参数爆速(D)和爆压(p)进行计算,结果见表2。由表2可知,化合物1~8的氮含量高于60 %。除化合物2和化合物6外,其他化合物的爆热均高于TNT。化合物1~8的生成焓均为正,介于647.4~1597.4kJ/mol。这是因为其结构中含有大量的N-N键及N=N键,含能化合物骨架中N-N、C=N、N=N键的存在对化合物的生成焓均有较大的贡献,有利于提高分子的爆热。此外,除化合物1和化合物7外的其他化合物在标准状况下的气体产生量均高于RDX(739L/kg),其中化合物5的气体产生量为854L/kg。各化合物的爆压介于19.4~25.7GPa,爆速为7652~8389m/s,优于TNT的爆轰性能(爆速6881m/s,爆压19.5GPa)。除化合物2、化合物7外的其他化合物的爆速均高于8000m/s,优于TNT。

表2 化合物1~8物理性质及爆轰性能
注:M为分子质量;w(N)为氮含量;Ω为氧平衡;Tdec为热分解温度;ρ为密度;ΔfHm为标准摩尔生成焓;D为爆速;p为爆压;Q为放热量;V0为标况下的气体产生量。
3 结 论
(1)以4,5-二氰基-1,2,3-三唑为原料,经过重氮化偶联反应、[2+3]偶氮环加成反应合成了4,5-二(1H-5-四唑基)-1,2,3-三唑,并经过复分解反应合成了一系列高氮含能盐。DSC分析表明,化合物1~8的热分解温度介于274.41~309.06℃,表明所合成的化合物均具有良好的热稳定性。
(2)由于大量N-N键及N=N键的存在,化合物1~8均具有较高的正生成焓及较好的爆轰性能。各化合物的爆速均大于TNT,除化合物2爆压与TNT相当外,其他化合物的爆压均大于TNT,综合比较各化合物,化合物5的性能较佳。
(3)化合物1~8氮含量高、生成焓高、气体产生量大且不对环境造成污染,是潜在的气体发生剂。
[1]HervéG,RousselC,GraindorgeH.Selectivepreparationof3,4,5-trinitro-1H-pyraz-ole:astableall-carbon-nitratedarene[J].AngewandteChemieInternationalEdition, 2010, 49(18):3177 -3181.
[2]LiS,WangY,QiC,etal. 3Denergeticmetal-organicframeworks:synthesisandpropertiesofhighenergymaterials[J].AngewandteChemieInternationalEdition, 2013, 52(52): 14031-14035.
[3]ZhangQ,ShreeveJM.Growingcatenatednitrogenatomchains[J].AngewandteChemieInternationalEdition, 2013, 52(34): 8792-8794.
[4]ZhangM,EatonPE,GilardiR.Hepta-andoctanitrocubanes[J].AngewandteChemieInternationalEdition, 2000, 39(2): 401-404.
[5]MandalAK,PantCS,KasarSM,etal.ProcessoptimizationforsynthesisofCL-20 [J].JournalofEnergeticMaterials, 2009, 27(4):231-246.
[6] 毕卫宇, 刘愆, 张志忠, 等.TNAZ的硝基甲烷法合成研究 [J]. 火炸药学报, 2002, 25(4):31-32.BIWei-yu,LIUQian,ZHANGZhi-zhong,etal.SynthesisofTNAZvianitromethane[J].ChineseJournalExplosives&Propellants(HuozhayaoXuebao), 2002, 25(4):31-32.
[7]HeP,ZhangJ,YinX,etal.EnergeticsaltsbasedontetrazoleN-oxide[J].Chemistry, 2016, 22(23):7670-7685.
[8] 刘晓建, 林秋汉, 庞思平, 等. 唑类含能离子化合物的合成研究进展 [J]. 火炸药学报, 2010, 33(1):6-10.LIUXiao-jian,LINQiu-han,PANGSi-ping,etal.Progressofstudyonthesynthesisofazoleenergeticioniccompounds[J].ChineseJournalExplosives&Propellants(HuozhayaoXuebao), 2010, 33(1):6-10.
[9] 黄晓川, 郭涛, 葛忠学, 等. 联唑类含能化合物及其含能离子盐研究进展 [J]. 含能材料. 2015, 23(3):291-301.HUANGXiao-chuan,GUOTao,GEZhong-xue.Reviewonbis-azolesanditsenergeticionderivatives[J].ChineseJournalofEnergeticMaterials, 2015, 23(3):291-301.
[10] 翟连杰, 樊学忠, 毕福强, 等. 4,5-二(1H-5-四唑基)-1,2,3-三唑的合成方法:CN,105037330[P]. 2015.ZHAILian-jie,FANXue-zhong,BIFu-qiang,etal.Thesynthesisof4,5-bis(1H-tetrazol-5-yl)-2H-1,2,3-trizole:CN, 105037330[P]. 2015.
[11]DippoldAA,IzsákD,KlapötkeTM,etal.Combiningtheadvantagesoftetrazolesand1,2,3-triazoles: 4,5-bis(tetrazol-5-yl)-1,2,3-triazole, 4,5-bis(1-hydroxytetrazol-5-yl)-1,2,3-triazole,andtheirenergeticderivatives[J].EuropeanJournalofChemistry, 2016, 22(5):1768 -1778.
[12] 任晓雪. 国外富氮化合物技术研究进展 [J]. 飞航导弹,2016(7):87-90.RENXiao-xue.Researchprogressofnitrogen-richcompoundsabroad[J].AerodynamicMissileJournal, 2016(7):87-90.
[13]CrawfordMJ,KaraghiosoffK,KlapötkeTM,etal.Synthesisandcharacterizationof4,5-dicyano-2H-1,2,3-tri-azoleanditssodium,ammonium,andguanidiniumsalts[J].InorganicChemistry, 2009, 48(4):1731-1743.
[14]KlapötkeTM,MayrN,StierstorferJ,etal.Maximumcompactionofionicorganicexplosives:bis(hydroxylammonium)5.5′-dinitromethyl-3,3′-bis(1,2,4-oxadiazolate)anditsderivatives[J].Chemistry-AEuropeanJournal, 2014, 20(5):1410-1417.
[15]SuceskaM.EvaluationofdetonationenergyfromEXPLO5computer[J].Propellants,Explosives,Pyrotechnics, 1999, 24(5):280-285.
[16]SuceskaM.CalculationofdetonationparametersbyEXPLO5computerprogram[J].MaterialsScienceForum, 2004, 465/466:325-330.
[17]TangY,YangH,ShenJ,etal. 4-(1-Amino-5-aminotetrazolyl)-methyleneimino-3-methylfuroxananditsderivatives:synthesis,characterization,andenergeticproperties[J].EuropeanJournalofInorganicChemistry, 2014, 2014(7):1231-1238.
Synthesis and Characterization of 4,5-Bis(tetrazol-5-yl)-1,2,3-triazole and Its Energetic Salts
ZHANG Yan-fang, XIONG Hua-lin, LIN Qiu-han, CHENG Guang-bin, YANG Hong-wei
(School of Chemical Engineering, Nanjing University of Science and Technology, Nanjing 210094, China)
4,5-Bis(tetrazol-5-yl)-1,2,3-triazole was synthesized by diazotization coupling reaction and [2+3] azo cycloaddition reaction and seven types of energetic nitrogen-rich salts were synthesized via. metathesis reactions using 4,5-dicyano-1,2,3-triazole as raw material. The structures of compounds were characterized by IR,1H NMR and13C NMR.Their thermal behaviors were studied by DSC. Theoretical densities and standard enthalpies of formation of each compound were calculated based on B3LYP/6-311G**method, and the detonation velocities and detonation pressures of compounds were estimated by EXPLO5. The results show that eight types of compounds have better thermal stability. Their enthalpies of formation are between 647.4 kJ/mol and 1579.4kJ/mol.Their detonation velocities are between 7652m/s and 8389m/s.The detonation pressures are higher than 20 GPa except for compound 2. The amounts of gas production of other compounds are greater than 800L/kg under the standard condition, except for compounds 1,7 and 8, which are potential gas generators.
organic chemistry; high nitrogen compound; tetrazole; triazole;energetic ion salt
10.14077/j.issn.1007-7812.2017.02.007
2016-10-10;
2016-11-04
国家自然科学基金(No.21376121;No.21676147)
张艳芳(1992-),女,硕士研究生,从事含能材料的合成研究。E-mail: zhangyanfang000@163.com
杨红伟(1979-),女,副教授,从事含能材料的合成与应用研究。E-mail: hyang@mail.njust.edu.cn
TJ55;O621
A
1007-7812(2017)02-0041-06

