优选维Vitamin C测定方法在果蔬中的应用
陈 蓉,唐弼熙,李 敏,周虹延,张 佩,朱源志,苏 远,陈兴华,何纯莲
(湖南师范大学医学院,长沙410006)
优选维Vitamin C测定方法在果蔬中的应用
陈 蓉,唐弼熙,李 敏,周虹延,张 佩,朱源志,苏 远,陈兴华,何纯莲
(湖南师范大学医学院,长沙410006)
目的:为完善药品、食品中维生素C含量测定方法,指导合理摄入维生素C,正确推广健康饮食,找到一种准确快速测定维生素C含量的方法。方法:采用直接碘量法、2,6-二氯酚靛酚法、紫外分光光度法、荧光分光光度法测定维生素C的含量,系统比较维生素C含量测定的方法优缺点。结果:直接碘量法、2,6-二氯酚靛酚法、紫外分光光度法、荧光分光光度法(邻苯二胺体系、苯甲酸体系)测得维生素C片中维生素C的含量绝对误差分别为0.094mg/mL,0.095mg/mL,0.357mg/mL,0.120mg/mL,0.009mg/mL。结论:在苯甲酸体系,采用荧光分光光度法测得维生素C的含量准确度高,操作简易,方便应用于果蔬中 维生素C测定。
维生素C;荧光分光光度法;紫外分光光度法;2,6-二氯酚靛酚法
维生素C(VitaminC)是人体必需营养素,其药理及多种生理活性已得到证实[1-4],作为纯粹药物或食品添加剂已被广泛应用。然而,研究表明过高剂量的VC(达2g/d)可能增加细胞DNA对H2O2或其它有害物质损害的敏感性[5],同时对DNA可能产生多方面的损伤,如阻碍DNA修复合成、抑制DNA半保留复制、破坏核苷酸、断裂DNA、引起基因突变或染色体损伤等,因此建立快速准确测定VC的方法尤为重要。目前维生素 C含量的测定方法很多,有碘滴定法、高效液相色谱法、2,6-二氯酚靛酚法、极谱法、2,4-二硝基苯肼比色法、荧光分光光度法、电化学法、钼蓝比色法、过氧化酶法等。但这些方法都有一定的缺陷,如中国药典中采用的置换碘量法在测定深色样品时,准确度欠佳[6];反相HPLC 法用于复杂基体的样品测定比较困难[7];2,6-二氯酚靛酚法利用 DCIP 染料滴定果蔬提取液,滴定终点为红色,如果待测果蔬呈红色,提取液本身颜色会干扰滴定终点的观察,若对果蔬提取液进行脱色处理后利用该法测定深色果蔬中维生素C的含量,准确度和精密度依然欠佳。极谱法测定实验过程中所用汞蒸气有毒,且毛细管易堵塞[8]。酶分析法成本低廉,快速,且不需要对被分析物预先提纯,由于目前提高常规法自动化程度的趋势限制酶分析法的广泛应用[9]等。
本研究通过对维生素C含量测定方法进行系统比较研究,旨在找到一种准确快速维生素C分析方法,完善药典和食品中维生素C含量测定的国家标准,指导合理摄入维生素C,正确推广健康饮食。
1 资料与方法
1.1 仪器、试剂和材料
1.1.1 仪器 紫外分光光度计:LabTech BlueStar,电热恒温水浴锅:DK-98-1A型,天津市泰斯特仪器有限公司,荧光分光光度计:LS-45/55(美国PE公司),高速冷冻离心机(thermo scientific FRESC017)。
1.1.2 试剂 抗坏血酸,无水乙酸钠,十六烷基三甲基溴化铵,冰醋酸,乙酸钠,硼酸,邻苯二胺,碘化钾,氧化砷,碳酸氢钠,2,6-二氯靛酚钠,盐酸(国药集团化学试剂有限公司),硫酸(株洲磺化玻有限公司),偏磷酸(天津市科密欧化学试剂有限公司),高岭土,苯甲酸(上海山浦有限公司),硫酸铜(天津市博迪化工有限公司)。实验所用试剂均为分析纯;实验所用水均为二次蒸馏水。
1.1.3 材料
1.1.3.1 维生素C 标准溶液,精密称定1.0g维生素C标准品,溶解,定容至1000mL容量瓶,得到1.0mg/mL维生素C标准溶液,备用。
1.1.3.2 果蔬样品 称水果(橙子,草莓等)样品各 100 g 加 100 mL偏磷酸-乙酸溶液,倒入研钵内研成匀浆。用百里酚蓝指示剂调试匀浆酸碱度,若呈红色,立即用偏磷酸-乙酸溶液稀释;若呈黄色或蓝色则用偏磷酸-乙酸-硫酸溶液稀释。用干净纱布过滤一次,再用高速冷冻离心机离心取上清液,备用。
2 结果
通过直接碘量法、2,6-二氯酚靛酚法、紫外分光光度法、荧光分光光度法(邻苯二胺体系、苯甲酸体系),从精密度、准确度、检测限、回收率考察VC含量的测定方法,完善药典和食品中维生素C含量测定的国家标准,指导合理摄入维生素C,正确推广健康饮食。
2.1 直接碘量法 维生素C烯二醇基具有还原性,能被I2定量地氧化成二酮基,因而可用I2标准溶液直接测定。C6H8O6+I2= C6H6O6+2HI
2.1.1 方法 精确量取维生素C标准溶液1.00mL,加入10mL HAc(2mol/L)和1mL淀粉指示剂(10g/L),立即用0.05mol/Ll I2标准滴定溶液滴定至稳定的浅蓝色,即为终点。计算维生素C浓度。
2.1.2 结果性染料,可将还原态的维生素C氧化成脱氢维生素C,而染料本身从深蓝色被还原成无色的衍生物。2,6-二氯酚靛酚钠在酸性条件下呈红色。在滴定终点之前,滴下的2,6-二氯酚靛酚钠立即被还原成无色。当溶液从无色转变成微红色时,即为滴定终点。

表1 直接碘量法
2.2.1 方法 取2,6-二氯酚靛酚230mg,加入适量4%HCl使其溶解,加210mgNaHCO3,500 mL蒸馏配成标准溶液,使用前过滤,取续滤液。精确量取标准维生素C标准溶液5.00 mL,加入10 mL 2mol/L HAc 至锥形瓶中,用2,6-二氯酚靛酚标定,直至出现微红色30秒不退色为终点。计算VC的含量
2.2.2 结果

表2 2,6-二氯酚靛酚法
2. 3 紫外分光光度法 维生素 C 在紫外区 246.0nm 处有最大吸收,并且线性良好因此可以采用紫外分光光度法进行测量。
2.3.1 方法
2.3.1.1 建立标准曲线 取维生素C标准溶液10.00mL,用10%HCl定容至100.00mL,得维生素C标准储备液,从中取0.00mL、1.00mL,2.00mL,3.00mL,4.00mL,5.00mL,6.00mL维生素C标准储备液,定容至50.00mL,以蒸馏水做参比,在246.0nm处测定吸光度,绘制吸光度A与浓度C的标准曲线。
2.3.1.2 VC含量的测定 精确量取维生素C标准样品溶液1.00mL,用10%HCl定容至100.00mL,以蒸馏水做参比,波长246.0nm处测定吸光度。
2.3.2 结果

图1 紫外分光光度法标准曲线

表3 紫外分光光度法
2.4 荧光分光光度法-邻苯二胺体系 维生素C样品在酸性条件下经活性炭氧化成脱氢抗坏血酸,与邻苯二胺反应生成有荧光的喹唔啉,测定喹唔啉荧光值,计算维生素 C 的含量。
2.4.1 方法
2.4.1.1 建立标准曲线 精密量取10.00mL维生素C标准液至100.00mL容量瓶用蒸馏水稀释至刻度,加入2g活性炭,过滤,收集续滤液,作为标准氧化储备液,备用,精密量取1.00mL,2.00 mL,3.00 mL,4.00 mL标准氧化储备液,于50mL容量瓶中,加入5mL硼酸-醋酸钠(3%),用蒸馏水定容至50.00mL,摇匀,得标准氧化液,取上述标准氧化液5.00mL,加入邻苯二胺溶液(0.02%)5mL,混合反应35分钟,测定荧光强度。以不含邻苯二胺作为空白对照液,以浓度为横坐标、荧光强度为纵坐标建立标准曲线。
2.4.1.2 含量的测定 精确量取10.00mL维生素C标准样品液置100.00mL容量瓶,用水稀释至刻度,摇匀,加入2g活性炭,过滤,弃去初滤液,收集滤液,作为标准样品氧化储备液,备用。取1.00mL标准样品氧化储备液置于50mL容量瓶中,加入5mL硼酸-醋酸钠,用水稀释至刻度,摇匀,从中取1.00mL,加入邻苯二胺溶液5mL,混合反应35分钟,测定荧光强度,以不含邻苯二胺作为空白对照液。
2.4.2 结果

表4 荧光分光光度法-邻苯二胺体系
2.5 荧光分光光度法-苯甲酸体系
2.5.1 原理 维生素 C经Cu2+氧化为脱氢抗坏血酸,与苯甲酸及十六烷基三甲基溴化铵产生荧光协同增敏作用。
2.5.2 方法
2.5.2.1 建立标准曲线 精密量取维生素C标准溶液5ml,加入适量10%盐酸溶液,加蒸馏水定容至
100.00 mL,得到5μg/mL VC稀释液。取5个50mL容量瓶,加入1.20mL硫酸铜(0.2%)、4.00mL十六烷基溴化铵溶液(0.06%)、4.00mL苯甲酸(0.01%),再向5个容量瓶中依次加入1.00mL,2.00mL,3.00mL,4.00mL,5.00 mL 维生素C稀释液后加入10.00mL磷酸氢二钠-磷酸氢二钾缓冲溶液,定容,摇匀。在35℃恒温水浴加热
30min,在发射波长417nm处测定荧光强度F,无VC试剂为空白F0,记为△F=F-F0。
2.5.2.2 含量的测定 精确量取维生素C标准样品溶液10mL,加入适量10%HCl,于100mL容量瓶中,定容,摇匀,得维生素C标准样品储备液。在50mL的容量瓶中加入1.20mL硫酸铜、4mL十六烷基溴化铵溶液、4mL苯甲酸,一定体积维生素C标准样品储备液,10mL磷酸氢二钠-磷酸氢二钾缓冲溶液,定容。在35℃恒温水浴加热30min,冷却至室温,在发射波长417nm处测定荧光强度F,无VC试剂为空白F0,记为△F=F-F0。
2.5.3 结果
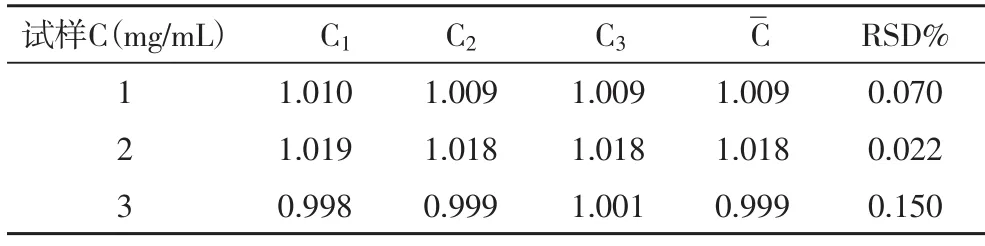
表5 荧光分光光度法-苯甲酸体系
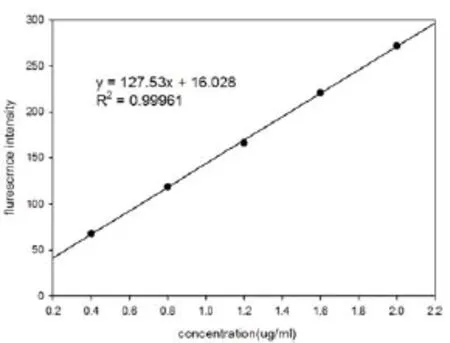
图2 荧光分光光度法-苯甲酸体系

图3 荧光分光光度法-苯甲酸试验
2.6 橙子中VC含量测定,优选测定方法

表6 五种方法测定橙子比较结果(n=3)
经过五种方法的比较,我们发现荧光法(苯甲酸)体系测定VC含量准确度高,由此构建荧光法(苯甲酸)体系进行方法学验证。
2.7 荧光法(苯甲酸)体系方法学验证。
2.7.1 稳定性试验 将体系放置不同的时间进行测定。当放置 15min时,体系的荧光强度达到最大值并趋于稳定。

图4 稳定性试验
2.7.2 共存离子干扰试验 测定浓度为 2μg / m L的维生素 C时,当允许误差在5%以内时,共存离子的允许量如表7所示。

表7 共存离子允许量
2.7.3 工作曲线、线性范围、检出限 配制浓度为0.00,0.01,0.02,0.08,0.10,0.50,5.00,6.00,7.00,8.00,9.00,10.00,12.00,14.00 u g/mL的系列维生素C标准工作溶液。按实验方法进行测定,以荧光强度F对维生素C的浓度。(μg/mL)进行线性回归,结果见图5。维生素C浓度在0.02 ~8.0 μg /mL范围内,与荧光强度呈良好的线性关系,线性回归方程为F = 124.18c+ 14.63相关系数为0 9998;检出限为0.0065μg/mI。
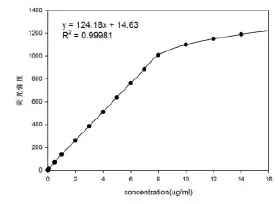
图5 工作曲线
2.7.4 精密度试验 对3.0 μg /mL的维生素C标准工作溶液测定6次,测定结果见表8。由表8可知,其相对标准偏差为 0. 12%。

表8 精密度试验结果
2.7.5 测定果蔬中VC 用荧光分析法(苯甲酸体系)以下五种果蔬中的维生素C进行测定,实验结果见表9。
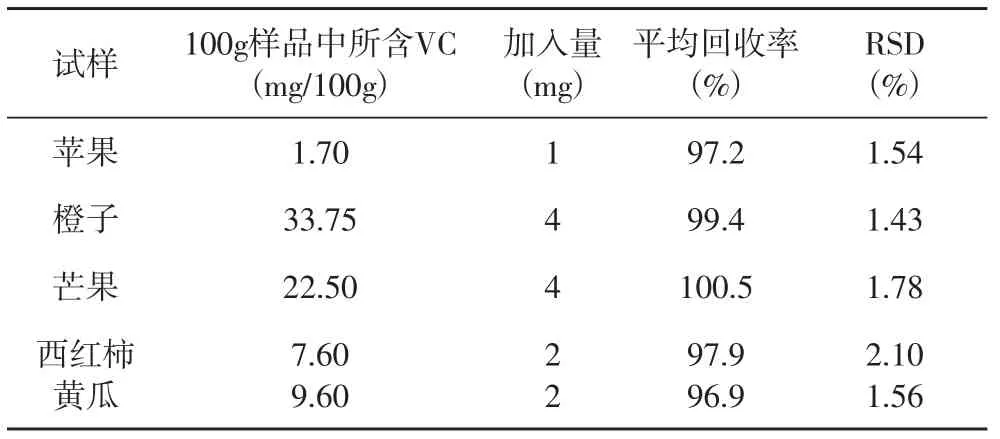
表9 果蔬中VC测量结果
3 讨论
通过用多种方法对比和分析同一批次的维生素C含量,发现在苯甲酸体系中,荧光分光光度法测定维生素C具有操作简单,准确度高,检出限低,专属性强等优点,优选为维Vitamin C 测定方法,该法可应用于水果、蔬菜和药物中维生素C的检测,适于推广。
[1] 汪东风. 食品化学 [M]. 北京: 化学工业出版社, 2009 .
[2] Fenech M. Chromosomal damage rate, aging and dims[J]. Acad Sci, 1998: 854: 23-36.
[3] Jacobson EL, Shieh WM, Huang AC. Maping the role of NAD metabolism in prevention and treatment of carcinogenesis[J]. Mol Cell Biochem, 1999, 193: 59-74.
[4] 张健, 曹恩华, 秦静芬, 等. 抗氧化剂对DNA损伤的保护作用机制的研究[J]. 生物物理学报, 1997, 13(1): 123-126.
[5] 田晓华, 顾景范, 孙存普. 氧化应激与抗氧化维生素的作用[J]. 国外医学卫生学分册, 1996, 23(4): 229-233.
[6] 国家药典委员会编. 中华人民共和国药典[M]. 化学工业出版社, 2010, 901.
[7] 孙振艳, 赵中一, 郭小慧, 等. 荧光分析法测定维生素C[J]. 化学分析计量, 2006, 4: 18-20.
[8] 李润丰, 赵希艳, 高亚弟.2, 6-二氯靛酚反滴定法测定红色果蔬中还原型VC[J]. 营养学报, 2012, 05: 507-509.
[9] 王佳露, 刘军. 极谱法检测芒果中的维生素C[J]. 齐齐哈尔医学院学报, 2008, 22: 2748.
[10] L. Casella, 朱仕兄. 利用过氧化物酶分析果蔬维生素C的快速酶法[J]. 四川果树, 1993, 02: 43-45.
The preferentialvitamin Canalysis methods apply to fruits and vagetables
Chen Rong, Tang Bi-xi, Li Min, Zhou Hong-yan, Zhang Pei, Zhu Yuan-zhi, He Chun-lian
(Medical College, Hunan Normal University, Changsha 410006, China)
Objective To find a accurate and easier acceptable analysis methods, perfecting the pharmacopoeia and the national standard for the determination of vitamin C content in food, and to guide the reasonable intake of vitamin C, right to promote a healthy diet. Methods Comparing with five kinds of method systemly for determination of vitamin C content[2, 6-Dichlorophenol indophenol method, uv spectrophotometry, fluorescence spectrophotometry(o-phenylendiamine), fluorescence spectrophotometry(benzoic acid)], and analysis the advantages and disadvantages of each method. Results The results shows that 2, 6-Dichlorophenol indophenol method, uv spectrophotometry, fluorescence spectrophotometry(o-phenylendiamine), fluorescence spectrophotometry(benzoic acid)measured the content of vitamin C in the vitamin C absolute error were 0.095mg/mL, 0.094mg/mL, 0.357mg/mL, 0.120mg/mL, 0.009μg/mL Conclusion The method of the most suitable for determination of vitamin C is fluorescence spectrophotometry(benzoic acid system), The vitamin Canalysis methods easy to be applied to fruits and vagetables.
vitamin C; fluorescence spectrophotometry; uv spectrophotometry; 2, 6-Dichlorophenol indophenol method
R652.1
A
1673-016X(2017)02-0186-04
2016-12-10
教育厅重点项目(NO.12A085);湖南师范大学大学生创新实验通讯作者: 何纯莲,E-mail:chunlianhe68@163.com

