气相色谱法测定车用汽油中含氧化合物和苯胺类化合物
李长秀
(中国石油化工股份有限公司石油化工科学研究院, 北京 100083)
研究论文
气相色谱法测定车用汽油中含氧化合物和苯胺类化合物
李长秀*
(中国石油化工股份有限公司石油化工科学研究院, 北京 100083)
利用中心切割技术和双毛细管色谱柱系统,采用两次进样的方式,建立了气相色谱测定车用汽油中含氧化合物和苯胺类化合物的分析方法。第一次进样分析,组分首先进入非极性DB-1色谱柱(30 m×0.32 mm×1.0 μm),按沸点由低到高的顺序分离,通过电磁阀切换将沸点小于2-己酮的组分切割至强极性GS-OxyPLOT色谱柱(10 m×0.53 mm×10 μm)或CP-Lowox色谱柱(10 m×0.53 mm×10 μm),其余重烃组分通过阻尼柱进入FID检测器。在GS-OxyPLOT或CP-Lowox色谱柱上,烃类组分与含氧化合物分离并进入检测器检测,消除了大量的烃类组分对含氧化合物测定的影响。第二次进样分析,设定电磁阀切换时间为间-甲基苯胺从非极性色谱柱流出的时间,苯胺类化合物在GS-OxyPLOT或CP-Lowox色谱柱上与烃类和含氧化合物分离并进入检测器检测。以乙二醇二甲基醚为内标化合物进行内标法定量。实现了在一套系统上同时测定车用汽油中添加的甲基叔丁基醚(MTBE)、甲醇、甲缩醛、乙酸仲丁酯、乙酸乙酯、苯胺、邻/间/对-甲基苯胺和N-甲基苯胺的含量,各组分的检测范围为0.01%~10%(质量分数),回收率为86.0%~102.6%。该法可以为车用汽油的质量控制提供有效的检测手段。
气相色谱;中心切割;含氧化合物;苯胺类化合物;甲缩醛;车用汽油
车用汽油中会加入一定量的含氧化合物,如甲基叔丁基醚(methyltert-butyl ether, MTBE)等,以提高车用汽油的辛烷值。目前国家对车用汽油的质量控制日趋严格,在GB 17930-2016 《车用汽油》国家标准中对车用汽油中含氧化合物的含量有明确规定,同时也明确指出不得人为加入甲缩醛(又名二甲氧基甲烷,methylal/dimethoxymethane)和苯胺类化合物。甲缩醛、苯胺类和酯类化合物被称为非常规添加组分,这些组分会对车用汽油的使用性能造成影响,如甲缩醛对橡胶有较强的溶解性,会对汽车橡胶密封圈造成影响;乙酸仲丁酯(sec-butyl acetate, SBA)和苯胺类化合物可以在一定程度上提高汽油的辛烷值,但会影响汽油的氧化安定性。
目前,国内外还未见采用气相色谱法同时测定车用汽油中甲缩醛、苯胺类和酯类化合物的文献报道。国内车用汽油中含氧化合物通常采用NB/SH/T 0663-2014 《汽油中某些醇类和醚类化合物的测定 气相色谱法》或SH/T 0720-2002 《汽油中含氧化合物测定法(气相色谱及氧选择性火焰离子化检测器法)》进行测定,但其均存在甲缩醛或乙酸仲丁酯与醇醚化合物共流出或分离不完全而无法准确定量的问题。赵彦等[1]利用现有的测定汽油中苯含量的双色谱柱系统,建立了测定乙酸乙酯、碳酸二甲酯和乙酸仲丁酯的分析方法,但该方法无法同时测定甲缩醛和苯胺类化合物;钟少芳等[2]采用强极性毛细管色谱柱测定汽油中的苯胺类化合物,但实际应用中发现部分芳烃组分会与个别苯胺类化合物共流出而影响定量结果的准确性。有文献报道采用气相色谱-质谱法检测汽油中甲缩醛等组分[3],采用液液萃取结合气相色谱-质谱法测定汽油中苯胺类化合物[4],但这两种方法采用的仪器设备成本较高,且样品需要预处理,操作过程复杂,不利于方法的推广。
目前已有文献[5-8]报道采用带有中心切割的双柱系统测定汽油中的微量含氧化合物,将采用第一根非极性柱无法分离的烃类和含氧化合物切割至第二根对含氧化合物有较强保留能力的色谱柱上,实现含氧化合物和烃类组分的有效分离和检测。但这些报道主要针对汽油中微量的醇、醚及酮类化合物,没有涉及甲缩醛、酯类和苯胺类化合物的测定。任成龙等[9]采用类似的方法测定了液化石油气中的微量甲缩醛;张继东等[10]采用第一根为极性柱、第二根为非极性柱的中心切割-双柱系统测定了汽油中的醇醚类含氧化合物;费旭东等[11]在类似的系统上测定了汽油中的酯类、醚类和甲缩醛,但需要对每一组分设定不同的阀切换时间,操作实用性受到限制;高枝荣等[12]采用了第一根为非极性柱、第二根为极性柱的双柱系统,同样通过为每个组分设定不同的切阀时间,建立了测定汽油中甲缩醛、乙酸仲丁酯等酯类和N-甲基苯胺(N-methyl aniline)的方法,但没有测定其他苯胺类化合物;闻环等[13]采用第一根为非极性柱、第二根为对含氧化合物有特殊保留的强极性柱的双柱系统,建立了测定汽油中甲缩醛的方法,并与汽油中常见的13种醇醚化合物获得了良好分离,但没有涉及酯类和苯胺类化合物的测定。
本文利用中心切割-双毛细管色谱柱系统,采用两次进样的方式,建立了气相色谱分离车用汽油中含氧化合物和苯胺类化合物的分析方法,并实现了车用汽油中MTBE、甲醇、甲缩醛、乙酸仲丁酯、乙酸乙酯、苯胺、邻/间/对-甲基苯胺(o/m/p-methyl aniline)和N-甲基苯胺的定量分析,且样品无需预处理,操作简便,便于推广应用。
1 实验部分
1.1 仪器和试剂
Agilent 7890A气相色谱仪(配有双氢火焰离子化检测器(FID)、Deans Switch中心切割组件、自动进样器和Agilent ChemStation色谱工作站)、DB-1色谱柱(30 m×0.32 mm, 1.0 μm)、GS-OxyPLOT色谱柱(10 m×0.53 mm, 10 μm)和CP-Lowox色谱柱(10 m×0.53 mm, 10 μm)均购自美国Agilent公司。
甲醇(纯度99.0%)、乙酸乙酯(纯度99.0%)购自北京化工厂;MTBE(纯度99.0%)购自北京国药集团试剂公司;甲缩醛(纯度98.0%)购自上海阿达玛斯试剂公司;乙酸仲丁酯(纯度98.0%)购自北京百灵威科技有限公司;苯胺类化合物包括苯胺(纯度98.0%)、N-甲基苯胺(纯度98.0%)、邻/间/对-甲基苯胺(纯度98.0%)均购自美国Fluka公司;内标物乙二醇二甲基醚(dimethoxy-ethane, DME,纯度99.5%)、2-己酮(2-hexanone,纯度99.5%)购自上海阿拉丁试剂公司;其他用于定性的试剂包括乙醇、异丙醇、正丙醇、异丁醇、仲丁醇、叔丁醇、叔戊醇、甲基叔戊基醚(methyltert-amyl ether, TAME)、二异丙醚(diisopropyl ether, DIPE)和溶剂异辛烷、正壬烷、二甲苯均为分析纯。
1.2 色谱系统的建立
双毛细管色谱柱系统连接的示意图见图1。系统包含2根色谱柱,色谱柱1为非极性DB-1色谱柱,一端与色谱进样口相连,另一端与中心切割组件的入口相连;中心切割组件的两个出口分别与强极性色谱柱2(GS-OxyPLOT或CP-Lowox色谱柱)及阻尼柱相连接,色谱柱2和阻尼柱的出口分别连接两个FID。当汽油样品注入色谱系统后,首先按图1a所示,将电磁阀设定为开(ON),汽油样品中的组分经过色谱柱1,并按沸点由低到高顺序分离后进入色谱柱2,当沸点小于2-己酮的烃类和非烃组分进入色谱柱2后,按图1b所示,将电磁阀设定为关(OFF),使沸点高于2-己酮的组分流出色谱柱1后流经阻尼柱进入FID 1进行检测。在色谱柱2上沸点小于2-己酮的烃类组分和含氧化合物实现分离,并进入FID 2进行检测,从而消除烃类组分对含氧化合物测定的影响。随后进行第二次进样分析,当甲基苯胺全部从色谱柱1流出时,对电磁阀进行切换,苯胺和甲基苯胺与烃类化合物切割至色谱柱2以进一步分离,并进入FID 2进行检测。
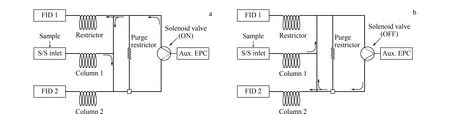
图 1 色谱系统连接示意图Fig. 1 Diagrams of the chromatographic systemsa. solenoid valve ON, components elute from column 1 into column 2; b. solenoid valve OFF, components elute from column 1 into restrictor. S/S Inlet: split/splitless inlet; Aux. EPC: auxiliary carrier supplied by electric pneumatic pressure control.
1.3 分析条件
色谱柱1(预切柱): DB-1色谱柱(30 m×0.32 mm×1.0 μm);色谱柱2(分析柱): GS-OxyPLOT(10 m×0.53 mm×10 μm)或CP-Lowox色谱柱(10 m×0.53 mm×10 μm);汽化室温度:250 ℃;检测器温度:280 ℃;升温程序:初始温度100 ℃,保持5 min,以5 ℃/min升温至210 ℃,保持8 min;载气:N2;恒压模式;柱前压:68.95 kPa;压力控制模块(PCM)压力:29.51 kPa;分流比:80∶1;进样量:0.2 μL;氢气流量:30 mL/min;空气流量:350 mL/min;尾吹气(N2)流量:25 mL/min。
电磁阀切换时间:第一次进样分析含氧化合物,0.1 min电磁阀打开,4.0 min电磁阀关闭。第二次进样分析苯胺类化合物,采用GS-OxyPLOT色谱柱时,0.1 min电磁阀打开,11.0 min电磁阀关闭;采用CP-Lowox色谱柱时,3.2 min电磁阀打开,11.0 min电磁阀关闭。
2 结果和讨论
2.1 色谱柱的选择
本实验考察了不同长度(15 m、30 m和50 m)的非极性DB-1色谱柱对分离效果的影响。结果显示,采用15 m色谱柱时,沸点小于2-己酮的组分和其他组分达不到有效分离;采用50 m色谱柱时,沸点与2-己酮接近的烃类组分在第一根色谱柱上的保留时间过长,进入第二根极性柱时在某些含氧化合物后出峰,对含氧化合物的分离产生干扰。因此最终选择30 m的DB-1色谱柱作为预切柱。分析柱一般采用强极性色谱柱,与聚乙二醇为固定相的极性色谱柱相比,CP-Lowox和GS-OxyPLOT色谱柱具有更强的极性,对含氧化合物具有更强的保留能力,因此本实验选择CP-Lowox和GS-OxyPLOT色谱柱作为分析柱。
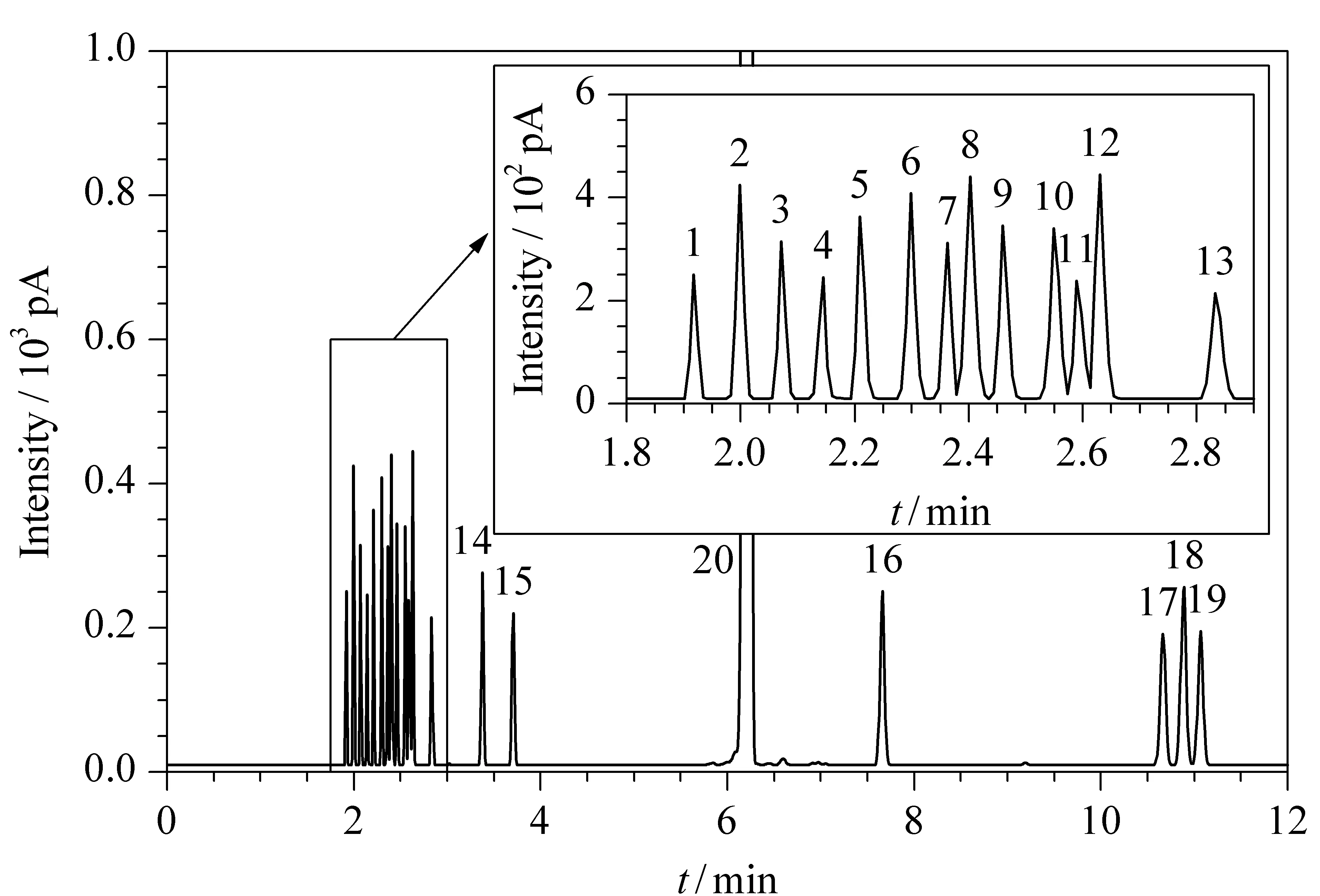
图 2 采用DB-1色谱柱时含氧化合物和苯胺类化合物的色谱图Fig. 2 Chromatograms of the oxygenates and anilines by DB-1 columnConditions: solenoid valve stays OFF in 0.1 min, all the components were eluted through the restrictor to FID 1.Peaks: 1. methanol; 2. ethanol; 3. iso-propanol; 4. methylal and tert-butanol; 5. n-propanol; 6. methyl tert-butyl ether (MTBE); 7. sec-butanol; 8. ethyl acetate and diisopropyl ether; 9. iso-butanol; 10. tert-amyl alcohol; 11. dimethoxy-ethane (DME); 12. n-butanol; 13. methyl tert-amyl ether (TAME); 14. sec-butyl acetate (SBA); 15. 2-hexanone; 16. aniline; 17. N-methyl aniline; 18. o/p-methyl aniline; 19. m-methyl aniline; 20. nonane (solvent).
2.2 阀切换时间的确定
配制含有2%(质量分数)的含氧化合物和苯胺类化合物的正壬烷溶液,并对其进行分析,整个分析过程中电磁阀始终处于关闭状态。当所有组分通过色谱柱1后,经与之相连的阻尼柱进入FID 1进行检测,得到的组分在色谱柱1上的色谱图见图2。可以看出,当2-己酮流出时,样品中的其他含氧化合物已全部从色谱柱1流出。因此在分析含氧化合物时,将电磁阀的切换时间设为2-己酮全部流出时的时间,这时保留时间大于2-己酮的重烃组分不进入色谱柱2。
由于苯胺类化合物的沸点远大于2-己酮的沸点,如果在间-甲基苯胺全部流出色谱柱1后切换电磁阀,此时汽油中大部分高沸点烃类组分已进入色谱柱2,并会与某些含氧化合物共流出或在含氧化合物之后出峰,对含氧化合物的测定产生干扰。因此,采用两次进样分析的方式,第二次进样分析时,设定在间-甲基苯胺全部从色谱柱1流出后切换电磁阀。在色谱柱1上与苯胺类化合物沸点相近的烃类组分的极性小于苯胺类化合物,因此,其在色谱柱2上先于苯胺类化合物流出,不会干扰苯胺类化合物的测定。
2.3 组分定性
用异辛烷-二甲苯(1∶1, v/v)混合溶液配制含质量分数为1%的待测含氧化合物和苯胺类化合物的混合溶液。在1.3节的色谱条件下,以GS-OxyPLOT色谱柱为分析柱,对该混合溶液进行分析。沸点小于2-己酮的组分切割至GS-OxyPLOT色谱柱上的分离情况见图3a,沸点大于2-己酮的组分通过阻尼柱进入FID 1检测器的出峰情况见图3b。第二次进样分析时,苯胺类化合物的色谱图见图4。
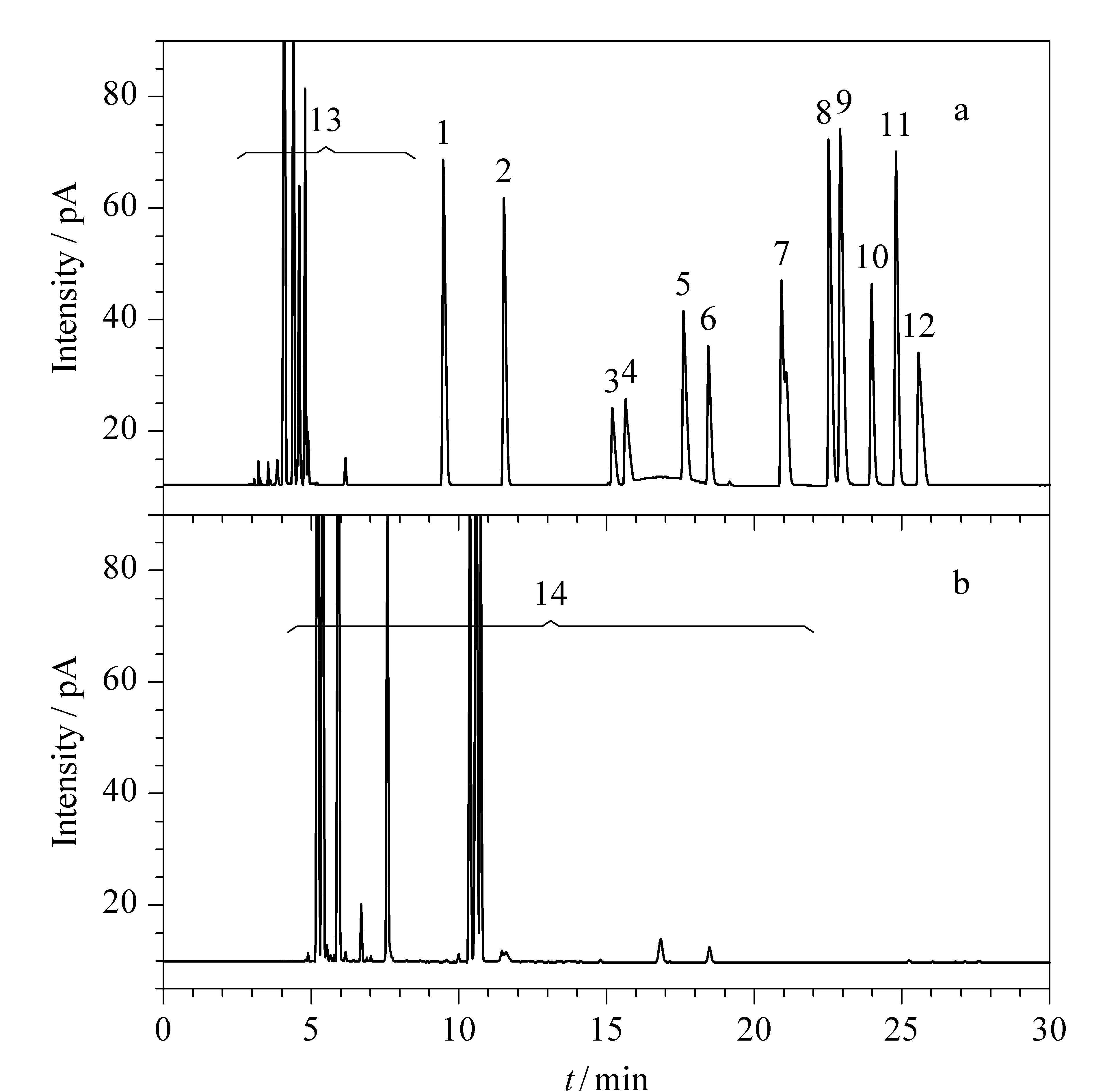
图 3 采用GS-OxyPLOT柱分离含氧化合物的色谱图(第一次进样)Fig. 3 Chromatograms of the oxygenates by GS-OxyPLOT column (first run)a. signal of FID 2 by GS-OxyPLOT column; b. signal of FID 1 by restrictor.Peaks: 1. MTBE; 2. TAME; 3. methanol; 4. methylal; 5. ethyl acetate; 6. ethanol; 7. iso/n-propanol; 8. SBA; 9. iso/sec/tert-butanol; 10. n-butanol; 11. tert-amyl alcohol; 12. DME (internal standard); 13. light hydrocarbons; 14. heavy hydrocarbons.
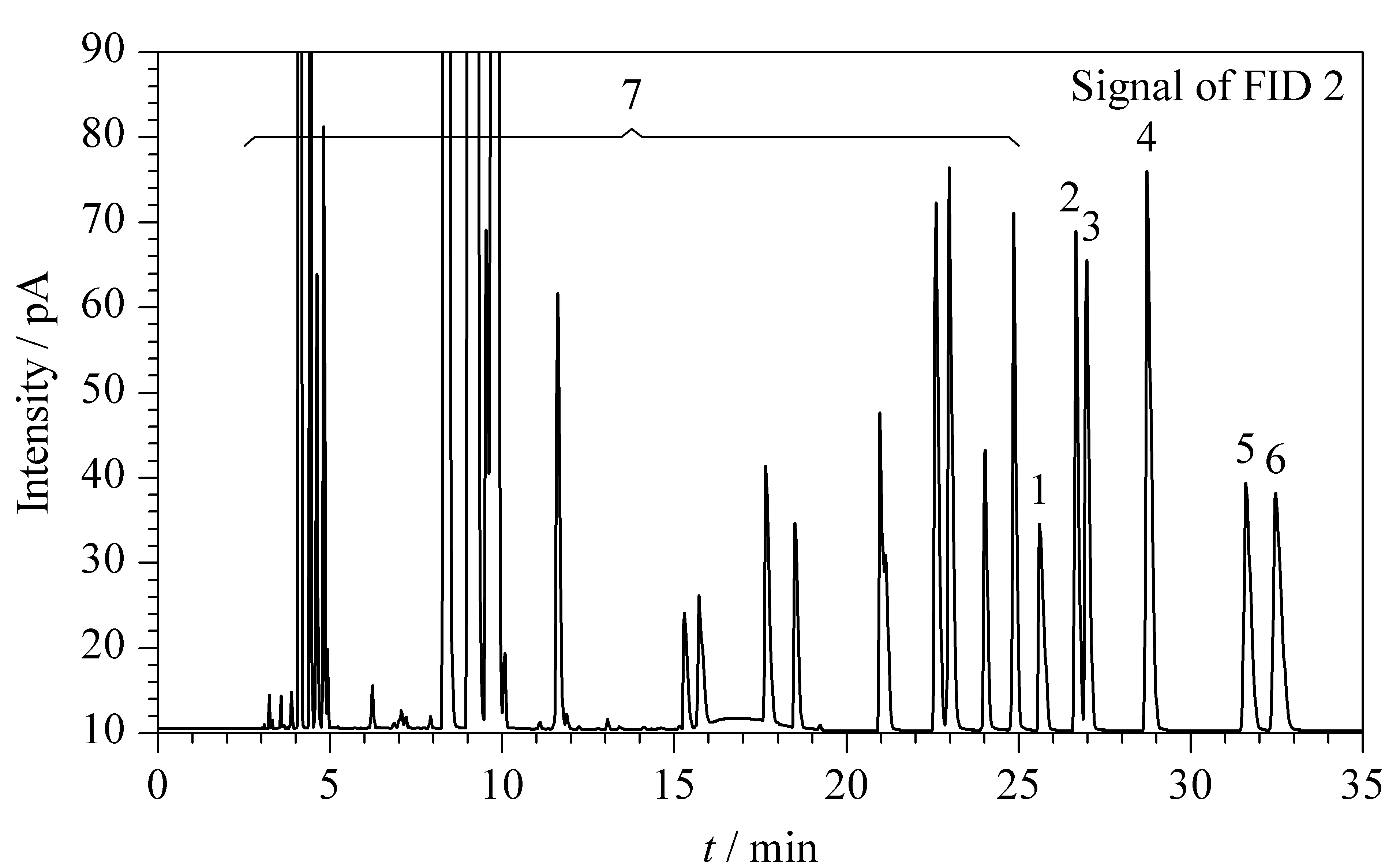
图 4 采用GS-OxyPLOT柱分离苯胺类化合物的色谱图(第二次进样)Fig. 4 Chromatogram of the anilines by GS-OxyPLOT column (second run)1. DME (internal standard); 2. N-methyl aniline; 3. aniline; 4. o-methyl aniline; 5. m-methyl aniline; 6. p-methyl aniline; 7. hydrocarbons and oxygenates.
采用CP-Lowox色谱柱分析含质量分数为1%的待测含氧化合物和苯胺类化合物的混合溶液,其色谱图分别见图5和图6。采用CP-Lowox色谱柱时,乙二醇二甲基醚与N-甲基苯胺为共流出峰,因此选择2-己酮为内标物。第二次进样时,在乙酸仲丁酯即将从色谱柱1流出前(3.2 min),将阀设为ON,在间-甲基苯胺完全从色谱柱1流出后(11.0 min),将阀设为OFF,以阻止碳四正构醇和异构醇进入色谱柱2,从而消除可能对2-己酮色谱峰产生的干扰。
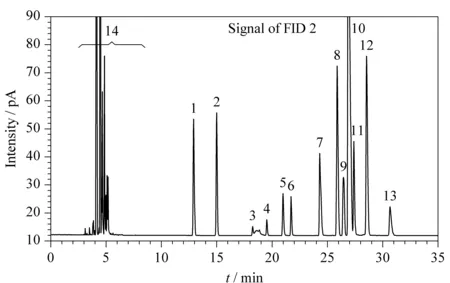
图 5 采用CP-Lowox柱分离含氧化合物的色谱图(第一次进样)Fig. 5 Chromatogram of the oxygenates by CP-Lowox column (first run)1. MTBE; 2. TAME; 3. methanol; 4. methylal; 5. ethyl acetate; 6. ethanol; 7. iso/n-propanol; 8. SBA; 9. iso/sec/tert-butanol; 10. 2-hexanone (internal standard); 11. n-butanol; 12. tert-amyl alcohol; 13. DME; 14. light hydrocarbons.
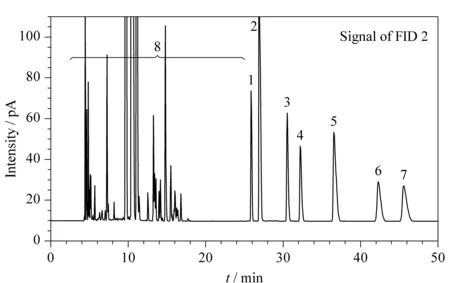
图 6 采用CP-Lowox柱分离苯胺类化合物的色谱图(第二次进样)Fig. 6 Chromatogram of the anilines by CP-Lowox column (second run)1. SBA; 2. 2-hexanone (internal standard); 3. N-methyl aniline; 4. aniline; 5. o-methyl aniline; 6. m-methyl aniline; 7. p-methyl aniline; 8. hydrocarbons and oxygenates.
2.4 酯类化合物的分离
由于GS-OxyPLOT和CP-Lowox色谱柱为多孔层毛细管色谱柱,该色谱柱的分离能力受环境的影响较为明显,如果长时间在低温下放置,色谱柱会吸收水分,使其对含氧化合物的保留能力下降。新的色谱柱使用前必须在300 ℃下充分老化;日常使用中,在进样前也应将色谱柱置于方法的最终温度(210 ℃)短暂老化。由于酯类化合物中含有两个氧原子,因此在色谱柱上表现出较强的保留,同时酯类化合物的保留情况随色谱柱的老化和使用情况而发生改变,因此在定性时必须根据酯类化合物标准样品的保留时间进行确认。
2.5 利用中心切割消除组分测定的干扰
本方法采用可以用于中心切割的Dean Switch色谱系统,其优点是可以对某个色谱峰进行准确切割。因此,可以根据组分在色谱柱1上的分离情况,选择对目标化合物进行准确切割,以消除其他组分可能对定量产生的干扰。可以根据图2所示的组分在色谱柱1上的保留时间来确定合适的阀切换时间,以实现某个组分的切割,消除组分间的干扰。
OxyPLOT色谱柱的柱容量较小,会引起高含量物质的色谱峰峰形明显前伸。而乙醇和乙酸乙酯、乙酸仲丁酯和碳四异构醇、N-甲基苯胺和苯胺的出峰时间十分接近,当乙醇、碳四异构醇、N-甲基苯胺的含量较高时,会使分离效果变差。
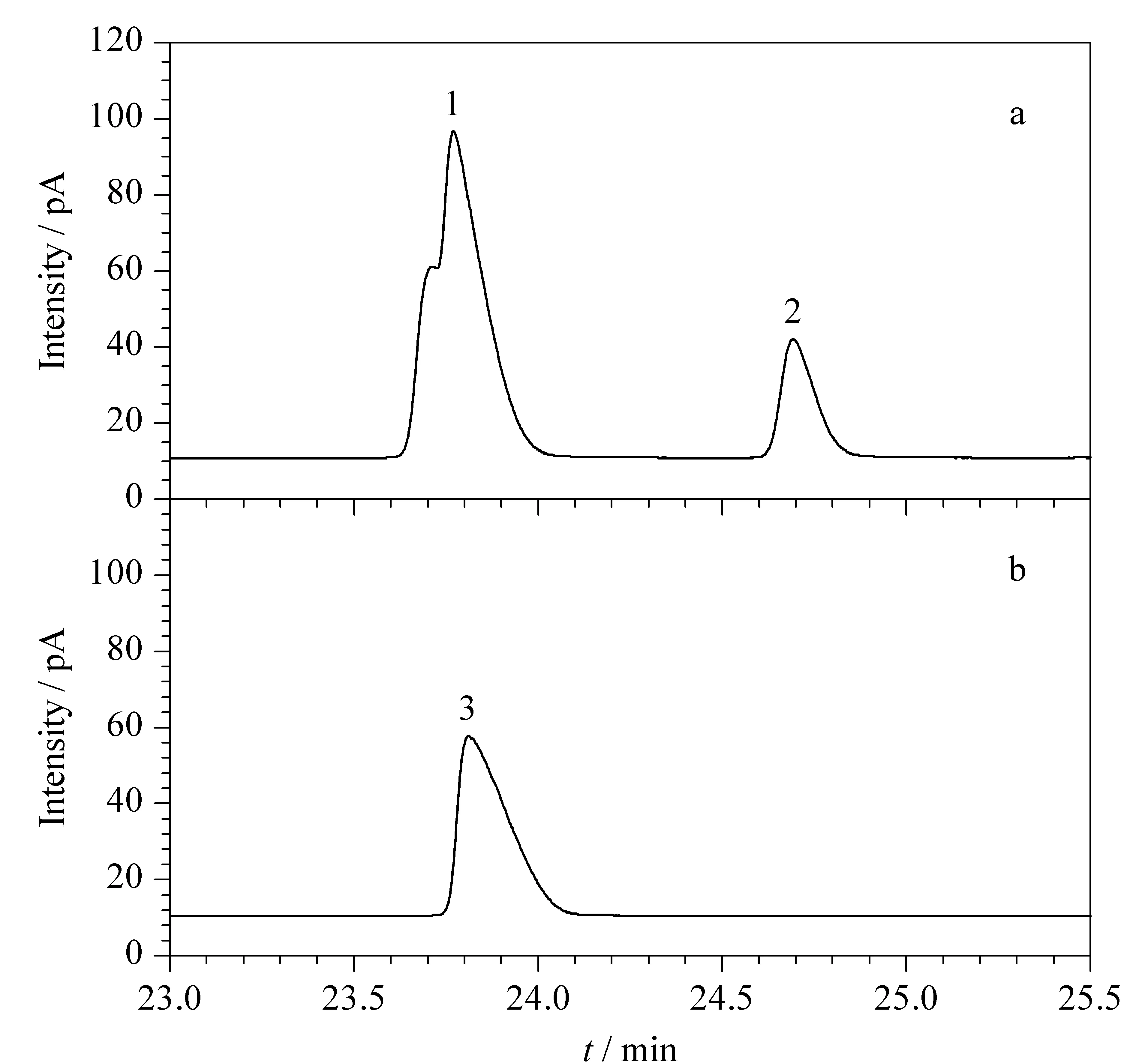
图 7 采用中心切割得到的乙酸仲丁酯的色谱图Fig. 7 Chromatograms of SBA by heart-cutConditions: a. 0.1 min solenoid valve ON, 4.0 min solenoid valve OFF; b. 3.1 min solenoid valve ON, 3.5 min solenoid valve OFF.Peaks: 1. SBA and iso/sec/tert-butanol; 2. n-butanol; 3. SBA.
以乙酸仲丁酯为例,当乙酸仲丁酯和碳四异构醇的分离较差,影响定量时,可以采用中心切割的方式。进样后,首先将电磁阀关闭,使组分流出色谱柱1后进入阻尼柱,根据图2中含氧化合物在色谱柱1上的保留时间,在乙酸仲丁酯从色谱柱1流出前将阀设为ON,当乙酸仲丁酯全部从色谱柱1流出,并进入色谱柱2后,将电磁阀设为OFF,此时乙酸仲丁酯进入色谱柱2,碳四异构醇进入阻尼柱,从而可以对乙酸仲丁酯进行准确的定量分析。当0.1 min电磁阀设为ON、4.0 min电磁阀设为OFF,碳四异构醇与乙酸仲丁酯均进入色谱柱2时的色谱图见图7a,碳四异构醇与乙酸仲丁酯分离不完全。在乙酸仲丁酯从色谱柱1流出前(3.1 min),将电磁阀设为ON;在乙酸仲丁酯全部流出色谱柱1时(3.5 min),将电磁阀设为OFF,此时只有乙酸仲丁酯进入色谱柱2,其色谱图见图7b。
当乙醇和乙酸乙酯、苯胺和N-甲基苯胺等物质在色谱柱2上难以达到基线分离时,也可以通过设定不同的切阀时间获得二者精确的峰面积。
2.6 线性关系
以异辛烷-二甲苯(1∶1, v/v)混合溶液为溶剂,采用称量法配制两个系列的混合标准溶液。第一个系列含有MTBE、甲醇、甲缩醛、乙酸乙酯、乙酸仲丁酯和苯胺,其中MTBE的质量分数分别为0.01%、0.1%、1.5%、7.5%和15.0%,其余5种物质的质量分数分别为0.01%、0.1%、1.0%、5.0%和10.0%;第二个系列含有N-甲基苯胺、邻-甲基苯胺和间-甲基苯胺,质量分数分别为0.01%、0.1%、1.0%、5.0%和10.0%。准确称量系列标准溶液的质量,加入5%(质量分数)的DME内标,混合均匀后按1.3节中采用GS-OxyPLOT色谱柱的条件进行分析,并记录色谱图。
以待测组分与内标物色谱峰面积的比值为纵坐标(Y)、待测组分与内标物的质量比为横坐标(X),根据最小二乘法绘制标准曲线。各组分在其线性范围内线性关系良好,相关系数(r2)均大于0.99(见表1)。
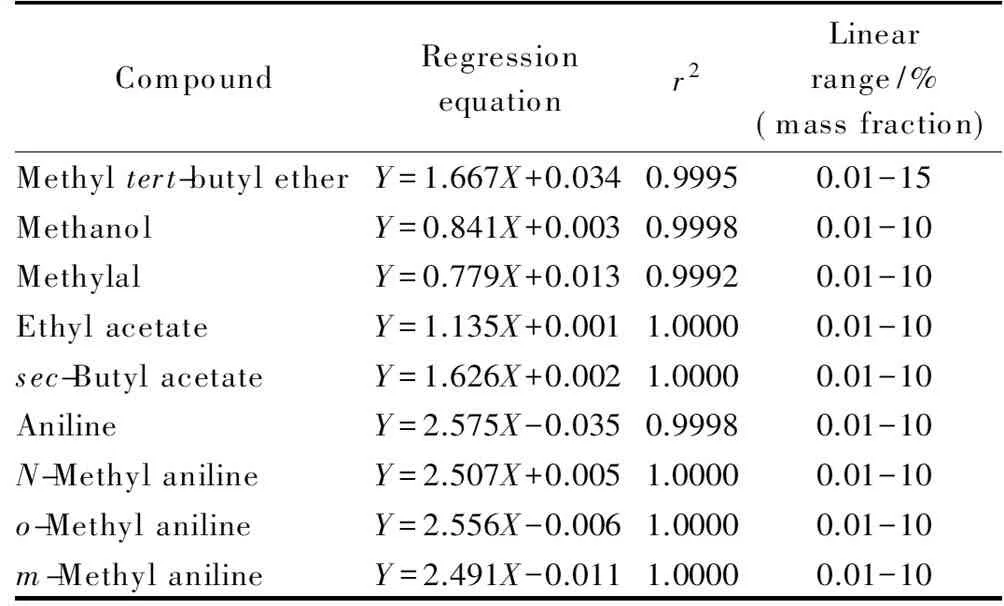
表 1 含氧化合物和苯胺类化合物的回归方程、相关系数和线性范围
Y: peak area ratio of the compound to the internal standard;X: mass ratio of the compound to the internal standard.
实际样品测定时,预先在样品中加入质量分数为5%的DME内标,并记录加入样品和内标物的质量,采用内标法计算待测组分的含量。由于对-甲基苯胺和间-甲基苯胺为同分异构体,在FID上有近似相等的质量响应因子,间-甲基苯胺的标准曲线也可用于对-甲基苯胺的定量计算。
2.7 回收率
取不含含氧化合物和苯胺类化合物的典型催化汽油和重整生成油,按体积比6∶4混合配制成汽油试样,分别加入不同含量的待测组分,制备得到3个不同质量分数的试样。准确称取一定质量的试样,加入质量分数为5%的DME内标,混合均匀后,按1.3节GS-OxyPLOT色谱柱的条件进行分析。结果表明,不同待测组分的加标回收率为86.0%~102.6%(见表2),满足一般分析要求。

表 2 实际样品中含氧化合物和苯胺类化合物的加标回收率
2.8 检出限
取2.6节配制的含氧化合物和苯胺类化合物质量分数为1%的两种混合标准溶液(MTBE质量分数为1.5%),采用异辛烷进行逐级稀释,考察方法的检出限(LOD,S/N=3)。甲醇的检出限为0.003%(质量分数),其他组分的检出限为0.002%(质量分数)。将定量限(LOQ)定义为检出限的5倍,甲醇的LOQ为0.015%(质量分数),其他组分的LOQ为0.01%(质量分数)。
3 结论
采用带有中心切割的双毛细管色谱柱系统,利用两次进样分析的方式,建立了气相色谱同时测定车用汽油中的含氧化合物和苯胺类化合物的方法。该方法可以用于车用汽油中甲基叔丁基醚、甲醇等常规含氧化合物的检测,也可为车用汽油中非常规添加组分的准确检测提供方案,为规范管理成品汽油的质量及打击劣质汽油的生产销售提供技术支撑。
[1] Zhao Y, Xu D Y, Lin H X, et al. Chinese Journal of Chromatography, 2014, 32(6): 662
赵彦, 徐董育, 林浩学, 等. 色谱, 2014, 32(6): 662
[2] Zhong S F, Wen H, Xu L, et al. Chinese Journal of Spectroscopy Laboratory, 2012, 29(6): 3564
钟少芳, 闻环, 徐玲, 等. 光谱实验室, 2012, 29(6): 3564
[3] Gao Z R, Li J W, Wang C. Petrochemical Technology, 2013, 42(2): 230
高枝荣, 李继文, 王川. 石油化工, 2013, 42(2): 230
[4] Zhao Y, Xu D Y, Huang K S, et al. Petroleum Processing and Petrochemicals, 2013, 44(2): 94
赵彦, 徐董育, 黄开胜, 等. 石油炼制与化工, 2013, 44(2): 94
[5] Huang S M, Huang H L. Guangdong Chemical Industry, 2007, 34(9): 103
黄山梅, 黄河柳. 广东化工, 2007, 34(9): 103
[6] Tong L, Guo X. Petrochemical Technology and Application, 2013, 31(4): 329
童玲, 郭星. 石化技术与应用, 2013, 31(4): 329
[7] Nan X Q, Ba H P. Petrochemical Technology, 2014, 43(1): 106
南秀琴, 巴海鹏. 石油化工, 2014, 43(1): 106
[8] Li C X, Wang Y M, Jin K. Petroleum Processing and Petrochemicals, 2016, 47(8): 102
李长秀, 王亚敏, 金珂. 石油炼制与化工, 2016, 47(8): 102
[9] Ren C L, Wen H, Zhong S F, et al. Guangdong Chemical Industry, 2014, 41(19): 199
任成龙, 闻环, 钟少芳, 等. 广东化工, 2014, 41(19): 199
[10] Zhang J D, Wei Y F, Chen J S, et al. ACTA Petrolei Sinica (Petroleum Processing Section), 2013, 29(3): 501
张继东, 魏宇锋, 陈俊水, 等. 石油学报(石油加工), 2013, 29(3): 501
[11] Fei X D, Wei Y F, Qiu F, et al. Modern Chemical Industry, 2015, 35(7): 178
费旭东, 魏宇锋, 邱丰, 等. 现代化工, 2015, 35(7): 178[12] Gao Z R, Li J W, Wang C. ACTA Petrolei Sinica (Petroleum Processing Section), 2014, 30(4): 712
高枝荣, 李继文, 王川. 石油学报(石油加工), 2014, 30(4): 712
[13] Wen H, Xu L, Lü H M, et al. Petrochemical Technology, 2015, 44(5): 630
闻环, 徐玲, 吕焕明, 等. 石油化工, 2015, 44(5): 630
Determination of oxygenates and anilines in motor gasoline by gas chromatography
LI Changxiu*
(ResearchInstituteofPetroleumProcessing,SINOPEC,Beijing100083,China)
A test method for the determination of oxygenates and anilines in motor gasoline was established using a gas chromatograph (GC) with heart-cut accessories and two chromatographic columns. A nonpolar DB-1 column (30 m×0.32 mm×1.0 μm) was used as the pre-column and a polar GS-OxyPLOT or CP-Lowox column (10 m×0.53 mm×10 μm) was used as the analysis column. In a test run, the gasoline sample was first separated according to the boiling points on the nonpolar column. By solenoid valve switching, the compounds of boiling points below 2-hexanone were cut to the GS-OxyPLOT or CP-Lowox column, whereas the other compounds were put through a restrictor to a flame ionization detector (FID). The oxygenates were separated from the hydrocarbons on the GS-OxyPLOT or CP-Lowox column and detected by the FID. When a second run was performed, the solenoid valve switching time was set at the point whenm-methyl aniline was all eluted from the nonpolar column into the polar column. Anilines were separated from hydrocarbons and oxygenates on the GS-OxyPLOT or CP-Lowox column. Dimethoxy-ethane was used as the internal standard for quantitation. Methyltert-butyl ether (MTBE), methanol, methylal,sec-butyl acetate, ethyl acetate, aniline,N-methyl aniline ando/m/p-methyl aniline in motor gasoline were detected and quantitated. The linear ranges were 0.01%-10% (mass fraction) with recoveries of 86.0%-102.6%. The method provides an effective way for quality control of motor gasoline.
gas chromatography (GC); heart-cut; oxygenates; anilines; methylal; motor gasoline
10.3724/SP.J.1123.2016.11018
2016-11-18
国家标准化管理委员会标准化项目(20131688-T-469).
Foundation item: National Standardization Project of Standardization Administration of the People’s Republic of China (No. 20131688-T-469).
O658
A
1000-8713(2017)05-0551-07
* 通讯联系人.Tel:(010)82368727,E-mail:licx.ripp@sinopec.com.

