粪便中血红蛋白和转铁蛋白联合检测在消化道出血诊断中的应用价值
张家超,薛国平,叶纪纲
(佛山市南海区第七人民医院,广东佛山528247)
粪便中血红蛋白和转铁蛋白联合检测在消化道出血诊断中的应用价值
张家超,薛国平,叶纪纲
(佛山市南海区第七人民医院,广东佛山528247)
目的观察分析粪便中血红蛋白和转铁蛋白联合检测在消化道出血诊断中的应用价值。方法选取2015年3月至2016年5月我院100例消化道出血患者作为研究对象,同期选择50例体检健康人作为对照组;采集三组对象的粪便标本,分别应用单克隆双抗体胶体金法检测粪便中血红蛋白(Hb)与转铁蛋白(Tf)。统计比较两种单独检测与联合检测的效果。结果转铁蛋白单独检测方式,上消化道出血患者的阳性检测率为50.00%,下消化道出血患者的阳性检测率为54.00%,健康人员的阳性检出率为2.00%;血红蛋白单一检测,上消化道出血患者的阳性检测率为48.00%,下消化道出血患者的阳性检测率为58.00%,健康人员的阳性检出率为0.00%;联合检测法检测上消化道出血阳性检出率为86.00%,下消化道出血的阳性检出率为88.00%,健康人员的阳性检出率为2.00%,联合检测方式诊断效果显著高于转铁蛋白以及血红蛋白单独检测方式,误诊率更低,差异具有统计学意义(P<0.05)。结论联合检测粪便中的血红蛋白与转铁蛋白能够大幅提高消化道出血的阳性检出率,同单一诊断相比,更具诊断价值。
粪便;血红蛋白;转铁蛋白;消化道出血
粪便隐血试验是内科临床中较为常见的一种检测技术,其广泛应用于消化道、胃肠道病变等内科疾病的诊断中,对消化道出血的诊断具有极其重要的价值[1]。但临床研究显示,消化道出血致病机制复杂,容易受药物和饮食的影响,因此常规方式检测中漏诊、误诊现象频发,效果不佳[2]。本文就粪便中血红蛋白和转铁蛋白联合检测对于消化道出血诊断的应用价值进行统计分析,报告如下。
1 资料与方法
1.1 一般资料选取2015年3月至2016年5月我院门诊及住院治疗的100例消化道出血患者作为本次研究对象,分成上、下消化道两组。上消化道出血患者50例,其中男26例,女24例,年龄16~65岁,平均年龄(39.38±5.15)岁;下消化道出血患者50例,其中男25例,女25例,年龄16~68岁,平均年龄(40.93±3.37)岁;同期,选择50例体检健康人员作为对照组,其中男24例,女26例,年龄11~69岁,平均年龄(38.99±7.27)岁;分别对3组观察对象进行血红蛋白、转铁蛋白单一与联合检测,统计比较两种单一检测方式与联合检测的临床诊断效果。3组对象在性别、年龄等一般的资料差异不显著(P>0.05),具有可对比的价值。
1.2 方法
1.2.1 试剂血红蛋白胶体金法选用广州万孚生物科技股份有限公司生产的“万孚”大便隐血试纸条;转铁蛋白检测法选用安徽深蓝医疗科技股份有限公司生产的“深蓝”转铁蛋白试纸条。
1.2.2 实验方法⑴分别用采便棒采集3组研究对象的粪便样本,放置于编号的试管内,加入1ml生理盐水,充分搅拌均匀。⑵分别将两种检测试纸插入试管内部停留1min后取出,放置5min,观察试纸反应结果。
1.3 观察指标统计3组观察对象消化道出血的阳性检出率及误诊(假阳性)情况,比较粪便样本中血红蛋白和转铁蛋白单独检测方式与联合检测的临床诊断效果。
1.4 统计学处理运用SPSS 21.0应用软件对本次的统计数据进行统计学分析和处理,3组观察对象消化道出血检测结果应用百分数(%)表示,并且配合χ2值检验,P<0.05表示差异具有统计学意义。
2 结果
2.1 转铁蛋白单独检测与联合检测方式临床诊断效果比较转铁蛋白单独检测方式,上消化道出血患者的阳性检测率为50.00%,下消化道出血患者的阳性检测率为54.00%,健康人员的阳性检出率为2.00%;联合检测法检测上消化道出血的阳性检出率为86.00%,下消化道出血的阳性检出率为88.00%,健康人员的阳性检出率为2.00%,联合检测方式诊断效果显著高于转铁蛋白单独检测方式,差异具有统计学意义(P<0.05),见表1。
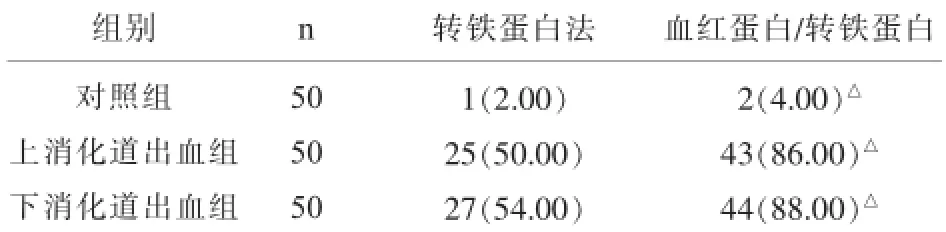
表1 转铁蛋白单独检测与联合检测方式临床诊断效果比较[n(%)]
2.2 血红蛋白单一检测法与联合检测方式的诊断效果比较同血红蛋白单一检测法相比,联合检测法的阳性检出率更高,误诊率更低,差异具有显著性(P<0.05),见表2。
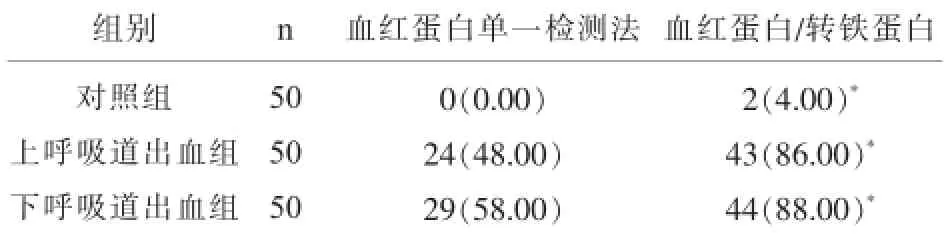
表2 血红蛋白单一检测法与联合检测方式的诊断效果比较[n(%)]
3 讨论
消化道主要由人体食管、胃部、十二指肠、空肠、回肠、盲肠、结肠以及直肠等组织器官组成[3]。而消化道出血疾病则是内科临床中极为常见的一种证候群,临床症状包含上、下消化道出血,可由多种慢性疾病引发。其中,上消化道出血症指的是患者食管、胃、十二指肠、胰腺管以及胆管等组织出现出血症状;而下消化道出血则是指患者的盲、结及直肠出血[4]。消化道出血症的高危诱发因素众多,致病机制十分复杂,不仅可以由消化道炎症、机械性损伤、主要脏器血管病变甚至恶性肿瘤诱发,也可由于消化道临近的组织器官病变累积至消化道,从而导致发病[5]。上消化道出血量小于5ml时肉眼看不到血液存在;红细胞受到破坏时,粪便显微镜检查也见不到红细胞;此时只有通过粪便隐血试验才能证明有无出血[6]。在临床中,粪便隐血试验是消化道隐形出血、慢性胃肠道出血及恶性肿瘤早期诊断的常用筛选指标,其理论和检测技术均已成熟,具有比较好的检测效果和价值[7]。研究统计数据显示,传统常用的化学检测方式由于技术单一,影响因素众多,容易出现漏诊和误诊现象,诊断结果并不理想[8]。这是因为消化道出血患者的诊断结果极易受到药物以及日常饮食的影响,导致假阳性、假阴性结果的频繁出现,严重影响诊断效果,给治疗带来一定的负面影响[9]。随着临床诊断医学水平的不断提高,单克隆双抗体胶体金法诊断的准确性、灵敏度以及特异性都有很大的提升。但是由于消化道出血患者胃内消化酶的作用,单一的血红蛋白与转铁蛋白检测法仍会具有一定的局限性,诊断效果无法满足患者实际需求[10]。而血红蛋白与转铁蛋白检测法联合检测能够互补两种诊断技术的优势,相互配合,互相验证,能够大幅提高粪便隐血试验检测效率,降低误诊、漏诊概率,临床诊断效果更为明显。
本结果显示,转铁蛋白单独检测方式,上消化道出血患者的阳性检测率为50.00%,下消化道出血患者的阳性检测率为54.00%,健康人员的阳性检出率为2.00%;血红蛋白单一检测,上消化道出血患者的阳性检测率为48.00%,下消化道出血患者的阳性检测率为58.00%,健康人员的阳性检出率为0.00%;联合检测法检测上消化道出血阳性检出率为86.00%,下消化道出血的阳性检出率为88.00%,健康人员的阳性检出率为2.00%,消化道出血联合检测的阳性率与廖卫等[11]报道的基本一致;联合检测方式诊断效果显著高于转铁蛋白以及血红蛋白单独检测方式,误诊率更低,差异具有统计学意义(P<0.05),说明血红蛋白和转铁蛋白联合诊断能够起到互补的作用,其阳性检出率相比血红蛋白与转铁蛋白单一检测的特异性、敏感性以及精确度更高,同时减少临床检测假阳性、假阴性的发生机率,降低误诊、漏诊比例,具有较高的临床诊断价值。
综上所述,单一血红蛋白与转铁蛋白检测法均具有一定的局限性,而Hb(血红蛋白)/Tf(转铁蛋白)联合检测方式能够有效将二者的优势进行互补,从而大幅提高临床诊断准确性,诊断价值更高,值得积极应用和推广。
[1]宓庆梅,周琳,仲人前,等.粪便中血红蛋白与转铁蛋白联合检测对于消化道出血的诊断价值[J].求医问药(下半月刊),2012,10(12):361-362.
[2]蒋玥,田薇薇,胡金川.便血红蛋白与转铁蛋白联合检测在慢性肾衰患者消化道病变诊断中的价值[J].国际检验医学杂志,2014,35(6):769-770.
[3]冯丽梅,刘静,孙德华.探讨粪便血红蛋白和转铁蛋白联合检测对肠癌诊断的临床价值[J].国际检验医学杂志,2012,33(10):1263-1264.
[4]娄国平,李显东,张昭勇.联合检测粪便血红蛋白和转铁蛋白在肠癌疾病防治中的应用[J].检验医学与临床,2015,12(9):1193-1195.
[5]许国胜,陈慧.血红蛋白与转铁蛋白联合检测在消化道出血疾病中的临床价值研究[J].中国保健营养月刊,2012,22(8):2438-2440.
[6]伍志莲,赖书台.粪便隐血胶体金法和氨基比林法的对比及意义[J].实验与检验医学,2015,33(2):213-215.
[7]黄胜,梁华英,何艳,等.三种粪便隐血试验的临床应用评价[J].实验与检验医学,2011,29(1):69-70.
[8]石祖亮,王维鹏.血红蛋白和转铁蛋白联合检测法对新生儿应激性消化道出血的筛查作用[J].微循环学杂志,2011,21(2):55-56.
[9]Pathak AK,Dutta N,Banerjee PS,et al.Influence of dietary supplementation of condensed tannins through leafmeal mixture on intake,nutrient utilization and performance of haemonchus contortus infectrd sheep[J].Asian-Australas J Anim Sci,2013,26(10):1446-1458.
[10]王学晶,朱凤霞,董峰,等.血清尿素氮联合便潜血检测在上消化道出血诊断中的应用价值[J].实用医技杂志,2015,22(1):75-76.
[11]廖卫,邢志广,王华,等.两种粪便隐血联合检测在消化道出血诊断中的应用[J].中国临床研究,2014,27(1):100-101.
R446.13+2,R573.2
A
1674-1129(2017)02-0267-02
10.3969/j.issn.1674-1129.2017.02.044
2016-10-19;
2017-03-12)

