利用室间质评数据对HBsAg ELISA检测试剂的技术性能评价
杨丽华,张裕,彭萍,焦芳艳
(湖南省临床检验中心,湖南省第二人民医院,湖南长沙416007)
·质量控制·
利用室间质评数据对HBsAg ELISA检测试剂的技术性能评价
杨丽华,张裕,彭萍,焦芳艳
(湖南省临床检验中心,湖南省第二人民医院,湖南长沙416007)
目的评价乙型肝炎病毒表面抗原(HBsAg)酶联免疫吸附实验(ELISA)检测试剂的技术性能。方法统计分析2011年至2015年5年间湖南省HBsAg项目室间质量评价(EQA)的数据,评价本省实验室使用的HBsAg ELISA检测试剂的基本技术性能指标:分析敏感性、阴性符合率、阳性符合率、室间精密度。结果七种HBsAg ELISA检测试剂(六种国产试剂,一种进口试剂)EQA数据统计总体样本阴阳性符合率无统计学差异;0.5、0.3、0.2IU/ml三个低浓度样本的检测符合率无明显差异,但这三个浓度的样本检测符合率高于浓度为0.1IU/ml(《中国药典》第3部(2010版批批检HBsAg检测灵敏度)的样本检测符合率,其差异有统计学意义;进口试剂检测符合率明显好于其他试剂,在浓度为0.1IU/ml的样本时尤为明显;各种试剂检测的S/CO值其室间精密度值差异与《中国药典》第3部(2010版)中对精密性的要求是CV≤15%的标准相比,只有进口试剂E7 P>0.05无差异;其它六种国产试剂与之相比较,其P<0.05,均有显著性差异,其数据有统计学意义。结论我省当前实验室使用的6种ELISA国产主流检测试剂基本技术性能相近,其主要差异体现在浓度为0.1IU/ml附近样本的检出符合率和精密度。进口HBsAg ELISA试剂各个性能指标均优于国产HBsAg ELISA试剂。
HBsAg;ELISA;室间质量评价;技术性能
HBsAg是临床诊治乙型肝炎病毒(HBV)感染应用最多的血清检测标志物,该项目是WHO公认的判断HBV感染的关键指标[1]。自第一批HBsAg表面抗原检测试剂问世至今,随着免疫学检测技术不断发展,微粒子酶免疫化学发光,化学发光免疫分析等逐渐更多的应用于临床,近5年来,更多的国内外文献趋向于比较其它方法学优于ELISA[2-4],但据国家卫计委临床检验中心的检验质量年度报告显示【全国临床检验年度质量报告(2013),国家卫计委临床检验中心(201404,内部资料)】,当前我国HBsAg检测现状为ELISA检测仍占主流。虽然ELISA方法的临床应用已较为成熟,但由于ELISA方法学技术的特殊性,不同厂家试剂盒的分析性能差别不一,本文参照我国EQA相关标准[5,6],利用全省HBsAg检测室间质评数据分析主要不同ELISA检测试剂的基本技术性能,给同行提供该项目ELISA检测试剂的应用参考,且对国家药品监督管理部门评审试剂生产及批批检制度有补充作用。
1 材料与方法
1.1 资料2011年至2015年5年间湖南省HBsAg项目EQA的数据。
1.2 EQA样本购于北京康彻思坦生物技术有限公司,每支0.5ml。靶值溯源至国家卫生计生委(原国家卫生部)临床检验中心(NCCL)标准物质,编号:GBWE090038-090042。
1.3 主要HBsAg ELISA检测试剂全省EQA系统数据统计大于10家实验室使用的六种国内主流试剂及一种进口试剂。试剂编码为:E1,E2,E3,E4,E5,E6,E7。E7为进口ELISA检测试剂,其他均为国产ELISA检测试剂。
1.4 数据处理用北京科临易检公司开发的CLInet EQA软件进行EQA活动的统计分析,用SPSS 17.0统计软件对各种评价指标进行统计分析,P<0.05有统计学意义。
2 结果
2.1 HBsAg EQA评价不同试剂总体差异本省临床检验中心5年组织10次HBsAg EQA,每次5个批次的标本,共计50个批次。省内6种国内主流HBsAg检测试剂及1种进口试剂共七种检测试剂EQA统计分析结果见表1:7种HBsAg检测试剂检测结果评价指标经单因素方差分析,阳性符合率检验F=2.052,P=0.092,说明七种试剂检测结果阳性符合率总体差异无统计学意义;阴性符合率检验F=1.689,P=0.161,说明七种试剂检测结果阴性符合率总体差异无统计学意义;总符合率检验F=2.496,P=0.046,说明七种试剂检测结果总符合率总体差异有统计学意义。不同试剂间阳性符合率经单因素方差分析两两比较,试剂编码为E7的试剂检测结果阳性符合率明显高于编码为E1、E3、E4、E6试剂组,为(P=0.043,0.007,0.007,0.014<0.05)差异有统计学意义,其他组间两两对比均无统计学意义(P>0.05);试剂编码为E5的检测试剂阳性符合率明显高于试剂编码为E2、E1、E3、E6试剂组,为(P=0.049,0.049,0.049,0.049,<0.05),差异有统计学意义。其他组间两两对比均无统计学意义(P>0.05);试剂E7总符合率明显高于E1、E2、E3、E4、E6试剂组,差异有统计学意义(P= 0.023,0.033,0.003,0.005,0.005<0.05),其他组间两两对比均无统计学意义(P>0.05)
2.2 HBsAg EQA低值样本检测合格率2011年至2015年共设计低值样本14个批次,低值浓度设计随每年检测统计合格率逐年下降,分别为0.5、03、0.2及0.1IU/ml,各个不同浓度的实验室合格率见表2。4种低值浓度样本检测实验室合格率经单因素方差分析,合格率检验F=11.319,P=0.000,说明4种低值浓度样本检测实验室合格率总体差异有统计学意义。不同样本浓度及格率经单因素方差分析两两比较,0.2、0.3、0.5IU/ml浓度样本合格率明显高于0.1IU/ml组,差异有统计学意义(P= 0.000,0.000,0.000<0.05);其他组间两两对比均无统计学意义(P>0.05)。
2.3统计七种HBsAg ELISA试剂检测低值浓度样本的实验室总合格率七种试剂检测总合格率间经单因素方差分析,合格率检验F=1.723,P=0.130,说明七种试剂检测合格率总体差异无统计学意义。不同试剂间总合格率经单因素方差分析两两比较,试剂编码为E7的实验室检测合格率明显高于E2、E3、E5、E6试剂组,差异有统计学意义(P= 0.040,0.006,0.031,0.010<0.05);其他组间两两对比差异均无统计学意义(P>0.05)。
2.4七种HBsAg ELISA试剂检测CV(%)差异性比较经单因素方差分析,F=10.545,P<0.05,差异有统计学意义。七种试剂两两比较分析,编码为E1,E2,E3,E4,E5,E6的试剂组两两之间比较P值均大于0.05,其CV差异无统计学意义。编码为E7的试剂组与其他6种试剂两两比较,P=0.000<0.05,差异有统计学意义。七种不同试剂与临床免疫学检验精密度要求CV<15%比较,进行单样本t检验,除编码为E7的试剂组外,其p值均小于0.01,其差异有统计学意义。编码为E7的试剂组其P=0.163>0.05,差异无统计学意义。
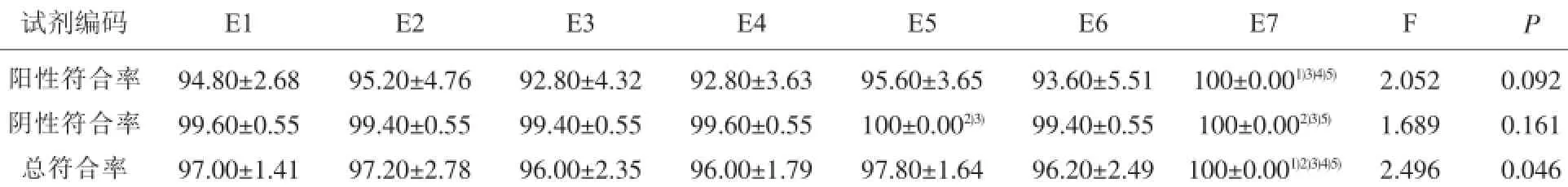
表1 湖南省临床免疫学实验室2011年至2015年HBs Ag EQA评价不同试剂符合率(%)比较(x±s)

表2 低值样本EQA活动实验室检测合格率(%)

表3 低值不同浓度样本不同试剂检测实验室合格率(%)比较(x±s)
3 讨论
ELISA是一种固相酶免疫检测技术,主要用S/CO比值判断检测结果。该检测方法的技术性能指标主要包括灵敏度(阳性符合率),特异性(阴性符合率)这两种准确性评价指标和总符合率及精密度等试验可靠性指标[7]。我省临床检验中心EQA活动所使用北京科临易检公司开发的CLInet EQA软件设计的评价功能亦是囊括上述指标,本文将评估分析如下。

表4 七种不同试剂的EQACV值(%)差别比较

表5 七种试剂与临床免疫定性分析质量控制批间CV<15%的标准差异性比较(单样本t检验)
表1的数据统计显示六种国产试剂的检测技术性能较好,阴阳性符合率及实验室总合格率相差不大。E7为进口试剂,其基本性能参数优于国产试剂,与前些年的文献描述的差异不大[8,9],说明国产HBsAg ELISA检测试剂的总体技术性能和进口试剂相比还有很大的进步空间。表1的数据统计还说明国产试剂之间的基本性能技术参数之间的差异,总体优劣体现为试剂编码E5的试剂依次优于编码E1,E4,E2,E3,E6的试剂。
表2的统计数据显示HBsAg ELISA检测试剂在低浓度样本的检出率差别。样本浓度为0.5IU/ml的EAQ检测合格率其逐年升高,至2013年时其检测率合格率基本接近100%,据此一说明随着当前免疫学技术的发展,ELISA方法检测试剂的分析灵敏度性能不断提高,其次说明在该浓度范围内不论国产还是进口试剂其检出率都优于《中国药典》批批检要求[10],基本符合临床诊断使用。表3的统计数据显示在0.2~0.5IU/ml浓度范围内其试剂检测合格率无统计学意义,但浓度为0.1IU/ml的样本各种不同试剂的检测符合率相差较大。CLInet EQA软件统计显示个别试剂在浓度为0.1IU/ml时其检测符合率不足50%。一则说明当前国产试剂的临界值浓度范围在0.1IU/ml左右,与我国HB-sAg ELISA检测试剂的批批检标准规定中的最低检出量基本一致[11];二则我们临床实验室在做HBsAg ELISA检测试剂性能验证时可以借鉴此浓度;三则提示如此类试剂应用于临床,处于试剂盒临界值范围的感染者漏检可能性极大。
《中国药典》第3部(2010版)中对精密性的要求是CV≤15%,有学者做过国产HBsAg ELISA检测试剂的专项抽验调查,其各试剂批间,同一批试剂间的精密性均能达到标准要求[9]。我省EQA统计的室间精密性与之相差甚远(见表4),理论上来讲,不同试剂批间的精密性应该和不同试剂的室间精密性均应与标准相符(见表4、表5)。但进口试剂的精密性CV值与《中国药典》第3部(2010版)中对精密性的要求相符,进一步说明进口HB-sAg ELISA检测试剂的基本性能优于国产试剂。
本文所统计数据均来自室间质评样本的实验室检测,不排除质控样品的基质效应,但该研究为本省区域5年来的大样本总结,对同行在选择、应用HBsAg ELISA检测试剂方面仍有一定的参考价值。针对新鲜样品与质控品的互通性在不同ELISA试剂的检测结果研究不同文献也鲜见的情况,建议同行参考相关标准[12,13]多做这方面的工作。同时希望临床定性免疫学检验重要常规项目分析质量要求[14]能早日出台,让与之相关的免疫检测质量有标准可循,促进医疗机构实验室检验结果的互认工作,加强临床实验室风险管理[15,16],改进实验室质量。
[1]Seeger C,Mason WS.Hepatitis B virus biology[J].Micorobiol Mol-Biol Rev,2000,(64):51-68.
[2]马连学,李艳菊,魏巍.化学发光微粒免疫法和酶联免疫吸附法检测乙肝表面抗原的结果对比分析[J].中国实用医药,2014,3(9):89-90.
[3]李美忠,姜庆波.化学发光微粒子免疫法检测乙型肝炎表面抗原的临床应用评价[J].实用医技杂志,2010,17(4):343-344.
[4]Sonneveld MJ,Rijckborst V,Bouchuer CA,et al.A comparion oftwo assays for quantification of Hepatitis B surface Antigen in patients with chronic hepatitis B[J].J Clin Virol,2011,51(3):175-178.
[5]中华人民共和国国家卫生和计划生育委员会.WS/T414-2013:室间质量评价结果应用指南[S].北京:中国标准出版社,2013.
[6]中华人民共和国标准GB/T20470-2006.《临床实验室室间质量评价要求》[S].北京:中国标准出版社,2006.
[7]杨有业,张秀明.临床检验方法学评价[M].北京:人民卫生出版社,2008,296-311.
[8]贾志远.ELISA检测试剂的评价方法[D].北京:中国协和医科大学,2007.
[9]孙文利,张献清,穆士杰,等.国产与进口HBsAg ELISA试剂盒的质量比较[J].中国生物制品学杂志,2006,19(1):71-72.
[10]国家药典委员会.中华人民共和国药典第Ⅲ部[S].北京:中国医药科技出版,2010:333-334.
[11]李克坚,周诚,蓝海云,等.2013年我国乙型肝炎病毒表面抗原诊断试剂盒专项抽验调查[J].中国生物制品杂志,2016,29(1):45-50.
[12]中华人民共和国卫生部.中华人民共和国卫生行业标准WS/ T356-2011[S].2011.
[13]Clinical and Laboratry Standards Institute.Evaluation of Matrix Effects;Approved Guideline-Second Edition[S].Clinical and Laboratry Standards Institute document EP14-A2.2005.
[14]李金明.临床定性免疫检验重要常规项目分析质量要求[C].//中国医院协会临床检验管理专业委员会第七届全国临床检验实验室管理学术会议暨中华医学会第十次全国检验医学学术会议(2013NCLM)论文集.2013:87-87.
[15]曾黎峰,雷良华,万本愿.室间质量评价与临床检验结果互认的可行性研究[J].实验与检验医学2013,31(2):121-124.
[16]康凤凤,王薇,王治国.风险管理与临床实验室改进[J].实验与检验医学,2013,31(1):1-2.
R512.6+2,R446.62
A
1674-1129(2017)02-0219-03
10.3969/j.issn.1674-1129.2017.02.025
2016-05-13;
2016-12-29)
湖南省卫生厅课题(编号:2014-104)

