药品微生物实验室高压蒸汽灭菌锅的规范化使用
鲍方名
(苏州市食品药品检验所,江苏苏州 215104)
药品微生物实验室高压蒸汽灭菌锅的规范化使用
鲍方名
(苏州市食品药品检验所,江苏苏州 215104)
高压蒸汽灭菌锅是药品微生物实验室培养基、实验器具、阳性废弃物最常用的、有效的灭菌设备。高压蒸汽灭菌锅从验证到灭菌状态的维护应严格遵守操作规范。为了确保高压蒸汽灭菌锅的有效使用,必须从安装确认、操作确认、工艺确认等方面进行好验证工作,在使用过程中要用参数监测、化学监测、生物监测等手段对灭菌质量有效评价。
药品微生物实验室;高压蒸汽灭菌;规范化
高压蒸汽灭菌技术广泛应用于药品微生物实验室培养基、实验器具、阳性废弃物的日常灭菌,是药品无菌检验质量的基础保障。根据质量技术监督局的要求,操作人员需经过一定课时的培训经考试后获得压力容器操作证才可操作高压蒸汽灭菌锅[1]。但是,这项培训仅仅针对高压蒸汽灭菌锅的安全使用,对如何规范化使用保障药品检验质量没有涉及。本文通过介绍高压蒸汽灭菌锅的验证、日常使用及监测,为高压蒸汽灭菌锅在药品微生物实验室的规范化使用提出一些建设性的建议。
1 高压蒸汽灭菌锅的验证
1.1 安装确认
1.1.1 公共设施的确认
(1)供电要求。根据灭菌锅的要求设置符合要求的工作电流电压。如果有多台灭菌锅同时放在灭菌间,必须考虑总负荷能否承受,最好留有余量。
(2)空间要求。培养基灭菌锅应设置在工作流程的前端,如果使用双扉灭菌锅应与洁净区一起设计。处理阳性垃圾的灭菌锅应该设置在工作流程的末端。若有二级生物安全水平要求时,应在靠近实验室的位置配备高压灭菌器或其他清除污染的工具[2]。
(3)消防安全。烟雾报警器位置不能设置在灭菌锅开门或开口的正上方,否则在灭菌锅打开时产生的蒸汽容易引起误报警甚至洒水。
(4)其他要求。纯化水水源、排水、压缩空气等也应在设备要求范围之内。
1.1.2 灭菌锅本身仪表确认
(1)安全阀按照国家强制检查要求校准。
(2)压力表校准。
1.1.3 仪器附带文件是否齐全,按照灭菌锅自带文件目录核对
1.1.4 灭菌锅操作及维护文件是否齐全,防烫手套是否配备,操作人员是否具备使用压力容器上岗证
1.2 操作确认
1.2.1 温度分布
核查灭菌锅腔室内的温度分布均匀性,确定腔室内可能存在的“冷点”位置及温度差应≤1℃。由表1可知,在2015版药典中对培养基的灭菌条件多集中在121℃和115℃。可根据灭菌锅的具体使用对象选择相应的温度进行温度分布确认。可采用足够的温度压力探头固定在腔室内不同位置,其中蒸汽进口,冷凝水出口,灭菌锅自带探头处需各固定一个探头,其他探头在腔体内部平均分布。空载情况下连续灭菌三次,看设备本身性能是否能达到温度差应≤1℃。满载的情况下,除了在空间平均布局探头之外,灭菌物品的内部等蒸汽不容易到达的地方也需要设置探头。不同类型的灭菌锅根据灭菌条件的不同,是否满载对灭菌效果的影响大不一样。脉动真空式灭菌柜由于不需要高的真空度,被灭菌品装载过密时,灭菌效果差[3]。现在无菌实验室流行使用的双扉灭菌锅多为脉动真空式灭菌柜,装载时一定要注意不要装载过密并加强监控。

表1 2015版药典培养基及灭菌条件Tab.1 Culture media and autoclave cycle of ChP 2015
1.2.2 生物指示剂
市售的湿热灭菌用生物指示剂含有一定数量的耐受性最强的微生物制备的孢子,而且数量超过实际的微生物污染水平。就是在这样一个过度杀灭的灭菌中,生物指示剂的被灭杀程度是评价一个灭菌程序有效性最直观的的指标。腔室满载的情况下,在冷点位置设置生物指示剂,检验灭菌效果。

表2 湿热灭菌工艺常用生物指示剂Tab.2 Biological indicator for moist heat sterilization process
1.3 蒸汽灭菌工艺确认
1.3.1 有效性
使用高压蒸汽灭菌锅对物品进行灭菌时达到理论无菌是最基本的要求。针对不同的灭菌物品选择不同的灭菌程序,最后确认灭菌的有效性。
由于操作方便及有限的灭菌锅数量限制,操作时会在液体程序中混合灭菌空瓶及其他器具。实验表明,蒸汽很难穿过拧紧的蓝盖瓶进入内部。如果使用液体程序灭菌空瓶,要注意拧松或者在内部预先装好培养基或缓冲液。而且传统的纱布包装在液体程序灭菌后湿透,不利于无菌状态的保持,最好使用透气的灭菌袋。
1.3.2 功能性
由于在实际操作过程中无法对每次灭菌物品的初始污染菌含量进行准确识别,所以现在通用的灭菌程序都是过量灭菌。过量灭菌的高温高压过程会对某些培养基的有效成分引起破坏,有些培养基的灭菌温度就比常规的121℃低,相应的灭菌时间适当延长,如RV沙门菌增菌液体培养基。高压蒸汽灭菌锅工艺确认中必须选择此类培养基进行相应的功能性确认,证明在当前的灭菌条件下培养基的功能没有受到影响,或者可以整合培养基的适用性检查的数据体现在高压蒸汽灭菌锅工艺确认报告中。
1.3.3 灭菌后的转移
培养基是在密闭的容器中灭菌,灭菌后只要进行表面消毒即可以保持灭菌状态。实验器具如果是使用纱布包装,无论液体程序或者器具程序都会存在湿包情况,无菌状态不易于保持,最好使用透气的灭菌袋。双扉灭菌锅的使用更加有利于灭菌状态的保持。
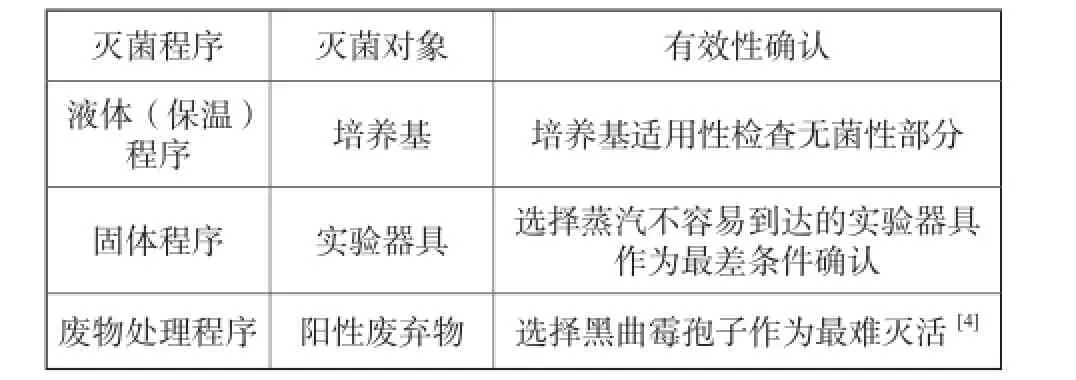
表3 常见灭菌程序及有效性确认Tab.3 Sterilization cycle and effective conf i rmation
2 验证状态的维护
2.1 参数监控
灭菌锅每次灭菌均应记录并打印灭菌开始时间、升温时间、灭菌温度维持时间等具体灭菌工艺参数。控制灭菌物品装载数量和位置。西方国家已经有药品灭菌通过灭菌参数放行的先例,而不需要做无菌检查[5]。
2.2 化学指示胶带
在规定的饱和蒸汽压力下灭菌条件持续一定时间,印在胶带上的指示显色剂条纹发生分解,并与助色剂发生化学反应,随之引起不可逆颜色变化有浅至深,从而间接指示是否满足灭菌条件。
化学指示胶带对灭菌条件(温度、蒸汽饱和度、持续时间)的敏感性均体现在从开始显色到灰黑-黑-深黑的显色过程中。对颜色深浅判断个人主观因素较多,不容易判断灭菌条件是否完全满足。更有研究表明,115℃时化学指示胶带就会开始显色[6]。化学指示胶带只能作为灭菌条件监测的辅助手段。
2.3 B-D试验
用于预真空(包括脉动真空)压力蒸汽灭菌器冷空气排放效果的检测,冷空气是造成预真空(包括脉动真空)压力蒸汽灭菌失败的主要因素之一。对预真空和脉动真空压力蒸汽灭菌,每日进行一次B-D试验。
(1)检测方法 B-D试验要求做前预热、空载监测每天一次,将B-D试纸放入标准测试包,中间包好,水平放入灭菌柜内灭菌车的前底层,靠近柜门与排气口底前方(上方)灭菌柜内除测试包无任何物品。
(2)结果判定 经134℃,3.5 ~ 4 min后,取出B-D测试纸观察颜色变化。若变色均匀一致,说明冷空气排放效果良好,灭菌器可以使用。
2.4 质控标准
参数监测应每锅进行,化学指示胶带应该贴于每个独立灭菌包装上,生物指示剂监测应每周一次[7]。
3 结束语
高压蒸汽灭菌锅是使用量很大的灭菌设备。药品微生物实验室由于其特殊性,如何规范化使用必须引起足够的重视。药品检测时,可能同时配制多种灭菌条件的培养基,这就需要多台灭菌锅同时工作,附属设施必须足够使用。药品检测完成时会产生一部分阳性污染物,如何布置灭菌锅和灭菌程序如何设计必须考虑。灭菌有效性一直是灭菌锅关注的重点,培养基由于其特殊性除了灭菌有效性之外,功能有没有受到影响也应该得到关注,最好能和培养基适用性检查结合起来一起做。灭菌锅在药品微生物实验室中使用频率非常高,如何规范的进行验证状态的监测是验证状态维护的根本。为了更好地合理使用高压蒸汽灭菌锅,操作人员除了安全培训之外,还要学习灭菌锅在药品检测中发挥的作用才能做到规范化使用。
[1]国家安全生产监督管理总局安监总局令第80号,特种作业人员安全技术培训考核管理规定[S],2010.
[2]实验室生物安全手册第三版[M],世界卫生组织,2004.
[3]国家食品药品监督管理局,药品生产验证指南[M],北京:化学工业出版社,2003.
[4]刁宁宁,张建国.高温高压条件下黑曲霉孢子的失活参数计算[J],微生物学杂志,2015,4(35):33-36.
[5]FDA工业指南-最终湿热灭菌的人用药和兽用药的参数放行申报[M],2010.
[6]郑会乐,黄成棣,等. 压力蒸汽灭菌指示胶带的研制及效能测试[J],中国医疗器械杂志,1997,21(1): 16-19.
[7]中华人民共和国卫生部,WS 310.3-2009医院消毒供应中心清洗消毒及灭菌效果监测标准[S],2009.
Standardizing Use of High pressure steam autoclaves in Microbiology Laboratory
Bao Fangming
(Suzhou Institute for Food and Drug Inspection, Suzhou 215104)
Autoclave is most effectively sterilizing equipment commonly used in placing culture medium and positive contaminants. But it is necessary to strictly conform to the standards in validation of autoclave and the maintenance of its sterilizing function. In order to ensuring the effective use of autoclave, the validations in installation, operation and process are very important. Thus the methods of parameter monitor, chemical monitor and biological monitor should be applied in practice to make effective evaluation.
pharmaceutical microbiology laboratory; high pressure steam; standardization
TQ 052.6
A
2095-817X(2017)01-0045-003
2016-05-30
鲍方名(1982—),男,主管药师,主要从事药品微生物检测及净化工程检测。

