急性肺栓塞致右心功能不全兔模型的建立
贾振宇,卢光东,张金星,赵林波,刘 圣,施海彬
(南京医科大学第一附属医院放射科,江苏 南京 210029)
急性肺栓塞致右心功能不全兔模型的建立
贾振宇,卢光东,张金星,赵林波,刘 圣,施海彬*
(南京医科大学第一附属医院放射科,江苏 南京 210029)
目的 建立一种制作简单、可重复性高的急性肺栓塞(APE)伴有右心功能不全(RVD)的动物模型。方法 采用实验用新西兰白兔12只,利用明胶海绵可压缩特性经股静脉注入5 mm×5 mm×10 mm明胶海绵条2条,随血流栓塞肺动脉。监测血流动力学参数,行CT肺血管成像(CTPA)及肺组织病理学分析。结果 所有明胶海绵条均恒定栓塞于双侧下肺动脉。建模前平均肺动脉压(mPAP)[(9.75±1.75)mmHg]与建模后即刻mPAP[(20.58±5.86)mmHg]、建模后 1 h的mPAP[(18.78±4.80)mmHg]差异均有统计学意义(P均<0.001)。建模前后体循环收缩压(sBP)变化不显著 (P=0.640)。建模前右心室/左心室横径比(RV/LV)为0.67±0.09,建模后45 min复查为1.90±0.28,差异有统计学意义(P<0.001)。结论 本研究建立的兔伴有RVD的APE动物模型制作简单,可重复性高,适用于APE诊治的相关研究。
肺栓塞;心功能障碍,右;模型,动物
急性肺动脉栓塞(acute pulmonary embolism, APE)是一种常见的心血管急症,是由于肺血管突然阻断引起肺动脉压急剧升高,从而导致右心功能不全(right ventricle dysfunction, RVD),甚至右心衰竭[1-2]。溶栓治疗是高危APE患者的一线治疗方案,其能迅速解除血栓对肺血管的阻断。当患者存在溶栓禁忌证或溶栓效果不理想时,对于中央型APE的患者可考虑接受外科手术取栓或血管内碎栓等治疗[3]。因此,一个制作简单、可重复性高的中央型APE动物模型可用于评价取栓或碎栓治疗的有效性,亦可用于APE伴发RVD的相关研究。既往建立中央型APE模型时,首先需在体内的大静脉原位诱导血栓形成,然后释放血栓造成肺动脉主干栓塞,但其血栓量并不能精确控制,并且操作复杂[4-5]。故笔者认为,建立中央型APE模型需解决2个关键问题:①如何将大尺寸栓子引入肺动脉;②如何有效控制肺栓塞程度。因此,本研究拟以兔为实验动物,建立一种制作简单、可重复性高的伴有RVD的中央型APE动物模型,以期用于科研工作。
1 材料与方法
1.1研究对象 健康成年新西兰白兔12只,体质量2.5~3.0 kg,雄性,购自南京莱芜动物养殖场,符合医学实验动物标准。本研究获南京医科大学动物伦理委员会批准。
1.2仪器与方法
1.2.1 模型建立 实验动物禁食12 h,采用21G静脉留置针经兔耳缘静脉建立静脉通道,3%戊巴比妥钠溶液按30 mg/kg体质量经兔耳缘静脉缓慢推注。将家兔仰卧位保定于实验台上,常规备皮,接心电图,解剖右侧股静脉并置入5F导管鞘。将5 mm×5 mm×10 mm明胶海绵条碾压成细海绵条,置于另外一根5F鞘管内,与右侧股静脉预置的5F导管鞘管尾端连接后推注进入下腔静脉,海绵条随血流栓塞肺动脉,每只兔注入2条海绵条(图1)。
1.2.2 血流动力学测定 分别在建模前、建模后即刻和建模后1 h行肺动脉造影,对比剂经右侧股静脉留置导管鞘注入,速率4 ml/s,总量8 ml。分别在建模前、建模后即刻和建模后1 h引入3F微导管至肺动脉主干,测量平均肺动脉压(mean pulmonary arterial pressure, mPAP);于建模前、建模后即刻及1 h测量心率(heart rate, HR);于建模前、建模后1 h由左侧股动脉置入20G动脉留置针,测量体循环收缩压(systolic blood pressure, sBP);建模前及建模后1 h取动脉血用于血气检测。
1.2.3 CT肺血管成像(CT pulmonary angiography, CTPA) 采用Siemens Definition AS 64 排CT机,分别于建模前、建模后45 min行CTPA扫描。扫描范围为肺尖至肺底,扫描参数:管电压120 kV,管电流130 mAs,准直64×0.625 mm,转速0.33 s/rot,螺距0.5,层厚5.0 mm。团注对比剂跟踪肺动脉主干CT值达到100 HU后延迟3 s触发扫描。对比剂采用欧乃派克(300 mgI/ml),经右侧股静脉以3.5 ml/s流率应用双筒高压注射器注射,剂量4 ml/kg体质量;注射完毕后再以相同的流率注射20 ml生理盐水。扫描完成后,重建层厚1.5 mm图像,选择三尖瓣层面测量右心室横径(RV,右心室内侧壁至室间隔表面最宽的距离),选择二尖瓣层面测量左心室横径(LV,左心室内侧壁至室间隔表面最宽的距离),计算右心室/左心室横径比(RV/LV)[6]。
1.2.4 病理学检查 模型建立后4 h,静推3%戊巴比妥钠100 mg/kg体质量处死实验兔。开胸取出双肺,用10%甲醛固定,行HE染色。
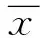
2 结果
本组12只实验兔均成功建立了APE模型,其中5只实验动物于建模后4 h内死亡。
2.1血流动力学指标及血气分析 建模前mPAP [(9.75±1.75)mmHg]与建模后即刻mPAP [(20.58±5.86)mmHg]、建模后1 h的mPAP[(18.78±4.80)mmHg]差异有统计学意义(P均<0.001)。建模前HR[(243.1±28.2)次/分]与建模后即刻HR[(177.7±43.5)次/分;P<0.001]、建模后1 h HR[(199.2±32.9)次/分;P=0.04]差异有统计学意义。建模前sBP [(127.8±16.5)mmHg]与建模后1 h sBP[(126.9±12.9)mmHg]差异无统计学意义 (P=0.640)。建模前血氧饱和度[(96.0±1.3)%]与建模后1 h血氧饱和度[(72.3±4.7)%]差异有统计学意义(P<0.001)。建模前血氧分压[(98.3±1.3)mmHg]与建模后1 h血氧分压[(69.1±5.8)mmHg]差异有统计学意义(P<0.001)。建模前二氧化碳分压[(41.3±2.1)mmHg]与建模后1 h二氧化碳分压[(32.7±3.0)mmHg]差异有统计学意义(P<0.001)。
2.2 肺动脉造影及CTPA结果 所有明胶海绵条均位于双侧下肺动脉,位置恒定。建模前RV/LV为0.67±0.09、建模后45 min为1.90±0.28,差异有统计学意义(P<0.001),见图2、3。
2.3 病理学结果 建模后4 h处死实验动物,发现所有实验动物下肺均出现肺组织充血,病理切片显示明胶海绵条位于直径约3~4 mm的下肺动脉内(图4)。
3 讨论
中央型肺栓塞是指栓子位于肺叶及其上级分支的动脉内,周围型肺栓塞是指栓子位于肺段及其下级分支的肺动脉内[7]。既往报道[8-11]用于建立肺动脉栓塞模型的栓子有:自体血栓、明胶海绵条、医用组织胶或医用栓塞微粒等。通常用于引入栓子的外周静脉为颈静脉或股静脉,因为受限于外周静脉血管的直径,所以仅能引入直径较小的栓子,造成周围性肺栓塞。虽然通过节段性阻断下腔静脉能够在原位形成较大血栓,释放后形成中央型肺栓塞,但是这种方法操作复杂,并且血栓大小不易控制,肺动脉栓塞程度难以一致[11]。本研究发现将5 mm×5 mm×10 mm大小的明胶海绵条碾压成致密细条后能收入5F的鞘管内,并且应用注射器推出明胶海绵条能即刻恢复原状。DSA造影、CTA及病理学检查均显示栓子恒定地嵌顿于双侧下肺动脉内,因此不同个体间肺栓塞程度趋于一致。

图1 明胶海绵栓子制作过程 A.将明胶海绵切割成5 mm×5 mm×10 mm的条状; B.手指旋转碾压后的细海绵条置于5F的鞘管内(箭); C.尾端连接注射器,将明胶海绵条推出,明胶海绵条恢复原状
图2 实验兔肺动脉造影图 A.建模前肺动脉造影完整显示双侧肺动脉; B.建模后即刻肺动脉造影显示双侧下肺动脉截断,双下肺灌注缺失 图3 实验兔CTPA图 A、B.建模前、后CTPA右心室及左心室横径测量,建模后RV/LV显著增大; C.CTPA显示栓子位于双侧下肺动脉内(箭) 图4 病理示明胶海绵条嵌顿于直径约3~4 mm的肺动脉内(HE,×1 000)
实验动物的血流动力学结果显示,建模后平均肺动脉压可稳定于基础值2~3倍之间,体循环动脉压可维持相对稳定。临床上增强CT评价右心室扩张可以评估患者短期预后,包括住院期间死亡率、30天死亡率以及3个月死亡率[12-15]。美国心脏病协会推荐CT上显示RV/LV>0.9作为右心室功能不全的诊断标准之一[16]。本实验中12只兔建模前RV/LV的均值为0.67±0.09,建模后为1.90±0.28,符合右心功能不全的标准。5只实验动物于建模后4 h内死亡,考虑为右心功能急性损伤失代偿所致。但人类的标准毕竟不完全适用于兔,因此RV/LV具体比值是多少才是评判兔右心室功能不全的标准,尚需进一步确定。
本实验模型建立成功后,血氧饱和度及氧分压均下降,且栓塞前后差异均具有统计学意义。虽然既往报道[11]肺动脉栓塞后,因为血氧水平的降低会出现心率上升现象,但本研究观察到肺栓塞后心率下降的现象,并且其中5只实验动物死亡的过程中,可观察到心率逐渐减缓最终停搏的过程。这可能与大面积肺栓塞后右心后负荷显著增加有关,是一个右心功能不全向右心功能衰竭演变的过程。
本研究尚存在以下不足:①APE后肺动脉高压的发生机制复杂,不仅包括栓子对肺血管的机械性阻塞,还包含血栓刺激机体释放的血管活性物质所致的血管痉挛性收缩的参与,因此以明胶海绵作为栓塞物质制作的动物模型不能完全模拟人肺血栓栓塞的全部机制。②虽然肺动脉压升高及RV/LV比增大均表明右心室功能不全,但尚缺乏脑钠肽及肌钙蛋白等实验室指标的验证。③本研究选择了单一数量的栓塞颗粒,尚需探讨不同量的栓子对机体的影响。
总之,本实验利用明胶海绵压缩后可迅速恢复原状的特性,经股静脉引入大的栓子成功制作了兔伴有RVD的中央型APE模型,此种方法简单,可重复性高,可用于外科取栓或导管碎栓治疗效果的评估,及用于APE伴发RVD的相关研究。
[1] 中华医学会心血管病学分会肺血管病学组,中国医师协会心血管内科医师分会.急性肺血栓栓塞症诊断治疗中国专家共识.中华内科杂志,2010,49(1):74-81.
[2] Goldhaber SZ, Bounameaux H. Pulmonary embolism and deep vein thrombosis. Lancet, 1994,379(9828):1835-1846.
[3] Kucher N, Rossi E, De Rosa M, et al. Massive pulmonary embolism. Circulation, 2006,113(4):577-582.
[4] Mercier O, Tivane A, Dorfmüller P, et al. Piglet model of chronic pulmonary hypertension. Pulm Circ, 2013,3(4):908-915.
[5] Arias-Loza A, Jung P, Abeßer M, et al. Development and characterization of an inducible rat model of chronic thromboembolic pulmonary hypertension. Hypertension, 2016,67(5):1000-1005.
[6] John G, Marti C, Poletti PA, et al. Hemodynamic indexes derived from computed tomography angiography to predict pulmonary embolism related mortality. Biomed Res Int, 2014,2014:363756.
[7] Wittram C, Maher MM, Yoo AJ, et al. CT angiography of pulmonary embolism: Diagnostic criteria and causes of misdiagnosis. Radiographics, 2004,24(5):1219-1238.
[8] Kjaergaard B, Kristensen SR, Risom M, et al. A porcine model of massive, totally occlusive, pulmonary embolism. Thromb Res, 2009,124(2):226-229.
[9] Schmitz-Rode T, Vorwerk D, Günther RW, et al. Percutaneous fragmentation of pulmonary emboli in dogs with the impeller-basket catheter. Cardiovasc Intervent Radiol, 1993,16(4):239-242.
[10] Biederer J, Charalambous N, Paulsen F, et al. Treatment of acute pulmonary embolism: Local effects of three hydrodynamic thrombectomy devices in an ex vivo porcine model. J Endovasc Ther, 2006,13(4):549-560.
[11] Barbash IM, Schenke WH, Halabi M, et al. Experimental model of large pulmonary embolism employing controlled release of subacute caval thrombus in swine. J Vasc Interv Radiol, 2011,22(10):1471-1477.
[12] Nural MS, Elmali M, Findik S, et al. Computed tomographic pulmonary angiography in the assessment of severity of acute pulmonary embolism and right ventricular dysfunction. Acta radiol, 2009,50(6):629-637.
[13] Ghuysen A, Ghaye B, Willems V, et al. Computed tomographic pulmonary angiography and prognostic significance in patients with acute pulmonary embolism. Thorax, 2005,60(11):956-961.
[14] Schoepf UJ, Kucher N, Kipfmueller F, et al. Right ventricular enlargement on chest computed tomography: A predictor of early death in acute pulmonary embolism. Circulation, 2004,110(20):3276-3280.
[15] van der Meer RW, Pattynama PM, van Strijen MJ, et al. Right ventricular dysfunction and pulmonary obstruction index at helical CT: Prediction of clinical outcome during 3-month follow-up in patients with acute pulmonary embolism. Radiology, 2005,235(3):798-803.
[16] Jaff MR, McMurtry MS, Archer SL, et al. Management of massive and submassive pulmonary embolism, iliofemoral deep vein thrombosis, and chronic thromboembolic pulmonary hypertension: A scientific statement from the American Heart Association. Circulation, 2011,123(16):1788-1830.
Establishment of rabbit model of acute pulmonary embolism with right ventricular dysfunction
JIAZhenyu,LUGuangdong,ZHANGJinxing,ZHAOLinbo,LIUSheng,SHIHaibin*
(DepartmentofRadiology,theFirstAffiliatedHospitalofNanjingMedicalUniversity,Nanjing210029,China)
Objective To establish an easily reproducible rabbit model of acute pulmonary embolism (APE) with right ventricular dysfunction (RVD). Methods Two gelfoam strips (5 mm×5 mm×10 mm) were squeezed and were introduced into the pulmonary arteries of each healthy rabbit (n=12). Pulmonary and systemic hemodynamic function were recorded. All rabbits underwent CT pulmonary angiography (CTPA) and pathological examination after the introduction of APE. Results All gelfoam strips located in the bilateral lower lobe arteries. Compared with baseline mean pulmonary artery pressure (mPAP) ([9.75±1.75] mmHg), mPAP increased to (20.58±5.86)mmHg immediately after embolism (P<0.001), and then decreased to (18.78±4.80) mmHg 1 h after embolism (P<0.001). Right ventricle/left ventricle diameter ratio (RV/LV) increased from baseline (0.67±0.09) to (1.90±0.28) 45 min after embolism (P<0.001). Conclusion An easily reproducible rabbit model of APE with RVD are established and may be suitable for study of APE pathophysiology.
Pulmonary embolism; Ventricle dysfunction, right; Model, animal
国家自然科学基金(81271678)、江苏省科技项目(BL2014087)。
贾振宇(1982—),男,河北玉田人,博士,主治医师。研究方向:介入放射学。E-mail: zhenyu_jia@sina.com
施海彬,南京医科大学第一附属医院放射科,210029。
E-mail: shihb@njmu.edu.cn
2016-11-08
2016-12-19
R-332; R563.5
A
1672-8475(2017)03-0178-04
10.13929/j.1672-8475.201611008