9株Ⅰ群禽腺病毒的分离鉴定及hexon基因的遗传变异分析
初欢欢,单虎,郑秀云,王述柏,宋化强
(1.青岛农业大学动物科技学院,山东青岛266109;2.青岛奕奕和农牧科技有限公司,山东青岛266109)
9株Ⅰ群禽腺病毒的分离鉴定及hexon基因的遗传变异分析
初欢欢1,单虎1,郑秀云1,王述柏1,宋化强2
(1.青岛农业大学动物科技学院,山东青岛266109;2.青岛奕奕和农牧科技有限公司,山东青岛266109)
为了解山东省肉鸡场禽腺病毒的感染流行特点,为其科学防治提供依据,通过临床症状观察、病毒分离鉴定、鸡胚致病性试验、血凝试验、PCR检测及克隆测序等方法进行病原检测分析。结果表明,发病肉鸡主要表现为精神沉郁、采食减少等临床症状。鸡胚致病性试验可见死亡胚体呈全身出血、体型小、肝肿大现象。血凝试验显示,分离株不具凝集鸡、鸭、大鼠红细胞的特性。对hexon基因进行克隆测序分析显示,LY9株与Ⅰ群禽腺病毒血清8型亲缘性近,与参考株(58株)的核苷酸同源性为98.8%,氨基酸同源性为98.6%。其余8株分离株间的核苷酸同源性为91.3%~99.8%,氨基酸同源性为97.8%~100%;与Ⅰ群禽腺病毒血清4型参考株(HB1510株)属同一进化分支,核苷酸同源性为93.1%~100%,氨基酸同源性为98.9%~100%。结论:从山东省4家肉鸡场分离到的9株病毒均为Ⅰ群禽腺病毒。
肉鸡;禽腺病毒;hexon基因;遗传变异
禽腺病毒病(FAdv)是家禽常见传染病,多为隐性感染,在健康动物体内复制而不表现明显的临床症状,当产生应激因素或感染其他疾病时,该病毒则很快发挥致病性作用[1]。FAdv分为3个群,其中,Ⅰ群FAdv是从鸡、鹅和鸭的呼吸道感染分离得到的,有5个种和12个血清型[2]。能引起生长迟缓、呼吸道疾病、产蛋鸡产蛋下降等症状,在世界范围内分布广,对鸡的危害严重[3-6]。由于Ⅰ群FAdv为隐性感染不易察觉,且拥有多种血清型,对本病的临床检测具有重要意义。本试验对Ⅰ群FAdv进行分离鉴定及遗传变异分析,了解该病的感染流行特点,旨在为其科学防治提供依据,促进家禽养殖业健康发展。
1 材料与方法
1.1 参考毒株实验室保存Ⅰ群FAdv毒株。
1.2 方法
1.2.1 病料处理采取患鸡心、肝和肺组织研磨至匀浆状态,加入适量PBS制成20%无菌悬液。
1.2.2 病毒的分离及鸡胚致病性试验将无菌悬液卵黄囊接种6~8日龄SPF鸡胚,每个样品接种5枚,0.2 mL/枚,设置2枚阴性对照,37℃温箱孵育,每日观察4次鸡胚病变,收获死胚尿囊液[7]。
1.2.3 血凝试验(HA)参考文献方法[8],检测收集新鲜鸡胚尿囊液对鸡、鸭、大鼠红细胞的凝集性。
1.2.4 PCR扩增试验(1)引物的设计与合成:参考GenBank公布的基因序列,设计用于扩增hexon基因loop L1区域的引物序列,扩增目的片段大小为839 bp;(2)病毒DNA的提取:参考文献方法[9],提取尿囊液的DNA;(3)PCR反应:PCR反应体系25 μL,试剂按顺序依次加入ddH2O 17 μL;10×Ex Taq Buffer 2.5 μL;DNA 2 μL;dNTP 2 μL;上游引物0.5 μL;下游引物0.5 μL;Ex Taq 0.5 μL.PCR反应程序为:95℃5 min;94℃45 s;55℃1 min;72℃2 min;共35个循环,最后72℃延伸10 min。将PCR扩增结果经1.0%的凝胶电泳检测;(4)PCR产物的克隆及序列测定分析:将PCR产物纯化回收后进行克隆测序,将获得的毒株基因序列与GenBank发表的FAdv基因序列进行同源性比较和遗传进化分析,绘制遗传进化树[10]。
2 结果
2.1 发病鸡群的主要临床症状和流行病学特点从87份疑似病料中共检测到9株Ⅰ群FAdv,分别编号为WH1、WH2、WH3、MP4、MP5、MP6、MP7、HY8、LY9。发病鸡的主要临床症状和流行特点见表1。

表1 发病鸡群的主要临床症状和流行特点
2.2 鸡胚致病性试验鸡胚致病性试验结果见表2,毒株接种鸡胚第5~7天为死亡高峰。死亡胚胎多表现为全身出血,以头颈、四肢为重;胚胎发育不良,较正常发育胚体小;有肝肿大现象。

表2 鸡胚致病性试验结果
2.3 分离株的凝集特性9株分离株对鸡、鸭和大鼠的不同浓度的红细胞均不具有凝集性。
2.4 PCR检测结果PCR扩增结果与预期片段大小相符,见图1。
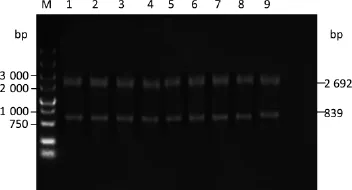
图1 Ⅰ群FAdv hexon基因PCR扩增电泳图M:DL-2000;1~9:WH1、WH2、WH3、MP4、MP5、MP6、MP7、HY8、LY9
2.5 质粒酶切鉴定结果酶切鉴定结果经1.0%琼脂糖凝胶电泳检测与预期片段大小一致,结果如图2。
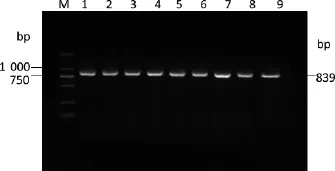
图2 质粒酶切鉴定结果M:DL-5000;1~9:WH1、WH2、WH3、MP4、MP5、MP6、MP7、HY8、LY9
2.6 测序结果及遗传变异分析经分析可见,LY9株与Ⅰ群FAdv血清8型参考株58(AF508957)处于同一遗传进化分支,核苷酸、氨基酸同源性均为98%以上。其余8株分离株间的核苷酸同源性为91.3%~99.8%,氨基酸同源性为97.8%~100%;与Ⅰ群禽腺病毒血清4型参考株HB1510株(KU587519)属同一进化分支,核苷酸同源性为93.1%~100%,氨基酸同源性为98.9%~100%。与CELO标准株的同源性较低,为64.7%~70.8%。所有分离株与Ⅱ群的HEV和Ⅲ群的EDS76的亲缘性低,核苷酸同源性低于20%。
3 讨论
Ⅰ群FAdv感染需多种实验室检验方法的综合判断。刘东[10]通过临床诊断、病理组织学观察、病毒分离、PCR检测及测序、动物回归试验等方法对我国355份疑似样品进行检测,结果显示,2010年至2014年间,Ⅰ群FAdv感染率由30%升至70%,临床表现包涵体肝炎的为FAdv-8a/b型,表现心包积液综合征的为FAdv-4型。本试验亦采用上述试验方法,并对hexon基因进行扩增,该基因是区别不同毒株间同源性和遗传特异性的分子基础,也是判断主要的属、亚属以及次要的种的抗原依据[11]。Niczyporuk[12]通过扩增loop L1区域,将96株波兰FAdv分离株与GenBank发表的不同国家地区代表毒株的基因序列构建系统发育进化树,分析出不同分离株的血清型,确定了波兰和世界其他地区FAdv分离株间的关系。

图3 Ⅰ群FAdv分离株与参考毒株hexon基因系统进化树
4 结论
本试验共分离到9株Ⅰ群FAdv,其中LY9株与I群FAdv血清8型参考株(58株)的亲缘性近,核苷酸同源性达98.8%;其余8株与Ⅰ群FAdv血清4型参考株HB1510株)在进化树中属同一分支,核苷酸和氨基酸同源性分别为93.1%~100%和98.9%~100%。
[1]李丽,李波.腺病毒Ⅰ群研究现状[J].北方牧业,2016,07: 28-30.
[2]Niczyporuk,Jowital.Phylogenetic and geographic analysis of fowl adenovirus field strains isolated from poultry in Poland[J].Archives of Virology,2016(1):33-42.
[3]Dinesh Mittal,Naresh Jindal,Ashok Kumar Tiwari,et al.Characterization of fowl adenoviruses associated with hydropericardium syndrome and inclusion body hepatitis in broiler chickens[J].Virus Disease,2014(1):114-119.
[4]宗玉霞,王李辉,张和平.一种新型鸡腺病毒病的流行特点及防治措施[J].当代畜牧,2016,06:52.
[5]Ayse Günes,Ana Marek,Beatrice Grafl,et al.Real-time PCR assay for universal detection and quantitation of all five species of fowl adenoviruses(FAdV-A to FAdV-E)[J].Journal of Virological Methods,2012(No.2):147-153.[6]Helena Grgil,Peter J Krell,Eva Nagy.Comparison of fiber gene sequences of inclusion body hepatitis(IBH)and non-IBH strains of serotype 8 and 11 fowl adenoviruses[J].Virus Genes,2014 (No.1):74-80.
[7]郝东敏.山东地区Ⅰ群禽腺病毒的分离鉴定及多价油乳剂灭活疫苗的研制[D].泰安:山东农业大学,2014.
[8]国纪垒,刁有祥,薛聪,等.Ⅰ群禽腺病毒山东株的分离鉴定及hexon基因的克隆与分析[J].中国兽医学报,2012,32(12): 1773-1777.
[9]王小辉.Ⅰ群禽腺病毒的分离鉴定及其生物学特性研究[D].扬州:扬州大学,2008.
[10]刘东,刘红祥,于静,等.Ⅰ亚群腺病毒在我国鸡群的流行病学调查[J].中国家禽,2015,37(15):70-73.
[11]Niczyporuk J S,Wozniakowski G,Samorek-Salamonowicz E.Application of cross-priming amplification(CPA)for detection of fowl adenovirus(FAdv)strains[J].Archives of Virology,2015(4): 157-163.
[12]Niczyporuk,Jowital.Phylogenetic and geographic analysis of fowl adenovirus field strains isolated from poultry in Poland[J].Archives of Virology,2016(1):859-862.
Separation Identification of 9 Fowl Adenovirus GroupⅠStrains and Genetic Variation Analysis of Hexon Gene
CHU Huan-huan1,SHAN Hu1,ZHENG Xiu-yun1,WANG Shu-bai1,SONG Hua-qiang2
(1.College of Animal Science and Technology,Qingdao Agricultural University,Qingdao 266109,China; 2.Qingdao Yiyihe Agro-pastoral Technology Co.,Ltd,Qingdao 266109,China)
The aim of the experiment was to provide basis for scientific prevention and control of the disease and to understand infection prevalence of FAdv in broiler farms in Shandong province.The main pathogen identification methods included clinical symptoms observation,virus isolation and identification,chicken embryo pathogenicity test,blood clotting test,PCR detection and cloning sequencing analysis.The results showed that,the main symptoms in chicken were depressed spirit,appetite reduction,swelling degeneration liver and other clinical symptoms.The chicken embryo pathogenicity test showed that the embryos were systemic bleeding,smaller and hepatomegaly.They hadn't agglutination properties to red cells of chicken,duck and rat.The results of hexon gene amplification and cloning sequencing analysis showed that the relationship between LY9 isolate and FAdv groupⅰserum 8 reference strain(58 strain)was close,nucleotide homology was 98.8%,and amino acids homology was 98.6%.Among the other 8 isolates,nucleotide homology was 91.3%~99.8%,and amino acids homology was 97.8%~100%.These isolates and FAdv groupⅰserum 4 reference strain(HB1510 strain)belonged to the same evolutionary branch.Their nucleotide homology was 93.1%~100%,and amino acids homology was 98.9%~100%.The conclusion is that 9 isolates from 4 broiler farms in Shandong province are FAdv groupⅰisolates.
Broiler;Fowl adenovirus;Hexon gene;Genetic variation
WANG Shu-bai
S855.3
A
0529-6005(2017)01-0007-03
2016-05-18
山东省自主创新及成果转化专项(2014ZZCX07105);山东省现代农业产业技术体系创新团队项目(SDAIT-11-14)
初欢欢(1991-),女,硕士生,研究方向为预防兽医学,E-mail:15275210115@126.com
王述柏,E-mail:wshubai@163.com

