手性流动相添加剂法拆分西那卡塞原料及中间体
姚艳云,孙孔春,王永茜,杨 倩,王 乐,陈喜龙,沈报春
(昆明医科大学 药学院暨云南省天然药物药理重点实验室,云南 昆明 650500)
手性流动相添加剂法拆分西那卡塞原料及中间体
姚艳云,孙孔春,王永茜,杨 倩,王 乐,陈喜龙,沈报春*
(昆明医科大学 药学院暨云南省天然药物药理重点实验室,云南 昆明 650500)
以自制1-萘万古霉素(Na-VAN)为手性固定相(CSP),D-酒石酸(D-Tar)、L-酒石酸二乙酯(L-TADE)、D-酒石酸二乙酯(D-TADE)分别为手性流动相添加剂(CMPA),建立了西那卡塞原料1-(1-萘基)乙胺(化合物1)及西那卡塞中间体(化合物2)的高效液相色谱手性拆分方法。考察了流动相中醇类改性剂、CMPA对对映体分离的影响,初步探讨了手性识别机理。以Na-VAN为CSP,正相模式下,添加不同种类的CMPA,化合物1、化合物2均可获得一定程度的分离,其中以D-TADE为CMPA时,化合物1、化合物2获得最佳分离。结果表明,醇的分子体积、CMPA的立体构型均对手性分离有影响。
1-(1-萘基)乙胺;西那卡塞中间体;1-萘万古霉素;手性流动相添加剂;对映体分离
1-(1-萘基)乙胺(化合物1)是一种手性芳香胺类化合物,是非常重要的手性药物原料,也是其他手性对映体的常用拆分剂和手性助剂[1]。以化合物1为原料可制备出一系列手性配体和高手性效率催化剂,为许多不对称药物的合成提供了一条高选择性、高收率、低成本的途径。与此同时它在医药、农药、化工、材料等领域也得到非常广泛的应用[2]。
盐酸西那卡塞是FDA批准上市的第一个拟钙剂[3],分子中含1个手性中心,临床使用的是单一对映体R-西那卡塞,而S-西那卡塞的存在严重影响了西那卡塞的有效性和安全性[4-5]。化合物1是合成西那卡塞的重要原料[6],其酰胺衍生物(化合物2) 是西那卡塞的最新合成路线中间体[7-8](结构见图1),化合物1和化合物2的立体构型决定了西那卡塞的最终立体构型。因而,建立一种高效、准确的西那卡塞合成原料和中间体的拆分方法对西那卡塞的结构确定和立体构型控制具有重要意义[9]。
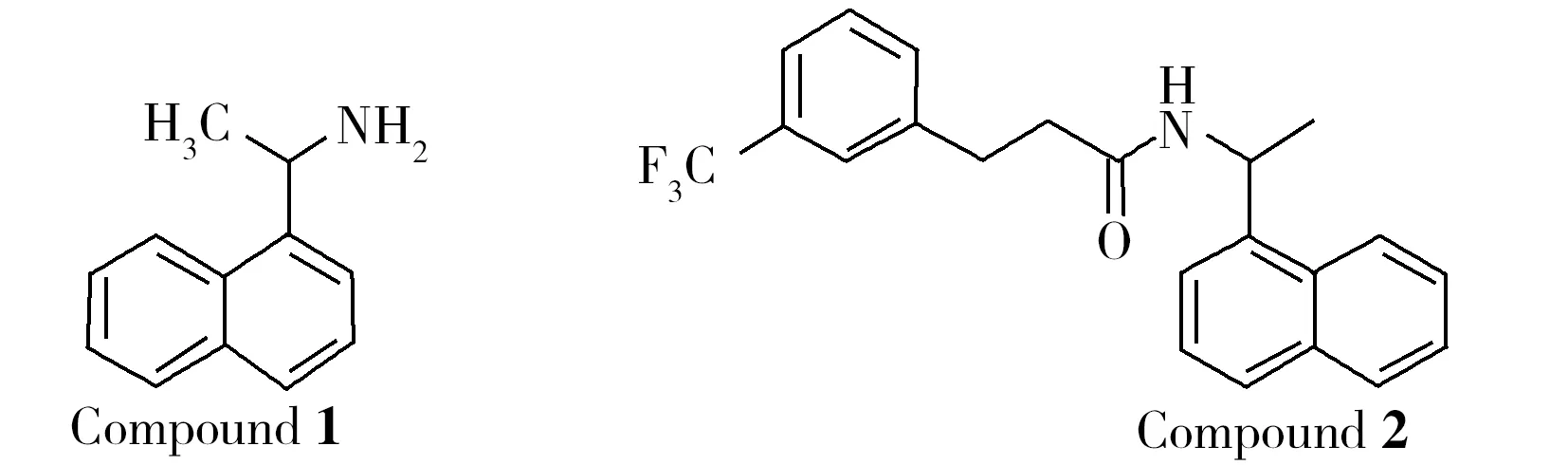
图1 化合物1与化合物2的分子结构Fig.1 Molecular structures of compound 1 and 2
手性药物对映体拆分主要有非色谱法和色谱法,最常用的是色谱法,特别是高效液相色谱法(HPLC)已成为首选方法[10-11]。HPLC法拆分对映体有直接法和间接法两类方法[12]。直接法有手性固定相法(CSP)[13]、手性流动相添加剂法(CMPA)[14],间接法为手性试剂衍生化法(CDR)[15]。酒石酸及其衍生物含有手性中心,在不对称合成、对映体拆分和高效液相手性流动相添加剂中应用广泛[16]。化合物1单一对映体的获取方法有化学拆分、酶拆分、不对称合成等[17],化合物2的拆分未见报道。
在自制1-萘万古霉素手性固定相(Na-VAN CSP)[18]上,未添加CMPA时,化合物1、化合物2均无分离趋势。本文以D-酒石酸(D-Tar)、L-酒石酸二乙酯(L-TADE)、D-酒石酸二乙酯(D-TADE)为CMPA,对化合物1、化合物2进行对映体分离研究。探讨了醇类改性剂以及CMPA的种类和浓度对手性分离的影响。目前,以D-Tar,L-TADE,D-TADE为CMPA用于高效液相色谱手性拆分西那卡塞原料(化合物1)及中间体(化合物2)尚未见报道。
1 实验部分
1.1 仪器与试剂
Agilent1260高效液相色谱仪,二极管阵列检测器;1-萘万古霉素色谱柱(Na-VAN CSP实验室自制,5 μm,250 mm×4.6 mm);1-(1-萘基)乙胺(北京百灵威科技有限公司,纯度98%);西那卡塞中间体(重庆医科大学药学院提供);正己烷、正丙醇(分析纯,天津市风船化学试剂科技有限公司);D-酒石酸、叔丁醇(分析纯,成都化夏化学试剂有限公司);L-酒石酸二乙酯、D-酒石酸二乙酯(分析纯,九鼎化学科技有限公司);无水乙醇、异丙醇(分析纯,天津市永大化学试剂有限公司);正丁醇(分析纯,利安隆博华医药化学有限公司)。
1.2 样品制备
样品以正己烷-乙醇(9∶1,体积比)溶解,经0.22 μm微孔膜过滤,取续滤液备用。所有流动相使用前均经0.45 μm微孔膜过滤并超声脱气。
1.3 色谱条件
1-萘万古霉素色谱柱(实验室自制,250 mm×4.6 mm),流动相由不同体积比的正己烷、醇类改性剂和手性流动相添加剂组成(手性流动相添加剂直接加入醇中)。手性流动相添加剂分别为D-酒石酸(D-Tar)、L-酒石酸二乙酯(L-TADE)、D-酒石酸二乙酯(D-TADE),柱温25 ℃,进样量2 μL,流速1.0 mL/min,检测波长254 nm。
2 结果与讨论
2.1D-Tar CMPA
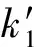

表1 醇类改性剂的种类对化合物1、化合物2手性分离的影响Table 1 Influence of alcohol modifier on enantioseparation of compound 1 and 2
stationaryphase:1-napthalenevancomycinchiralcolumn(5μm,250mm×4.6mm);mobilephase:hexane-alcohol-D-Tar=95∶5∶0.3;flowrate:1.0mL/min;temperature:25 ℃;detectionwavelength:254nm
由表1可见,D-Tar为CMPA,以正丙醇作为醇类改性剂时,化合物1、化合物2对映体获得一定程度的分离,表明正丙醇的空间结构与溶质和CSP之间的适应性最强,选择性最好。在同一条件下,化合物2比化合物1的保留更强,选择因子更大。从结构上看,化合物2比化合物1多1个羰基以及更大的π-π共轭基团,该结果表明,溶质和CSP之间的偶极-偶极作用、π-π作用有利于待测物的保留和分离。
2.1.2D-Tar的浓度对分离的影响 采用正己烷/正丙醇/D-Tar为流动相,考察不同D-Tar浓度对化合物1、化合物2对映体拆分效果的影响。分离结果见表2,色谱图见图2的(1)a和(2)b。其中,(1)和(2)分别表示化合物1和化合物2,a和b,x,c,d表示不同的流动相条件。

表2 D-Tar浓度对化合物1、化合物2手性分离的影响Table 2 Influence of D-Tar concentration on enantioseparation of compound 1 and 2
mobile phase:hexane-n-propanol-D-Tar;the other chromatographic conditions are the same as Table 1
从表2数据可知,增大D-Tar的浓度,化合物1的保留基本不变,选择因子逐渐减小,说明D-Tar不影响化合物1的保留,而低浓度D-Tar有利于分离。D-Tar浓度的增加会使得化合物2的保留因子逐渐减弱,但其分离因子基本不变,说明D-Tar的浓度对分离影响不大。
2.2L-TADE CMPA
在正己烷-醇正相条件下,以L-TADE作为CMPA时,考察了流动相中醇类改性剂的种类对对映体分离的影响,分离结果见表3。
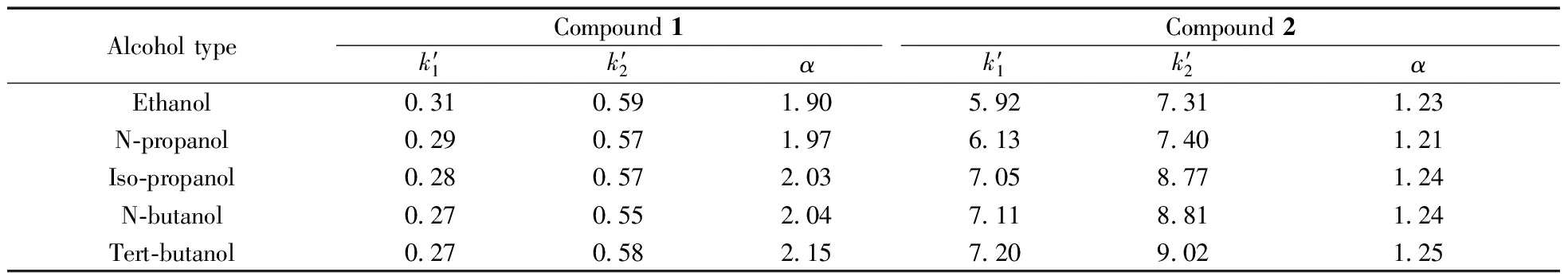
表3 醇类改性剂的种类对化合物1、化合物2手性分离的影响Table 3 The influence of alcohol modifier on the enantioseparation of compound 1 and 2
mobile phase:hexane-alcohol-L-TADE=95∶5∶0.3;the other chromatographic conditions were shown in Table 1
由表3可见,对于化合物1,从乙醇、丙醇到丁醇,保留基本不变,选择因子逐渐增大,说明醇的种类不影响化合物1的保留;但醇分子体积的增大对化合物1对映体的分离有利。
化合物2则随醇类改性剂(乙醇,丙醇,丁醇)改变时,其保留因子逐渐增大,选择因子基本不变,说明醇类改性剂不影响化合物2对映体的分离。随着不同醇(乙醇,丙醇,丁醇)体积的逐渐增大,化合物2的空间位阻逐渐增大,极性减弱,醇类与手性固定相的作用力减弱,溶质与固定相的结合力增强,导致洗脱能力逐渐减弱,保留逐渐增强。
在上述正相条件下,以L-TADE作为CMPA时,化合物2比化合物1的保留更强,但化合物1的选择因子大。
2.3D-TADE CMPA
在正己烷-醇正相条件下,以D-TADE作为CMPA,考察了流动相中醇类改性剂的种类对对映体分离的影响,分离结果见表4,色谱图见图2的(1)d和(2)d。
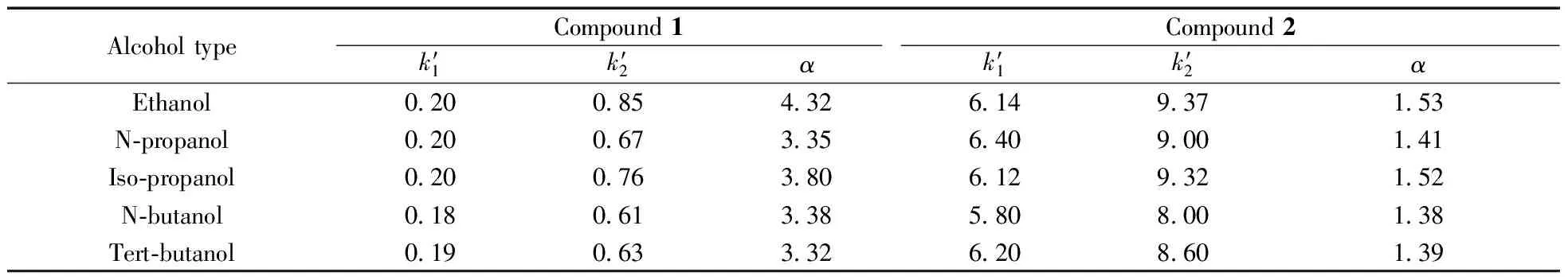
表4 醇类改性剂的种类对化合物1、化合物2手性分离的影响Table 4 Influence of alcohol modifier on enantioseparation of compound 1 and 2
mobile phase:hexane-alcohol-D-TADE=95∶5∶0.3;the other chromatographic conditions were shown in Table 1
由表4可以看出,以D-TADE为CMPA,化合物1的保留基本不变,乙醇为醇类改性剂时,分离因子最大,说明小体积的醇类改性剂对分离有利。化合物2的分离趋势与化合物1类似,其保留更强,分离因子更小。
与L-TADE CMPA相比,以D-TADE为CMPA时,化合物1的保留减弱,但选择因子更大,这是因为,与L-TADE相比,D-TADE与溶质之间更容易形成氢键,竞争了溶质与CSP之间的氢键作用力,使得溶质保留更弱。说明氢键作用力对保留有所贡献。此外,D-TADE的立体构型使溶质易于和CSP,CMPA产生氢键作用和π-π作用,这些作用力有利于溶质的手性识别。
化合物1以L-TADE 为CMPA时,叔丁醇为最佳醇类改性剂;D-TADE为CMPA时,乙醇是最佳醇类改性剂。这些结果表明,除了CMPA的立体构型,流动相中醇类改性剂的分子体积大小也影响着化合物1的对映体分离。
与化合物1类似,醇类改性剂的分子体积大小、CMPA的立体构型等对化合物2的对映体分离均有所影响。如前所述,化合物2结构中增加了偶极-偶极作用位点,CMPA、溶质、CSP之间的氢键作用,偶极-偶极作用,π-π作用共同决定了保留和分离。
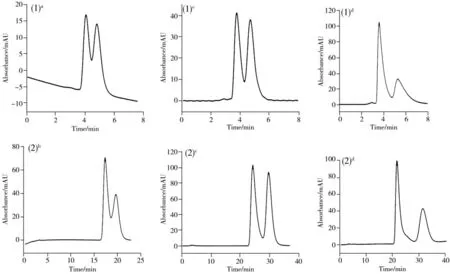
图2 化合物1、化合物2在不同流动相条件下的对映体分离色谱图Fig.2 Chromatograms of enantiomers of compound 1 and 2 under different mobile phases(1):compound 1;(2):compound 2;mobile phase,a:hexane-n-propanol-D-Tar(99∶1∶0.3);b:hexane-n-propanol-D-Tar(95∶5∶0.3);c:hexane-tert-butanol-L-TADE(95∶5∶0.3);d:hexane-ethanol-D-TADE(95∶5∶0.3);the other chromatographic conditions were shown in Table 1
3 结 论
本文以D-酒石酸、L-酒石酸二乙酯、D-酒石酸二乙酯为手性流动相添加剂,自制1-萘万古霉素为手性固定相,对1-(1-萘基)乙胺和西那卡塞中间体的对映体进行分离研究。在实验条件下,两个溶质均获得一定程度的分离,醇类改性剂的分子体积,手性流动相添加剂的立体结构和溶质的结构对手性拆分效果的影响较大。结果表明,酒石酸类衍生物作手性流动相添加剂拆分1-(1-萘基)乙胺及西那卡塞中间体时,溶质、固定相和手性流动相添加剂之间的氢键作用、偶极-偶极作用、π-π作用等共同影响了手性识别。因此,该拆分是手性流动相和手性固定相共同作用的结果。
[1] Hu J.TheSynthesesofChiralNaphthylethylaminesandCalcimimetieCinacalcet.Shanghai:East China University of Science and Technology(胡键.手性萘乙胺和拟钙剂Cinacalcet的合成.上海:华东理工大学),2010.
[2] Lu D Q,Xia F J,Wang Q,Sun S B,Ling Y Q.Mod.Chem.Ind.(卢定强,夏芙洁,王琦,孙生柏,凌岫泉.现代化工),2014,34(5):30-34.
[3] Bijukumar G,Maloyesh B,Bhaskar B S,Rajendra A.Synth.Commun.,2008,38(10):1512-1517.
[4] Zhang M Q.ShanghaiMed.Pharm.J.(张明清.上海医药),2004,25(7):329-330.
[5] Zhang F,Zheng R,Xia B Y,Zeng Y,Zhang D.WestChin.J.Pharm.Sci.(张锋,郑蓉,夏彬一,曾洋,张丹.华西药学杂志),2014,29(1):75-76.
[6] Shinde G B,Niphade N C,Toche R B,Mathad V T.Org.Proc.Res.Dev.,2011,15(2):455-461.
[7] Lei F,Qu B Y,Li X L,Guo L,Guan M,Hai L,Jin H,Wu Y.Synth.Commun.,2014,44(19):2879-2885.
[8] Li L L,Hu X F,Yang Y L,Zhu X Y,Yuan Z D.Chin.NewDrugsJ.(李林羚,胡雪峰,杨玉雷,朱雪焱,袁哲东.中国新药杂志),2013,22(7):834-836.
[9] Lu D Q,Sun S B,Ling Y Q,Wang Q,Xia F J.Chem.Res.Appl.(卢定强,孙生柏,凌岫泉,王琦,夏芙洁.化学研究与应用),2015,27(6):882-885.
[10] Lajkó G,Orosz T,Grecsó N,Fekete B,Palkó M,Fülöp F,Lindner W,Péter A,Ilisz I.Anal.Chim.Acta,2016,921:84-94.
[11] Yang C Y,Wang Y F,Sun W W,Yang J R,Lu Z Y,Yuan L M.J.Instrum.Anal.(杨璨瑜,王一帆,孙维维,杨江蓉,路振宇,袁黎明.分析测试学报),2014,33(10):1142-1147.
[12] Liu Z X,Yong T P,Li Y S,Zhou Y P,Dai G L,Lu Y.Chin.J.Clin.Pharm.(刘子修,雍太萍,李燕思,周艳萍,戴国梁,陆瑜.中国临床药学杂志),2013,22(1):59-62.
[13] Song J F,Feng S W,Xu X D,Liu L J,Song C K,Wen X K,Chen J Y,Li F K,Okamoto Y.Chin.J.Chromatogr.(宋佳枫,冯四伟,徐晓冬,刘立佳,宋超坤,温晓琨,陈进勇,李芳坤,冈本佳男.色谱),2016,34(1):74-79.
[14] Yang L,Liao Y,Zhou Z Q,Jiang S R,Wang P.J.Instrum.Anal.(杨丽,廖勇,周志强,江树人,王鹏.分析测试学报),2004,23(5):133-135.
[15] Dan M J,Hao P,Zhao Y,Li P F.Chin.Terminol.(淡美俊,郝鹏,赵怡,李鹏飞.中国科技术语),2016,3:62-64.
[16] Ye X X.HighPerformanceLiquidChromatographySeparationofChiralEnantiomersUsingChiralMobilePhaseAdditives.Shanghai:Northeastern University(叶祥喜.高效液相色谱手性流动相添加剂法拆分手性对映体.上海:东华大学),2014.
[17] Chen Y J.China Patent,CN104152528A,2014.11.19.
[18] Yu X Y,Gu X J,Xie Y,Qu S L,Shen B C.Phys.Chem.Anal.:Chem.Anal.(余小燕,谷晓娟,谢宇,屈尚蓝,沈报春.理化检验:化学分册),2012,48(8):884-892.
Enantiomeric Separation of Raw Material and Intermediate of Cinacalcet Using Chiral Mobile Phase Additives
YAO Yan-yun,SUN Kong-chun,WANG Yong-xi,YANG Qian,WANG Le,CHEN Xi-long,SHEN Bao-chun*
(School of Pharmaceutical Science & Yunnan Key Laboratory of Pharmacology for Natural Products,Kunming Medical University,Kunming 650500,China)
An HPLC method was established for the chiral separation of cinacalcet raw material,1-(1-naphthyl) ethylamine(compound 1) and intermediate of cinacalcet(compound 2),by using self-made 1-naphthalene vancomycin as chiral stationary phase(Na-VAN CSP),andD-tartaric acid(D-Tar),L-tartaric acid diethyl ester(L-TADE) andD-tartaric acid diethyl ester(D-TADE) as chiral mobile phase additives(CMPA),respectively.The influences of alcohol modifiers and CMPA types were studied.The mechanism of enantioseparation was also discussed.On Na-VAN CSP,compound 1 and 2 got certain degree of enantioseparation with different CMPA under normal phase conditions.WhenD-TADE was used as CMPA,the optimal enantioseparation for both compound 1 and 2 was obtained.The results showed that the size of alcohol modifier and the three dimensional configuration of CMPA played an important role in the enantioseparation.
1-(1-naphthyl) ethylamine;intermediate of cinacalcet;1-naphthalene vancomycin;chiral mobile phase additive;enantioseparation
2016-08-31;
2016-09-25
国家自然科学基金资助项目(81102408)
10.3969/j.issn.1004-4957.2017.02.015
O657.72;TQ460.72
A
1004-4957(2017)02-0242-05
*通讯作者:沈报春,博士,教授,研究方向:色谱柱制备和手性化合物分离,Tel:0871-65922780,E-mail:shen_baochun@126.com

