一种强阴离子交换树脂的制备及用于蜂蜜中喹诺酮类药物的富集检测
张田丽,胡 坪,曲芳慧,王月荣,章弘扬
(华东理工大学 化学与分子工程学院 上海市功能性材料化学重点实验室,上海 200237)
一种强阴离子交换树脂的制备及用于蜂蜜中喹诺酮类药物的富集检测
张田丽,胡 坪,曲芳慧,王月荣*,章弘扬*
(华东理工大学 化学与分子工程学院 上海市功能性材料化学重点实验室,上海 200237)
采用沉淀聚合法,合成了对氯甲基苯乙烯-二乙烯基苯共聚物(VBC-DVB),并通过与三甲胺修饰反应,获得了一种含季铵基团的强阴离子交换树脂(SAX)。表征结果显示,树脂是呈单分散形态的微球,平均粒径为(3.8±1.5) μm,且具有较高的离子交换容量(0.83 meq/g)及良好的选择性吸附性能,对5种喹诺酮类药物(诺氟沙星、环丙沙星、洛美沙星、加替沙星、司帕沙星)的饱和吸附容量明显高于同类型商品化Oasis MAX固相萃取柱。将其用于蜂蜜样品中5种喹诺酮药物的选择性富集和HPLC分析。结果显示,该方法在一定范围内线性关系良好(r2≥0.998 9),平均加标回收率为86.8%~120.3%,日内重复性RSD不大于7.0%,日间RSD不大于8.5%。研究结果表明,所制备的SAX材料可用于复杂基质中喹诺酮类药物残留的高效前处理分析。
强阴离子交换;三甲胺修饰;固相萃取;蜂蜜;喹诺酮类药物;HPLC分析
阴离子交换树脂在环境废水处理[1]、蛋白质的分离纯化[2]、食品安全[3]以及金属离子检测[4-5]等方面,有着广泛的应用。传统方法制备阴离子交换树脂,主要是将苯乙烯-二乙烯基苯共聚物(ST-DVB)进行氯甲基化,再通过胺化反应获得[6]。但是,在氯甲基化过程中使用的氯甲醚、二氯甲醚等试剂具有较强的致癌性[7],因此该方法在一定程度上受到限制。为此,本文在Ezzeldin等[8]研究的基础上,采用沉淀聚合法将对氯甲基苯乙烯(VBC)和二乙烯基苯(DVB)作为反应原料合成共聚物,再以三甲胺为修饰试剂进行胺化反应,得到一种强阴离子交换树脂(SAX)。该制备方法不仅避免了氯甲醚等致癌性试剂的使用,且胺化反应时间缩短至文献方法[8]用时的1/4,用料安全,步骤简单。
喹诺酮是一类合成抗生素类药物,作为预防和治疗药物普遍用于动物饲养中[9]。为了预防和治疗蜜蜂下痢病,蜂农们常在饲料中添加喹诺酮类药物,因此蜂蜜中喹诺酮类药物的残留已引起普遍关注[10]。目前,蜂蜜中喹诺酮类药物的检测较多采用HPLC-FLD[11-12]及LC-MS/MS[13]进行测定。虽然这些方法灵敏度高(主要依赖仪器),但其前处理分析大多使用溶液提取结合Oasis HLB柱[14-15]进行净化,这些步骤的选择性和除杂富集效果还有待提高。本研究在成功制备出SAX材料的基础上,将其作为固相萃取填料,用于蜂蜜样品中喹诺酮类药物(诺氟沙星、环丙沙星、洛美沙星、加替沙星、司帕沙星)的选择性富集和HPLC分析,从而为复杂基质中该类药物残留的检测提供了新思路。
1 实验部分
1.1 仪器与试剂
DF-101S集热式恒温加热磁力搅拌器(河南省巩义市予华仪器有限责任公司);TDL-5A台式离心机(江苏省无锡市瑞江分析仪器有限公司);DZX-3真空干燥箱(上海福玛实验设备有限公司);GZX-9140 MBE数显鼓风干燥箱(上海博迅实业有限公司);PB1501-N精密天平(瑞士梅特勒-托利多公司);EPED-E2-10TF实验室超纯水机(南京易普易达科技发展有限公司);KQ-500DE型数控超声波清洗器(江苏省昆山市超声仪器有限公司);Nicolet 380红外光谱仪(美国赛默飞世尔科技有限公司);JSM-6360LV扫描电子显微镜(日本日立S-3400N公司);ASAP 2020全自动比表面积及微孔物理吸附分析仪(美国麦克默瑞提克有限公司);激光粒度分析仪(珠海欧美克仪器有限公司);12位固相萃取装置,0.22 μm微孔滤膜(日本岛津技迩公司);DC-12氮吹仪(上海安谱科学仪器有限公司);振动涡旋混合器(江苏省金坛市医疗设备厂);固相萃取空柱管及筛板(上海德里安仪器有限公司);Oasis MAX固相萃取柱(美国Waters公司);Shimadzu LC-20AT高效液相色谱仪(日本岛津公司)。
中性氧化铝(200~300目)、无水三氯化铁、氢氧化钠、硝基甲烷、甲醇(上海国药集团化学试剂有限公司);偶氮二异丁腈(AIBN)、甲苯、丙酮、乙醚、1,2-二氯乙烷(DCE)、硝酸、甲酸、氨水(上海凌峰化学试剂有限公司);对氯甲基苯乙烯(VBC,90%,日本TCI公司);二乙烯基苯(DVB,80%)、尿酸(上海阿拉丁试剂公司);乙腈(HPLC级,德国Merck公司);硫氰酸铵(湖州市菱湖食品化工厂);三甲胺水溶液(33%)、安替比林(99%)、诺氟沙星(98%)(上海麦克林生化科技有限公司);环丙沙星(98%,北京百灵威科技有限公司);洛美沙星(>98%)、加替沙星(>99%)(上海思域化工科技有限公司);司帕沙星(99%,上海萨恩化学技术有限公司);蜂蜜样品(宜春市景福实业有限公司)。
1.2 SAX树脂的制备
在装有球形冷凝管、氮气保护装置和磁力搅拌装置的三口圆底烧瓶(1 000 mL)中加入800 mL乙腈,冰浴条件下依次加入12 g VBC,4 g DVB和0.464 g AIBN。温度从室温缓慢升至60 ℃,并保持在该温度继续反应46 h。反应结束后,冷却至室温,离心过滤,滤饼依次用甲醇、甲苯和丙酮超声洗涤,40 ℃真空干燥,得共聚物的母体微球(Precursor particles,PP)[16]。
在250 mL三口圆底烧瓶中加入3 g PP微粒和30 mL DCE,在氮气氛围下使PP微粒充分溶胀,滴加30 mL三甲胺溶液,以无水三氯化铁作为催化剂,磁力搅拌下快速升温至80 ℃,并保持在该温度反应24 h[1,8]。反应结束后,冷却至室温,离心过滤,滤饼先用甲醇超声洗涤,再用硝酸溶液(pH 1.0)洗涤至上清液用硫氰酸铵检测不变红为止。随后以丙酮为提取剂,再用索氏提取器回流提取12 h。依次用甲醇和乙醚超声洗涤,真空干燥得SAX微粒。三甲胺修饰的SAX树脂的合成过程如图1所示。称取60 mg上述SAX微粒,用甲醇分散,均匀紧密地装填于3 mL固相萃取空柱管中,制得60 mg/3 mL固相萃取柱。
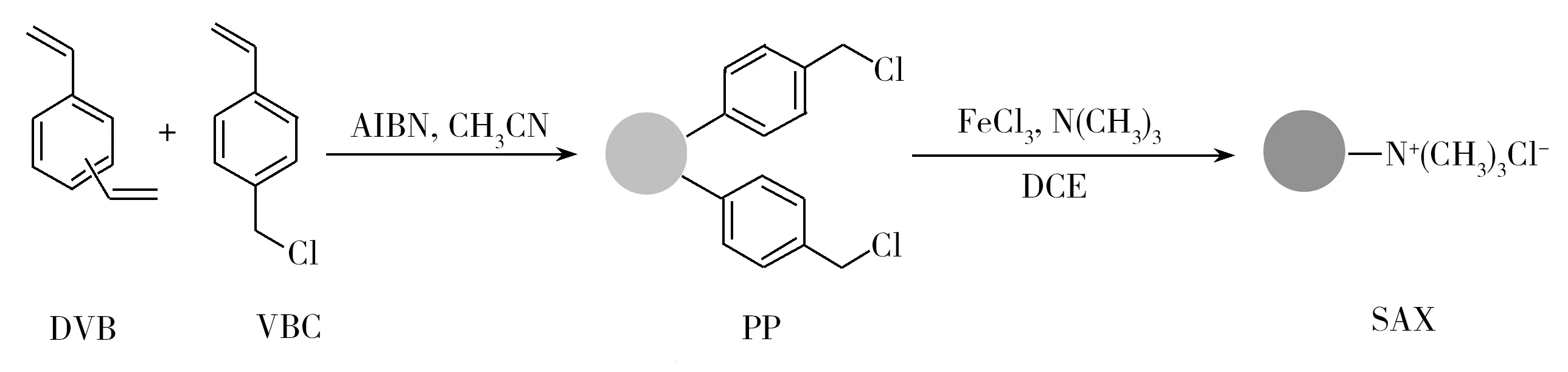
图1 阴离子交换树脂的合成过程Fig.1 Synthetic procedure of the SAX particles
1.3 吸附性能考察
1.3.1 吸附选择性考察 将弱酸性物质(尿酸)、两性物质(洛美沙星、司帕沙星)和碱性物质(安替比林) 4种标样,配制成浓度为10 μg/mL的混合标准溶液。取1 mL混合标液上样,依次用3 mL 5%氨化甲醇和3 mL甲醇淋洗,再用3 mL 10%甲酸-甲醇溶液洗脱。将收集的上样液过滤后,直接进行HPLC分析;将淋洗液及洗脱液氮吹浓缩至干,用500 μL 0.1%甲酸水溶液复溶,过滤后进行HPLC分析。根据相应的色谱峰面积比,分别计算目标物在SAX和Oasis MAX柱上各步萃取过程中的回收率。
1.3.2 饱和吸附容量测定 取诺氟沙星、环丙沙星、洛美沙星、加替沙星和司帕沙星5种喹诺酮标样,分别配制成1 000 μg/mL的标准溶液。每种单标液的上样体积均为3 mL,连续收集流出液,并分别进行HPLC分析,直至SPE柱吸附达到饱和(流出液与上样液的浓度相当)。以单标液单点校正法,分别计算各流出液中5种物质的浓度,计算其饱和吸附容量。
1.3.3 HPLC分析 色谱柱:ACE 5 AQ-C18反相柱(250 mm×4.6 mm,5 μm);流动相:A为0.1%甲酸水溶液,B为乙腈;梯度洗脱程序:0~5 min,15%B;5~8 min,15%~40%B;8~12 min,40%B;12~12.01 min,40%~80%B;12.01~35 min,80%B;检测波长:275 nm;进样量:10 μL;流速:1 mL/min;柱温:25 ℃;样品室温度:4 ℃。
1.4 蜂蜜中5种喹诺酮类药物的测定
称取1 g蜂蜜于50 mL离心管中,加入1 mL不同浓度的喹诺酮混合标液,混合均匀后,再加入10 mL乙腈提取,涡旋3 min,超声60 min后,高速离心,收集上清液。沉淀物中再加入10 mL乙腈,重复上述操作3次,将所有上清液合并,45 ℃旋蒸至近干,加入1 mL超纯水复溶,得到蜂蜜提取液[17]。
将制备的蜂蜜提取液上样至活化的SPE柱(依次用3 mL甲醇和3 mL超纯水活化)。待样品完全流出后,依次以5%氨化甲醇和甲醇溶液淋洗SPE柱,最后用10%甲酸-甲醇溶液洗脱。收集洗脱液,氮吹至干,用200 μL 0.1%甲酸水溶液复溶,经滤膜过滤后进HPLC测定。色谱条件除了采用进样量为20 μL以及梯度程序中0~5 min流动相为17%B外,其余条件同“1.3.3”。
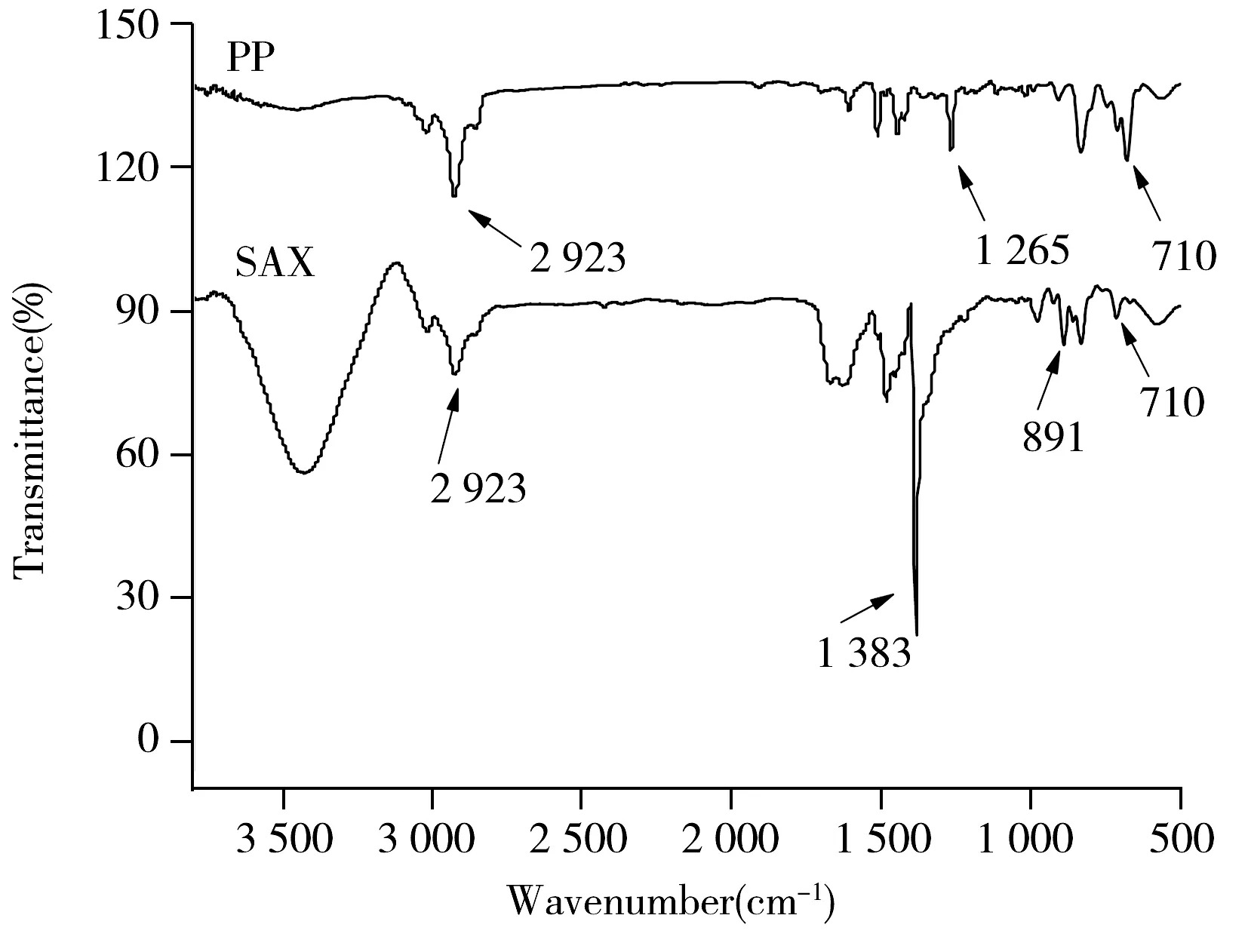
图2 PP和SAX的红外光谱图Fig.2 FTIR spectra of PP and SAX resins
2 结果与讨论
2.1 SAX树脂的合成及表征
SAX树脂的合成如图1所示,与以往方法相比[1,8],该反应操作简便、安全,且成本低。所得树脂(PP,SAX)的红外光谱如图2所示,其中PP微粒在1 265 cm-1和710 cm-1处的吸收峰,分别为CH2—Cl上的C—H弯曲振动和C—Cl伸缩振动吸收峰。而SAX微粒在这两处的吸收峰强度明显降低,说明C—Cl键在修饰反应过程中明显减少。此外,SAX微粒在891 cm-1处的吸收峰为R—N+—(CH3)3的特征伸缩振动[8],在1 383 cm-1处的吸收峰为—CH3的弯曲振动峰,说明已成功地将季铵基修饰到树脂上。
SAX树脂的扫描电镜图如图3所示。可见树脂呈大小均匀(粒径为2~4 μm)、单分散状态的微球,远小于商品化Oasis MAX的粒径(~30 μm)。通过测定,该树脂的比表面积为6.6 m2/g,孔径大小为77 Å,粒径分布在(3.8±1.5) μm之间。通常对于固相萃取填料而言,其粒径越小,吸附容量越高。此外,采用国标法[18]测定SAX树脂的离子交换容量为0.83 meq/g,显著高于Oasis MAX的离子交换容量(0.29 meq/g,测定方法[18])。说明本文所研制的SAX树脂表面修饰了更多的季铵基团。
2.2 SAX树脂的吸附选择性与饱和吸附容量考察
2.2.1 吸附选择性考察 为了考察本研究合成的SAX树脂的吸附选择性,选择了酸性的尿酸、2种两性喹诺酮类药物(洛美沙星和司帕沙星)及碱性的安替比林标准混合溶液(浓度均为10 μg/mL)进行实验。以1 mL上样,在本研究所合成的SAX柱和商品化Oasis MAX柱上各步萃取过程中的回收率如表1所示。结果发现,使用SAX柱对弱酸性的尿酸及两性的洛美沙星、司帕沙星有良好的选择性吸附,回收率为88.9%~91.3%,相对标准偏差(RSD,n=3)不大于5.5%,且在甲醇淋洗液中未检测到尿酸、洛美沙星和司帕沙星的色谱峰。这说明该树脂与弱酸性及两性化合物之间不仅存在反相作用力,同时存在离子作用力,且离子作用力起主要作用,因此即使采用甲醇作为淋洗液也不能将其淋洗下来。而对于碱性物质安替比林,在5%氨化甲醇淋洗条件下,几乎全部被淋洗下来,说明其与树脂间只存在反相作用力。因此,本研究所合成的SAX树脂具有对碱性物质除杂和对弱酸性及两性物质选择性富集的效果。与之相比,Oasis MAX柱对弱酸性的尿酸及两性的洛美沙星、司帕沙星的吸附回收率为70.1%~86.4%,RSD(n=3)≤13.2%,其吸附选择性效果不及SAX柱。
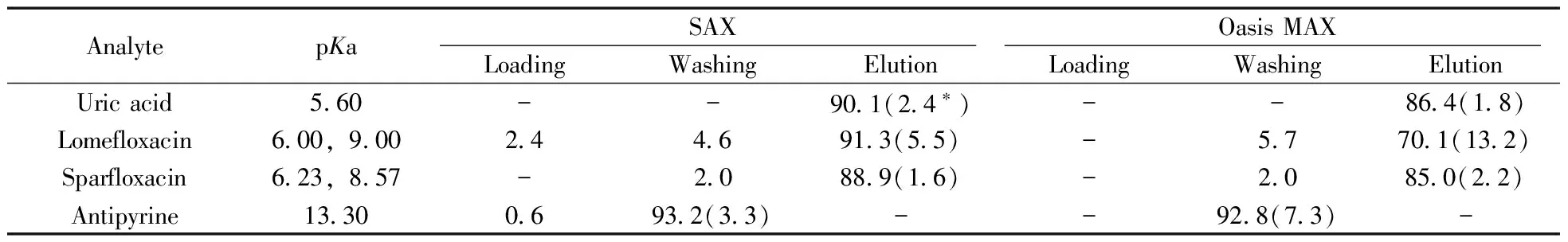
表1 4种被测物在SAX和Oasis MAX柱上各步萃取过程中的回收率与相对标准偏差(%,n=3)Table 1 Recoveries and RSDs of four analytes extracted by SAX and Oasis MAX in different steps(%,n=3)
*:RSD values(n=3);-:no peak signal
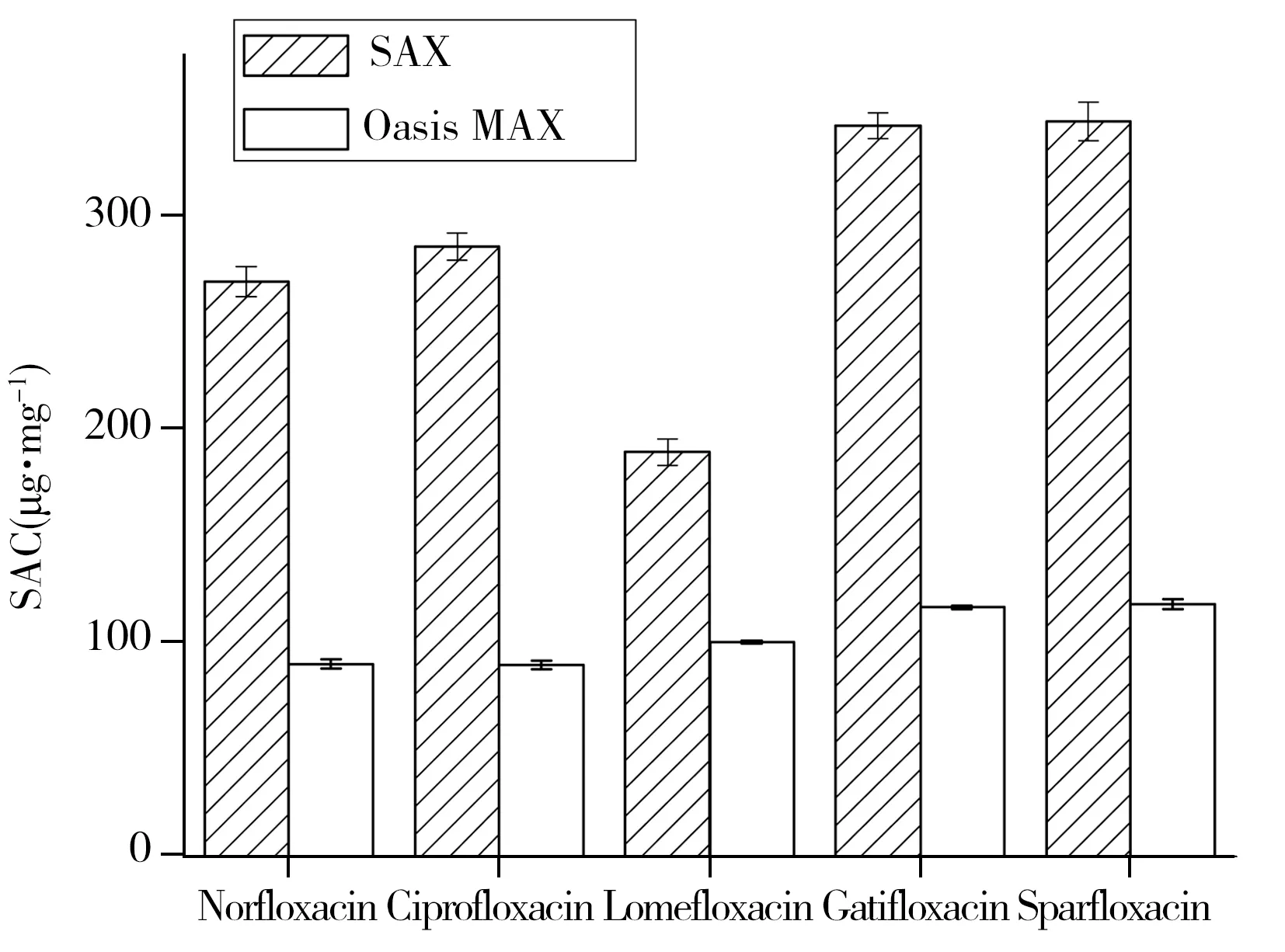
图4 SAX和Oasis MAX树脂对5种喹诺酮类药物的饱和吸附量Fig.4 Saturated adsorption capacities of five quinolone drugs in SAX and Oasis MAX sorbents
2.2.2 饱和吸附容量测定 按照“1.3.2”方法测得SAX和Oasis MAX柱对5种喹诺酮类物质的饱和吸附容量如图4所示。结果表明,SAX固相萃取柱对这些物质的饱和吸附容量,均明显高于商品化Oasis MAX柱,RSD(n=3)≤9.1%。
2.3 SAX固相萃取柱用于蜂蜜中5种喹诺酮类药物的分析
2.3.1 蜂蜜中喹诺酮药物的固相萃取-HPLC分析 在优化色谱条件下,未经固相萃取和经SAX固相萃取的蜂蜜加标提取液的色谱图如图5所示。由图可见,在经过固相萃取处理后,不仅可去除大量的基质干扰(如4 min左右基质峰),而且可选择性吸附和富集喹诺酮类成分,从而提高了检测灵敏度和选择性,有利于对其进行准确定量分析。

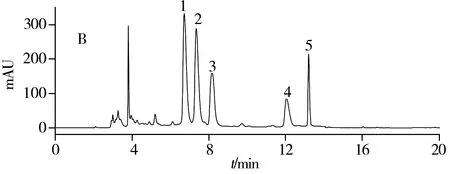
图5 未经固相萃取(A)和经过SAX固相萃取(B)的蜂蜜加标提取液的色谱图Fig.5 HPLC chromatograms of the spiked honey extracts without(A) or with SAX SPE treatment(B)1.norfloxacin,2.ciprofloxacin,3.lomefloxacin,4.gatifloxacin,5.sparfloxacin;spiked concentrations are 5 μg/g for each compound
2.3.2 方法的线性范围、检出限及定量下限 按照“1.4”方法对蜂蜜样品进行处理,获得不同浓度(0.010 23~10.71 μg/g)的5种喹诺酮类混合标液,经SAX固相萃取后,进HPLC分析。其中,检出限和定量下限分别设定为信噪比的3倍和10倍。线性关系、检出限以及定量下限结果如表2所示。5种喹诺酮类药物在一定范围内均呈现良好的线性关系(r2≥ 0.998 9),其LOD为3~10 ng/g,LOQ为10~34 ng/g。根据我国规定动物食品中喹诺酮类药物的最高残留量为0.01~1.9 μg/g[9],可知该方法的灵敏度较高,可以满足实际样品的分析要求。
2.3.3 方法的准确度与重复性 对5种喹诺酮类药物,分别设定0.2,0.5,1.0 μg/g 3个加标水平,按照“1.4”步骤获得不同浓度的蜂蜜加标提取液1 mL,上样至活化的SAX柱。收集3 mL 10%甲酸甲醇洗脱液,氮吹至干,用200 μL 0.1%甲酸水溶液复溶,经滤膜过滤后进行HPLC分析,按照表2中的线性方程,分别计算5种喹诺酮类药物的浓度和回收率。平行配制6份0.5 μg/g的蜂蜜加标样品,在同1 d内连续测定,计算5种药物含量变化的RSD值,即为日内重复性;3天内配制和测定9份0.5 μg/g的蜂蜜加标样品(每天平行配制和测定3份),计算3天内5种药物含量变化的RSD值,即为日间重复性。由表3可见,5种待测物的加标回收率为86.8%~120.3%,RSDs≤7.1%,日内RSDs≤7.0%,日间RSDs≤8.5%,方法的准确度与精密度能够满足实际样品分析的要求。

表2 蜂蜜中5种喹诺酮类药物的线性关系、检出限及定量下限Table 2 Linearity relations,limits of detection and limits of quantitation of five quinolone drugs in honey samples
LOD:limit of detection,LOQ:limit of quantitation;y:integrated peak area,x:concentration of corresponding standard
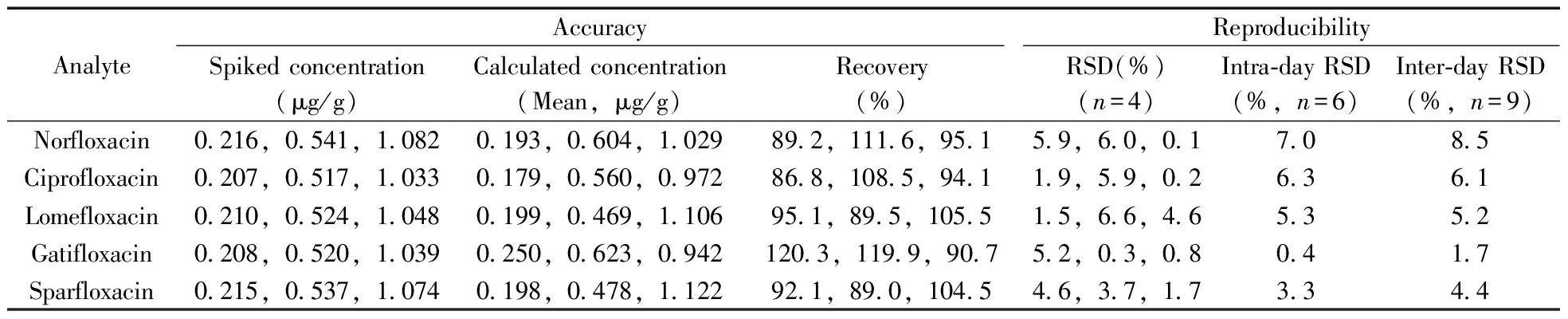
表3 蜂蜜中5种喹诺酮类药物的测定准确度及重复性Table 3 Accuracy and reproducibility of five quinolone drugs in honey samples
3 结 论
本文通过将三甲胺修饰VBC-DVB共聚物,制备了一种SAX树脂。表征结果显示,树脂为呈单分散形态的微球,其粒径范围为(3.8±1.5) μm,具有较高的离子交换容量(0.83 meq/g)。该树脂填料对弱酸性物质(尿酸)及两性物质(洛美沙星和司帕沙星)的选择性吸附结果良好(回收率≥ 88.9%),且对5种喹诺酮类药物的饱和吸附容量明显高于同类型商品化Oasis MAX固相萃取柱。将所制备的SAX树脂用于蜂蜜中5种喹诺酮类药物的选择性富集和HPLC分析,方法的灵敏度较高,重现性好,准确度高,可为复杂基质中喹诺酮类药物残留的测定提供一种简单有效的方法。
[1] Bratkowska D,Davies A,Fontanals N,Cormack P A,Borrull F,Sherrington D C,Marce R M.J.Sep.Sci.,2012,35(19):2621-2628.
[2] Xie H Q,Zhou C S.Chem.Res.Appl.(谢红旗,周春山.化学研究与应用),2006,(2):211-213.
[3] Díaz-Alvarez M,Turiel E,Martín-Esteban A.Anal.Bioanal.Chem.,2009,393(3):899-905.
[4] Li X,Wei R Q,Gao Z,Liu X N.Chin.J.Process.Eng.(李响,魏荣卿,高展,刘晓宁.过程工程学报),2008,8(3):494-498.
[5] Dai J,Qu J G,Zhang J.J.Instrum.Anal.(戴洁,瞿建国,张经.分析测试学报),2012,31(8):903-908.
[6] Xu J W.Chem.World(许景文.化学世界),1958,12:551-554.
[7] Kuschner M,Laskin S,Drew R T,Cappiello V,Nelson N.Arch.Environ.Health,1975,30(2):70-72.
[8] Ezzeldin H A,Apblett A,Foutch G L.Int.J.Polym.Sci.,2010,2010:1-9.
[9] Li Y L,Xu C L.FoodSci.(李雅丽,胥传来.食品科学),2007,28(11):628-633.
[10] Wang A H,Zhang M N,Li Y X,Bao J M.NewChem.Mater.(王爱华,张梦娜,李优鑫,包建民.化工新型材料),2014,42(5):198-201.
[11] Gao Q,Zheng H B,Luo D,Ding J,Feng Y Q.Anal.Chim.Acta,2012,720:57-62.
[12] He X M,Zhu G T,Zheng H B,Xu S N,Yuan B F,Feng Y Q.Talanta,2015,140:29-35.
[13] Mottier P,Hammel Y A,Gremaud E,Guy P A.J.Agric.FoodChem.,2008,56:35-43.
[14] SN/T 2578-2010.Determination of Fifteen Quinolones Residues in Royal Jelly for Import and Export-LC-MS/MS.In and Out of Inspection and Quarantine of the People's Republic of China Industry Standard(进出口蜂王浆中15种喹诺酮类药物残留量的检测方法 液相色谱-质谱/质谱法.中华人民共和国出入检验检疫行业标准).
[15] Hou J B,Xie W,Chen X M,Xi J Y,Qian Y,Wang F,Liu H S.Chin.J.Chromatogr.(侯建波,谢文,陈笑梅,奚君阳,钱艳,王峰,刘海山.色谱),2011,29(6):535-542.
[16] Xu Y T,Liu J,Zhang H Y,Jiang M,Cao L L,Zhang M,Sun W,Ruan S L,Hu P.Talanta,2016,151:172-178.
[17] Li Y Z,Li Z Q,Wang W P,Zhong S X,Chen J R,Wang A J.J.Chromatogr.A,2016,1447:17-25.
[18] GB/T 11992-2008.Determination of Exchange Capacity of Strong Basic Anion Exchange Resins in Chloride Form.National Standards of the People's Republic of China(氯型强碱性阴离子交换树脂交换容量测定方法.中华人民共和国国家标准).
Synthesis of a Strong Anion-exchange Resin and Its Application in Enrichment and Determination of Quinolone Drugs in Honey
ZHANG Tian-li,HU Ping,QU Fang-hui,WANG Yue-rong*,ZHANG Hong-yang*
(Shanghai Key Laboratory of Functional Materials Chemistry,School of Chemistry and Molecular Engineering,East China University of Science and Technology,Shanghai 200237,China)
The chloromethyl styrene-divinylbenzene copolymer(VBC-DVB) was synthesized by the precipitation polymerization.The strong anion-exchange resin(SAX) containing quaternary ammonium group was then functionalized with trimethylamine.The resulting resins were characterized in the form of monodisperse microspheres,with mean diameters of(3.8±1.5) μm.The resin possessed a high ion-exchange capacity(0.83 meq/g) and a good adsorption performance in selectivity,and its saturated adsorption capacities for five quinolone drugs(norfloxacin,ciprofloxacin,lomefloxacin,gatifloxacin,sparfloxacin) were higher than those of conventional commercially available Oasis MAX SPE sorbents.The resin was used for the selective extraction and HPLC analysis of five quinolone drugs in honey samples.The method showed a good linear relationship in the certain concentration with correlation coefficients(r2) not less than 0.998 9.The average spiked recoveries were between 86.8%and 120.3%.The RSDs of intra-day and inter-day were not more than 7.0%and 8.5%,respectively.The results mentioned above indicated that the SAX material prepared was suitable for the efficient pretreatment of quinolone drug residues in complex matrices.
strong anion-exchange;trimethylamine modification;solid-phase extraction;honey;quinolone drugs;HPLC analysis
2016-08-18;
2016-09-20
国家自然科学基金项目(81202493)
10.3969/j.issn.1004-4957.2017.02.013
O657.72;TQ460.72
A
1004-4957(2017)02-0230-06
*通讯作者:章弘扬,博士,副教授,研究方向:复杂样品前处理与分离分析,Tel:021-64252844,E-mail:hongyang_zhang@ecust.edu.cn 王月荣,博士,讲师,研究方向:色谱及其联用分析,Tel:021-64252844,E-mail:wangyuerong@ecust.edu.cn

