氧化石墨阳离子交换容量测定过程中结构的变化
王泉珺 孙红娟 彭同江 冯明珠
(1西南科技大学理学院,四川 绵阳 621010;2西南科技大学矿物材料及应用研究所,四川 绵阳 621010;3西南科技大学分析测试中心,四川 绵阳 621010)
氧化石墨阳离子交换容量测定过程中结构的变化
王泉珺1孙红娟2,*彭同江2,3冯明珠2
(1西南科技大学理学院,四川 绵阳 621010;2西南科技大学矿物材料及应用研究所,四川 绵阳 621010;3西南科技大学分析测试中心,四川 绵阳 621010)
氧化石墨(GO)结构层上的碳羟基(―C―OH)和边缘羧基(―COOH)在水介质中发生质子化反应解离出的 H+具 有 阳离子可交换性 。 实 验 采用甲醛缩合法 测 量 了 GO 的 阳离子交换容量(CEC), 用 X 射线衍射(XRD)、傅里叶变换红外(FTIR)光谱和X 射线光电子能谱(XPS)分析测试手段对 GO 阳离子交换过程中间产物的结构变化进行了分 析。结 果表明 ,GO 的 CEC 高 达 541.48 mmol/100 g。NH4+和 Ca2+交换后 的 GO,保 持稳定的层状结构,c 轴方向层间距分别增大了 0.1499 和 0.2905 nm。NH4+和 Ca2+主要以层间可交换阳离子形式存在于层间域中,并与水分子形成可交换水化阳离子层,部分以[NH4(H2O)6]+和[Ca(H2O)6]2+的形式存在于结构层的边缘附近,共同平衡结构层水解产生的负电荷。
氧化石墨;含氧官能团;阳离子交换容量;层间域;结构变化
1 引言
阳离子交换容量(CEC)是层状或架状硅酸盐矿物1,2和 阳 离子交 换 树脂3中可交 换 性阳离子 能 力的重要度量指标。氧化石墨(GO)结构层中含氧官能团如碳羟基(―C―OH)和羧基(―COOH)由于质子化作用而具阳离子交换性4,5,研究 GO 阳离子交换过程中结构的规律性变化对于新型GO材料的功能化改性具有重要意义。
甲醛缩合法6测定CEC的方法简单易操作,在工业上被广泛使用1,2,7。常见层状结构硅酸盐矿物的 CEC 约 10-180 mmol/100 g6,8,9,负电荷主要源自结构中异价阳离子之间的类质同象代替,而酸性阳离子交换树脂(CER)的 CEC 约为 400-482 mmol/ 100 g10,11,数倍黏土矿物,这与 CER 立体网状骨架中含有活性基团如磺酸基(―SO3H)和―COOH 等基团可解离出 H+有关,溶液中其它阳离子可与 H+发生离子交换反应12。理论研究已表明 GO 的每个酸性位点对应于约 10 个碳原子,即对应于 100 g GO则包含能够参与阳离交换反应的酸性位点 500-800 mmol13,14。 冯 明 珠 等4研究了不同氧化程度 GO的 CEC,最大值为 450 mmol/100 g,结果表明并非GO的氧化程度越高CEC越大,而是与GO结构层接入―C―OH的含量密切相关。
GO保持着类似石墨的层状结构,具有相对稳定的结构层和开放的层间域,由于结构层含有―C―OH、环氧基(C―O―C)和―COOH 等含氧官能团使结构层厚度增加15,而且由于含氧官能团具有良好的亲水性16可将水分子引入层间域中,这导致 GO 层 间 距 进 一 步 增 大17, 受 到 环 境 湿 度 的 影响,GO 的底面间距在 0.6-1.1 nm 之间变化18。Liu等18研究了不同链长的季铵盐阳离子插入 GO 层间后c轴方向层间距发生了规律性变化,并且有机物插入GO层间域中形成的纳米复合材料能够提升GO 原有的物理化学性质19。当前对 GO 的无机阳离子交换过程的研究还未引起足够重视,阳离子交换过程中GO结构的变化及交换后阳离子在GO层间域中结构形态的研究尚未见报道。
本文基于前期对GO制备、结构和理化性质20的研究,为查明阳离子交换容量测定过程中GO结构的变化及阳离子在层间的结构形态,采用甲醛缩合法对制备的GO的CEC进行了测定,采用X射线衍射(XRD)、傅里叶变换红外(FTIR)光谱和 X 射线光 电 子 能谱(XPS)等对阳离 子 交 换过程中 NH4+和 Ca2+交换后 GO 产物进行表征 ,以揭示 GO 在阳离子交换过程中的结构变化,这对于改变GO层间阳离子种类,用于催化反应和吸附分离,以及通过离子交换插层制备纳米复合材料和环境吸附材料具有重要理论和实际意义。
2 实验部分
2.1 原料与试剂
原料:GO 自制。基于改进 Hummers法20制备GO 的步骤:(1)在冰水浴条件下向 140 mL 98%的浓 H2SO4中缓慢加入 4 g 天然鳞片石墨粉末(碳含量~99%,过 200 目标准筛),磁力搅拌 30 min 使其混合均匀后低温下超声(<15 °C,200 W)10 min,而后将 16 g KMnO4粉末(200 目)缓慢分散于上述浓硫酸和石墨混合液中,继续在冰水浴中搅拌3 h后升温至 37 °C,保持 37 °C 搅拌 1 h;(2)将盛有反应液的烧杯再次置于冰水浴中磁力搅拌,并将 250 mL蒸馏水少量多次滴加到反应液中,控制其温度在60-65 °C,待反应液降温至 40 °C时,逐滴加入5%(w,质 量分 数)H2O2, 直 至 反应 液不 再 冒 泡 ,继续磁力搅拌 1 h 获得反应产物;(3)用超纯水反复透析反应产物至接近中性后在 9000 r·min-1条件下离心除去杂质,得到GO水凝胶样品(GO-g0),真空冷冻干燥24h,得到氧化石墨粉末样品(GO-p0)。
试剂:浓硫酸(98%,分析纯,AR),高锰酸钾(AR), H2O2(30% , AR), 甲 醛 (AR), 氨 水 (AR),氯化铵(优级纯,GR),氢氧化钠(GR)和氯化钙(GR)均购自成都科龙化工试剂厂;实验用水为超纯水(ULUP-I,四川优普超纯科技有限公司,中国,电阻率 > 18 MΩ·cm)。
2.2GO的CEC测定
采用甲醛缩合法,实验步骤如下:
(1) 将 5 份 0.1 g GO-p0 样品置于 5 个 100 mL 离心管中,分别加入 0.5 mol·L-1的 NH4Cl-氨水交换液 40 mL, 在 恒 温 水 浴 振 荡 器 内 (25 °C, 250 r· min-1)震 荡 120 min 后 静 置 30 min, 离 心 (9000 r· min-1)15 min 后剔除上清液,获得 5 份交换产物凝胶,记为GO-g1,待处理后分析;
(2)用超纯水离心洗涤 GO-g1 数次,并用纳氏试剂检测洗涤液中 NH4+,直到洗涤液观察不到颜色变化为 止 , 获得 4 份凝胶 产 物 ,其中 1 份加 入 0.5 mol·L-1的 CaCl2交换液 25 mL,重复步骤(1)恒温水浴振荡和离心操作等获得交换产物凝胶,记为GO-g2,待处理后分析;另3份由离心管移至3个100 mL 锥 形 瓶中 , 分 别 用 0.5 mol·L-1的 CaCl2溶 液 25 mL洗涤离心管内壁并倒入相对应锥形瓶中;
(3) 向锥 形 瓶中加 入 1.25 mL 甲醛溶 液 恒 温振荡(25 °C,250 r·min-1)120 min 后静置 30 min;再加入两滴酚酞试剂,用 0.050 mol·L-1NaOH 标准液滴 定 至 稳 定 的 粉 红 色 , 3 min 不 褪 色 即 为 滴 定 终点,记录样品消耗NaOH标准溶液的体积。根据CEC=C × V/G × 100(其中:C 为 NaOH 标准液浓度,V为滴定所消耗NaOH标准液的体积,G为氧化石墨质量)4计算 GO的CEC,3 个平行实验的平均值为 541.48 mmol/100 g,相对标准偏差 1.42%。
为分析 GO-p0 样品在 NH4+和 Ca2+交换后产物的结构变化,将步骤(1)和(2)获得的样品 GO-gn(n= 0,1,2)分为两组,取一组冷冻干燥至恒重获得样品GO-pn(n=0,1,2),并放入装有干燥变色硅胶的干燥器内(25 °C,湿度 ≤ 20%)密封保存,待测;另一组样品GO-gn(n=0,1,2)放入装有饱和氯化钠溶液(25 °C,湿度~75.3%)的干燥器内密封保存,待测。
2.3 样品表征
XRD 分析采用荷兰帕纳科公司生产的 X′pert MPD Pro 型 X 射线衍射仪,测试条件:Cu 靶,管压 40 kV,管流 40 mA,发射狭缝(DS):(1/2)°,防散 射 狭 缝 (SS): 0.04 rad, 接 收 狭 缝 (AAS): 5.5 mm,扫描范围:3°-80°;FTIR分析采用美国尼高力仪器公司生产的 Nicolet-5700 型红外光谱仪,扫描范围:4000-400 cm-1,KBr压片法制样;XPS分析采用英国 Kratos公司的 XSAM800 型多功能表面分析电子能谱仪,Al靶(1486.6 eV),X 光枪功率12 kV × 15 mA,采用固定能通(FAT,fixed analyzer transmission mode)方 式 , 数 据 采 用 污 染 碳 C 1s (284.8 eV)校正。
3 结果与讨论
3.1 NH4+和 Ca2+交换后 GO 样品的层间距变化
图1 为 GO 样 品 和 经 NH4+和 Ca2+交 换 后 对 应 样品在湿润状态(a)及干燥状态(b)下的 XRD 图。由图1a可知,GO-gn样品在2θ为28°附近都出现无序结构的宽缓衍射峰,并且 GO-g1 和 GO-g2 样品在 2θ为10°左右出现了与干燥样品相似的衍射峰,表明和 Ca2+交换进 GO-g0 的层间域后形成了具有一定厚度的水化阳离子层, 并 使 GO-g1 和 GO-g2 保持较为有序的层状结构。对于干燥后的样品(图 1b),在2θ为10°左右出现的是GO的最大底面特征衍射峰,对应 GO-pn(n=0,1,2)样品的 d00l值分别为 0.8289、0.9788 和 1.1194 nm, 峰 形 尖 锐 , 都 表现出较有序的层状结构;GO-pn(n=1,2)样品的最大底面间距增大,表明 GO-p0 样品经 NH4+和 Ca2+交换后明显改变了GO的层间距。
图1结果表明,阳离子交换前后的样品处于湿润和干燥状态时,分别表现出不同的结构特点。当样品处于湿润状态时,GO-g0样品由于GO结构层中―C―OH和―COOH与层间域中的水分子作用发生去质子化反应形成―C―O-和―COO-15,解离出的H+进入层间域的水分子层中或水化形成H3O+。在高湿度或水介质中,由于浓差扩散作用水分子不断进入GO的层间域,使层间域吸水溶胀,层间距进一步增大。并因GO各结构层氧化程度的差异21导致―C―O-和―COO-
分布不一致,使不同层间域引入的水分子含量不同,引起层间域的厚度不一致,进而使GO-g0在2θ约28°附近呈现宽缓的无序叠层结构的衍射峰(图 1a)。当 GO-g0 样品干燥后,层间域中的自由水分子被脱去,仅保留与含氧官能团以氢键相连接的水分子,这使层间域中水分子的厚度一致,因而GO-p0样品表现出有序的叠层结构。
当 GO-p0 样 品 在 加 入 NH4Cl-氨 水 交 换 液 后 ,GO-g0 样品层间域中的 H+与 NH4+发生阳离子交换作用而被交换出来,交换出来的H+在弱碱性环境中被 中 和 形 成 水 , 进 入 层 间 域 中 的 NH4+由 于 水 合 作用形成的[NH4(H2O)6]+,并与 GO 结构上去质子化的―C―O-
发生配合作用,致使GO层间域中形成稳定的双水分子层结构,NH4+位于水分子层构成的八面体孔隙中,各层间域在水饱和状态下形成2层完整的水分子层15,厚度一致,因而 GO-g1 样品表现出有序的叠层结构。当 GO-g1 样品干燥后,层间域中的自由水分子被脱去,仅保留与 NH4+配位和与含氧官能团以氢键结合的水分子,从而导致GO-p1样品的最大底面间距较GO-g1样品的小。
GO-g2 与GO-g1 样品情形类似,当在GO-g1样品 中 加 入 CaCl2交 换 液 后 , 离 子 交 换 作 用 使 NH4+被Ca2+交换出来,进入层间域中的 Ca2+与水分子形成[Ca(H2O)6]2+水合阳离子为较稳定的八面体配位结构,水饱和条件下在层间域中可形成完整的双水分子层结构。当 GO-g2样品干燥后,层间域中不与 Ca2+结合的水分子由双层结构变为不连续的双层结构或单层结构,导致 GO-p2 的最大底面间距小于GO-g2,峰强度减弱。
由 于 Ca2+离 子 的 水 合 半 径 (~0.41 nm)较 NH4+(~0.33 nm)的大22,因此,在相同状态下,GO-g2较GO-g1、GO-p2 较 GO-p1的底面间距大。
3.2 阳离子交换前后 GO 的 FTIR 光谱特征变化
图2 为 GO-pn(n=0,1,2)样 品 的 FTIR 图谱 。在 3700-3000 cm-1波数范围内较宽较强的吸收带与水的伸缩振动相关,3434 cm-1吸收峰为层间水包括吸附水分子的伸缩振动,3275 cm-1附近为与GO结构层上含氧官能团以氢键结合的水分子的伸缩 振 动23。 1630 cm-1处 为 水 分 子 的 弯 曲 振 动24,1400 cm-1归属 GO 结构中―C―OH 或 N―H 键的弯曲 振 动 ,1019-1097 cm-1吸 收 带 为 GO 结 构 层 上C―O伸缩振动区域。
对比 GO-pn(n=0,1,2)样品的红外吸收峰发现 , 在 3500-3000 cm-1低 波 数 一 侧 的 阴 影 范 围 ,经 NH4+交 换 后 的 GO-p1 样 品 在 3125 cm-1处 出 现 了 N―H键伸缩振动峰,而其他波数区域相对于GO-p0 样品,NH4
+和 Ca2+交换后的 GO-p1 和 GO-p2 样品并未出现新的吸收峰,但峰位和相对强度有一定变化。GO-p0 样品位于 1263 cm-1的―COO-中 C―O 键的伸缩振动峰24在离子交换后的 GO-p1 和 GO-p2 样品中向高波数偏移至 1274 cm-1,并 且 峰 强 度明 显 增 加 , 说 明 NH4+或 Ca2+的 配 位 水 合 离 子 与―COO-的静电作用力较 H+的弱,使―COO-中的C―O键能增加,进而引起C―O键的伸缩振动峰发生蓝移。而 1097 cm-1处的―C―O-中C―O键的伸缩振动峰向低波数偏移至 1074 cm-1,说明 GO 骨架中―C―O-
与层间域中的水分子层形成更强氢键,加之水合阳离子[NH4(H2O)6]+和[Ca(H2O)6]2+的配合作用使 C―O 键能相对减弱24,进而发生峰位红移。
GO-p1 样品在 3125 cm-1处产生的 N―H 键伸缩振动吸收峰,以及 GO-p2样品在 3125 cm-1吸收峰消失与 GO-p0 的相似,表明 NH4+进入层间域中交换出了 H+,而后 Ca2+进入层间域又将 NH4+交换出来。GO-p1和GO-p2样品在 3434 cm-1水分子的伸缩振动峰展宽,吸收强度增大,峰位略有红移,进一步说明NH4+和 Ca2+交换进入 GO 层间域后水分子与含氧官能团形成强的氢键,并预示[NH4(H2O)6]+和[Ca(H2O)6]2+结构排布更为有序,这与XRD分析结果一致。
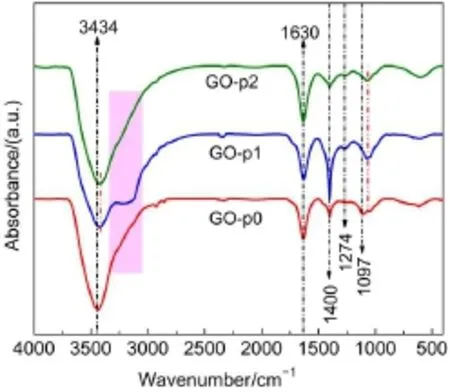
图2 阳离子交换前后干燥GO样品的FTIR图Fig.2 FTIR spectra of dry GO samples before and after the cation exchange processes
3.3 阳离子交换前后GO含氧官能团结合能的变化
图3a 为 GO-pn(n=0,1,2)样品的 XPS 全 谱 ,各元素百分含量见表1,可以看出,发生阳离子交换 后 NH4+和 Ca2+进 入 了 GO 层 间 域 。 图 3(b - d)为GO-pn 的 C 1s分峰拟合谱图,多峰拟合采用 80% Gaussian 和 20%Lorentzian 曲线25,各官能团的相对百分含量列于表 2。图 3b 中结合能为 286.7 eV 的―C―O(H)和 289.0 eV 的 ―COO(H)总 含 量 约 占45.13%,解离出的 H+是产生阳离子交换的本质。图 3(c,d)中阳离子交换后 GO-p1 和 GO-p2 样品 XPS的 C 1s分峰谱中可以看出,羰基(C=O)含量变化很小,在误差范围内,而 C―O(R)和(R)O―C=O含量在离子交换后略有减小,碳碳键(C―C/C=C)有一定增加,分析认为,这与H+被交换后交换液体系由酸性变为碱性及平衡―C―O-负电价层间阳离子改变相关,并使少量 C―O(R)和(R)O―C=O由于环境的改变而被还原15。

图3 阳离子交换前后干燥 GO 样品的 XPS 全谱(a)和 GO-pn(n=0,1,2)的 C 1s谱图(b-d)Fig.3 XPS whole spectra of dry GO samples before and after with cation exchange processes(a)and C 1s XPS spectrum of GO-pn(n=0,1,2)(b-d)

表1 阳离子交换前后干燥GO样品各元素百分含量变化Table 1 Exchange of percentage of atomicity of dry GO samples before and after the cation exchange processes
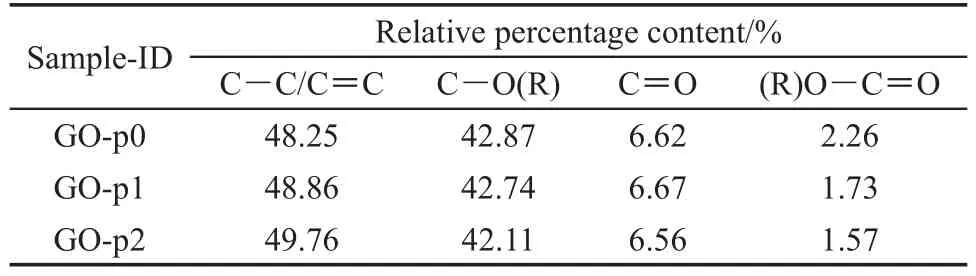
表2 GO-pn样品各官能团相对百分含量Table 2 Relative percentage content of various functional groups of GO-pn samples
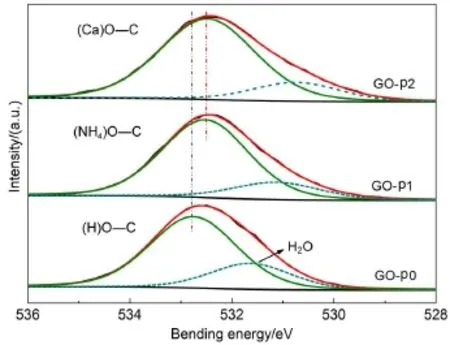
图4 阳离子交换前后 GO 样品的 XPS O 1s谱图Fig.4 XPS O 1s spectra of dry GO samples before and after the cation exchange processes
为了进一步验证阳离子交换前后的GO-pn 样品中含氧官能团与层间水化阳离子相互作用的强度,分别对 GO-pn(n=0,1,2)的 O 1s谱线进行了拟合(图 4),获得了各官能团结合能及含量(表 3)。可以看出,GO-p0 样品层间域中的 H+分别被 NH4+和Ca2+交换后,C―O 键的结合能减小了 0.2 eV,说明GO骨架中―C―O-与[NH4(H2O)6]+和[Ca(H2O)6]2+发生配合作用使C―O键能减弱,结合能减小;GO-p1和GO-p2样品中水分子的结合能也分别减小了0.5 和 0.9 eV, 进 一 步 说 明 NH4+和 Ca2+交 换 进 入 GO层间域后水分子与―C―O-形成了更强的氢键及可能更规则的排布,与FTIR分析结果吻合。

表3 阳离子交换前后GO 样品的 XPS O 1s结合能变化Table 3 XPS O 1s binding energy changes of dry GO samples before and after the cation exchange processes
4 结论
采 用 甲 醛 缩 合 法 测 定 GO 的 CEC 为 541.48 mmol/100 g,测定结果稳定,具有良好的重复性。GO的CEC高于黏土矿物和传统的酸性CER。
GO结构―C―OH与层间域中的水分子作用发生去质子化反应形成―C―O-,解离出的H+进入层间域的水分子层中,具有可交换性。水介质中,NH4+进 入 GO 层 间 域 中 将 H+交 换 出 来 , 形 成 NH4-GO,Ca2+又可将 NH4+交换出来,形成 Ca-GO。水饱和状态下,[NH4(H2O)6]+和[Ca(H2O)6]2+以双水分层结构在GO层间域形成水化阳离子层,并平衡GO结构层水解所产生的负电荷,干燥状态下,[NH4(H2O)6]+和[Ca(H2O)6]2+以水合阳离子形式在层间域内与GO结构层上的―C―O-以氢键结合。
GO阳离子交换过程产物的结构变化研究表明,GO阳离子的交换是可逆过程,这对认识GO层间域(物)可改造性具有重要理论和实际意义,同时可为建立GO结构模型提供实验基础。
(1)Hadi,J.;Tournassat,C.;Lerouge,C.Appl.Clay Sci.2016,119, 393.doi:10.1016/j.clay.2015.03.017
(2)Sharma,A.;Weindorf,D.C.;Wang,D.;Chakraborty,S.Geoderma2015,239,130.doi:10.1016/j.geoderma.2014.10.001
(3)Jiang,Y.;Lu,J.;Sun,K.;Ma,L.;Ding,J.Energy Convers. Manage.2013,76,980.doi:10.1016/j.enconman.2013.08.011
(4)Feng,M.Z.;Peng,T.J.;Sun,H.J.;Wang,P.C.Chin.J.Inorg. Chem.2016,32(3),427.[冯明珠,彭同江,孙红娟,王培草.无机化学学报,2016,32(3),427.]doi:10.11862/CJIC.2016.047
(5)Szabó,T.;Berkesi,O.;Forgó,P.;Josepovits,K.;Sanakis,Y.; Petridis,D.;Dékány,I.Chem Mater2006,18(11),2740. doi:10.1021/cm060258+
(6)Peng,T.J.;Liu,F.S.;Huang,J.;Belzile,N.;Sun,H.J.Acta Petrologica et Minerallogica2003,22(4),391.[彭同江,刘福生,Huang,J.,Belzile,N.,孙红娟 .岩石矿物学杂志,2003,22(4),391.]
(7)Iturri,L.A.;Buschiazzo,D.E.Catena2014,121,81. doi:10.1016/j.catena.2014.04.021
(8)Vazquez,A.;López,M.;Kortaberria,G.;Martín,L.; Mondragon,I.Appl.Clay Sci.2008,41(1),24.doi:10.1016/j. clay.2007.10.001
(9)Ma,C.;Eggleton,R.A.Clay Clay Min.1999,47(2),174.
(10)Chakrabarti,A.;Sharma,M.React.Polym.1993,20(1),1. doi:10.1016/0923-1137(93)90064-M
(11)Millar,G.J.;Miller,G.L.;Couperthwaite,S.J.;Papworth,S.Sep.Purif.Technol.2016,163,79.doi:10.1016/j. seppur.2016.02.045
(12)Amin,N.;Abdelwahab,O.;El-Ashtoukhy,E.S.Desalin.Water Treat.2015,55(1),199.doi:10.1080/19443994.2014.913208
(13)Hofmann,U.;Holst,R.Berichte Der Deutschen Chemischen Gesellschaft2006,72(4),754.doi:10.1002/cber.19390720417
(14)Clause,A.;Plass,R.;Boehm,H.P.;Hofmann,U.Z.Anorg.Allg. Chem.1957,291(5-6),205.doi:10.1002/zaac.19572910502
(15)Dimiev,A.;Kosynkin,D.V.;Alemany,L.B.;Chaguine,P.; Tour,J.M.J.Am.Chem.Soc.2012,134(5),2815.doi:10.1021/ ja211531y
(16)Boukhvalov,D.J.Phys.Chem.C2014,118(47),27594. doi:10.1021/jp509659p
(17)Hontoria-Lucas,C.;Lopez-Peinado,A.;López-González,J.D. D.;Rojas-Cervantes,M.;Martin-Aranda,R.Carbon1995,33(11),1585.doi:10.1016/0008-6223(95)00120-3
(18)Liu,Z.H.;Wang,Z.M.;Yang,X.;Ooi,K.Langmuir2002,18(12),4926.doi:10.1021/la011677i
(19)Liu,P.;Gong,K.;Xiao,P.;Xiao,M.J.Mater.Chem.2000,10(10),933.doi:10.1039/A908179H
(20)Sun,H.J.;Peng,T.J.Graphene Materials Prepared by Oxidation-Reduction Method from Graphite;Science Press: Beijing,2015;pp 52-79.[孙红娟,彭同江 .石墨氧化-还原法制备石墨烯材料.北京:科学出版社,2015:52-79.]
(21)Rozada,R.;Paredes,J.I.;López,M.J.;Villar-Rodil,S.;Cabria, I.;Alonso,J.A.;Martínez-Alonso,A.;Tascón,J.M.Nanoscale2015,7(6),2374.doi:10.1039/c4nr05816j
(22)Volkov,A.G.;Paula,S.;Deamer,D.W.Bioelectrochem. Bioenerg.1997,42(2),153.doi:10.1016/S0302-4598(96) 05097-0
(23)Huang,Q.;Sun,H.J.;Yang,Y.H.Chin.J.Inorg.Chem.2011,27(9),1721.[黄 桥,孙红娟,杨勇辉.无机化学学报,2011,27(9),1721.]
(24)Lee,D.;De Los Santos V,L.;Seo,J.;Felix,L.L.;Bustamante D.A.;Cole,J.;Barnes,C.J.Phys.Chem.B2010,114(17), 5723.doi:10.1021/jp1002275
(25)Ganguly,A.;Sharma,S.;Papakonstantinou,P.;Hamilton,J.J. Phys.Chem.C2011,115(34),17009.doi:10.1021/jp203741y
Structure Development during the Cation Exchange Processes of Graphite Oxide
WANG Quan-Jun1SUN Hong-Juan2,*PENG Tong-Jiang2,3FENG Ming-Zhu2
(1School of Science,Southwest University of Science and Technology,Mianyang 621010,Sichuan Province,P.R.China;2Institute of Mineral Materials&Application,Southwest University of Science and Technology,Mianyang 621010,Sichuan Province,P.R.China;3Center of Forecasting and Analysis,Southwest University of Science and Technology, Mianyang 621010,Sichuan Province,P.R.China)
Oxygen-containing hydroxyl(―C―OH)and carboxyl(―COOH)functional groups on both the basal planes and edges of the graphite oxide(GO)structure can dissociate to form H+in water,thus providing cation exchange ability.The cation exchange capacity(CEC)of GO was measured accurately using the Stiasny method and the intermediate products of cation exchange processes of oxygen-containing functional groups and structure development were analyzed by X-ray diffraction(XRD),Fourier transform infrared(FTIR)spectroscopy, and X-ray photoelectron spectroscopy(XPS).The results indicated that the CEC of GO was up to 541.48 mmol/ 100 g.After NH4+and Ca2+exchange processes,GO still maintained a stable lamellar structure,and the c axis spacing increased by 0.1499 and 0.2905 nm,respectively.NH4+and Ca2+were mainly in the form of exchangeable cations in the interlayer space of GO,and formed a hydrated cation layer with water molecules,part of the containing[NH4(H2O)6]+or[Ca(H2O)6]2+formed near the edge of the structural layer,balancing the negative charges originating from hydrolysis of the carboxyl groups of the GO structural layer.
Graphite oxide;Oxygen-containing functional group;Cation exchange capacity;Interlayer space;Structure development
O647;O641
10.3866/PKU.WHXB201610241
Received:August 26,2016;Revised:October 24,2016;Published online:October 24,2016.
*Corresponding author.Email:sunhongjuan@swust.edu.cn;Tel:+86-816-2419276.
The project was supported by the National Natural Science Foundation of China(41272051),Doctor Foundation of Southwest University of Science and Technology,China(11ZX7135),and Postgraduate Innovation Fund Project by Southwest University of Science and Technology,China(15ycx073).
国家自然科学基金(41272051),西南科技大学博士基金(11ZX7135)及西南科技大学研究生创新基金(15ycx073)资助项目© Editorial office of Acta Physico-Chimica Sinica

