籼米淀粉-庚醇包合物的制备及其释放动力学研究
金姗姗,张舒,李雅琴,周裔彬
(安徽农业大学 茶与食品科技学院,安徽 合肥,230036)
籼米淀粉-庚醇包合物的制备及其释放动力学研究
金姗姗,张舒,李雅琴,周裔彬*
(安徽农业大学 茶与食品科技学院,安徽 合肥,230036)
采用热熔法制备籼米淀粉-庚醇包合物。单因素正交实验结果表明:籼米淀粉-庚醇包合物的最佳包合条件为主客投料比为10∶0.3(g∶μL)、包合温度30 ℃、萃取温度60 ℃时,此时包合率为77.01%。通过x-衍射、13C-NMR及SEM从结构方面表明了包合物的形成。引入Avrami方程研究了该包合物在不同温度及相对湿度下风味物质的释放规律。结果表明:温度越高、相对湿度越大时,庚醇释放越快。
籼米淀粉;庚醇;包合;释放动力学
庚醇是一种具有特有芳香气味的小分子风味物质,天然存在于水果、蔬菜中,通常被用作调配草莓、香蕉、蘑菇等食用香料[1]。庚醇具有的低沸点、易挥发及水溶性较差等特点限制了其在食品工业中的应用。微胶囊技术是将易挥发、低沸点的液体状风味成分包合成稳定的固体化合物,提高产品的稳定性及延长贮藏期[2]。
籼米淀粉由直链淀粉及支链淀粉组成,其中直链淀粉通过α-D-1,4糖苷键形成多糖链,其空间结构为无规则的线圈或者由6个葡萄糖残基而形成的螺旋结构。直链淀粉的螺旋链形成了空腔结构,其中C3、C5上的氢和氧原子形成了内部疏水结构,外部则因为羟基而形成了亲水结构,由于这种内疏水、外亲水的结构,使得淀粉可以与环糊精一样成为许多风味物质包合物壁材的选择[3]。
选择价格低廉、来源丰富的籼米淀粉作为包合壁材包合庚醇,通过单因素、正交实验确定了该包合物的最佳制备条件。利用x-衍射、13C-NMR及SEM等方法证明了包合物的形成,并对庚醇的释放特性进行了探讨,为籼米淀粉的开发应用及庚醇类小分子风味物质的应用提供了理论参考。
1 材料与方法
1.1 材料与试剂
籼米,合肥市金玉超股份有限公司;籼米淀粉(直链淀粉含量17.54%),实验室自制。庚醇(99%),西格玛奥德里奇公司;无水乙醇(AR),国药集团化学试剂有限公司。
1.2 仪器与设备
BSA224S型电子天平,北京赛多利斯科学仪器有限公司;QL-901 Vortex 漩涡混合器,海门市其林贝尔仪器制造有限公司;DK-S26型电热恒温水浴锅,上海精宏实验设备有限公司;KQ-250DE型数控超声波清洗机,昆山市超声仪器有限公司;JW-3021HR高速冷冻离心机,安徽嘉文仪器装备有限公司;FD-1A-50型冷冻干燥机,北京博医康实验仪器有限公司;7890B气相色谱仪,美国安捷伦科技有限公司;D8ADVANCE多晶X射线粉末衍射仪,德国布鲁克仪器有限公司;400MHz布鲁赫核磁共振波谱仪,德国布鲁克仪器有限公司;S-4800扫描电镜,日本日立公司。
1.3 方法
1.3.1 籼米淀粉-庚醇包合物的制备
包合物的制备采用热熔法[4-5]。称取0.15 g籼米淀粉于20 mL的具塞试管中,加入15 mL蒸馏水,在漩涡振荡器上充分振荡后于100 ℃水浴中水浴1 h。将试管取出冷却至室温,加入庚醇醇溶液,振荡摇匀后,在超声仪中于30~70 ℃的条件下超声30 min。取出试管于4 ℃环境中放置12 h,将反应液倒入平皿中-18 ℃条件下预冻12 h。-48 ℃,真空度为15 Pa冷冻干燥24 h后得到白色绒状物质,于4 ℃密封干燥保存。
籼米淀粉-庚醇物理混合样:称取0.15 g籼米淀粉于20 mL的具塞试管中,加入15 mL蒸馏水,在漩涡振荡器上充分振荡后于100 ℃水浴中水浴1 h。将试管取出冷却至室温,加入庚醇醇溶液,将溶液倒入平皿中-18 ℃条件下预冻12 h。-48 ℃,真空度为15 Pa冷冻干燥24 h后得到白色绒状物质,于4 ℃密封干燥保存。
样品原样:称取0.15 g籼米淀粉于20 mL的具塞试管中,加入15 mL蒸馏水,在漩涡振荡器上充分振荡后于100 ℃水浴中水浴1 h。将试管取出冷却至室温,将溶液倒入平皿中-18 ℃条件下预冻12 h。-48 ℃,真空度为15 Pa冷冻干燥24 h后得到白色绒状物质,于4 ℃密封干燥保存。
1.3.2 包合物中风味物质的提取(萃取)
称取包合物60 mg分散于7 mL乙醇中,密封混匀后在50~70 ℃下超声30 min,使得风味物质从包合物中充分分离出来。然后10 000 r/min,4 ℃,离心10 min,取上清液,过滤膜后通过气相色谱测得相应的峰面积,根据标准曲线计算得出包合物中风味物质的含量,即包合率。
1.3.3 包合率的计算
包合率按式(1)计算:

(1)
1.3.4 籼米淀粉-庚醇包合物的单因素实验
(1)主客比对包合率的影响
籼米淀粉-庚醇包合物的制备按照主客比为10∶0.1、10∶0.2、10∶0.4、10∶0.6、10∶0.8、10∶1(g∶μL)进行包合,得到包合物后测其包合率,考察不同的主客比投料比对包合率的影响。
(2)超声温度对包合率的影响
选择1.3.4(1)中所确定的最佳主客比,分别在30、40、50、60、70 ℃下超声30 min,测所得包合物的包合率,比较不同超声温度对包合率的影响。
(3)萃取温度对包合率的影响
选择1.3.4(1)及(2)中分别确定的2种包合物各自的最佳主客比及超声温度,得包合物后,分别在30、40、50、60、70 ℃下进行萃取实验,考察2种包合物的包合率,确定萃取温度对包合率的影响。
1.3.5 籼米淀粉-庚醇包合物制备的条件优化
在1.3.4单因素实验的基础上,选取包合物主客比、包合温度及萃取温度为影响因素,以所得包合物的包合率为指标,设计3因素3水平L9(34)的正交实验,见表1。

表1 正交实验因素水平表
1.3.6 包合率的测定
(1)标准曲线的绘制
将庚醇分散于乙醇中,配制成不同体积浓度的庚醇-乙醇溶液,体积浓度比(庚醇/乙醇)分别为:0.08、0.16、0.24、0.32、0.40 μL/mL。使用气相色谱得出相应的峰面积,以体积浓度比为横坐标,峰面积为纵坐标绘制标准曲线,得到相应的回归方程y=1 210.5x-17.257,R2=0.995 62。
1.3.7 气相色谱条件
色谱柱为DB-WAX极性毛细管柱(30 m×0.32 nm×0.25 μm),载气为氮气,流速为1 mL/min,分流比为10∶1,检测器为FID,进样口温度和检测器温度分别为250 ℃、275 ℃,柱箱温度为50 ℃保持1 min后,以2.5 ℃/min升至80 ℃,保持5 min,以25 ℃/min升至240 ℃,保持5 min。
1.4 包合物的结构表征
1.4.1 X-衍射
为了研究包合物包合后物质的结晶度及晶体结构的变化,分别对糊化籼米淀粉、籼米淀粉-庚醇物理混合样及籼米淀粉-庚醇包合样进行X-衍射测定。测定条件为电压40 kV,电流200 mA,用Cu Kα射线扫描。扫描范围4~50°,扫描步长为0.02°[6]。相对结晶度[7]的计算方程如下:
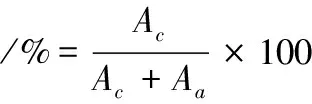
(2)
其中,Ac为X-衍射图谱中的结晶区域面积,Aa为非结晶区域面积。
1.4.2 固体核磁共振(13C-NMR)
分别对糊化籼米淀粉、包合物及物理混合样进行测试。将样品置于7mm固体核磁管,磁场为400 Hz,探头温度为20 ℃[8]。
1.4.3 扫描电镜(SEM)
分别对糊化籼米淀粉、包合物及物理混合样进行扫描电镜测试。使用导电双面胶将样品固定在样品台上,镀金后在3 kV进行观察,观察倍数为2 000倍[9]。
1.5 包合物的释放
为了更好地理解包合物中风味物质的释放,引进Avrami方程[10]对风味物质释放进行拟合,方程如下:
R=exp[-(kt)n]
(3)
式中:R表示风味物质在释放之后的保留值,t表示时间(s),n表示释放机理,k表示释放速率常数。
该公式最早用于研究结晶成长速度,近年来也用来表征固-气反应以及固-液反应。SUN[10]等人成功地利用该公式对蛋白质在蔗糖以及海藻糖溶液中随时间的变化其活性的变化进行了分析。n=1时,代表反应为一级反应;n=0.54时,反应为扩散限制反应。
对公式两边取对数,得到公式:
ln(-lnR)=nlnk+nlnt
(4)
以lnt为横坐标,ln(-lnR)为纵坐标作图,根据所得线性回归方程可以计算出n和k的值。
释放实验主要考察包合物在冷藏温度4 ℃和室温25 ℃,相对温度为33%和93%的条件下的情况。准确称取(0.150±0.000 2) g籼米淀粉-庚醇包合物平铺于干燥皿中,放入用MgCl2、KCl饱和盐溶液配制好相对湿度RH在33%和93%的干燥器中,分别在释放1、3、5、7、14、21 d后取出一个干燥皿,测其中风味物质的保留率,代入Avrami方程进行拟合分析。
2 结果与分析
2.1 籼米淀粉-庚醇包合物单因素实验结果
图1为籼米淀粉-庚醇包合物的单因素实验结果。从主客比来看,当籼米淀粉/庚醇为10∶0.2(g∶μL)时,籼米淀粉-庚醇包合物的包合率达到最高,为59.98%。当主客比升至10∶0.4、10∶0.6、10∶0.8、10∶1(g∶μL)时,包合率分别为39.84%、36.17%、35.67%、30.23%,包合率是一直在下降的,这是由于包合物中被包合的客体物质饱和后,增加客体物质的量会降低包合物的包合率。从包合温度这个因素来看,当包合温度在40 ℃时,包合率达到最大,为63.25%,继续升高温度有可能使得被包合的风味物质脱离包合主体或者与包合壁材结合不紧密的客体物质也易在高温的条件下脱离、挥发。在萃取温度为60 ℃时,籼米淀粉-庚醇包合物的包合率达到最大值,为88.10%,继续升温后,包合率开始下降。这可能是当萃取温度过高时,被包合的风味成分被萃取出来后挥发导致的。所以萃取温度不宜过高,否则会造成不必要的损失。籼米淀粉-庚醇包合物的单因素实验结果表明当主客比为10∶0.2(g∶μL)、包合温度40 ℃、萃取温度60 ℃时包合效果达到最好,此时的包合率为88.10%。
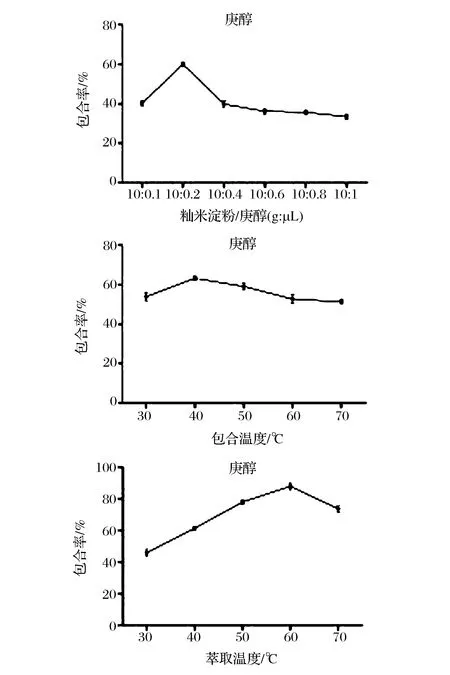
图1 籼米淀粉-庚醇包合物单因素实验结果Fig.1 Single factor experiments results of the indica rice starch-2-heptanol inclusion complexes
2.2 籼米淀粉-庚醇包合物正交实验结果
极差分析结果(表2)表明:3个因素对包合效果的影响顺序是:A>C>B,即主客比>萃取温度>包合温度,其中主客比对包埋率的影响最为显著。方差结果(表3)表明:主客比对包合率的影响显著,而包合温度及萃取温度对籼米淀粉-庚醇的包合率影响不显著。最佳组合是A3B1C2,即以乙醇为萃取剂、主客比为10∶0.3(g∶μL)、包合温度30 ℃、萃取温度60 ℃。同时进行了最佳组合的包合率测定实验,包合率为77.01%。
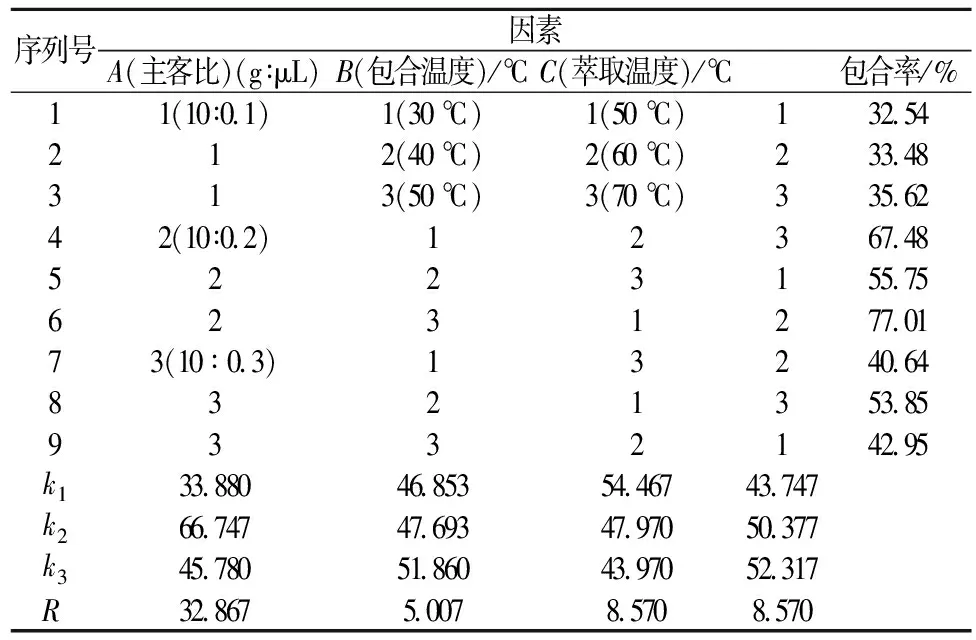
表2 籼米淀粉-庚醇包合物的正交实验结果
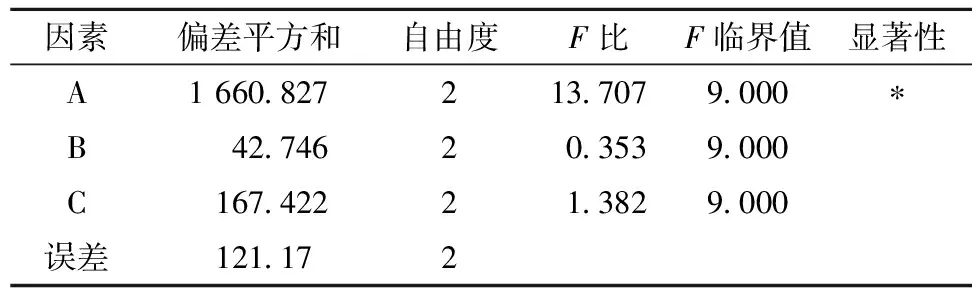
表3 籼米淀粉-庚醇包合物的方差分析结果
2.3 X-衍射分析
图2为糊化籼米淀粉、籼米淀粉-庚醇包合物及其物理混合样的X-衍射图谱。从图2中可以看出,籼米淀粉在糊化的过程中结晶度有所下降,形成了无定型区域。李冰[11]等人研究表明,包合物的XRD衍射峰一般皆为Vh型。包合物及物理混合样在2θ = 13°、20°处存在明显的尖锐的峰型,表明包合物和物理混合样的XRD衍射峰均为Vh型,这可能是在物理混合样混合的过程中由于庚醇分子较小,有部分分子进入淀粉空腔内,形成了一定的结合作用。从相对结晶度上来看,包合样的相对结晶度为19.23%,物理混合样的相对结晶度为22.36%。其中包合物的相对结晶度较物理混合样的有所下降,这可能是由于在包合过程中形成了更加稳定的结构,使得结晶度有所下降。这也在一定程度上证明了包合物的形成。
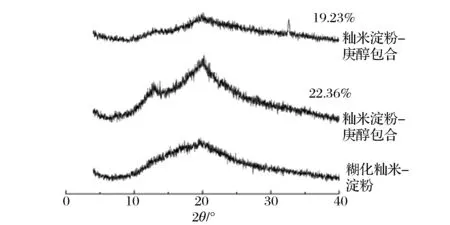
图2 糊化籼米淀粉及包合物、物理混合样的XRD衍射图谱Fig.2 X-ray diffraction patterns of gelatinized indica rice starch, mixtures and inclusion complexes
2.4 固体核磁共振(13C-NMR)
图3中可以看出,糊化籼米淀粉的C1-C6峰分别在102.22、93.59、81.53、 71.85、 60.61和31.09 ppm处。籼米淀粉-庚醇包合物与糊化籼米淀粉相比C1-C6有部分化学位移,C1-C6峰分别在迁移至102.26、93.23、81.41、71.64、60.52和31.67 ppm处。在包合物中都有0~50 ppm的甲基、亚甲基及次亚甲基峰[12],此处为庚醇的C化学位移,这说明了在包合物中有庚醇的存在,也进一步说明了包合物的形成。与包合物相比,物理混合样的化学位移有明显不同,这说明包合物的形成而不是简单地物理混合。
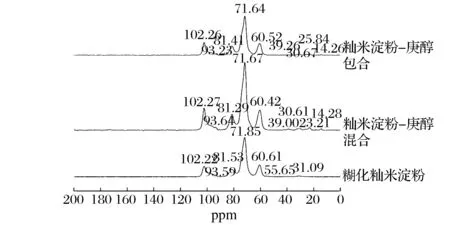
图3 糊化淀粉及包合物、混合物的核磁共振图谱Fig.3 13C-NMR spectra of the ingredients mixtures and inclusion complexes
2.5 扫描电镜(SEM)
通过扫描电镜观察包合物表面形态与糊化籼米淀粉的差异,从而判断包合物是否形成。从图4中可以看出糊化籼米淀粉表面光滑平整,呈现片状网状结构,这是籼米淀粉在糊化过程中,直链淀粉伸展开来,形成致密的网状结构。而籼米淀粉-庚醇包合物都呈现出片块状并且表面有许多小孔,这是由于小分子风味物质进入淀粉空腔时,产生了许多小孔,较糊化籼米淀粉而言,包合物的空间层次减弱,表面形态发生了明显变化,这说明了在包合过程中,籼米淀粉与风味物质之间产生了一定的相互作用,证明了包合物形成。物理混合样与包合物相比,其表面平整度降低,空间层次多,这也进一步说明了包合物不仅仅是简单的物理混合。

图4 糊化淀粉及包合物、混合物的扫描电镜图谱Fig.4 SEM graphs of the ingredients mixtures and inclusion complexes
2.6 释放实验结果
从图5中可以看出,当在4 ℃时,籼米淀粉-庚醇包合物释放1 d后,在相对湿度为33%时,庚醇的保留率为82.37%,而当相对湿度为93%时,包合物中庚醇的保留率还剩下27.48%,两者之间是有很大差异性的。而当释放结束时,相对湿度33%条件下,包合物中庚醇的保留率还剩29.81%,相对湿度为93%时包合物中的庚醇保留率还剩下17.39%,两者释放曲线的斜率表明了该环境下的释放速率。从斜率上来看,当温度一定时,相对湿度越大,包合物中客体分子释放得越容易[13]。造成这种差异存在的原因有2个:(1)当水分子的存在时,包合物处于与包合过程相反的逆向过程中,原来包合的主客体之间开始分离,从而使得处于结合态的被包合风味物质处于游离的状态,进一步加快了客体分子的释放速率;(2)是水分子与籼米淀粉空腔内的庚醇分子形成了竞争的关系,能够取代已经被包合的庚醇分子,将部分的客体分子挤到了反应环境中,从而离开包合物,加剧了客体物质的释放[14]。
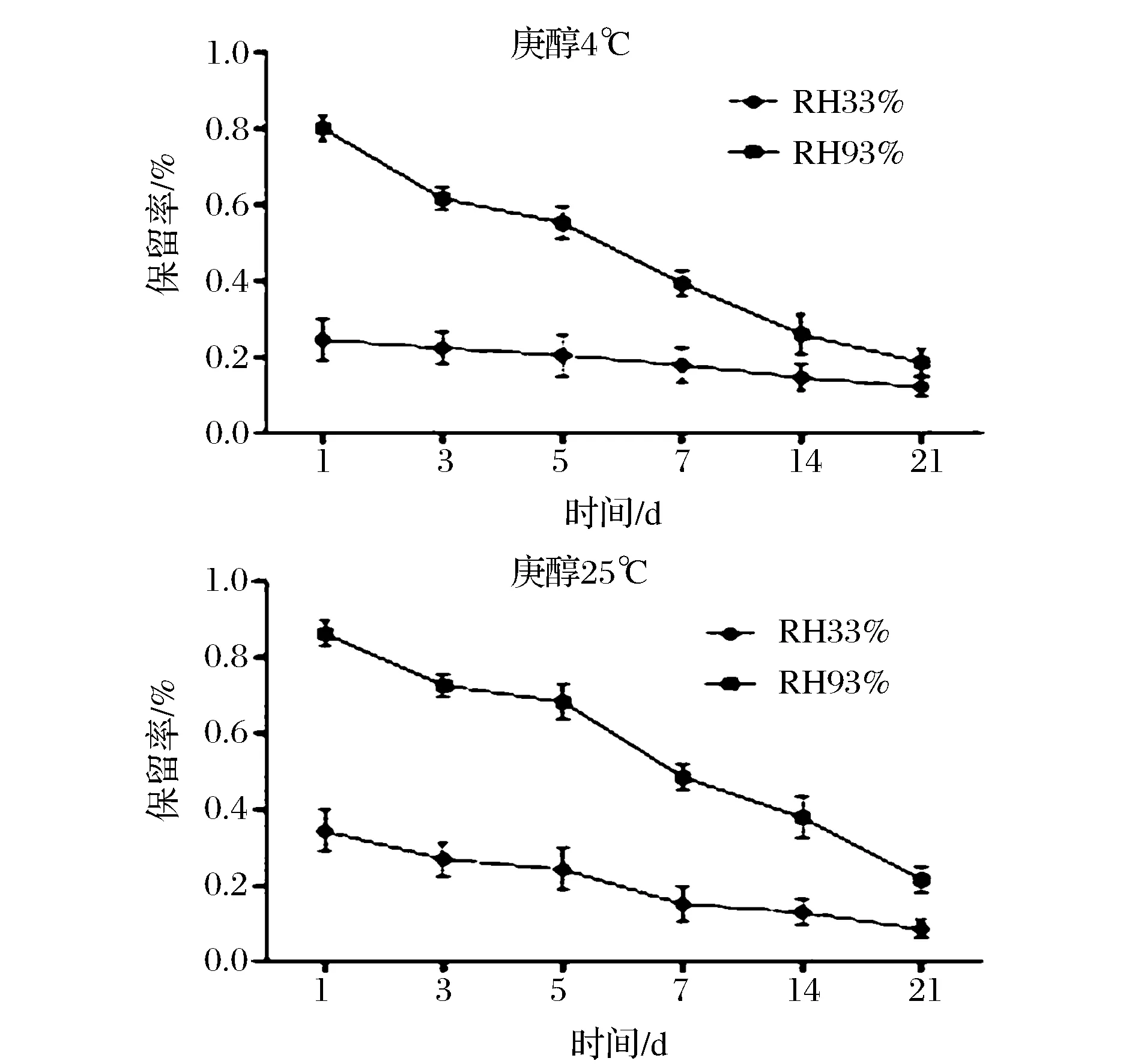
图5 不同贮藏条件下籼米淀粉-庚醇包合物的释放曲线Fig.5 Release behavior of the indica rice starch-2-heptanol inclusion complexes under different storage conditions
从表4可以看出,通过Avrami方程拟合,相关系数R2都在0.900 0以上,说明曲线拟合度较好。对于籼米淀粉-庚醇包合物来说,在4 ℃、25 ℃及相对湿度在33%、93%的条件下,其释放机制常数n在0.28~0.67之间,说明籼米淀粉-庚醇包合物释放介于扩散以及释放之间[15]。在4 ℃时,在相对湿度33%和93%的条件下,籼米淀粉-庚醇包合物的释放常数k分别为0.108 4 d-1和8.482 3 d-1,在25 ℃时,其释放常数分别是0.226 6 d-1和9.036 7 d-1,这说明在温度相同时,释放速率随相对湿度的增加而增加。我认为这主要因为庚醇包合物吸收空气中的水分,使得部分庚醇中的羟基易与空气中的水分形成氢键,从而使庚醇更易释放。而在相对湿度一定时,释放速率又随温度的增加而增加。这是因为当相对湿度一定时,环境温度升高也使得本来就极易挥发的庚醇离开包合主体,加剧释放。
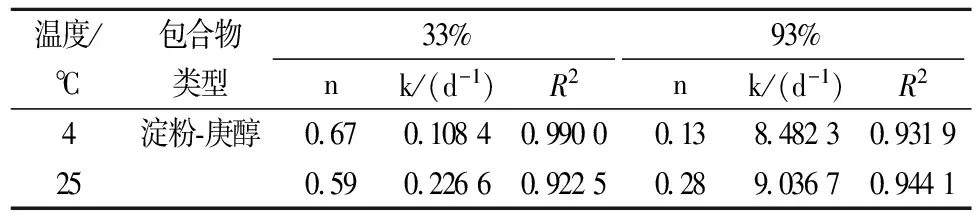
表4 包合物的释放相关常数
3 结论
在单因素实验的基础上,根据正交实验结果显示,制备籼米淀粉-庚醇包合物的最佳条件为主客比10∶0.3(g∶μL)、包合温度30 ℃、萃取温度60 ℃。同时进行了最佳组合的包合率测定实验,包合率为77.01%。
对所制备的包合物进行了X-衍射、固体核磁及扫描电镜分析结果表明包合物的形成。X-衍射分析可得包合物与糊化籼米的晶型有所改变,为Vh型;固体核磁证明了包合物中风味物质的存在,从而进一步说明了包合物的形成;扫描电镜淀粉在包合物形成的前后由光滑平整,片状网状结构变成片块状并且表面有许多小孔,也说明了包合物的形成。
在释放动力学研究中表明在温度相同时,庚醇的释放随湿度的增加而增加;在湿度相同时,庚醇释放随温度的增加而增加,说明籼米淀粉-庚醇包合物应该在低温干燥的条件下贮藏。
[1] BURDOCK G A.Fenaroli′s handbook of flavor ingredients[M]. 5th ed.Florida: CRC Press, 2004: 756-757.
[2] 马云标, 周惠明, 朱科学. VE微胶囊的制备及性质研究[J]. 食品科学, 2010, 31(2): 1-4.
[3] 荣志伟,冯涛.直链淀粉-风味物质包合物制备及结构表征[J].粮食与油脂,2011(9):1-5.
[4] 洪雁,顾正彪,刘晓欣.直链淀粉和支链淀粉纯品的提取及其鉴定[J].食品工业科技,2004(8):81-88.
[5] DOS SANTOS C, BUERA M P, MAZZOBRE M F. Influence of ligand structure and water interactions on the physical properties of β-cyclodextrins complexes[J]. Food Chemistry,2012, 132(4): 2 030-2 036.
[6] XIE W, SHAO L.Phosphorylation of corn starch in an ionic liquid[J]. Starch/Stärke,2009,61(12):702-708.
[7] CHANG Feng-dan, HE Xiao-wei, HUANG Qiang. The physicochemical properties of swelled maize starch granules complexes with lauric acid[J]. Food Hydrocolloids, 2013, 32:365-372.
[8] RONDEAU-MOURO C, BAIL P L, BULEON A. Structural investigation of amylose complexes with small ligands: inter-or intra-helical associations[J]. International Journal of Biological Macromolecules, 2004,34(34):309-315.
[9] PORZIO M. Flavour encapsulation: a convergence of science and art[J]. Food Technology, 2004,58(7): 40-47.
[10] SUN W D, DAVIDSON P. Protein inactivation in amorphous sucrose and trehalose matrices: effect of phase separation and crystallization[J]. Biochemical et Biophysical Acta, 1998,1 425(1): 235-244.
[11] XU S S, ZHANG J X, LI B, et al. Preparation and physical characteristics of resistant starch (type 4) in acetylated indica rice[J]. Food Chemistry,2012, 134(1): 149-154.
[12] QIAO L, TU G Z. NMR Nuclear Magnetic Resonance[M]. (1st ed). Bei Jing: Chemical Industry Press, 2009.
[13] ROSENBERG M, KOPELMAN I J, TALMON Y. Factors affecting retention in Spray-drying microencapsulation of volatile materials[J].J Agric Food Chem, 1990,38(5):1 288-1 294.
[14] 童林荟. 环糊精化学:基础与应用[M].北京:科学出版社,2001.
[15] YOSHII H, SOOTTITANTAWAT A, LIU X D, et al. Flavor release from spray-dried maltodextrin/gum arabic or soy matrices as a function of storage relative humidity[J]. Innov. Food Sci Emerg, 2001,2(1):55-61.
Preparation and release characterization of indica rice starch-2-heptanol
JIN Shan-shan, ZHANG Shu, LI Ya-qin, ZHOU Yi-bin*
(School of Tea and Food Technology, Anhui Agricultural University, Hefei 230036, China)
The indica rice starch-2-heptanol inclusion complex was prepared by melting method. The results showed that the highest inclusion efficiency of indica rice starch-2-heptanol was 77.01% under the following conditions: the ratio of the host and the guest 10∶0.3(g∶μL), the inclusion temperature 30 ℃ and the extract temperature 60 ℃. The formation of inclusion complex was confirmed by X-ray,13C-NMR and SEM. The release of indica rice starch-2-heptanol under different conditions were detected by Avrami equation. The results indicated that 2-heptanol released faster under higher temperature and humidity.
indica rice starch; 2-heptanol; inclusion; release kinetics
10.13995/j.cnki.11-1802/ts.201612024
硕士研究生(周裔彬教授为通讯作者,E-mail:zhouyibin@ahau.edu.cn)。
国家自然科学基金(31271960)
2016-02-16,改回日期:2016-05-26

