静电纺丝制备乙基纤维素纳米载药纤维
刘凯琳+吕瑶+桑青青+朱利民



摘要:本文通过静电纺丝技术制备了乙基纤维素/酮洛芬复合载药纳米纤维膜,利用傅里叶红外光谱仪(FTIR)、扫描电子显微镜(SEM)以及X射线衍射仪(XRD)对载药前后的乙基纤维素纳米纤维分别进行了表征。扫描电子显微镜观察结果表明,用六氟异丙醇为溶剂制备的纳米纤维膜表面光滑,没有粘结现象,纤维直径在500 ~ 600 nm之间;红外光谱分析表明,利用静电纺丝技术成功制备了载药乙基纤维素纤维;X射线衍射表明,酮洛芬以无定形的状态存在于纳米纤维中;释药结果表明,酮洛芬在7天左右的累积释药率达到50%左右,可以用作药物缓释材料模型。
关键词:静电纺丝;乙基纤维素;酮洛芬;纳米纤维膜;药物缓释
中图分类号:TS102.6;TQ340.64 文献标志码:A
Preparation of Ethyl Cellulose-based Drug-loaded Nanofibers Using Electrospinning
Abstract: The ethyl cellulose nanofibers loaded with ketoprofen were prepared by using the technology of electrospinning. Fouruer transformation infrared spectroscopy(FTIR), scanning electron microscopy(SEM)and X-ray diffraction(XRD)were used for characterizing the ethyl cellulose nanofibers before and after being loaded with ketoprofen. The results of SEM indicated that the prepared nanofibers using hexafluoroisopropanol as solvent has smooth surface and uniform morphology. The diameters of the nanofibers are between 500~600 nm. The results of FTIR indicated that ketoprofen was successfully loaded on the nanofibers. X-ray diffraction showed that the ketoprofen in the nanofibers changed from crystalline structure to amorphous state. The research of drug releasing indicated that the releasing rate of ketoprofen reached 50% in about 7 days, and the nanofibers can be used as a model for sustained release of drug.
Key words: electrospinning; ethyl cellulose; ketoprofen; nanofiber membrane; sustained release of drug
现阶段,静电纺丝技术已被广泛应用于纳米传感器、过滤材料、组织工程、药物缓释等领域。静电纺纳米纤维膜具有超高的比表面积,可促进细胞的粘附和物质的运输,而且可以模拟细胞外基质,利于细胞的生长。
乙基纤维素(EC)是一种不溶于水的纤维素衍生物,被广泛应用于药物制剂中的片剂粘合材料、薄膜包衣材料、骨架缓释片、缓释微丸及缓释微胶囊等中。乙基纤维素溶于无水乙醇等溶剂后有较大的粘度,在纺丝过程中性质稳定,成纤性能好,在伤口敷料和组织工程方面具有许多潜在应用。本试验中利用乙基纤维素的高可纺性制备纳米纤维膜,作为药物载体材料,达到药物缓释的效果。
酮洛芬(KET)是具有苯丙酸结构的非甾体类抗炎药物,在临床上广泛用于治疗各种类风湿关节炎、强直性脊柱炎、牙痛、术后疼痛等。但长期服用酮洛芬对肠胃刺激较大,会引起溃疡、出血等不良反应。因此,将其与静电纺丝法结合,利用纳米纤维膜的缓释,可减少药物毒副作用。
1 试验部分
1.1 试剂与仪器
1.1.1 试剂
乙基纤维素,阿拉丁试剂生产;酮洛芬(MW=254.29,98%),北京百灵威科技有限公司生产;六氟异丙醇(MW=168.04,99.5%),阿拉丁试剂生产;无水乙醇(MW=46.08,≥99.7%),江苏省常熟市杨园化工有限公司生产。试验中所用的水均为蒸馏水。
1.1.2 仪器
扫描电子显微镜(SEM);紫外可见分光光度计(UV);傅里叶变换红外光谱仪(FTIR);X射线衍射仪(XRD);磁力搅拌器;真空干燥箱;气浴恒温振荡器;静电纺丝机。
1.2 静电纺丝液的制备
取 1 g 乙基纤维素加入 5 mL六氟异丙醇(或者无水乙醇)中,在室温条件下用磁力搅拌器搅拌48 h以上,配成质量分数为20%的均匀溶液。然后在上述纺丝液中加入质量分数10%(相对于乙基纤维素来说)的酮洛芬,再在室温条件下用磁力搅拌器搅拌48 h以上,制成含有酮洛芬药物的均匀纺丝液。
1.3 静电纺丝法制备乙基纤维素载药纤维
将上述纺丝液小心装入 5 mL的注射器中,注射针头连接高压发生器的正极,铝箔接收装置连接负极,用于接收静电纺纳米纤维膜。针头到铝箔接收屏之间的距离为 15 cm,溶液在喷丝口处的流速为 0.3 mL/h,所施加的电压为13 kV,室温下操作。在高压电场作用下,纺丝液喷射最终形成纤维沉积在接收屏上,形成纤维膜,纺丝时间大约为 8 h。将纤维膜置于真空干燥箱中干燥过夜,以除去残留的溶剂。
1.4 载药纳米纤维表征
取载药前后的纳米纤维膜至于扫描电镜下观察其形貌,同时利用傅里叶红外光谱仪和X射线衍射仪进行红外光谱测试和结晶度分析。
1.5 载药纤维体外释药研究
将 4 份重量均为100 mg的乙基纤维素纤维分别浸入20 mL的pH值为 7 的PBS缓冲液中,置于恒温摇床中,参数设置为:温度37 ℃,速度100次/min,每隔一定时间取出 1 mL释放介质,同时补入相同体积的PBS缓冲液,采用紫外可见分光光度计测定释放介质在254 nm下的吸光度,并且利用药物标准曲线计算药物累计释放量。
2 结果与讨论
2.1 纳米纤维膜的扫描电镜及直径分析
图 1 为使用不同溶剂的情况下纳米纤维膜的扫描电镜照片。从图 1 中可以看出,用无水乙醇做溶剂纺出的纳米纤维膜,纤维直径粗细不匀较大,并且偶尔有串珠和粘连现象;而用六氟异丙醇作为溶剂的静电纺纳米纤维膜的纤维粗细均匀,没有粘连现象,说明采用六氟异丙醇作为溶剂的乙基纤维素膜具有更好的可纺性。同时,对比载酮洛芬前后的纳米纤维膜的形态可以看出,载药之后的纳米纤维的形态较好,纤维直径相对较小,粘连较少,说明药物酮洛芬的加入可以改善乙基纤维素的可纺性。
图 2 用Image J统计了溶剂为六氟异丙醇的两种纳米纤维的直径分布情况。可以发现,乙基纤维素纳米纤维平均直径为549.15 nm,呈现正态分布,其中直径在500 ~ 600 nm区间的占比较大,标准差为76.11 nm;乙基纤维素/酮洛芬纳米纤维的平均直径为530.62 nm,呈现正态分布,其中直径在500 ~ 550 nm区间的占比较大,标准差为73.31 nm,这与乙基纤维素纳米纤维的平均直径相比大约减少了20 nm,与前面所做的扫描电镜分析结果一致。说明了酮洛芬已成功负载在乙基纤维素纳米纤维上且粗细较均匀。
2.2 纳米纤维膜的红外光谱分析
图 3 为乙基纤维素纳米膜、乙基纤维素/酮洛芬纳米纤维膜以及酮洛芬纳米纤维的FTIR图谱。3 474.19 cm-1处为乙基纤维素的羟基峰,1 107.44 cm-1处的峰是由乙基纤维素分子内醚键的伸缩振动产生的。在乙基纤维素纳米膜、乙基纤维素/酮洛芬纳米纤维膜的红外图谱中都可以看到这两个特征峰的存在。在酮洛芬的红外光谱图中,1 695.63cm-1和1 655.13 cm-1处为酮洛芬上的碳氧双键的伸缩振动峰,在乙基纤维素/酮洛芬纳米纤维膜上出现相同的特征峰,表明酮洛芬成功负载于乙基纤维素纳米纤维膜上。
2.3 XRD分析
测得的X-衍射图谱如图 4 所示,从图 4 可见乙基纤维素纤维在2θ为44.3°处有一个高的衍射峰,在15.9°处有一个较低的衍射峰,而酮洛芬在载入纳米纤维前,在2θ为15°、18.3°、22.8°等处均有衍射峰值,而在载入纳米膜之后特征峰消失,说明酮洛芬在纳米纤维中呈无定形状态。
2.4 体外药物缓释性能
图 5 为乙基纤维素/酮洛芬纳米纤维膜中酮洛芬药物的体外累积释放率曲线图。由图 5 可知,酮洛芬的释放速率相对较慢,总的药物释放量较小,7 天左右达到一个最大释放量,为50%左右。这是因为乙基纤维素是一种疏水材料,在缓冲液中的溶解度很小,所以负载在纳米纤维膜中的药物很难被快速释放出来,但这也正好达到了药物缓慢释放的效果,延长了用药时间。因此,本文所述的乙基纤维素纳米纤维膜可以用作缓慢释药的载体模型,用于不同疾病的治疗。
3 结论
本文以乙基纤维素为原料,酮洛芬为药物模型,利用静电纺丝计算制备了乙基纤维素/酮洛芬纳米纤维膜,利用SEM和FTIR验证了纳米纤维膜中药物酮洛芬的存在,说明乙基纤维素载药纤维制备成功。XRD表征了结晶度变化情况,同时,还对其药物体外缓释性能进行了考察。试验结果表明:采用静电纺丝制备的乙基纤维素/酮洛芬纳米纤维膜,表面光滑无粘连,直径在500 ~ 600 nm之间,药物在其中由结晶状态变成了无定形状态。释药研究结果表明在 7 天左右的释药率达到50%左右,可以用作药物缓释材料模型。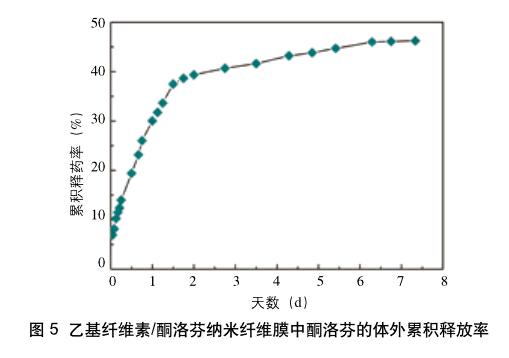
参考文献
[1] Yoon J, Y S Jung, J M Kim. A combinatorial approach for colorimetric differentiation of organic solvents based on conjugated polymer-embedded electrospun fibers[J]. Advanced Functional Materials, 2009, 19(2):209-214.
[2] Gopal R, Kaur S, Ma Z , et al. Electrospun nano fibrous filtration membrane[J]. Journal of Membrane Science, 2006 , 281(1-2):581-586.
[3] Fengxuan Han, Xiaoling Jia , Dongdong Dai, et al. Performance of a multilayered small-diameter vascular scaffold dual-loaded with VEGF and PDGF [ J]. Biomaterials, 2013, 34 (13);7302-7313.
[4] W Zhao, J Li,K Jin,et al. Fabrication of functional PLGAbased electrospun scaffolds and their applications in biomedical engineering[J]. Materials Science & Engineering C, 2015,59:1181-1194.
[5]Abidian M R, D H Kim, D C Martin. Conducting-polymer nanotubes for controlled drug release[J]. Advanced Materials, 2006, 18(4): 405.
[6] J Zhao,S Liu,B Li,et al. Stable acid-responsive electrospunbiodegradable fibers as drug carriersand cell scaffolds[ J]. Macromolecular Bioscience, 2013, 13(7):885-892.
[7] 巫寒冰,孙衎,丁兆强,等. 新型PVA/PEI/MWCNTs纳米纤维制备及其释药研究[J]. 化工新型材料,2015,34(4):115-121.
[8] Amara M,H Kerdjoudj. Modification of cation-exchange membrane properties by electro-adsorption of polyethyleneimine[J]. Desalination,2003,155(1):79-87.
[9] Srinivas M,Medaiah S,Girish S,et al.The effect of Ketoprofen in chronic periodontitis: a clinical double-blind study[J].Journal of Indian Society of Periodontology,2011,15 ( 3 ):255-259.
[10] Desai SN,Santhosh MCB.A randomized,double blind comparison of pethidine and Ketoprofen as adjuvants for lignocaine in intravenous regionalanaesthesia[J].Brazilian Journal of Anesthesiology: English Edition,2014,64 ( 4 ):221-226.
[11] Gigante A,Tagarro I.Non-steroidal anti-inflammatory drugs and gastroprotection with proton pump inhibitors: a focus on ketoprofen/ omeprazole[J].Clinical Drug Investigation,2012,32 ( 4 ) : 221-233.
[12] 李海刚,袁中文,关世侠,等. 酮洛芬微丸缓释片的制备及体外释放度考察[J]. 医院药学杂志,2011,31(20):1711-1713.

