正压通气对阻塞性睡眠呼吸暂停综合征患者夜间心脏自主神经调节功能的影响
, ,
(淮安市第一人民医院,江苏 淮安 223300)
·临床医学·
正压通气对阻塞性睡眠呼吸暂停综合征患者夜间心脏自主神经调节功能的影响
万宗仁,陈炜,徐靖
(淮安市第一人民医院,江苏 淮安 223300)
目的探讨正压通气治疗对阻塞性睡眠呼吸暂停综合征(OSAS)患者夜间心脏自主神经调节功能的影响。方法92例主诉睡眠打鼾患者夜间行8小时多导睡眠图监测,并同步动态心电图监测。本研究根据睡眠呼吸监测结果将患者分为三组:重度OSAS组(39例);轻中度OSAS组(32例);单纯鼾症组(21例)。其中重度OSAS组患者次日夜间经家用呼吸机正压通气治疗,并同步监测夜间动态心电图。结果重度OSAS组时域指标中SDNN、SDANN指数均显著低于轻中度OSAS组和单纯鼾症组,频域指标LF显著高于轻中度OSAS组和单纯鼾症组(P<0.05);Pearson相关分析显示氧减指数(ODI)、最低血氧饱和度(LSaO2)、血氧低于90%的时间比(T90)与SDNN、SDANN指数和LF显著相关(P<0.05)。与未使用呼吸机治疗时相比较,重度OSAS患者夜间经正压通气治疗时检测的时域指标SDNN、SDANN指数均显著降低,频域指标LF明显增高(P<0.05)。结论正压通气治疗可改善OSAS患者夜间心率变异性的降低。心脏自主神经调节功能的改变可能是OSAS患者夜间心律失常的重要机制之一。
睡眠呼吸暂停综合征; 正压通气; 心率变异性
阻塞性睡眠呼吸暂停综合征(obstructive sleep apnea syndrome,OSAS)是一种常见的睡眠相关性疾病,研究显示OSAS患者夜间心律失常的发生与睡眠中伴有间歇缺氧有关[1],但其相关机制尚不明确。心率变异性(heart rate variability,HRV)分析是一项反映心脏自主神经调节功能的敏感检测方法,是量化迷走、交感神经张力的重要指标之一。多导睡眠图(polysomnography,PSG)检测是目前公认诊断OSAS的金标准。本研究观察不同程度OSAS患者夜间心率变异性,以及正压通气治疗对其影响,以探讨心脏自主神经调节功能的变化在OSAS导致夜间心律失常过程中的作用。
1 资料与方法
1.1一般资料收集淮安市第一人民医院2014年11月至2015年12月因主诉睡眠打鼾就诊的住院和门诊患者共92例。其中男性88例,女性18例;平均年龄(49.01±11.8)岁;年龄24~77岁。根据中华医学会2011年OSAS诊治指南[2],按睡眠呼吸暂停指数(AHI)将入组患者分为重度OSAS组(AHI>30);轻中度OSAS组(5≤AHI≤30);单纯鼾症组(AHI<5)。受试者入组标准:(1)均为首诊,未进行有关OSAS方面的手术和呼吸机治疗;(2)排除已诊断心功能不全、冠心病、心律失常的患者。本研究得到淮安市第一人民医院伦理委员会批准。
1.2方法所有患者均采用多导睡眠图(PSG)检测,睡眠记录均从22:00开始至次日清晨06:00结束,监测当日均禁用咖啡、酒、茶等饮品,禁用抗心律失常药、镇静剂等药品。PSG记录分析参数:AHI、最低血氧饱和度(LSaO2)、血氧低于90%的时间比(T90)、氧减指数(ODI)。所有患者同步应用12导联长程心电图仪(迪姆软件有限公司)记录动态心电变化。各数据均经电脑自动回放,人工校正。动态心电图分析指标:时域指标①SDNN 指全部正常心动周期的标准差;②SDANNI 指每5min窦性RR间期均值的标准差;③rMSSD 指所有邻近窦性RR间期长度差异平方均值的平方根;④PNN50 指相邻两个正常窦性RR间期差值>50 ms的个数所占的百分数。频域指标①高频功率(HF)频带:0.15~0.40 Hz,受迷走神经影响;②低频功率(LF)频带:0.04~0.15 Hz,受交感神经和迷走神经共同影响。所有重度OSAS患者次日夜间采用家用呼吸机(万曼公司)正压通气治疗,并再次应用动态心电记录器记录动态心电图。
2 结 果
2.1不同组间一般临床资料和PSG参数的比较各组间比较,年龄和性别差异均无统计学意义(P=0.520和P=0.533);与轻中度OSAS组、单纯打鼾组比较,重度OSAS组BMI、LSaO2、ODI、血氧<90%的比例差异均有统计学意义(P<0.05)(表1)。
表1一般临床资料及PSG监测结果

项目重度OSAS组轻中度OSAS组单纯打鼾组性别(女/男)8/315/274/17年龄(岁)51.3±11.249.8±11.947.6±12.7BMI(kg/m2)27.2±3.7a25.9±3.3a22.9±2.7LSaO2(%)74.3±9.1ab83.5±6.7a91.6±4.6ODI(次/h)55.9±13.8ab18.5±9.12.9±2.3T90(%)26.2±15.2ab3.4±3.8a0.9±1.8
BMI:体重指数;AHI:呼吸暂停低通气指数;LSaO2:最低血氧饱和度;ODI:氧减指数。与单纯打鼾组比较,aP<0.05与轻中度OSAS组比较,bP<0.05
2.2比较各组间HRV时域指标和频域指标的差异:重度OSAS组时域指标SDNN、SDANNI明显低于轻度OSAS组、单纯打鼾组,频域指标LF高于轻度OSAS组、单纯打鼾组(P<0.05)。rMSSD、PNN50和HF值均有下降趋势,无显著性差异(表2)。
表2三组间HRV参数比较
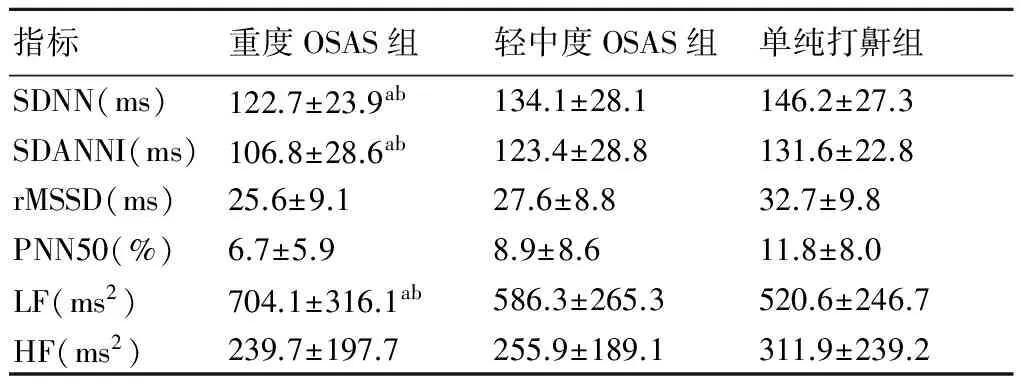
指标重度OSAS组轻中度OSAS组单纯打鼾组SDNN(ms)122.7±23.9ab134.1±28.1146.2±27.3SDANNI(ms)106.8±28.6ab123.4±28.8131.6±22.8rMSSD(ms)25.6±9.127.6±8.832.7±9.8PNN50(%)6.7±5.98.9±8.611.8±8.0LF(ms2)704.1±316.1ab586.3±265.3520.6±246.7HF(ms2)239.7±197.7255.9±189.1311.9±239.2
与单纯打鼾组比较,a:P<0.05;与轻中度OSAS组比较,b:P<0.05
2.3 Pearson相关分析显示AHI、ODI、血氧<90%的比例与时域指标SDNN、SDANNI成负相关,与频域指标LF成正相关;LSaO2与时域指标SDNN、SDANNI成正相关,与频域指标LF成负相关(P<0.01)。BMI与HRV各参数的相关性无统计学意义(表3)。
表3BMI、PSG检测各参数与HRV各参数的相关性
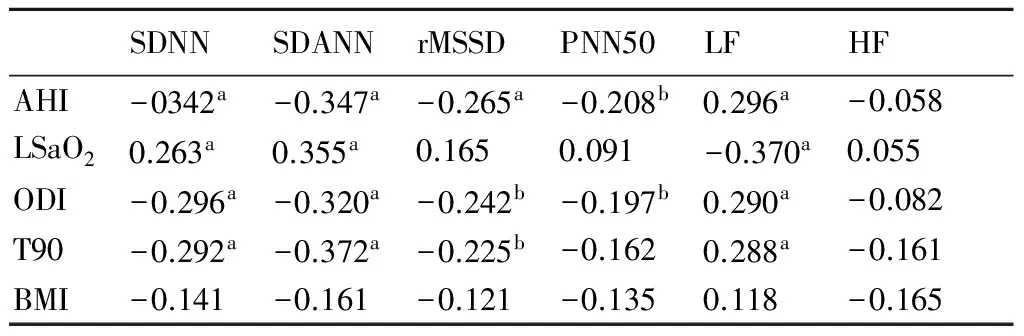
SDNNSDANNrMSSDPNN50LFHFAHI-0342a-0.347a-0.265a-0.208b0.296a-0.058LSaO20.263a0.355a0.1650.091-0.370a0.055ODI-0.296a-0.320a-0.242b-0.197b0.290a-0.082T90-0.292a-0.372a-0.225b-0.1620.288a-0.161BMI-0.141-0.161-0.121-0.1350.118-0.165
a:在0.01水平(双侧)上显著相关;b:在0.05水平(双侧)上显著相关
2.4与未用呼吸机治疗比较重度OSAS患者经正压通气治疗的时域指标SDNN、SDANNI显著升高,频域指标LF降低(P<0.01)(表4)。
表4重度OSAS患者正压通气治疗前与治疗中HRV参数比较
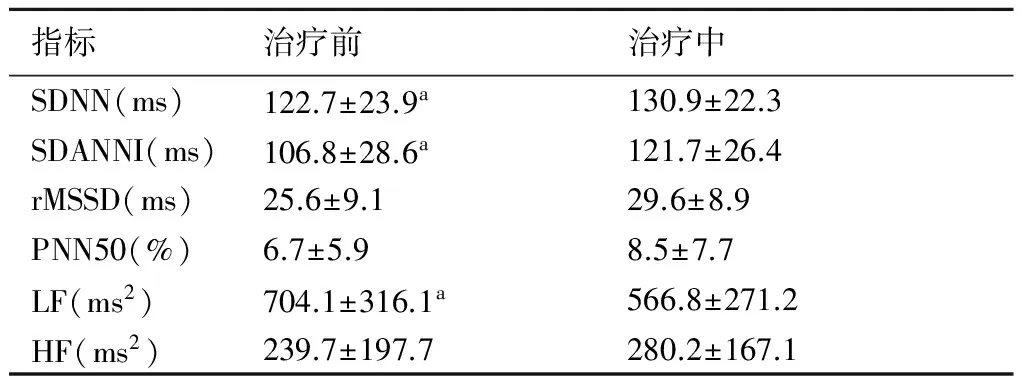
指标治疗前治疗中SDNN(ms)122.7±23.9a130.9±22.3SDANNI(ms)106.8±28.6a121.7±26.4rMSSD(ms)25.6±9.129.6±8.9PNN50(%)6.7±5.98.5±7.7LF(ms2)704.1±316.1a566.8±271.2HF(ms2)239.7±197.7280.2±167.1
与治疗后比较,a:P<0.05
3 讨 论
正常生理情况下,心电活动周期由自主神经系统和中枢有节律的进行调节,受交感和迷走神经的双重支配,心率变异性(HRV)参数是两者拮抗平衡的结果。目前,有部分研究者认为HRV可作为一种检测OSAS的初筛方法[3]。时域指标SDNN主要体现心脏自主神经功能的整体变化,SDANNI主要体现交感神经的张力情况,rMSSD、PNN50主要反映迷走神经张力对心率的调控影响;频域指标LF主要反映交感神经的张力,HF主要反映迷走神经的张力变化。本研究发现,重度OSAS组的时域指标SDNN、SDANNI明显低于单纯鼾症组和轻中度OSAS组,且频域指标LF明显高于单纯鼾症组和轻中度OSAS组,结果提示OSAS患者夜间出现迷走神经张力降低,伴或不伴交感神经张力增高。本研究结果与许多国内外的研究结果相似[4-6]。正压通气治疗的重度OSAS患者时域指标SDNN、SDANNI显著升高,频域指标LF降低,结果提示正压通气治疗的OSAS患者迷走神经张力明显改善。
夜间间歇低氧是OSAS导致夜间各种心律失常、冠心病等一系列疾病的病理生理学基础。Pearson相关分析显示AHI、ODI、T90、LSaO2与SDNN、SDANNI、LF具有显著相关性,本研究表明OSAS患者夜间反复低氧血症也是夜间心率变异性改变的病理生理学基础。其相关机制可能为:OSAS患者睡眠中反复出现呼吸暂停及低通气,导致反复的低氧血症,激活主动脉弓、颈动脉体内的自主神经调节感受器,导致夜间迷走神经活动下降,同时可能出现交感神经兴奋性增加,进而影响心率变异性。正压通气治疗改善OSAS患者夜间间歇缺氧过程,动态心电图监测结果表明夜间迷走神经张力得到部分改善。
本研究表明OSAS患者夜间出现心率变异性降低,正压通气治疗可提高OSAS患者夜间的心率变异性。OSAS患者夜间心率变异性降低可能与其夜间各种心律失常有一定的相关性。其可能机制为:OSAS患者睡眠中出现心脏自主神经调节的变化,夜间迷走神经张力出现下降,迷走神经抑制心律失常的保护作用减弱;夜间交感神经张力升高,可诱发心肌异位点兴奋性升高,易导致各种心律失常[7]。在OSAS导致夜间心律失常的过程中,心脏自主神经调节功能的改变可能发挥了重要作用。
[1] Andrew D,Virend K.Obstructive sleep apnea and cardiovascular disease[J].Curr Opin Cardiol,2009,24:516-520.
[2] 中华医学会呼吸病学分会睡眠呼吸障碍学组.阻塞性睡眠呼吸暂停低通气综合征诊疗指南[J].中华结核和呼吸杂志,2012,35(1):9-12.
[3] 张海澄,韩芳,郭继鸿,等.应用心率变异性时域和频域指标初筛阻塞性睡眠呼吸暂停综合征[J].中华心律失常学杂志,2005,9(1):25-28.
[4] Ng AC,Davis GM,Chow CM,et al.Impact of sleep disordered breathing severity on hemodynamics,autonomic balance and cardiopulmonary functional status in chronic heart failure[J].Int J Cardiol,2010,141(3):227-235.
[5] Ueno LM,Drager LF,Rodrigues AC,et al.Day-night pattern of autonomic nervous system modulation in patients with heart failure with and without sleep apnea[J].Int J Cardiol,2011,148(1):53-58.
[6] hoi JH,Yi JS,Lee SH,et al.Effect of upper airway surgery on heart rate variability in patients with obstructive sleep apnea syndrome[J].J Sleep Res,2012,21(3):316-321.
[7] Fletcher EC.Sympathetic activity and blood pressure in the sleep apnea syndrome[J].Respiration,1997,64(suppl 1):22-28.
10.15972/j.cnki.43-1509/r.2016.04.025
2015-02-25;
2016-04-19
R741
A
秦旭平)

