拉米夫定与阿德福韦酯联用治疗失代偿期乙型肝炎肝硬化的最佳时机探讨
张笛,杨丽,李良平,赵光斌
(1 四川省医学科学院 四川省人民医院,成都 610072;2 四川大学华西医院)
拉米夫定与阿德福韦酯联用治疗失代偿期乙型肝炎肝硬化的最佳时机探讨
张笛1,2,杨丽2,李良平1,赵光斌1
(1 四川省医学科学院 四川省人民医院,成都 610072;2 四川大学华西医院)
目的 探讨拉米夫定与阿德福韦酯联用治疗失代偿期乙型肝炎肝硬化的最佳时机。方法 选择105例失代偿期乙型肝炎肝硬化患者随机分为初始联合组、12周联合组及24周联合组,每组35例。三组均给予保肝、利尿等常规治疗,初始联合组同时给予拉米夫定100 mg/d和阿德福韦酯10 mg/d;12周联合组、24周联合组先予给予拉米夫定治疗(剂量同上),用药12、24周时检测血清HBV DNA,HBV DNA>1×103copies/mL者加用阿德福韦酯(剂量同上);均连续治疗1年。三组分别于治疗前及治疗1年(治疗后)检测血清ALT、总胆红素(TBIL)、白蛋白(ALB),计算ALT复常率及HBV DNA转阴率,行肝功能Child-Pugh分级,检测血清尿素氮(BUN)、肌酐(Cr)、肌酸激酶(CK)。结果 与治疗前比较,三组治疗后血清ALT均降低(P均<0.05),血清ALB水平均升高(P均<0.05);初始联合组、12周联合组血清TBIL水平均降低(P均<0.05);ALT复常率比较差异均无统计学意义(P均>0.05)。初始联合组HBV DNA转阴率高于12周联合组和24周联合组,且12周联合组高于24周联合组(P均<0.05)。治疗后初始联合组和12周联合组Child-Pugh A级患者数均多于、C级患者数均少于24周联合组(P均<0.05)。三组治疗前后血清CK、BUN、Cr比较差异均无统计学意义(P均>0.05)。结论 失代偿期乙型肝炎肝硬化患者初始治疗即应采用拉米夫定与阿德福韦酯联合应用。
失代偿期乙型肝炎肝硬化;拉米夫定;阿德福韦酯
失代偿期乙型肝炎肝硬化患者一般情况及肝脏情况较差,常合并腹水、肝性脑病等并发症,预后差,5年生存率仅14%[1]。研究发现,大部分失代偿期乙型肝炎肝硬化患者处于乙肝病毒持续复制状态,多数伴有肝细胞炎症坏死,肝脏炎症反复破坏肝脏细胞,导致肝功能衰竭、肝癌等。积极的抗病毒治疗可减轻肝脏炎症反应,抑制病毒复制,改善肝功能,延缓肝硬化进展[2,3]。拉米夫定联合阿德福韦酯是目前临床常用的抗病毒治疗方案,但两药配伍的最佳时间一直存在争议。为此我们进行了如下研究。
1 资料与方法
1.1 临床资料 选择2012年10月~2014年1月四川省人民医院消化内科就诊且完成完整1年随访的失代偿期乙型肝炎肝硬化患者105例,年龄30~70(53.2±11.1)岁,男64例、女41例,ALT 85.4~125.8(101.1±60.9)U/L,HBV-DNA 2.25~7.68(5.43±14.5)×106copies/mL,Child B级52例、C级53例。纳入标准:符合我国2010年版“慢性乙型肝炎防治指南”中关于失代偿期乙型肝炎肝硬化的诊断标准[4],HBsAg阳性,有肝硬化的实验室及影像学检查依据,血清HBV DNA>1×103copies/mL;完成1年随访;入组前无其他抗病毒药物治疗史,治疗过程中遵医嘱调整药物,无自行停药或调整药物等;随访过程中无明显肝性脑病、食管胃底静脉曲张出血、肝癌、肾功能异常等并发症发生。将105例患者随机分为初始联合组、12周联合组、24周联合组,每组35例,三组年龄、性别、ALT、HBV-DNA、Child分级等均具有可比性。
1.2 治疗方法 三组入院后均给予保肝、利尿等常规治疗。初始联合组同时给予拉米夫定100 mg/d、阿德福韦酯10 mg/d,连续治疗1年;12周联合组、24周联合组均予拉米夫定治疗(剂量同上),治疗12、24周时检测血清HBV DNA均>1×103copies/mL,加用阿德福韦酯(剂量同上)继续治疗12、24周,均连续治疗1年。
1.3 相关指标观察 三组分别于治疗前及治疗1年时(治疗后)采用雅培C-16000全自动生化分析仪检测血清ALT、总胆红素(TBIL)、白蛋白(ALB);计算ALT复常率,ALT复常率=复常患者数/总患者数;采用荧光PCR法(ABI 7500 Faster分析仪)检测血清HBV-DNA,计算HBV-DNA转阴率,HBV-DNA转阴率=转阴患者数/总患者数;进行肝功能Child-Pugh分级;采用雅培C-16000全自动生化分析仪检测血清尿素氮(BUN)、肌酐(Cr)、肌酸激酶(CK)。

2 结果
2.1 血清ALT、TBIL、ALB 治疗后三组血清ALT均较治疗前降低(P均<0.05),血清ALB均较治疗前升高(P均<0.05);初始联合组、12周联合组血清TBIL均较同组治疗前及24周联合组治疗后降低(P均<0.05)。见表1。
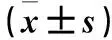
表1 三组治疗前后血清ALT、TBIL、ALB比较
注:与同组治疗前比较,*P<0.05;与24周联合组比较,△P<0.05。
2.2 ALT复常率、HBV DNA转阴率 治疗后三组ALT复常率比较差异均无统计学意义(P均>0.05);初始联合组HBV DNA转阴率高于12周联合组和24周联合组(P均<0.05),且12周联合组高于24周联合组(P<0.05)。见表2。
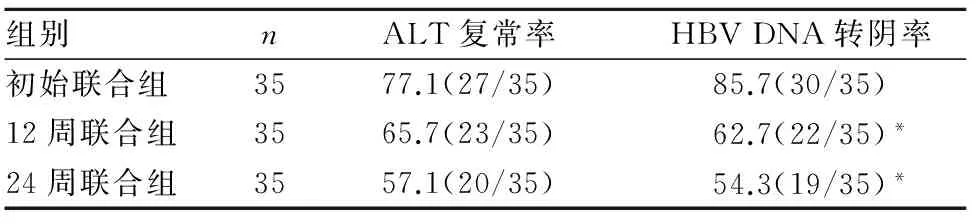
表2 三组治疗后ALT复常率、HBV DNA转阴率比较(%)
注:与初始联合组比较,*P<0.05;与12周联合组比较,△P<0.05。
2.3 Child-Pugh分级 治疗1年时,初始联合组和12周联合组Child-Pugh A级患者数均多于、C级患者数均少于24周联合组(P均<0.05)。见表3。
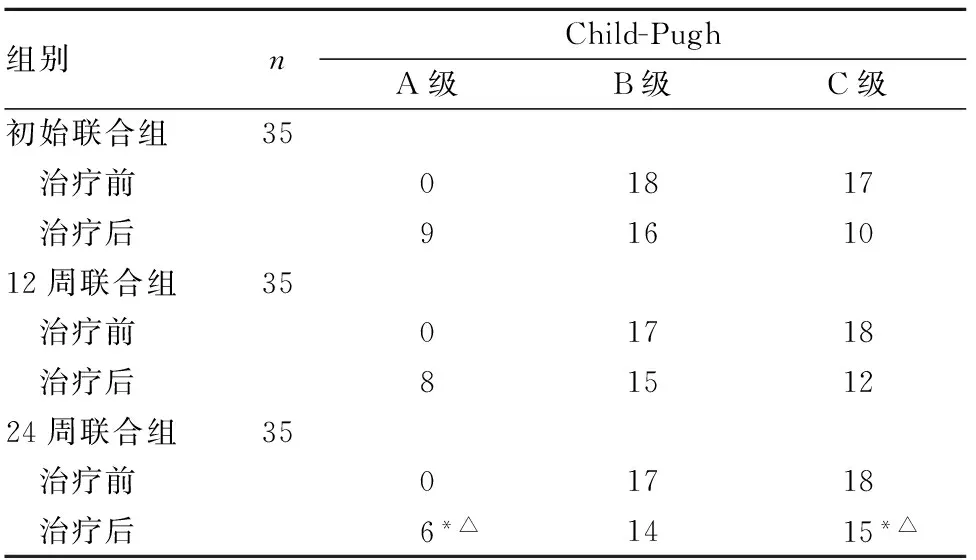
表3 三组治疗前后Child-Pugh分级比较(例)
注:与初始联合组比较,*P<0.05;与12周联合组比较,△P<0.05。
2.4 血清BUN、Cr、CK 三组治疗后血清BUN、Cr、CK比较均无明显差异(P均>0.05),见表4。
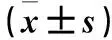
表4 三组治疗前后血清BUN、Cr、CK比较
注:与同组治疗前比较,*P<0.05。
3 讨论
近年来,失代偿期乙型肝炎肝硬化发病率逐渐升高,患者预后不佳[5,6]。目前临床多关注代偿期肝病的抗病毒治疗,对失代偿期乙型肝炎肝硬化的抗病毒治疗研究相对较少[7]。国内外多数指南均指出,对于失代偿期乙型肝炎肝硬化患者不论其血清转氨酶及HBeAg情况如何,均应尽早使用可快速抑制病毒复制且耐药风险低的核苷(酸)类药物进行抗病毒治疗,疗程为长期或终生[8~11],但单一使用核苷(酸)类似物治疗易发生耐药。
拉米夫定和阿德福韦酯是核苷(酸)类抗病毒药物的典型代表,拉米夫定单药耐药率高,其耐药位点主要位于rtM204V/I[12];阿德福韦酯耐药位点主要是rtA181V和rtN236T;二者耐药位点无交叉。研究发现,选择没有交叉耐药位点的拉米夫定与阿德福韦酯共同抗病毒治疗可能会防止耐药的发生[9]。万十千等[13]研究发现,拉米夫定联合阿德福韦酯治疗耐药性HBeAg阴性慢性乙型肝炎可以明显提高应答率、降低耐药率、改善肝脏功能、提高生存率。目前很多研究表明,失代偿期乙型肝炎肝硬化疾病初期给予拉米夫定、阿德福韦酯治疗能快速抑制DNA病毒复制,避免病毒学突破、ALT升高及组织学恶化,降低肝炎病毒对肝脏的影响,使肝脏炎症得到有效控制,避免肝炎急性恶化出现肝脏衰竭,降低肝癌发生的风险,改善预后,且可避免药物耐药[9,13~20]。但两药最佳配伍及应用时机的相关报道鲜见。
阿德福韦酯本身含磷酸基团,可竞争脱氧腺苷三磷酸底物而终止HBV DNA链的延长,抑制HBV DNA复制,在多种细胞内均具有较强活性,对YMDD变异株亦有较强的抑制作用;拉夫米定于细胞内代谢后生成具有活动的拉夫米定三磷酸盐,抑制HBV聚合酶的活性,进而阻断HBV DNA链的合成,但随着用药时间延迟可发生耐药,对该药物应答效应减弱,疗效降低;众多研究均证实阿德福韦酯和拉夫米定耐药位点无交叉,具有互补性,故猜想两者越早期联合应用抗病毒活性、抑制HBA DNA复制效果越佳且有利于肝功能改善,延缓病情进展[21]。本研究结果显示,与治疗前比较,三组治疗后血清ALT均降低,血清ALB均升高;初始联合组、12周联合组血清TBIL均降低;ALT复常率比较差异均无统计学意义。初始联合组HBV DNA转阴率高于12周联合组和24周联合组,且12周联合组高于24周联合组。初始联合组、12周联合组治疗后TBIL均明显降低但24周联合组TBIL降低不明显;初始联合组、12周联合组、24周联合组ALT复常率、HBV DNA转阴率均逐渐降低;初始联合组和12周联合组Child-Pugh A级患者数均多于、C级患者数少于24周联合组。上述结果证实拉米夫定初始联合阿德福韦酯治疗失代偿期乙型肝炎肝硬化患者效果最佳,拉米夫定使用24周应答不佳时加用阿德福韦酯效果最差。此外发现三组治疗后血清CK、BUN、Cr差异均无统计学意义,提示三种配伍方式均相对安全,对肝肾功能无明显影响。
综上所述,拉米夫定初始联合阿德福韦酯治疗对失代偿期乙型肝炎肝硬化患者初始治疗时即应选择拉米夫定与阿德福韦酯联用。但本研究观察时间较短、例数较少,需进一步扩大样本量、长期观察以明确结论。
[1] Fattovich G, Giustina G, Schalm SW, et al. Occurrence of hepatocellular carcinoma and decompensation in western European patients with cirrhosis type B[J]. Hepatology, 1995,21(1):77-82.
[2] 周学斌,肖绍树.拉米夫定治疗失代偿期乙型肝炎肝硬化的研究进展[J].实用病杂志,2009,12(2):150-152.
[3] 拉米夫定临床应用专家指导小组.2004年拉米夫定临床应用专家指导意见[J].中华肝脏病杂志,2004,12(7):425.
[4] 中华医学会肝病学分会.中华医学会感染病学分会.慢性乙型肝炎防治(2010年版)[J].中华肝脏病杂志,2011,19(8):13-24.
[5] Rerldi G, Fattovich G, Hadziyannis S, et al. Survival and prognostic factors in 366patients with compensated cirrhosis:a multicenter study[J]. J Hepatol, 1994,21(4):656- 666.
[6] Liaw YF, Sheen IS, Chen TJ, et al. Incidence,determinantsand significance of delayed clearance of serum HBsAg in chronic hepatitis B virus infection:a prospective study[J]. Hepatolgy, 1991,13(4):627-631.
[7] 张志沛,李果,王震.拉米夫定优化治疗失代偿期乙肝后肝硬化患者的效果及对预后的影响[J].中国实用医药,2013,8(32):145-147.
[8] 万谟彬.拉米夫定优化治疗慢性乙型肝炎专家会议纪要[J].肝脏,2009,14(2):167-169.
[9] 魏兆勇,张分明,许德军,等.拉米夫定联合阿德福韦酯治疗失代偿期乙型肝炎肝硬化临床观察[J].中华医院感染学杂志,2014,24(2):361-363.
[10] Lok AS, McMahon BJ. Chronic hepatitis B: update 2009[J]. Hepatology, 2009,50(3):661-662.
[11] European Association for the Study of the Liver. EASL clinicalpractice guidelines:management of chronic hepatitis B[J]. J Hepatol, 2009,50(2):227-242.
[12] Leung NW, Lai CL, Chang TT, et al. Extended lamivudine treatment patients with chronic hepatitis B enhances hepatitis B e antigen seroconversion rates: results after 3 years of therapy[J]. Hepatology, 2001,33(6):1527-1532.
[13] 万十千,石涵,万学发,等.阿德福韦酯联合拉米夫定治疗耐药性 HBeAg 阴性慢性乙型肝炎[J].中华医院感染学杂志,2010,20(16):2502-2503.
[14] 徐步惠,孙苏,王江华,等.拉米夫定优化治疗乙型肝炎肝硬化失代偿期临床观察[J].肝脏,2012,17(8):610-612.
[15] 马晓军,陈小苹,陈学福,等.拉米夫定与阿德福韦酯初始联合及48周时治疗慢性乙型肝炎[J].中华肝脏病杂志,2012,20(2):98-102.
[16] 张笛,赵光斌,李良平,等.拉米夫定与阿德福韦酯初始联合与优化治疗失代偿期乙型肝炎肝硬化疗效观察[J].实用肝脏病杂志,2015,18(1):51-53.
[17] 李芬.拉米夫定联合阿德福韦酯治疗失代偿期乙型肝炎肝硬化的临床疗效观察[J]. 临床医学,2015,35(1):80-81.
[18] 冯静,伦秀英.拉米夫定联合阿德福韦酯初始治疗慢性乙型肝炎患者临床观察[J].实用肝脏病杂志,2011,14(3):190-191.
[19] Lv GC, Yao JM, Yang YD, et al. Efficacy of combined therapy in with hepatitis B vieus-related decompensated cirrhosis[J]. World J Gastroenterology, 2013,19(22):3481 -3486.
[20] Fan XH, Geng JZ, Wang LF, et al. De novo combination therapy with lamivudine and adefovir dipivoxil in chronic heoatitis B patients[J]. World J Gastroenterology, 2011,17(43):4804-4809.
[21] 杨世华.乙肝肝硬化失代偿期治疗方案的成本效果分析[J].中国药物经济学,2014,9(2):9-10.
·作者·编者·读者·
《山东医药》参考文献著录要求
每篇论文须标引参考文献10~20条。正文中引用的文献采用顺序编码制,以引用文献的先后顺序连续编码,并将序号置于方括号中。文后参考文献按GB/T7714-2005《文后参考文献著录规则》采用顺序编码制标注,序号置于方括号中,排列于文后。内部刊物、未发表资料、个人通信等请勿作为文献引用,确需引用时,可将其在正文相应处注明。引用文献(包括文字和表达的原意)务请作者与原文核对无误。日文汉字请按日文规定书写,勿与我国汉字及简化字混淆。参考文献中的作者前1~3名全部列出,3名以上只列前3名,后依文种加表示“,等”的文字。作者姓名一律姓氏在前,名字在后,外国人的名字采用首字母缩写姓氏,缩写名后不加缩写点;不同作者之间用“,”隔开。外文期刊名称用缩写,以Index Medicus中的格式为准;中文期刊用全名。论文题目后加文献类型及标识,如专著[M]、期刊文章[J]等。每条参考文献均须著录卷、期及起止页。作者必须自行核对参考文献原文,无误后将其按引用顺序(用阿拉伯数字)排列于文末。举例:
[1] 杜贾军,孟龙,陈景寒,等.手辅助电视胸腔镜食管切除胃食管胸内吻合术[J].山东医药,2004,44(27):1-3.
[2] Takano M, Mizuno K, Okamatsu K, et al. Mechanical and structural characteristics of vulnerable plaques: analysis by coronary angioscopy and intravascular ultrasound[J]. J Am Coll Cardiol, 2002,38(1):99-104.
[3] 叶任高,陆再英.内科学[M].5版.北京:人民卫生出版社,2000:277-280.
Best time for treatment of decompensated hepatitis B cirrhosis with lamivudine and adefovir dipivoxil
ZHANGDi1,YANGLi,LILiangping,ZHAOGuangbin
(1SichuanAcademyofMedicalSciences,SichuanProvincialPeople′sHospital,Chengdu610072,China)
Objective To explore the best time for treatment of decompensated hepatitis B cirrhosis with lamivudine and adefovir dipivoxil. Methods Totally 105 cases of patients with decompensated hepatitis B cirrhosis were randomly divided into the initial combination group, 12-week combination group and 24-week combination group, 35 cases in each group. The three groups were given conventional treatment such as liver and diuresis. The initial combination group was given 100 mg/d lamivudine and 10 mg/d adefovir, while patients in the 12-week and 24-week combination groups first received lamivudine treatment (medication, dose ibid.) The serum HBV DNA was detected at week 12 and 24, and for patients with adefovir DNA>1 ×103copies/mL HBV, we added adefovir dipivoxil to them (the same dose). They were all treated continuously for 1 year. The serum ALT, total bilirubin (TBIL) and albumin (ALB) levels were detected in these three groups before and after treatment for 1 year as well as serum urea nitrogen (BUN), creatinine (Cre) and creatine kinase (CK). Then the recovery rate of ALT and HBV-DNA negative rate for Child-Pugh classification of liver function was calculated. Results Compared with before treatment, the serum ALT was decreased, and the serum ALB was increased in these three groups after treatment (allP<0.05). The serum levels of TBIL were both decreased in the initial combination group and 12-week combination group (allP<0.05), the recovery rate of ALT showed no significant difference (allP>0.05). HBV DNA negative conversion rate was higher in the initial combination group than those of 12-week and 24-week combination groups (allP<0.05), and the 12-week combination group was higher (P<0.05). After treatment, the number of patients with Child-Pugh class A were more, and the number of patients with C were less in the initial combination group and 12-week combination group that those of the 24-week combination group (allP<0.05). There were no significant differences in serum CK, BUN and Cre among these three groups (allP>0.05). Conclusion For patients with decompensated hepatitis B cirrhosis, we should use lamivudine and adefovir dipivoxil at the initial period.
decompensated hepatitis B cirrhosis; lamivudine; adefovir dipivoxil
四川省卫生厅科研基金资助项目(110184)。
张笛(1980-),女,硕士研究生、主治医师,研究方向为慢性肝脏疾病的诊断及治疗。E-mail: wendy602@sina.com
简介:杨丽(1963-),女,硕士研究生导师、主任医师,研究方向为消化系统疑难重症尤其是肝病(特别是肝硬化、脂肪性肝病、免疫性肝病)的诊治。E-mail: 1097197521@qq.com
10.3969/j.issn.1002-266X.2016.36.003
R657.3
A
1002-266X(2016)36-0009-04
2016-04-02)

