基于Mn掺杂ZnS量子点的室温磷光检测盐酸异丙嗪
许 梅,栗东霞,闫桂琴
(山西师范大学 生命科学学院,山西 临汾 041000)
基于Mn掺杂ZnS量子点的室温磷光检测盐酸异丙嗪
许 梅,栗东霞,闫桂琴*
(山西师范大学 生命科学学院,山西 临汾 041000)
以三巯基丙酸(MPA)为表面修饰剂,采用水相合成法制备了稳定且具有良好光学性质的Mn掺杂ZnS量子点。在pH 7.4的磷酸缓冲液中,盐酸异丙嗪的加入使MPA包裹的Mn掺杂ZnS量子点的室温磷光发生明显猝灭,据此建立了一种检测盐酸异丙嗪的新方法。磷光猝灭强度(ΔRTP)与盐酸异丙嗪浓度呈良好线性,其线性范围为3.2~32 μmol/L 与32~160 μmol/L,相关系数分别为0.998与0.999,检出限为0.553 μmol/L。将该方法用于人血清与尿液中盐酸异丙嗪的检测,加标回收率为96.4%~103.1%,结果满意。
Mn掺杂ZnS;量子点;室温磷光(RTP);盐酸异丙嗪(PMZ)
盐酸异丙嗪(Promethazine,PMZ)为吩噻嗪类药物,是一种抗组织胺药,具有明显的中枢安定作用,临床多用于治疗过敏性疾病、晕动症、呕吐及失眠等[1]。但使用PMZ会出现烦躁不安、神经错乱等现象,严重过量可致惊厥,继而抑制中枢,儿童若服用剂量较大,可产生谵妄(症状为胡言乱语、精神兴奋)[2]。因此,建立一种检测PMZ的新方法十分必要。目前,检测PMZ的方法主要有高效液相色谱法[3-4]、分光光度法[5]、流动注射化学发光法[6-7]、共振瑞利散射法[8]、拉曼光谱法[9]、荧光光谱法[10]、伏安法[11]、电化学法[12]等。但这些方法成本高、耗时长、灵敏度低、程序繁琐,而且大多建立于酸性环境中,因此,基于中性环境建立一种成本低、耗时少、灵敏度高、简便快速检测PMZ的新方法具有重要意义。
近年来,量子点作为一种新型的纳米材料而广受关注,其独特的光学性质,使之被用于各种领域,尤以作为探针居多[13-15]。相对于量子点的荧光而言,磷光具有选择性好、寿命长、Stokes位移大等优点,且在进行磷光检测时可避免自体荧光和散射的干扰[16-17],因此,发展量子点磷光探针是荧光分析的有力补充。此外,相较于普通量子点,掺杂量子点具有优良的稳定性和良好的光学特性[18-19]。
综上所述,本文首次利用掺杂量子点的室温磷光建立了快速检测体液中PMZ的分析方法。该方法于pH 7.4的环境中进行检测,异于其他已有方法。而且该方法能有效避免体液自体荧光和散射的干扰,同时也避免了金属离子、生物分子的干扰,因此,利用Mn掺杂ZnS量子点的室温磷光可以快速、准确、简便地检测人血清和尿液中的PMZ。
1 实验部分
1.1 仪器与试剂
采用Brucker D8-Advance X射线粉末衍射仪(德国)对量子点进行表征。荧光光谱和磷光光谱在 Cary Eclipse 荧光分光光度计(美国安里瓦公司)上进行测定,将待测溶液置于四面通石英比色池(1 cm×1 cm)中,激发和发射的狭缝宽度分别为10 nm 和20 nm。 UV-29100 紫外可见分光光度计(日本岛津公司),PHS-3C 型 pH 计(上海雷磁公司),AEU-200 电子天平(日本岛津公司)。
实验所用试剂均为分析纯。Zn(Ac)2·2H2O,Mn(Ac)2·4H2O,NaS·9H2O,NaH2PO4,Na2HPO4购自天津科密欧化学试剂有限公司;3-巯基丙酸(MPA)和PMZ购于北京百灵威科技有限公司;高纯水(18.2 MΩ·cm) 采用 WaterPro 水纯化系统(美国Labconco公司)制备。
1.2 实验方法
1.2.1 MPA包裹的ZnS∶Mn量子点的合成 参考相关文献[20-21]并做适当修改,在250 mL 三口烧瓶中,依次加入50 mL 0.04 mol/L 的MPA,2 mL 0.01 mol/L 的Mn(Ac)2和5 mL 0.1 mol/L 的Zn(Ac)2水溶液,用1 mol/L 的NaOH调节pH值至11.0,在室温下磁力搅拌,通氩气饱和30 min,确保稳定剂MPA与Zn2+和Mn2+充分络合。随后在隔绝空气的条件下用注射器快速加入5 mL 0.1 mol/L 的Na2S水溶液,室温下继续反应20 min后将得到的MPA包裹的 ZnS∶Mn 量子点溶液在50 ℃下陈化2 h,之后以相同体积的无水乙醇使量子点沉降,高速离心,倾去上层清液,于室温真空干燥24 h,即得MPA包裹的 ZnS∶Mn 量子点固体粉末。
1.2.2 室温磷光检测 以制备浓度为8.0×10-4mol/L 的PMZ溶液为母液,在一系列10 mL比色管中,依次加入50 μL 2 mg/L 的MPA包裹的 ZnS∶Mn 量子点水溶液,500 μL 0.1 mol/L 的磷酸缓冲液(PBS,pH 7.4),然后加入不同体积的PMZ溶液,用高纯水定容至5 mL,摇匀,制备成一系列含有不同浓度PMZ的待测样品,静置10 min后进行室温磷光检测。荧光分光光度计选取磷光模式,激发波长为295 nm,激发和发射的狭缝宽度分别为10 nm 和20 nm。
1.2.3 样品预处理 人体血清与尿液均来自健康志愿者,将其用高纯水稀释100倍后用于分析检测,样品无需进一步处理。

图1 MPA包裹的 ZnS∶Mn 量子点的XRD图谱Fig.1 XRD pattern of MPA-capped Mn-doped ZnS QDs
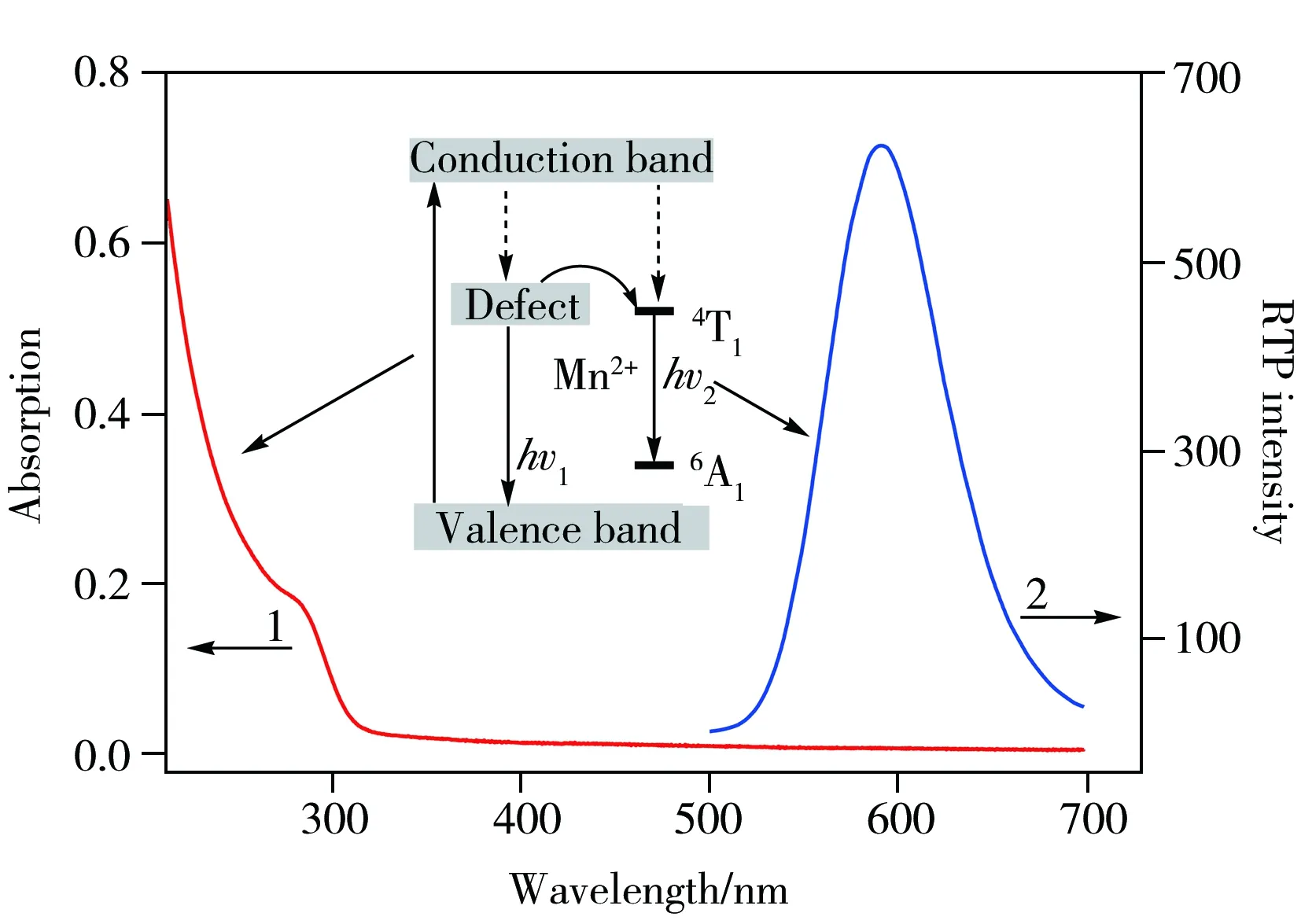
图2 MPA包裹的ZnS∶Mn 量子点的紫外吸收(曲线 1)和磷光光谱图(曲线 2)Fig.2 Absorption spectrum of MPA-capped Mn-doped ZnS QDs(curve 1) and RTP spectrum(curve 2)
2 结果与讨论
2.1 MPA包裹的ZnS∶Mn量子点的表征
图1为该量子点的XRD图谱,由图可知,所合成的MPA包裹的 ZnS∶Mn 量子点3个衍射峰分别对应立方闪锌矿结构的(111),(220),(311)3个晶面[17]。
MPA包裹的 ZnS∶Mn 量子点的紫外吸收和磷光光谱图见图2,由图可知该量子点的最大激发峰位于295 nm 处,最大发射峰位于590 nm处。在图2插图中,hυ1显示了该量子点的表面缺陷,而hυ2显示了该量子点的磷光性质是由Mn2+的三重态(4T1)到基态(6A1)的跃迁产生,ZnS是一种宽带隙半导体,其导带和价带为杂质离子提供较宽的能级范围,当激发光被ZnS主体吸收后,电子和空穴发生分离,且空穴被Mn2+捕获,由此出现电子和空穴在Mn2+上复合,从而导致Mn2+的激发,并以磷光形式释放能量[22-23]。

图3 不同浓度PMZ对MPA包裹的 ZnS∶Mn量子点磷光强度的影响Fig.3 RTP emission spectra of MPA-capped Mn-doped ZnS QDs with various concentrations of PMZ
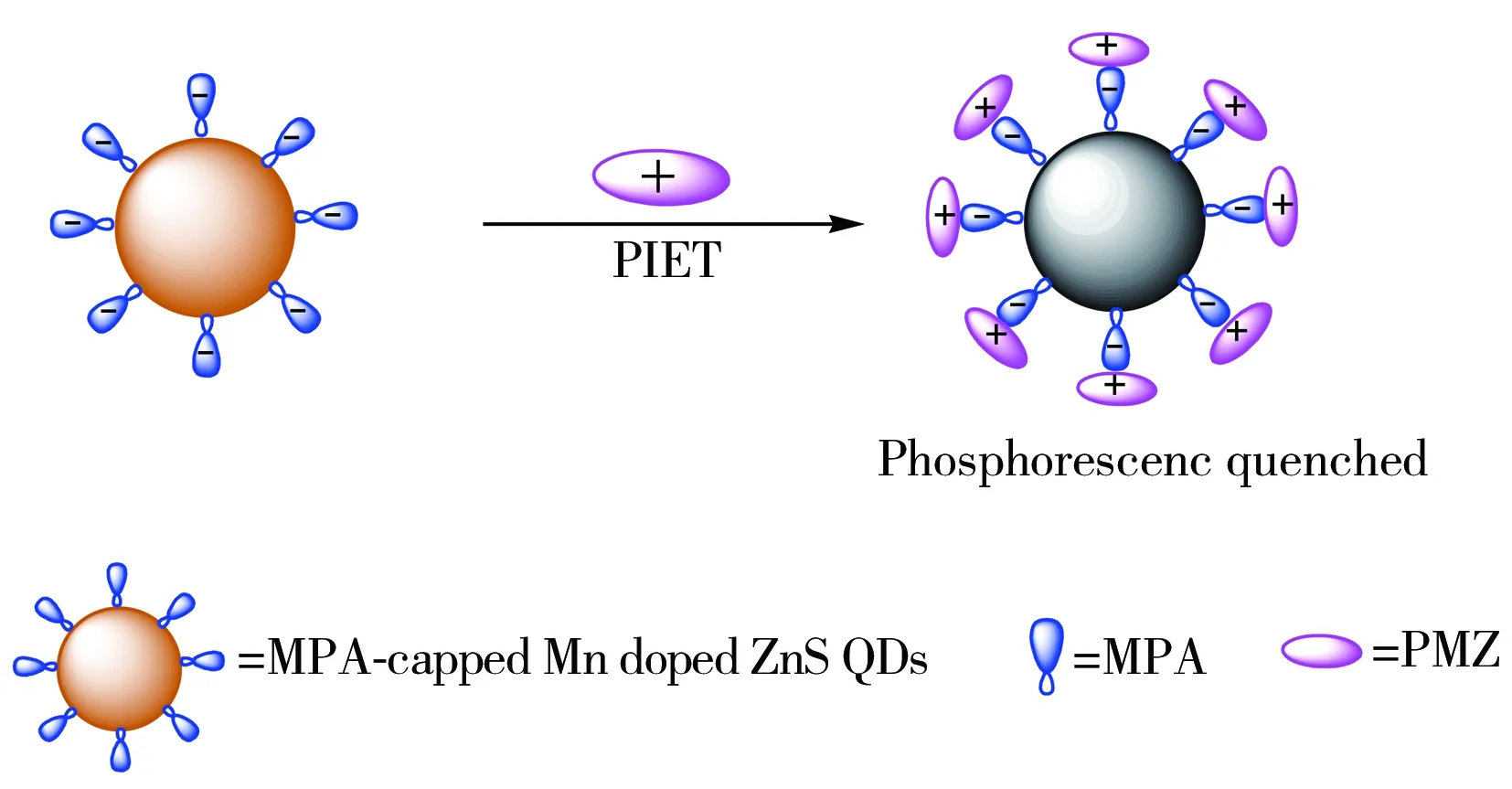
图4 基于MPA包裹的 ZnS∶Mn量子点检测PMZ的反应机理图Fig.4 Schematic illustration of PMZ detection used the MPA-capped Mn-doped ZnS QDs
2.2 选择MPA包裹的 ZnS∶Mn 量子点作为探针检测PMZ
随着PMZ浓度的增加,MPA包裹的 ZnS∶Mn量子点的磷光强度发生非常有规律的猝灭,据此建立了一种基于MPA包裹的 ZnS∶Mn 量子点的室温磷光检测PMZ的新方法。从图3可以看出,当未加入PMZ时,MPA包裹的 ZnS∶Mn 量子点有很高的磷光值,随着PMZ的加入,该量子点的磷光强度被迅速猝灭,直至PMZ浓度达到160 μmol/L 时,猝灭效果趋于稳定。
2.3 MPA包裹的 ZnS∶Mn 量子点与PMZ之间的反应机理
稳定剂MPA的加入不仅使 ZnS∶Mn 量子点的水溶性增强,也赋予该量子点表面大量的羧基,使其呈明显的负电性;而PMZ为吩噻嗪衍生物,其分子中的N原子和S原子上有孤对电子,故在水溶液中极易发生质子化后以阳离子形式存在,使其呈明显的正电性[24],因此二者可通过静电作用发生复合。除此之外,PMZ分子中的N原子和S原子上的孤对电子易通过获得电子而被氧化,因此,PMZ还可作为一种良好的电子受体;而MPA包裹的 ZnS∶Mn 量子点受到激发后,电子和空穴发生分离,空穴会被Mn2+俘获,之后电子和空穴各自在Mn2+上复合导致Mn2+激发,并以磷光形式释放能量[25],而一些小分子与量子点表面结合后会影响量子点中电子和空穴的复合过程,进而使量子点的发光强度发生改变。因此,当体系中加入PMZ后,PMZ作为一种阳离子电子受体,可能通过静电作用与MPA包裹的 ZnS∶Mn 量子点形成复合物,进而从量子点捕获电子并阻止量子点内电子与空穴的正常复合,导致MPA包裹的 ZnS∶Mn 量子点的室温磷光发生猝灭。图4为MPA包裹的 ZnS∶Mn 量子点与PMZ的反应机理图。
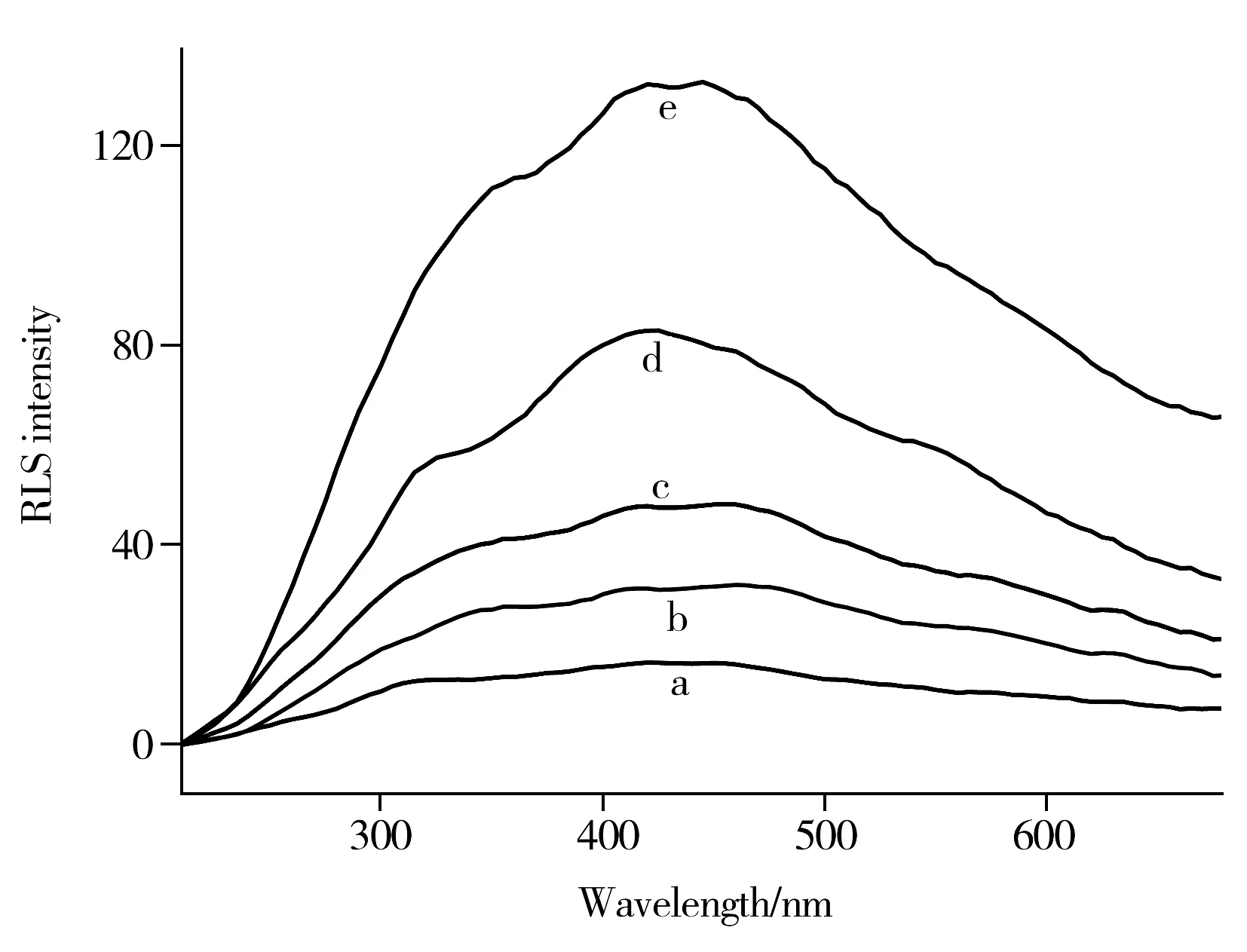
图5 PMZ与MPA包裹的 ZnS∶Mn量子点的共振散射图谱Fig.5 RLS spectra of PMZ and MPA-capped Mn-doped ZnS QDsa.48 μmol/L PMZ;b.QDs;c.curve a+curve b;d.QDs+48 μmol/L PMZ;e.QDs + 144 μmol/L PMZ
图5为PMZ与MPA包裹的 ZnS∶Mn 量子点的共振散射光谱图(RLS),由图5可见,单纯的PMZ和MPA包裹的 ZnS∶Mn 量子点的RLS强度较弱,而加入PMZ后,体系的RLS强度明显增强,且增强效应并非PMZ与量子点二者各自的RLS强度的简单叠加所致(曲线c)。此外,随着PMZ浓度的增加,RLS强度不断增强,说明MPA包裹的 ZnS∶Mn 量子点与PMZ之间可能通过静电作用结合形成了更大的散射粒子。
2.4 影响因素考察
利用MPA包裹的 ZnS∶Mn 量子点的室温磷光检测PMZ的影响因素主要有溶液的反应时间、pH值、盐(NaCl)浓度。经考察,反应时间对检测PMZ几乎无影响,因此该实验均在反应10 min后进行测定,在60 min内完成检测。在pH 5.7~7.4范围内,该体系的磷光强度明显增强;在pH 7.4~9.0范围内,该体系的磷光强度明显减弱,因此,该实验均在pH 7.4的PBS缓冲溶液中进行。盐(NaCl)浓度在0~0.25 mol/L范围时,该体系的磷光强度几乎保持不变,而人体液中的盐浓度为0.15 mol/L,因此,利用MPA包裹的 ZnS∶Mn 量子点的室温磷光可以检测人血清与尿液中的PMZ。
2.5 工作曲线
在最佳实验条件下,研究了MPA包裹的ZnS∶Mn量子点的室温磷光猝灭量(ΔRTP)与PMZ浓度之间的关系。结果显示,当PMZ浓度为3.2~160 μmol/L 时,该量子点的ΔRTP与PMZ浓度之间呈线性关系:当PMZ浓度为3.2~32 μmol/L 时,线性方程为ΔRTP=6.001cPMZ+6.657,相关系数为0.998;当PMZ浓度为32~160 μmol/L 时,线性方程为ΔRTP=1.489cPMZ+147.2,相关系数为0.999。检出限(3σ)为0.553 μmol/L。与已有方法相比(表1),本方法建立在pH 7.4的中性环境中,灵敏度较高、简便快速、成本低。
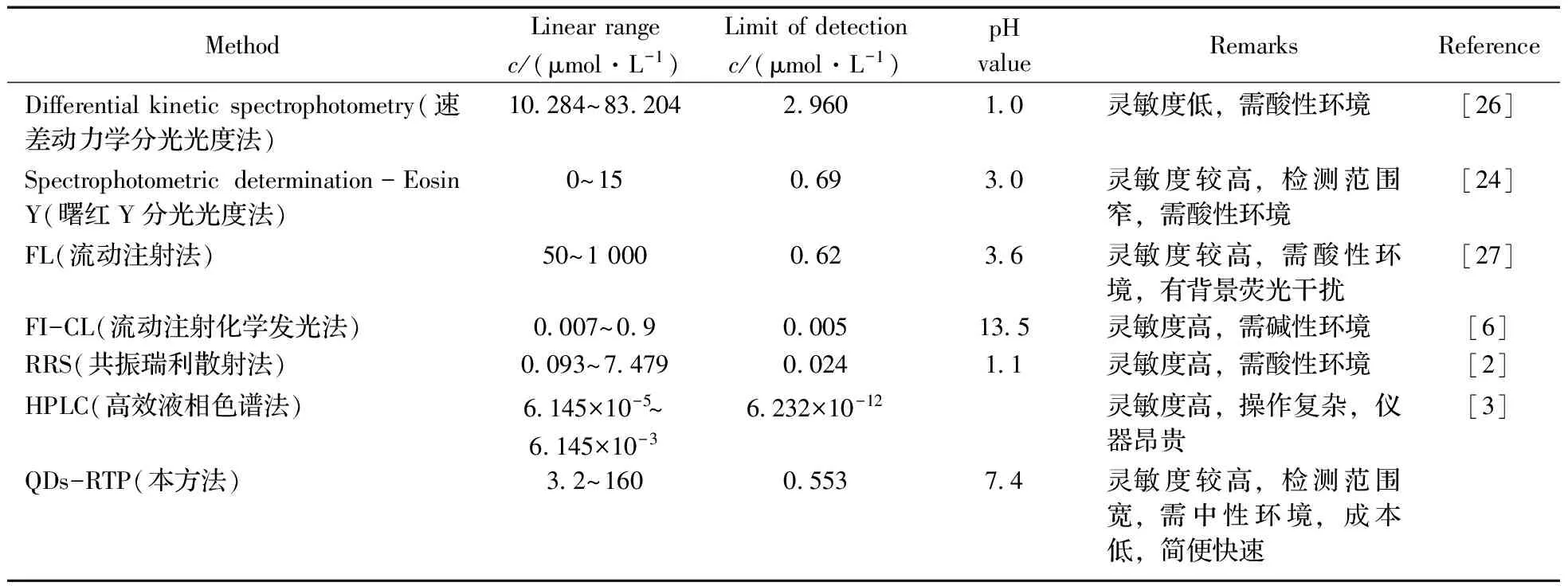
表1 测定PMZ方法的比较
2.6 共存物质的干扰
在优化实验条件下,考察了人体液中常见共存物质对PMZ检测体系的干扰。结果显示,当PMZ的浓度为48 μmol/L 时,100倍的Cl-和Na+,50倍的K+,Ca2+,葡萄糖、蔗糖,20倍的L-谷氨酸、L-赖氨酸、L-脯氨酸、L-丙氨酸、甘氨酸、酪氨酸对PMZ检测体系的磷光强度几乎无干扰(误差均不超过±5.0%)。这表明利用MPA包裹的 ZnS∶Mn 量子点的室温磷光检测PMZ具有很高的选择性。

图6 人尿液( 1,3)、血清(2,4)的磷光和荧光光谱图Fig.6 RTP and FL spectra of human urine( 1,3) and serum(2,4)1,2:RTP spectra;3,4:FL spectra
2.7 实际样品的测定
为考察利用MPA包裹的 ZnS∶Mn 量子点的室温磷光检测PMZ的可行性,本实验采用加标回收法检测健康人血清和尿液中的PMZ。图6显示,人血清和尿液有很强的背景荧光,却无背景磷光。因此,利用MPA包裹的 ZnS∶Mn 量子点的室温磷光检测PMZ能有效避免人血清和尿液自体荧光的干扰。该方法只需将待测液稀释,无需其他预处理。将人血清和尿液用高纯水稀释100倍后,进行3个浓度(8,48,144 μmol/L)水平的加标回收实验,测得加标回收率为96.4%~103.1%,相对标准偏差为0.6%~3.9%。方法的准确度可满足实际样品的检测需要。
3 结 论
本文以三巯基丙酸(MPA)为表面修饰剂,采用水相合成法制备了稳定且具有良好光学性质的 ZnS∶Mn 量子点,建立了一种检测PMZ的新方法。该方法与速差动力学、曙红Y、荧光等分光光度法相比,检测范围宽、灵敏度高,并且避免了自身荧光的干扰;与HPLC法相比,成本低、简便快速。此外,其他方法大都在酸性环境中进行检测,而该方法在pH 7.4的中性环境中进行。因此,MPA包裹的Mn掺杂ZnS量子点的室温磷光能有效应用于人体液中PMZ的检测。
[1] Lynch K L,Shapiro B J,Coffa D,Novak S P,Kral A H.DrugAlcoholDepend.,2015,150:92-97.
[2] Zhang S R,Yang J D.J.Instrum.Anal.(张书然,杨季冬.分析测试学报),2009,28(12):1362-1367.
[3] Pei Y M.Chin.Tradit.HerbalDrugs.(裴月梅.中草药),2014,45(23):3414-3417.
[4] Huang M,Gao J Y,Zhai Z G,Liang Q L,Wang Y M,Bai Y Q,Luo G A.J.Pharm.Biomed.Anal.,2012,62(2):119-128.
[5] Pan Z H,Chen L H,Han Y J.Chin.J.Anal.Lab.(潘自红,陈丽华,韩永军.分析试验室),2010,29(2):115-117.
[6] Zhao Z R,Kong D,Liu Y M.Chem.Res.(赵峥嵘,孔丹,刘彦明.化学研究),2015,26(2):175-178.
[7] Chen P L,Liu S P,Liu Z F,Hu X L.Chin.J.Anal.Chem.(陈佩丽,刘绍璞,刘忠芳,胡小莉.分析化学),2010,38(7):1007-1010.
[8] Chen Y H,Hao E J,Ye C L,Feng S L,Cui F L.Chin.J.Anal.Lab.(陈粤华,郝二军,叶存玲,冯素玲,崔凤灵.分析试验室),2012,31(4):1-3.
[9] Lai Y F,Hu J,Lin L L,Zhang Q G.Chin.Hosp.Pharm.J.(赖源发,胡佳,林丽丽,张启国.中国医院药学杂志),2015,35(7):612-615.
[10] He L L,Wang X,Liu B,Wang J,Sun Y G,Gao E J,Xu S K.J.Lumin.,2011,131(2):285-290.
[11] Marco J P,Borges K B,Tarley C R T,Ribeiro E S,Pereira A C.Sens.ActuatorsB,2013,177(1):251-259.
[12] Pereira P F,Marra M C,Cunha R R,Silva W P D,Munoz R A A,Richter E M.J.Electroanal.Chem.,2014,713(3):32-38.
[13] Yuan X Y,Wang T L,Guan T T,Wang J L,Huang H W,Yi S J,Tang C R,Zeng Y L.J.Instrum.Anal.(元晓云,王天伦,关婷婷,王金龙,黄昊文,易守军,唐春然,曾云龙.分析测试学报),2015,34(4):463-467.
[14] Mao Y Q,Li Z R,Wang J R,Ge F,Tian J X,Li N.J.Instrum.Anal.(毛永强,李卓然,王继仁,葛飞,田金星,李娜.分析测试学报),2015,34(1):96-100.
[15] Zhao Y C,Wei S Z,Tian J N,Zhao S L.J.Instrum.Anal.(赵彦春,韦盛志,田建袅,赵书林.分析测试学报),2009,28(6):655-660.
[16] Wang H F,He Y,Ji T R,Yan X P.Anal.Chem.,2009,81(81):1615-1621.
[17] Wei X,Zhou Z P,Dai J D,Hao T F,Li H J,Xu Y P,Gao L,Pan J M,Li C X,Yan Y S.J.Lumin.,2014,155(6):298-304.
[18] Pradhan N,Goorskey D,Thessing J,Peng X G.J.Am.Chem.Soc.,2005,127(50):17586-17587.
[19] Zhang X S,Li L,Huang Q S,Zhang G F,Xu J P,Xuan R W,Wei F W.J.Optoelectronics:Laser(张晓松,李岚,黄青松,张高峰,徐建萍,宣荣卫,魏凤巍.电子:激光),2011,22(1):1-4.
[20] Zhuang J Q,Zhang X D,Wang G,Li D M,Yang W S,Li T J.J.Mater.Chem.,2003,13(7):1853-1857.
[21] Wu P,He Y,Wang H F,Yan X P.Anal.Chem.,2010,82(4):1427-1433.
[22] He Y,Wang H F,Yan X P.Chemistry,2009,15(22):5436-5440.
[23] Chung J H,Ah C S,Jang D J.J.Phys.Chem.B,2001,105(19):4128-4132.
[24] Qin Z H,Liu S P,Kong L,Jiang H.Chin.J.Anal.Chem.(秦宗会,刘绍璞,孔玲,江虹.分析化学),2003,31(6):702-705.
[25] Yu Z S,Ma X Y,Zhang Q,Yu B.J.Instrum.Anal.(俞樟森,马锡英,张琪,余斌.分析测试学报),2011,30(7):789-794.
[26] Ni Y N,Qi Z B.Spectrosc.SpectralAnal.(倪永年,齐正保.光谱学与光谱分析),2006,26(7):1364-1367.
[27] Gao P F,Zeng G M,Niu C G.Chem.Sens.(高攀峰,曾光明,牛承岗.化学传感器),2006,26(1):49-53.
Detection of Promethazine Based on the Room Temperature Phosphorescence of MPA-capped Mn-doped ZnS Quantum Dots
XU Mei,LI Dong-xia,YAN Gui-qin*
(College of Life Science,Shanxi Normal University,Linfen 041000,China)
Using 3-mercaptopropionic acid(MPA) as surface modifiers,Mn doped ZnS quantum dots with stable and good optical properties were synthesized via water phase method.In phosphate-buffered saline solution,the addition of promethazine could obviously quench the room temperature phosphorescence of MPA-capped Mn-doped ZnS quantum dots.Thus,a new method for the detection of promethazine was established.The quenched phosphorescence intensity(ΔRTP) was linearly proportional to concentration of promethazine.The linear ranges of promethazine were 3.2-32 μmol/L and 32-160 μmol/L,with correlation coefficients of 0.998 and 0.999,respectively.The limit of detection for the method was 0.553 μmol/L.This method was used to detect promethazine in human serum and urine samples with satisfactory results,and the recoveries ranged from 96.4%to 103.1%.
MPA-capped Mn-doped ZnS;quantum dots(QDs);room temperature phosphorescence(RTP);promethazine(PMZ)
2016-04-07;
2016-05-01
国家教育部博士点联合基金项目(20111404110002);国家自然科学基金项目(31272258);山西省重点化学优势学科建设项目(912019)
10.3969/j.issn.1004-4957.2016.10.014
O657.3;TQ460.72
A
1004-4957(2016)10-1301-05
*通讯作者:闫桂琴,教授,研究方向:植物分子生物学及生物分子化学,Tel:0357-2051867,E-mail:gqyan2013@163.com

