人类白细胞抗原基因HLA—B58∶01基因型的快速低成本鉴别方法
初亚男 张婕妤 封利颖 周国华

摘要:采用焦磷酸测序技术和改进的全血基因组提取方法,建立了位于6号染色体的银屑病易感基因1候选基因1(Psoriasis susceptibility 1 candidate 1,PSORS1C1)rs9263726位点的焦磷酸测序方法,检出限达到0.4 ng/μL基因组DNA,20例标本的焦磷酸法和Sanger法测序结果完全一致。利用本方法对683例标本的rs9263726位点进行测序,得到中国人群该位点野生型(GG型)分布频率为87.6%,突变的GA型分布频率为11.7%、AA型分布频率为0.7%。通过对随机选取的46例标本rs9263726位点与人类白细胞抗原基因HLAB*58∶01基因型的连锁关系进行分析,结果表明,该位点预测HLAB*58∶01基因型的灵敏度为100%、特异性为91.3%。本方法可用于HLAB*58∶01基因型的检测。
关键词 :人类白细胞抗原基因HLAB*58∶01; 焦磷酸测序; rs9263726位点; 基因型
1 引 言
别嘌呤醇被广泛应用于临床高尿酸血症的常规治疗,但是其皮肤型不良反应在用药前无法预知,特别需要注意的是,发生不良反应的人群中约有1%~5%为StevensJohnson综合征(SJS,皮肤脱落小于体表面积的10%,死亡率为1%~5%),20%~30%为中毒性表皮坏死松解征(TEN,皮肤脱落大于体表面积30%, 死亡率25%~35%)[1,2],急剧增加了患者的死亡风险。2005年, Hung等[3]发现,由于别嘌呤醇引发SJS/TEN的51位中国汉族人,全部含有人白细胞抗原基因HLAB*58∶01;2009年,Tassaneeyakul等对泰国人别嘌呤醇致敏的分析发现,HLAB*58∶01等位基因预测别嘌呤醇诱发的SJS/TEN过敏的灵敏度(含有HLAB*58∶01等位基因的标本正确判定此标本会发生别嘌呤醇誘发的SJS/TEN过敏反应的比例)为100%,特异性(不含有HLAB*58∶01等位基因的标本正确判定此标本不会发生别嘌呤醇诱发的SJS/TEN过敏反应的比例)为87%[4]。据最新dbMHC等位基因频率数据库统计,HLAB*58∶01等位基因的携带频率欧洲为0.77%,北美洲为0.38%,大洋洲为2.5%,东北亚为6.1%,在世界不同地区人群中的携带频率有显著的差异。2010年国际组织相容性工作组报道华人携带率平均为8.8%~10.9%,远高于东北亚分布水平,因此中国汉族人群属于别嘌呤醇引发SJS/TEN的高风险群体。
HLA目前的分型方法主要有3类:血清学、细胞学和分子生物学分型法。其中血清学和细胞学分型法,由于高特异性的抗体和特异的细胞获取困难,且操作繁琐,因此目前很少使用。分子生物学分型方法主要有聚合酶链反应等位基因组特异性引物(PCRSSP)[5]、多聚酶链反应序列特异寡核苷酸探针(PCRSSOP)[6]、聚合酶反应直接测序法(PCRSBT)[7]。前两种方法属于低分辨HLA分型方法,容易产生假阳性;PCRSBT可以直接对HLA基因型的序列进行测定,分辨率高,能直接发现新的等位基因,但是由于杂合子的存在,需将同源染色体分离后才能得到各个单元型的准确结果,增加了操作的复杂性,检测成本也相应增高[8]。
2013年,Tohkin等[9]对日本14个别嘌呤醇诱发的SJS/TEN过敏人和991个正常健康人的全基因组关联研究分析表明,位于6号染色体的银屑病易感基因1候选基因1(Psoriasis Susceptibility1 Candidate1,PSORS1C1)上的rs9263726位点,存在G>A的多态性改变,该位点突变型A与HLAB*58∶01存在完全的等位基因关联。因此,如能证实中国汉族人群存在同样的等位基因关联,采用rs9263726位点代替HLA基因直接测序,进行别嘌呤醇用药前HLAB*58∶01高致敏基因型的筛查,可以有效降低SJS/TEN致死性皮肤性过敏发生的风险并节约成本。
焦磷酸测序技术具有操作简便、灵敏度高、无需荧光标记等技术优势[10~12],本研究选用焦磷酸测序技术建立了rs9263726位点的多态性分析方法。随机选择了683例库存核酸标本,进行了rs9263726位点多态性分型,首次得到中国人群该位点的基因频率。同时,对46例标本进行了HLAB基因的PCRSBT直接测序和rs9263726位点多态性分析,对两种方法的结果进行了比较。
2 实验部分
2.1 仪器与试剂
Q24焦磷酸测序仪(德国Qiagen公司);A200基因扩增仪(杭州朗基科学仪器有限公司);微量紫外分光光度计(南京伍义科技有限公司);VORTEXGENIE 2涡漩混匀器(美国Scientific Industries基因公司);Legand Micro 21R冷冻离心机(美国Thermo公司),BG200恒温混匀仪(杭州朗基科学仪器有限公司)。
PCR扩增体系试剂盒(日本Takara公司);全血基因组提取试剂盒(美国Promega公司);焦磷酸测序试剂盒及退火和结合缓冲液(德国Qiagen公司);其它试剂均为分析纯;实验用水为灭菌蒸馏水。
所有引物由上海Invitrogen公司合成,具体引物名称及序列见表1。
2.2 实验方法
2.2.1 改进的基因组DNA提取方法 本研究采用经过改进的Wizard Genomic DNA Purification Kit提取法,提取基因组核酸,具体步骤如下:首先将175 μL抗凝全血和450 μL Cell Lysis Solution 混合,室温放置6 min,13000 g离心20 s,弃上清液,保留底部沉淀和约20 μL上清液,涡旋至底部沉淀均匀分散至上清液中;加入180 μL Nuclei Lysis溶液,用移液器吹打混合均匀,36 ℃孵育5 min;降至室温后加入70 μL Protein Precipitation溶液,涡旋振荡30 s,13000 g离心5 min;上清液转管至300 μL异丙醇中,沉淀核酸,13000 g离心1 min;弃上清液后加入200 μL 70%乙醇洗涤沉淀,除去乙醇后晾干沉淀,加入80 μL DNA Rehydration Solution即得到基因组DNA溶液。
2.2.3 焦磷酸测序引物设计 扩增引物使用Primer 5.0软件进行设计,测序引物使用Qiagen公司的Assay Design Software 2.0软件设计。
2.2.4 PCR扩增 PCR反应体系体积为50 μL,包括dNTP 200 μmol/L,10×PCR Buffer 5 μL,MgCl2 1.5 mmol/L,Taq酶1.25 U,上下游引物0.4 μmol/L,基因组DNA 2.5 μL。PCR反应条件:94℃,5 min;94 ℃,30 s;55 ℃,30 s;72 ℃,30 s;35个循环;72 ℃,7 min。
2.2.5 焦磷酸测序 取20 μL PCR扩增产物和2 μL亲和素修饰的微球,与18 μL蒸馏水、40 μL结合缓冲液混合,振荡孵育7 min,使用单链制备模块制备测序需要的单链,加入含有10 μmol/L测序引物和24 μL退火缓冲液的24孔板中,85 ℃解链1 min,室温退火,放入焦磷酸测序仪中固定。设置测序推注顺序为“CAAGGT”,其中“C”为rs9263726位点前的一个参比碱基,同理碱基“T”为其后的参比碱基,第一个“A”为rs9263726位点的突变型信号峰,第二个“A”可获知A碱基的测序本底,同理G碱基为野生型信号峰。在焦磷酸测序仪的试剂仓中依次加入4种碱基A、C、G、T,测序底物(S)和酶(E),运行程序10 min后得到相应测序图谱。
3 结果与讨论
3.1 改进的基因组DNA提取方法
通过降低抗凝全血用量、缩短离心和孵育时间等步骤,对Wizard Genomic DNA Purification Kit法进行了改进,改进后仅需175 μL DETA抗凝全血就可以得到大于3 μg的基因组核酸,所需血量比原有方法减少了40%,提取时间减少了30%。得到基因组DNA浓度范围在50~100 ng/μL,A260/A280为1.8~2.0,能满足后续焦磷酸测序的需要。
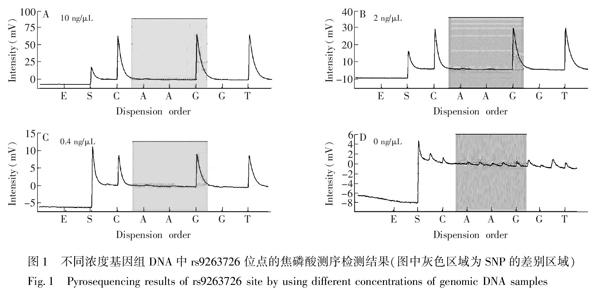
3.2 基因组DNA样本浓度对焦磷酸测序检测rs9263726位点的影响
设置3个浓度分别为10.0,2.0和0.4 ng/μL以及空白的人基因组DNA样品,考察建立的rs9263726位点测序方法,选择A260/A280比值在1.8~2.0之间、初始浓度约为50 ng/μL的人基因组DNA用蒸馏水进行梯度稀释。每个梯度平行扩增3管,以焦磷酸测序是否获得预期的信号峰来评判本方法中基因组DNA浓度对rs9263726位点的影响,结果如图1所示,图中灰色区域为SNP的判别区域,第一个“A”出现信号峰代表突变型信号,“G”出现信号峰代表野生型信号,可见本方法可检测浓度低至0.4 ng/μL的人基因组DNA模板样品。
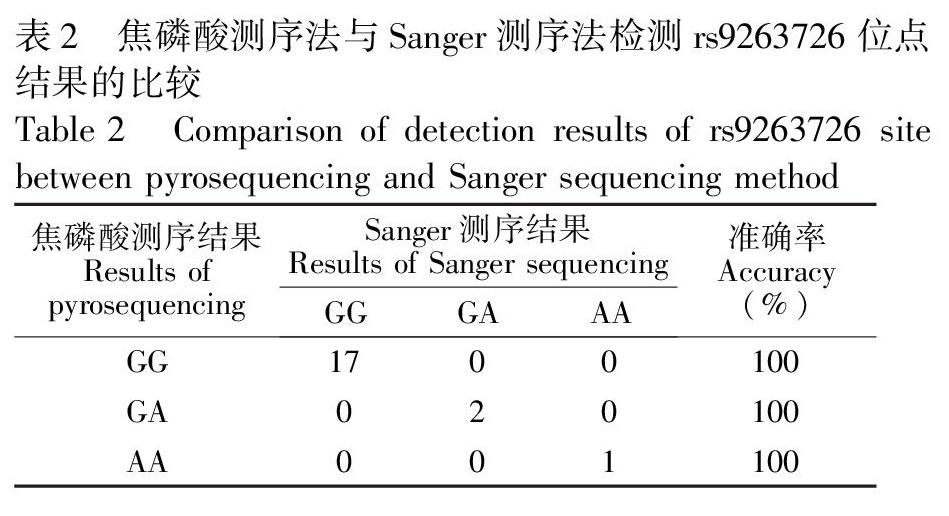
3.3 焦磷酸测序检测rs9263726位点的准确率
选择20例库存人基因组DNA标本,每个标本平行扩增2份,一份用焦磷酸测序方法进行检测,一份用Sanger测序方法检测,检测结果见表2,焦磷酸测序方法对rs9263726位点测序结果准确率为100%。
3.4 rs9263726位点在中国人群中基因分布频率
目前,还未见中国人群中rs9263726位点基因分布频率的相关文献报道,因此研究该位点在中国人群中的分布频率十分必要。本研究选择2013年7月~2014年7月期间本实验室核酸标本库中的683例人基因组核酸标本,进行rs9263726位点的测序分析,683例标本检出野生纯合型(GG型)标本598例,突变杂合型(GA型)标本80例,突变纯合型(AA型)标本5例。上述结果表明,rs9263726位点野生型分布频率为87.6%,突变杂合型分布频率为11.7%,突变纯合型分布频率为0.7%,突变型的总分布频率为12.4%。
3.5 rs9263726位点表征HLAB*58∶01基因型的特异性评价
虽然日本的研究者已经评价了日本人群中rs9263726位点与HLAB*58∶01基因型存在完全的等位基因关联,但是还未见表征该位点在中国人群中是否也具有类似的关联关系的报道,所以本研究随机选择了21例rs9263726位点检测结果为野生型、25例检测结果为突变型的标本送华大基因采用PCRSBT的方法进行HLAB分型。46例随机选择的标本验证结果表明,rs9263726位点表征HLAB*58∶01基因型的灵敏度(采用焦磷酸测序检测rs9263726位点正确判定检测标本含有HLAB*58∶01基因型的比例)达到100%,特异性(采用焦磷酸测序检测rs9263726位点正确判定检测标本不含有HLAB*58∶01基因型的比例)为91.3%。
4 结 论
rs9263726位点存在G>A的多态性改变,本研究结果表明,在中国人群中该位点突变型A与HLAB*58∶01基因型存在紧密的连锁关系,通过采用焦磷酸测序方法测定rs9263726位点的基因型,可以间接确定被检测对象是否携带有HLAB*58∶01基因型,与直接采用PCRSBT法对HLAB进行分型相比,可有效降低检测成本,节约检测时间,且无需专业的分型软件[11]。本研究表明,rs9263726位点对HLAB*58∶01基因型的检出灵敏度高达100%,特异性也达到了91.3%。这与文献[13]采用ILLumina公司的芯片对rs9262570位点检测HLAB*58∶01基因型得到的结果相近。Cao等[14]对572例中国汉族人的研究结果表明,HLAB*58∶01基因型分布频率为13.99%,这与本研究中rs9263726位点突变型的分布頻率12.4%非常接近。
采用焦磷酸测序检测rs9263726位点的基因型代替现有PCRSBT法对HLAB*58∶01的检测可节约检测时间,降低患者就医成本,避免由于携带HLAB*58∶01基因型而引发的高致死性SJS/TEN综合征的发生,具有非常广泛的临床应用价值。
References
1 Pavlos R, Mallal S, Phillips E. Pharmacogenomics, 2012, 13(11): 1285-1306
2 Kaniwa N, Saito Y. J. Hum. Genet., 2013, 58(6): 317-326
3 Hung S I, Chung W H, Liou L B, Chu C C, Lin M, Huang H P, Lin Y L, Lan J L, Yang L C, Hong H S. P. Natl. Acad. Sci. USA., 2005, 102(11): 4134-4139
4 Tassaneeyakul W, Jantararoungtong T, Chen P, Lin P Y, Tiamkao S, Khunarkornsiri U, Chucherd P, Konyoung P, Vannaprasaht S, Choonhakarn C. Pharmacogenet. Genom., 2009, 19(9): 704-709
5 Bunce M, Procter J, Welsh K. Tissue Antigens, 1999, 53(5): 498-506
6 Ng J, Nurlay C K, Baxterowe L A, Chepak M, Cappe P A, Hagland J, KaKuraya D, Manes D, Rosner G, Schmeckpaper B. Tissue Antigens, 1993, 42(5): 473-4797 Metzker M L. Genome. Res., 2005, 15(12): 1767-1776
8 XING XiaoQing, CHU YaNan, XIANG Zheng, SONG QinXin, ZHOU GuoHua. Chinese J. Anal. Chem., 2014, 42(11): 1574-1579
邢曉清, 初亚男, 项 铮, 宋沁馨, 周国华. 分析化学, 2014, 42(11): 1574-1579
9 Tohkin M, Kaniwa N, Saito Y, Sugiyama E, Kurose K, Nishikawa J, Hasegawa R, Aihara M, Matsunaga K, Abe M, Furuya H, Takahashi Y, Ikeda H,Muramatsu M, Ueta M, Sotozono C, Kinoshita S, Ikezawa Z. Pharmacogenomics J., 2013, 13(1): 60-69
10 YE Hui, LIU YunLong, ZOU BingJie, WU HaiPing, ZHOU GuoHua. Chinese J. Anal. Chem., 2013, 41(5): 744-748
叶 卉, 刘云龙, 邹秉杰, 武海萍, 周国华. 分析化学, 2013, 41(5): 744-748
11 XIANG Zheng, LIU YunLong, XING XiaoQing, CHU YaNan, ZHOU GuoHua. Chinese J. Anal. Chem., 2015, 43(1): 55-62
项 铮, 刘云龙, 邢晓清, 初亚男, 宋沁馨, 周国华. 分析化学, 2015, 43(1): 55-62
12 SONG QinXin, LIU YunLong, ZHOU GuoHua. Journal of China Pharmaceutical University, 2011, 42(6): 481-489
宋沁馨, 刘云龙, 周国华. 中国药科大学学报, 2011, 42(6): 481-489
13 Liu X, Sun J, Yu H, Chen H, Wang J, Zou H, Lu D, Xu J, Zheng S L. Pharmacogenomics J., 2015, 15(5): 467-472
14 Cao Z H, Wei Z Y, Zhu Q Y, Zhang J Y, Yang L, Qin S Y, Shao L Y, Zhang Y T, Xuan J K, Li Q L, Xu J H, Xu F, Ma L, Huang H Y, Xing Q H, Luo X Q. Pharmacogenomics, 2012, 13(10): 1193-1201
Abstract A new method for polymorphism detection of rs9263726 site on Psoriasis Susceptibility1 Candidate1(PSORS1C1) was established based on the pyrosequencing technology and the improved method of genomic DNA extraction from whole blood. The detection limit of the method was 0.4 ng/μL genomic DNA. A total of 20 samples were detected by pyrosequencing, and the results were consistent with those of Sanger sequencing. A total of 683 clinical samples were analyzed with pyrosequencing method. The polymorphism distribution of rs9263726 in Chinese populations was summarized as GG (87.6%), GA (11.7%) and AA (0.7%). 46 clinical samples were detected to analyze the relationship between rs9263726 genotype and human leukocyte antigen gene HLAB*58∶01 genotype. The results showed that the genotype of HLAB*58∶01 could be predicted by polymorphism detection of rs9263726 site sequence. The sensitivity of the proposed method was 100%, and the specificity was 91.3%. This study demonstrated a new method for HLAB*58∶01 genotyping.
Keywords Human leukocyte antigen gene HLAB*58∶01; Pyrosequencing; Rs9263726 site; Genotype

