两种化疗方案治疗小儿ALL疗效比较
张 博
两种化疗方案治疗小儿ALL疗效比较
张博
目的:探讨含左旋门冬酰胺酶与培门冬酶化疗方案治疗小儿急性淋巴细胞白血病临床疗效及安全性差异。方法:选取小儿急性淋巴细胞白血病患儿共130例,随机分为A组(65例)和B组(65例),分别给予含左旋门冬酰胺酶和培门冬酶化疗方案治疗;比较两组患儿完全缓解率,随访生存率及不良反应发生率等。结果:两组患儿完全缓解率和随访生存率比较差异无统计学意义(P>0.05);B组患儿肝功能损伤发生率显著低于A组(P<0.05)。结论:两种化疗方案治疗小儿急性淋巴细胞白血病临床疗效接近;但含培门冬酶化疗方案可有效降低小儿急性淋巴细胞白血病患儿肝功能损伤风险。
左旋门冬酰胺酶 培门冬酶 化疗 小儿 急性淋巴细胞白血病
本次研究以我院2009年2月-2013年7月收治小儿急性淋巴细胞白血病患儿共130例作为研究对象,分别给予含左旋门冬酰胺酶和培门冬酶化疗方案治疗,比较两组患儿完全缓解率,随访生存率及不良反应发生率等,探讨含左旋门冬酰胺酶与培门冬酶化疗方案治疗小儿急性淋巴细胞白血病临床疗效及安全性差异。
1 资料与方法
1.1 临床资料 研究对象选取安徽省肿瘤医院2009年2月-2013年7月收治小儿急性淋巴细胞白血病患儿共130例,均符合《血液病诊断及疗效标准》(3版)诊断标准[1],同时排除年龄>16岁及研究药物过敏者。入选患儿随机分为A组和B组,每组各65例;A组患儿中男32例,女33例,年龄2~15岁,平均年龄为(9.47±1.70)岁,其中标危型17例,中危型33例,高危型15例;B组患儿中男30例,女35例,年龄2~14岁,平均年龄为(9.41±1.68)岁,其中标危型15例,中危型34例,高危型16例。两组患儿一般资料比较差异无统计学意义(P>0.05)。
1.2 治疗方法 A组患儿采用VDLP诱导缓解方案(长春新碱+柔红霉素+左旋门冬酰胺酶+强的松);B组患儿则将左旋门冬酰胺酶改为培门冬酶,其他用法用量同A组;两组患者诱导缓解后行相同巩固强化、中间维持、延迟强化及最终维持治疗方案。
1.3 观察指标 ①参照《血液病诊断及疗效标准》(3版)[1]进行完全缓解判定,记录完全缓解例数,计算百分比;②随访2年,记录患者总生存例数和无进展生存例数,计算百分比;③记录患者不良反应发生例数,包括肝功能损伤、骨髓抑制及恶心呕吐,计算百分比。
1.4 统计学处理 本次研究数据处理软件选择SPSS16.0;统计学方法采用χ2检验,以百分比(%)表示;检验水准为α=0.05。
2 结 果
2.1 两组患儿完全缓解率比较 两组患儿完全缓解率比较差异无统计学意义(P>0.05),见表1。

表1 两组患儿完全缓解率比较
2.2 两组患儿随访生存率比较 两组患儿随访生存率比较差异无统计学意义(P>0.05),见表2。

表2 两组患儿随访生存率比较 例(%)
2.3 两组患儿不良反应发生率比较 B组患儿肝功能损伤发生率显著低于A组(P<0.05);两组患儿骨髓抑制和恶心呕吐发生率比较差异无统计学意义(P>0.05),见表3。
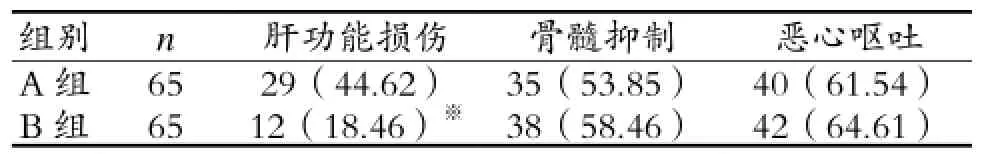
表3 两组患儿不良反应发生率比较 例(%)
3 讨 论
小儿急性淋巴细胞白血病是临床常见血液系统疾病类型之一,临床常规采用化疗方案以控制病情进展,改善临床预后[2];其中左旋门冬酰胺酶是化疗方案重要组成部分,可有效提高临床缓解率,延长无病生存时间[3];但大量研究显示,左旋门冬酰胺酶易诱发包急性胰腺炎、肝功能损伤及重度过敏反应,同时治疗过程中需保证低脂饮食亦降低治疗依从性[4]。
培门冬酶是一种由聚乙二醇与门冬酰胺酶人工合成产物,一方面其保留左旋门冬酰胺酶治疗活性,延长血药半衰期,效价约为普通左旋门冬酰胺酶4~5倍[5];另一方面显著降低药物免疫原性,对于降低过敏反应发生风险具有重要意义;已有研究证实,小儿急性淋巴细胞白血病患儿应用培门冬酶后过敏反应发生率较左旋门冬酰胺酶下降超过90%[6]。
本次研究结果中,两组患儿完全缓解率和随访生存率比较差异无统计学意义(P>0.05),提示含左旋门冬酰胺酶与培门冬酶化疗方案治疗小儿急性淋巴细胞白血病具有相似近远期疗效,均可有效控制病情进展,延长生存时间;而B组患儿肝功能损伤发生率显著低于A组(P<0.05);两组患儿骨髓抑制和恶心呕吐发生率比较差异无统计学意义(P >0.05),则证实含培门冬酶化疗方案用于小儿急性淋巴细胞白血病患儿治疗在降低肝功能损伤风险,提高用药安全性方面优势明显。
综上所述,含左旋门冬酰胺酶与培门冬酶化疗方案治疗小儿急性淋巴细胞白血病临床疗效接近;但含培门冬酶化疗方案可有效降低小儿急性淋巴细胞白血病患儿肝功能损伤风险,安全性更符合临床需要。
[1]张之南,沈悌.血液病诊断及疗效标准[M].第3版,北京∶科学出版社,2007∶132.
[2]林鸿,季迁,姜殿军,等.应用流式细胞术对123例急性白血病进行免疫表型分析[J].中国临床医生杂志,2015,43(3)∶85~86.
[3]Evans WE,Crews KR,Pui CH.A healthcare system perspective on implementing genomic medicine∶ pediatric acute lymphoblastic leukemia as a paradigm [J]. Clin Pharmacol Ther, 2013,94(2)∶224~229.
[4]苏萌,叶启东.白血病靶点治疗的研究进展[J].国际儿科学杂志,2014,41(3)∶270~273.
[5]刘芳,邹尧,张丽,等.培门冬酶治疗儿童初发急性淋巴细胞白血病的远期疗效[J].中国小儿血液与肿瘤杂志,2010,15(6)∶254~256.
[6]王岳,李学荣,仲任,等.培门冬酶和左旋门冬酰胺酶治疗儿童急性淋巴细胞白血病的疗效和安全性[J].药物不良反应杂志,2011,13(5)∶278~282.
Clinical effects comparison of two kinds of chemotherapy regimen for children with ALL
Anhui provincial hospital west tumor hospital,Hefei 230031,Anhui
ZHANG Bo
Objective:To study the amino acid containing left-handed door the enzymes and door winter chemotherapy regimen for children with acute lymphoblastic leukemia clinical efficacy and safety.Methods:The research object children with acute lymphoblastic leukemia children with a total of 130 patients treated, sinistral door winter amidase were randomly divided into group (65 cases) and Mr Dong enzyme group (65 cases), were given containing left-handed amino acid enzyme and cultivates door winter enzyme combination chemotherapy treatment;Compare two groups of children with complete remission rate, follow-up survival and incidence of adverse reactions, etc.
L-asparaginse;Pegaspargase;Chemotherapy;Children;Acutelymphoblastic leukemia
R733.71
A
1671-8054(2016)03-0051-02
(编审:刘付平 施仲赋)
安徽省肿瘤医院 合肥 230031
2016-03-26收稿,2016-05-13修回

