电位滴定法和永停滴定法的比较
巩 琪核工业二〇三研究所,陕西咸阳 712000
电位滴定法和永停滴定法的比较
巩 琪
核工业二〇三研究所,陕西咸阳 712000
在化学容量分析的过程当中,电位滴定法和永停滴定法是常用的两种滴定法,两种滴定方法都是利用电极的构建来确定滴定终点以及确定指示剂变色域的方法,但同时两种方法的电极选择是不同的,因此两种滴定方法的原理也不尽相同。目前化学容量分析已经影响到了人们生活的方方面面,多个行业领域都在日常工作中使用这两种滴定法,本文对这两种滴定法做简单介绍。
化学滴定法;电位滴定法;永停滴定法;两者比较
电位滴定法和永停滴定法主要通过选取两个适当电极来进行氧化还原法、中和法(水溶液或非水溶液)、沉淀法、重氮化法或水分测定法第一法等来进行滴定终点的确定和指示剂变色域的确定。但两种滴定法的两极选择不同——电位滴定法选用不同材料作为两极,而永停滴定法则用相同的材料(如铂电极)作为两极,两者的装置和工作原理也不同。
电位滴定法可以电位滴定仪(如图1)、酸度计或电位差计来实现,而永停滴定法则可以通过永停滴定仪或按照图2安装仪器来实现。
电位滴定法和永停滴定法的对比如表1。

表1 电位滴定法和永停滴定法的比较
1 电位滴定法
电位滴定法是将两极分别作为指示电极和参比电极,指示电极的电位会随着滴定溶液中的离子浓度变化而变化,而参比电极的电位只有在到达滴定终点时才发生突变,以此来判断滴定终点。也就是说,电位滴定法就实在滴定过程中根据电位变化来确定滴定终点的方法,当达到滴定终点时,溶液中的离子浓度会发生骤变,因此将会引起参比电极的突变(骤增或骤减),该突变点就称为突跃点。
不同的滴定类型将会影响到电位滴定法两个电极材料的选择,具体情况如表2。
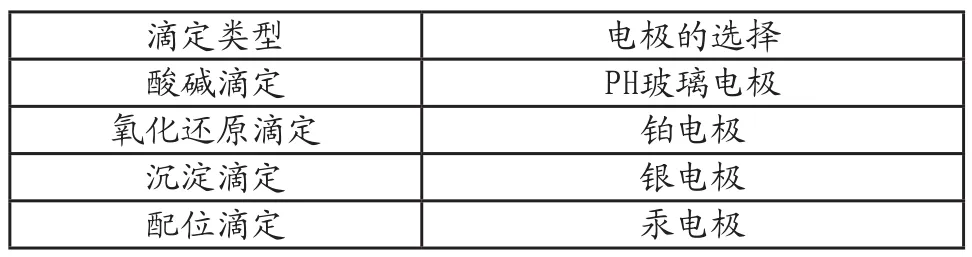
表2 电位滴定法的电极选择
电位滴定法实验过程如下:
1)将待测液体放入烧杯置于电磁搅拌器上;2)侵入电极,用电磁搅拌器进行搅拌,同时可多次加入滴定液并记录电位(开始室滴定液可大量加入);3)滴定液达到突跃点后,仍继续加入滴定液并记录电位。
电位滴定法滴定终点的确定通常有两种方法——作图法和计算法。
作图法是将电位滴定法试验过程当中记录的E(电极电位)-V(滴定液体积)分别作为纵坐标和横坐标,绘制滴定曲线,当出现突然上升或突然下降部分或拐点则达到滴定终点,将突然上升和突然下降部分的中点和拐点作为滴定终点,在图中读出坐标,以确定滴定终点时滴定液体的体积。但作图法很容易出现人为误差导致滴定终点难以保证其精确性。
计算法是将电位滴定法试验过程当中记录的E(电极电位)-V(滴定液体积)先做一级微商和二级微商,将一级微商(或二级微商)作为纵坐标,将V(滴定液体积)作为横坐标,绘制滴定曲线,其中一级微商的极值(或二级微商值等于零)时就是滴定终点。通过一级微商得到滴定终点的方法称为一阶导数法,达到滴定终点时的滴定液体积可根据达到极值时前后两个数据的平
均数来确定;通过二级微商得到滴定终点的方法称为二阶导数法,达到滴定终点时的滴定液体积可根据达到零时前后两个数据的线性内插法来确定。相较于作图法,计算法的准确性大大提高,但二阶导数法比一阶导数法计算结果更为精确,因此二阶导数法是目前最为常用的计算方法。
2 永停滴定法
永停滴定法又称死停滴定法,它的两极同为铂电极,实验过程中需要在两极之间附加一个很小的电压,通过观察滴定过程当中两个电极之间电流的变化来确定滴定终点。如果铂电极在溶液中发生极化,则在未达到滴定终点时,两个电极之间电流很小甚至可以忽略不计,但当达到滴定终点时,两个电极之间电流发生突变,电流计指针发生偏转并且不能回复。如果铂电极不能在溶液中发生极化,那么未达到滴定终点时两电极之间存在电流,在达到滴定终点后两电极之间电流为零并且不再变化。这两种情况的产生是由于溶液中存在的可逆电对和不可逆电对。
相较于电位滴定法,永停滴定法仪器装置简单,试验成本较低,同时还具有较高的准确性,因此永停滴定法在实际实验操作过程当中应用最为广泛。
3 结论
电位滴定法和永停滴定法作为常用的化学滴定法应用极其广泛,正影响着人们生活的方方面面,污水处理、环境保护、石油石化、制药工业、表面活性剂、化妆品、食品添加剂、涂料、工业溶剂、电镀材料、半导体材料等都有这两种滴定法的身影,它的出现和发展正深刻的影响着人们的衣食住行。两者从电极的设置、应用的化学原理和测量的物理量都不尽相同,根据不同的实验要求和实验条件来选择最为合适的滴定法。
[1]冯俊贤,李索娟,宋英丽,等.两点电位滴定法及其应用[J].分析化学,2002(3).
[2]俞学炜,丁荣敏.电位滴定法在在药物分析中的应用进展[J].理化检验:化学分册,2014(3):397-400.
[3]电位滴定法和永停滴定法操作规程.
O6-3
A
1674-6708(2016)168-0205-01
巩琪,核工业二〇三研究所。

