注射用曲克芦丁有效成分含量测定方法研究*
金荣富,陈 静,张 晖,梁丽丽,贺文欣,宫文武,林溪铖,薛洪宝
(1 安徽宏业药业有限公司,安徽 蚌埠 233045;2 蚌埠医学院 化学教研室,安徽 蚌埠 233030;3 安徽省蚌埠市食品药品监督管理局,安徽 蚌埠 233000)
注射用曲克芦丁有效成分含量测定方法研究*
金荣富1,陈静1,张晖2,梁丽丽2,贺文欣2,宫文武3,林溪铖3,薛洪宝2
(1 安徽宏业药业有限公司,安徽蚌埠233045;2 蚌埠医学院 化学教研室,安徽蚌埠233030;3 安徽省蚌埠市食品药品监督管理局,安徽蚌埠233000)
采用高效液相色谱法,建立药品生产企业检测中心快速、有效测定曲克芦丁注射液有效成分曲克芦丁含量的方法。条件为色谱柱:Zorbax Eclipse XDB-C18250 mm×4.6 mm, 5 μm Column (P/N 993967-902/5063-6600)填料色谱柱;柱温:室温;流动相:磷酸盐缓冲液:乙腈=80:20为流动相;流速:1 mL/min;检测波长:252 nm。该方法样品前处理简单、精密度高、准确可靠。能够满足药品生产企业对曲克芦丁含量检测要求,操作简捷易行,适合于曲克芦丁注射液的质量控制。
曲克芦丁; 高效液相色谱; 含量
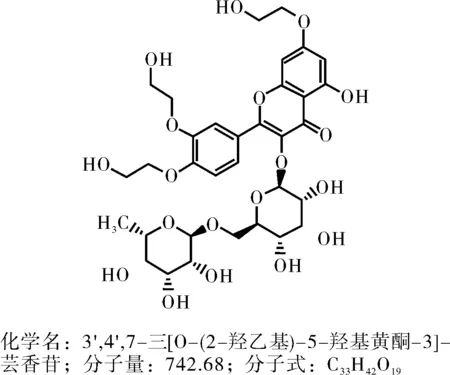
图1 曲克芦丁化学结构
曲克芦丁(Troxerutin)又名托克芦丁、三氧乙基芦丁、维脑路通、维生素P4、羟乙基芦丁等为芦丁经羟乙基化制成的半合成黄酮化合物[1],其化学结构见图 1。曲克芦丁可抑制红细胞和血小板聚集,防止血栓形成,同时能增加血中氧饱和度、改善微循环,在临床上主要用于治疗静脉障碍、血栓症、脑血管疾病、抗凝血药及溶栓药[2-3],此外,曲克芦丁还能对抗5-羟色胺、缓激肽引起的血管损伤进行修复,增加毛细血管抵抗力,降低毛细血管通透性,可防止血管通透性升高引起的水肿,对急性缺血性脑损伤有显著的保护作用等。由于芦丁分子中有4个酚羟基,其反应产物为多种羟乙基衍生物的混合物[4]。国内目前使用的曲克芦丁主要成分是7,3’,4’-三羟乙基芦丁,其它成分还包括单羟乙基芦丁、二羟乙基芦丁、三羟乙基芦丁异构体和四羟乙基芦丁等[5]。本研究拟采用高效液相色谱法测定曲克芦丁的含量,将其作为注射用曲克芦丁的质量控制方法。实验结果表明:该法精密度高、重现性好、结果准确可靠。
1 材料与方法
1.1仪器与试剂
仪器:Agilent 1260 LC System (G1312C VL型二元梯度泵,G1329B型自动控温自动进样器,G4121A/B型二极管阵列检测器),USA;FA/JA系列精密电子天平(精度:0.0001 g),天津天马衡基仪器有限公司;雷磁PHSJ-4A型酸度计 上海仪电科学仪器股份有限公司;微孔过滤器及滤膜(0.45 μm), 江苏省盐城市超宇电子科技有限公司。
试剂:曲可芦丁对照品(纯度≥98.5%),上海恒远生物科技有限公司;曲可芦丁注射液(60 mg/支),安徽宏业药业有限公司(批号:150401,150409,150421,150426);乙腈(色谱纯),江苏汉邦科技有限公司;磷酸二氢钠(分析纯);磷酸(分析纯);二次蒸馏水。
1.2相关溶液的配制
准确称取曲可芦丁对照品0.12 g(精确到0.0001 g),用流动相溶液配制成1000 mL标准溶液;分别取不同批次(4批)注射用曲克芦丁冻干粉针成品(净含量约60 mg/支)(5支/批),精确称取,用流动相溶液配制成100 mL样品溶液原液,取原液5 mL用流动相稀释至100 mL,所得样品溶液浓度约为0.1500 mg/mL;每两个批次为一组,再分别取批号为150401,150409的曲可芦丁注射液样品(2支/批),配制成两个批次的混合样品,浓度约为0.3750 mg/mL,作为曲克芦丁有关物质供试品溶液;采用同样的方法,配制两个批次的混合样品,浓度约为0.0750 mg/mL,作为曲克芦丁有关物质对照品溶液。采用同样的方法将批号为150421,150426的曲克芦丁注射液样品配成相应的溶液。将上述溶液4℃下保存,待测。样品溶液测定前使用0.45 μm滤膜过滤。
1.3实验方法
1.3.1色谱条件
色谱柱:Zorbax Eclipse XDB-C18250 mm×4.6 mm, 5 μm Column (P/N 993967-902/5063-6600)填料色谱柱;柱温:室温;流动相:磷酸盐缓冲液:乙腈=80:20为流动相(磷酸盐缓冲液为0.1 mol/L磷酸二氢钠溶液,用磷酸调节pH值至4.4);流速:1 mL/min;检测波长:252 nm。
分别取上述待测溶液20 μL,进行高效液相色谱分离分析,记录色谱图。在本实验条件下,曲克芦丁色谱峰保留时间约为5.7 min。根据外标定量法计算色谱峰面积。
1.4数据处理
试验所得数据采用Origin 7.0软件处理、统计、分析、作图。
2 结 果
2.1色谱条件的优化
2.1.1流动相的选择
由于曲克芦丁分子中含有多个酚羟基和多个邻位醇羟基(图 1),因此,化学性质具备酚和多元醇的性质,具有弱酸性。为了保证色谱分离过程中,曲克芦丁样品处于分子状态,而不是离子状态,流动相选择弱酸性流动相,采用磷酸调节pH值4.4左右。由于此化合物含多个酚羟基和多个邻位醇羟基,分子具有一定极性,流动相选择极性较大的体系,采用水:乙腈=80:20作为流动相。此流动相比例既能保证注射剂中曲克芦丁有效成分得到有效分离,又能保证保留时间尽可能短,以免保留时间过长产生纵向扩散,产生分离度降低的不利影响。
2.1.2检测波长的选择
曲克芦丁分子中有多个苯环结构(图 1),在254 nm附近具有较大紫外吸收峰。通过预实验发现高效液相色谱检测器波长设置为252 nm时,有最大紫外吸收。因此检测器波长选择252 nm。可能原因是曲克芦丁分子在水溶液中多个酚羟基产生的溶剂化作用,使检测最大波长比254 nm略有偏差。
2.2曲克芦丁的定性分析及重现性分析
分别取1.2中的曲可芦丁标准对照品溶液,连续重复5次进样,并以空白溶剂为对照。所得色谱图见图 2曲克芦丁标准对照品高效液相色谱图。曲克芦丁标准品平均保留时间约为5.728 min。对谱图进行积分,计算重现性结果见表 1。实验相对标准偏差<2.5%,表明本实验条件下精密度较高,重现性好。
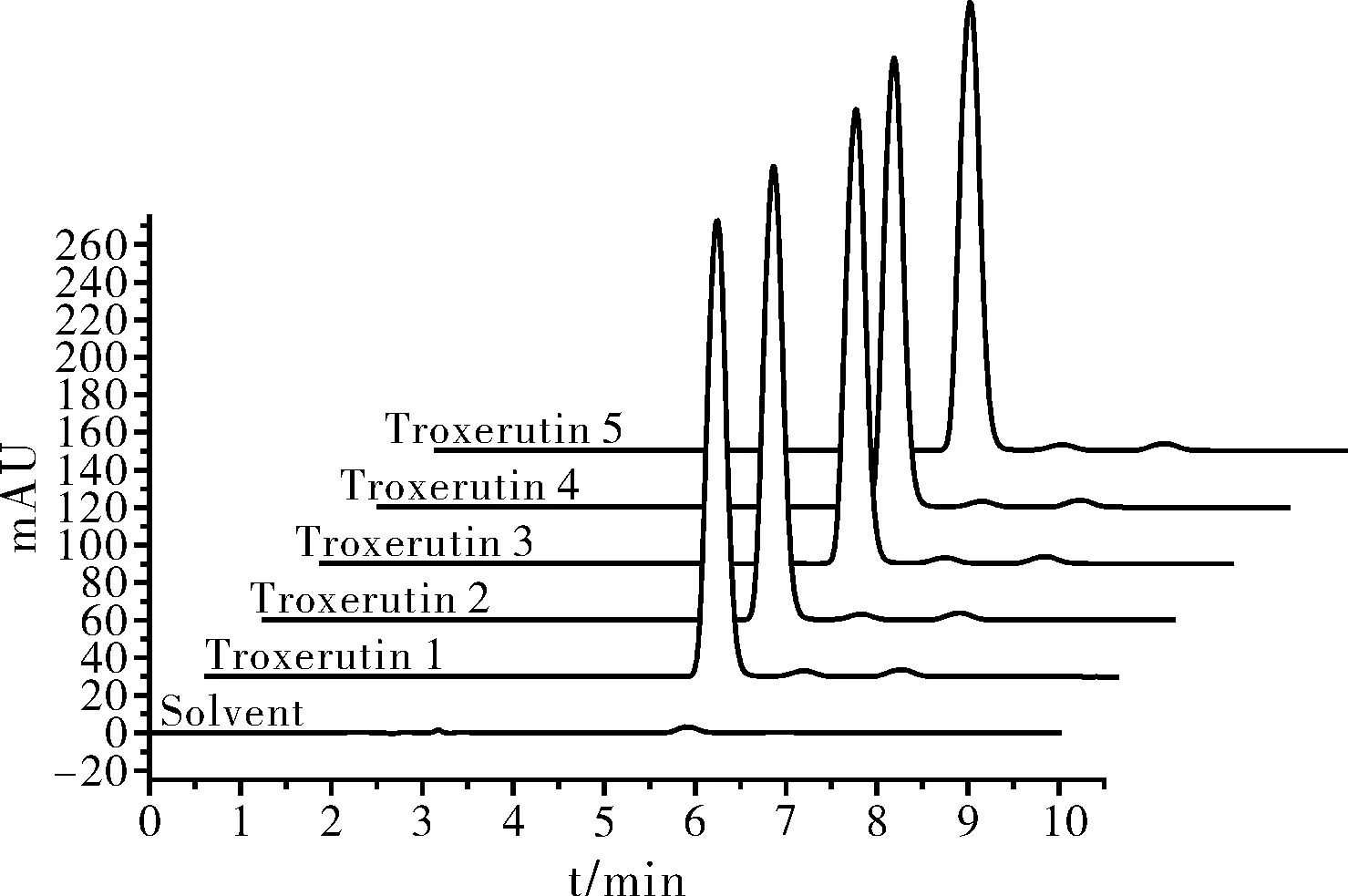
图2 曲克芦丁标准对照品高效液相色谱图(n=5)
曲克芦丁的定性分析结果和重现性试验结果满足《中华人民共和国药典》(2010版)中的定性分析实验要求,定性分析结果相对客观[6]。
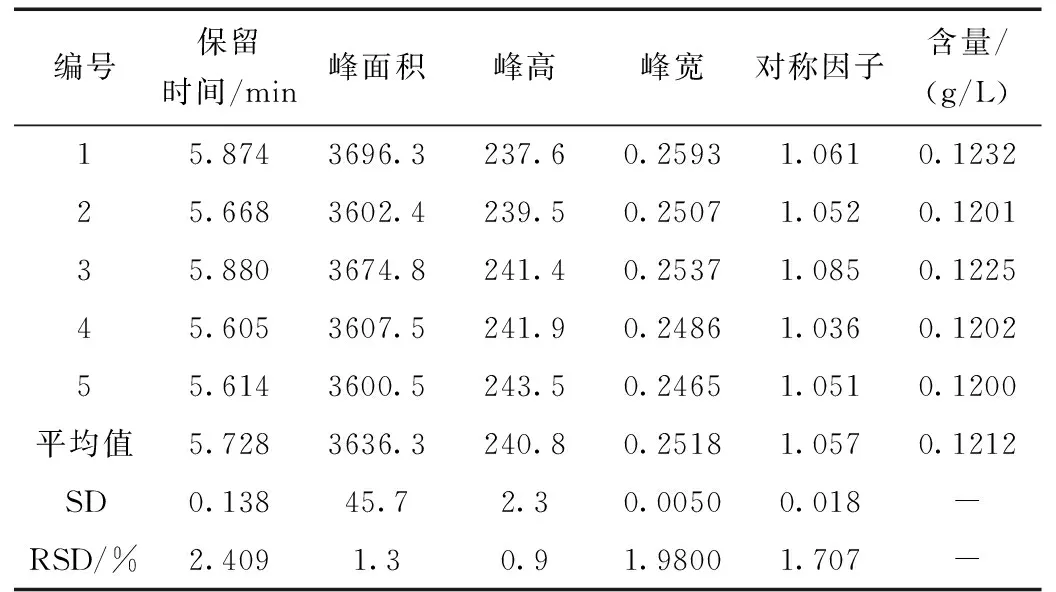
表1 曲克芦丁重现性实验结果
2.3定量分析方法的建立
分别取批号为150401,150409的曲可芦丁注射液样品,在给定的色谱条件下进样分析,每个样品重复两次,得出相应的待测样品色谱图(图 3 A, B),根据面积归一化法求出色谱峰面积。将峰面积、保留时间、峰宽对称因子等色谱峰定量信息汇总于表 2中。采用同样的方法测定批号为150401,150409的曲克芦丁有关物质对照品和曲克芦丁有关物质供试品溶液,得出色谱图定量分析信息汇总于表2中。计算出样品溶液平均值,偏差和相对标准偏差。根据测定的样品溶液曲克芦丁含量值计算出原批次中每支药效成分曲克芦丁含量。采用同样方法对批号为150421,150426的曲可芦丁注射液样品进行上述测定分析,所得实验结果汇总于表 2中。
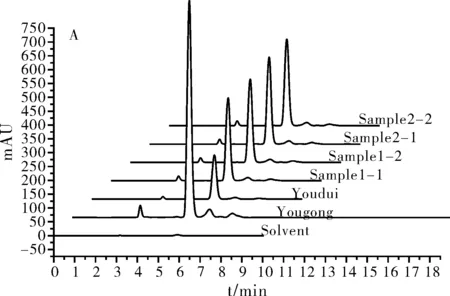
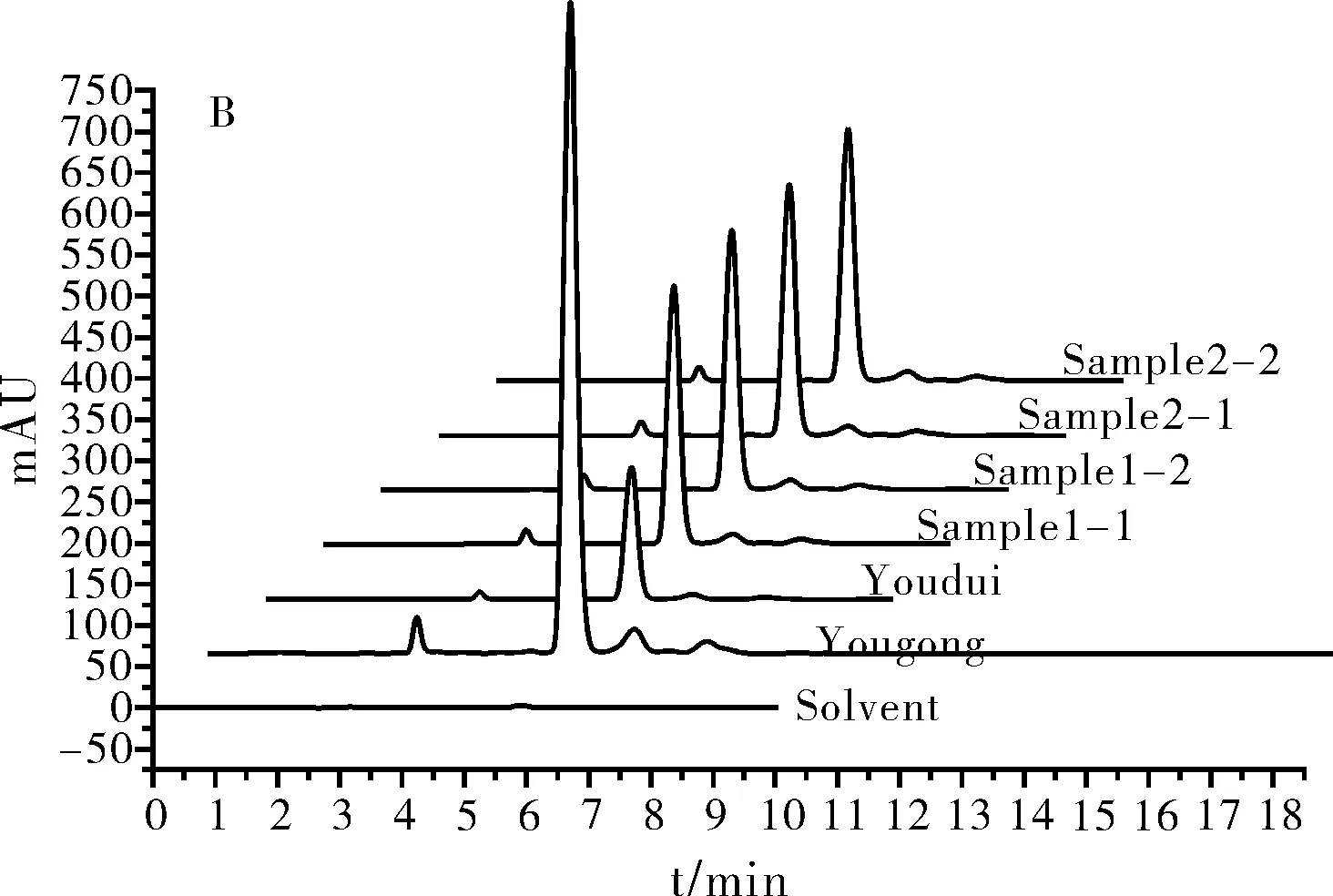
图3 曲克芦丁标准品及待测样品高效液相色谱图
曲克芦丁注射液样品有效成分测定结果表明:两个测试组中,曲克芦丁有关物质对照品和曲克芦丁有关物质供试品的保留时间与对应样品的保留时间基本接近,第一组RSD<1.1,第二组RSD<0.2.此结果验证了定性分析结果的客观性。两测试组中对应样品的色谱峰参数:峰面积、峰高、峰宽、对称因子等所产生的相对标准偏差均较小,符合定量分析实验要求。
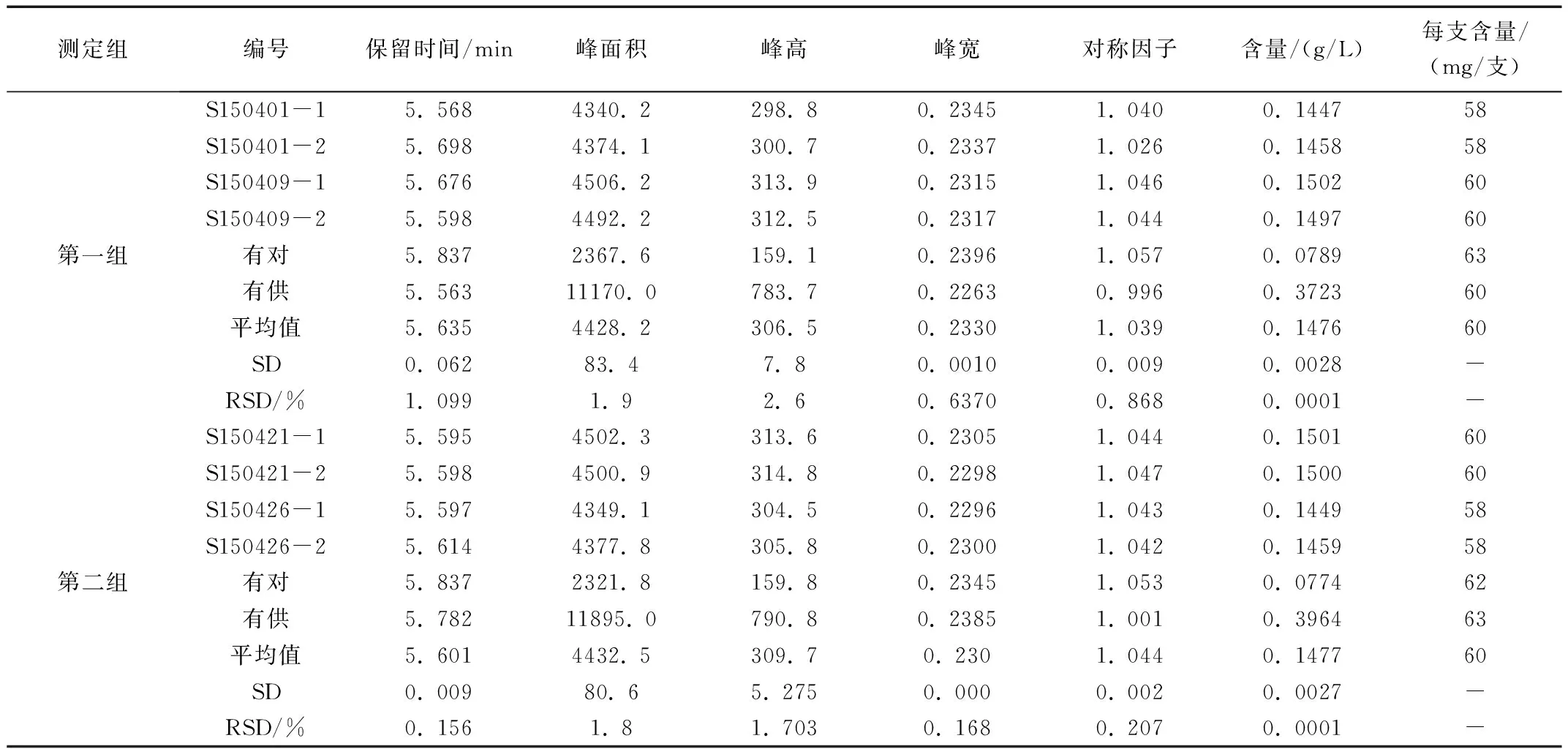
表2 曲克芦丁注射液样品有效成分测定结果
注:S150401-1表示批号,每一批号样品测定两次;有对:曲克芦丁有关物质对照品;有供:曲克芦丁有关物质供试品。
曲克芦丁注射液样品药效成分含量分析结果显示:每支注射用曲克芦丁所含药效成分曲克芦丁在(58~63) mg之间,区间范围在质量标准控制范围(60±5) mg/支之内,属于合格产品。
3 结 论
本研究建立了制药企业化验检测中心快速有效测定曲克芦丁注射液有效成分曲克芦丁含量的方法。该方法样品前处理简单、精密度高、准确可靠。能够满足药品生产企业对曲克芦丁含量检测要求,操作简捷易行,可靠性高。
[1]李正,王晓江,赵语. 反相高效液相色谱法测定血浆中曲克芦丁含量[J], 药物研究, 2009, 18(2):23-24.
[2]周昌奎,吴晓华. 曲克芦丁临床研究新进展[J]. 中国生化药物杂志, 2005, 26(5): 317-319.
[3]施洁明,陈伟盛,林玲. 梯度洗脱HPLC法测定曲克芦丁片的组分含量[J], 今日药学, 2012,22(5): 285-288.
[4]王厚全, 任慧霞, 王本杰, 等. 三羟乙基芦丁对照品的制备[J]. 中国药学杂志, 2004, 39(7): 548-549.
[5]李军,徐本明,刘珂. 曲克芦丁对照品的制备液相色谱法分离[J]. 中国医药工业杂志, 2004,35(5): 285-287.
[6]国家药典委员会. 中华人民共和国药典2010年版二部 [M], 北京:中国医药科技出版社,附录:890-891.
Determination of Active Ingredient Content in Injection Troxerutin*
JINRong-fu1,CHENJing1,ZHANGHui2,LIANGLi-li2,HEWen-xin2,GONGWen-wu3,LINXi-cheng3,XUEHong-bao2
(1 Anhui Hongye Pharmaceutical Co., Ltd., Anhui Bengbu 233045; 2 Department of Chemistry, Bengbu Medical College, Anhui Bengbu 233030; 3 Bengbu Food & Drug Administration in Anhui, Anhui Bengbu 233030, China)
The effective rapid measurement method to detect the Troxerutin active ingredient in injection Troxerutin was established based on High Performance Liquid Chromatography (HPLC). The method can be used in Laboratory Centre of the pharmaceutical production enterprises. The optimum conditions were as follows: Zorbax Eclipse XDB-C18250×4.6 mm, 5 μm Column (P/N 993967-902/5063-6600) packing column was used at room temperature, and phosphate buffer:acetonitrile=80:20 was applied as mobile phase in flow rate of 1 mL/min, and 252 nm detection wavelength were chosen by experiment. It provided a new, convenient, rapid, accurate and reliable method for the detection of Troxerutin active ingredient in injection Troxerutin. The method can be used on troxerutin quality control in the drug manufacturer.
troxerutin; HPLC; content
蚌埠市社会科学规划项目(No.BB15B016);安徽省高等学校省级优秀青年人才基金重点项目(No.2013SQRL051ZD);安徽省自然科学基金项目(No.1308085QB24);安徽省高等教育振兴计划重大教学改革研究项目(No.2015zdjy101);安徽省省级质量工程教学研究项目(No.2014jyxm211);安徽省高等教育振兴计划部分项目(No.201510367003);国家级大学生创新创业训练计划项目(No.201410367014);蚌埠医学院教学研究项目(No.jyxm1506)。
金荣富(1964-),男,安徽宏业药业有限公司质量负责人,本科,执业药师,主要从事药物生产质量控制研究工作。
薛洪宝(1979-),男,蚌埠医学院副教授,博士,硕士生导师。
R917
A
1001-9677(2016)03-0106-03

