持续口服华法林和肝素桥接对心房颤动消融术后并发症影响的Meta分析
吴慧婷,钱成,丁进叶,魏宝柱,皮阳,王扬淦
• 循证理论与实践 • 论著 •
持续口服华法林和肝素桥接对心房颤动消融术后并发症影响的Meta分析
吴慧婷1,钱成1,丁进叶1,魏宝柱1,皮阳1,王扬淦1
目的 比较持续口服华法林和肝素桥接两种不同的抗凝方案对心房颤动(房颤)消融术后并发症的影响。方法 系统检索Pubmed、The Cochrane Library、Embase、中国生物医学文献数据库(CBM)、中国知网(CNKI)及万方数据库,并查阅相关综述的参考文献,时间截至2015年6月31日,纳入满足入选标准的研究。结果 最终纳入文献共14篇,包括观察性研究13篇及随机对照试验1篇。总样本量为17 496例,其中持续华法林组7909例,肝素桥接组9587例。总体结果显示,与肝素桥接治疗相比,持续华法林治疗能减少围手术期卒中或短暂脑缺血事件(RR=0.29,95%CI:0.16~0.69,P<0.01)。在出血并发症发面,持续华法林治疗相比肝素桥接可降低大出血(RR=0.15,95%CI:0.08~0.29,P<0.01)和小出血风险(RR=0.70,95%CI:0.55~0.88,P<0.01)。结论 相比肝素桥接而言,房颤消融围手术期持续口服华法林可减少血栓栓塞事件,同时降低出血风险。
心房颤动;消融;抗凝;Meta分析
[Key words]Atrial fibrillation; Ablation; Anticoagulation; Meta-analysis
心房颤动(简称房颤)是临床上最常见的心律失常,其症状及栓塞并发症严重影响患者的生活质量。临床证据表明,导管消融术是房颤安全有效的治疗方式,尤其适用于药物疗效不佳、症状反复发作者[1]。房颤消融围手术期需充分考虑栓塞和出血风险,因此选择恰当的抗凝方案至关重要。目前临床上多采用围手术期停用华法林并加以肝素桥接(HB)的抗凝策略,然而,近几年有研究表明,导管消融围手术期持续华法林(CW)的抗凝方案相对更安全[2]。鉴于各研究的结果各异,因此有必要采用Meta分析的方法汇总相关试验结果,为房颤导管消融围手术期抗凝方案的选择提供更多的依据。
1 资料与方法
1.1纳入与排除标准 纳入研究需满足以下条件:①对比CW和HB抗凝方案对房颤导管消融围手术期并发症影响的临床试验;②样本量不少于60例;③提供以下至少一项临床终点数据,包括卒中或短暂脑缺血的复合终点、大出血事件、卒中、短暂脑缺血、小出血事件(本研究以前两者为主要终点)。排除联合其他药物抗凝的临床研究。
1.2文献检索 该Meta分析遵循PRISMA声明[3],以“atrial fibrillation”、“ablation”、 “warfarin”or“heparin”or“anticoagulation”为英文检索词检索PubMed、The Cochrane Library及Embase数据库,以“华法林”或“肝素”或“抗凝”、“心房颤动”及“消融”为中文检索词,检索中国生物医学文献数据库(CBM)、中国知网(CNKI)及万方数据库,并查阅相关综述的参考文献,时间截至2015年6月31日。
1.3数据提取与质量评价 由两位评论员独立提取数据资料,包括研究作者、年份、分组、样本量、患者基本特征(年龄、性别、阵发性房颤比例及CHADS2评分)、CW组国际标准化比值(INR)靶值、HB组低分子肝素(LMWH)剂量及随访时间等。观察性研究采用NOS评分[4]进行质量评价,大于6分者视为高质量研究;随机对照试验采用Jadad评分[5]评估方法学质量,3分以上提示质量较高。数据提取与质量评价的过程中若有分歧,则通过与第三位评论员讨论解决。
1.4统计学分析 采用STATA 12.0软件进行数据统计分析。因临床终点均为二分类变量,故以相对危险度(RR)及其95%置信区间(CI)作为效应指标。评估研究间的异质性采用χ2检验,其P <0.1考虑存在异质性。以I2值代表异质性大小,当I2<50%时,用固定效应模型合并效应量,否则用随机效应模型合并效应量,并以Meta回归方法探究异质性来源。根据导致异质性的因素、明显不同的基线特征进行亚组分析,亚组间差异采用Altman-Bland检验(Pab)[6];对主要终点进行敏感性分析,采取单次排除一个研究、排除低质量研究等两种方式。通过漏斗图直观判断是否存在发表偏倚,并采用Egger检验定量分析。当P <0.05时,认为差异具有统计学意义。
2 结果
2.1纳入研究基本信息 最初检索文献1201篇,阅读题目或摘要后,排除无关研究1035篇,重复文献108篇,动物实验15篇。进一步阅读全文后排除文献29篇,最终纳入14项临床研究[7-20],包括观察性研究13项及随机对照试验1项(图1)。总样本为1 7496例,其中7909例分布在CW组,9587例分布在HB组。患者的平均年龄范围为54~77岁,其中男性约占75.6%,阵发性房颤占47.8%。除1项研究[13]采用普通肝素外,其余研究均采用LMWH桥接抗凝。研究的随访时间为2天~12个月。观察性研究除2项外[12,14]其余NOS评分均大于6分,COMPARE随机试验Jadad评分为3分,表明纳入研究的整体质量较好(表1)。
2.2血栓栓塞事件Meta分析结果 11项研究提供了CW组和HB组卒中或短暂脑缺血事件的数据,共计患者17,054例,其中CW组7701例,HB 组9353例。研究间存在明显异质性(I2=54%,P <0.1),故采用随机效应模型合并数据。Meta分析结果显示,围手术期CW方案相比HB能减少卒中或短暂脑缺血发作事件(RR=0.29,95%CI:0.16~0.69,P<0.01;图2)。此外,对比HB方案,CW抗凝治疗还可分别降低卒中(RR=0.15,95%CI:0.08~0.29, P<0.01)和短暂脑缺血(RR=0.32,95%CI:0.12~0.80,P<0.05)的风险。
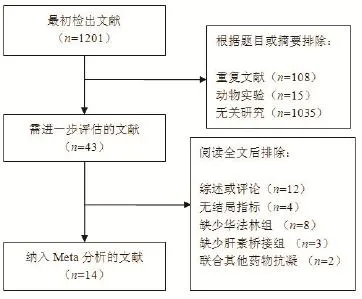
图1 文献纳入流程
2.3出血风险Meta分析结果 13项研究报道了CW组和HB组大出血的发生率,共计患者17202例,其中CW组7763例,HB组9439例。研究间无明显异质性(I2=0.2%,P=0.44),故采用固定效应模型合并数据。Meta分析结果显示,对比HB治疗,CW抗凝策略可降低房颤导管消融围手术期大出血风险(RR=0.70,95%CI:0.55~0.88,P <0.01;图3);同时,CW治疗相比HB抗凝方案也能降低小出血事件的风险(RR=0.42, 95%CI:0.24~0.74,P<0.01)。
2.4Meta回归及亚组分析 对卒中或短暂脑缺血的复合终点进行Meta回归分析,结果表明研究类型是异质性的来源(P<0.05),而样本量、平均年龄、性别、阵发性发颤比例、INR靶值、肝素桥接剂量、随访时间等均不是异质性来源。根据研究类型进行亚组分析发现,该指标在前瞻性和回顾性研究中都具有统计学意义(前瞻性:I2=43%,RR=0.12,95%CI:0.03~0.54,P <0.01;回顾性:I2=0%,RR=0.51,95%CI:0.27~0.96,P<0.05;Pab=0.07)。考虑随访时间差异较大,以3个月为界点进行亚组分析,结果表明主要终点在各亚组间无明显差异(卒中或短暂脑缺血:Pab=0.98; 大出血:Pab=0.86)。
2.5敏感性分析 单次排除一个研究后,剩余研究的合并RR值未见明显变化;排除低质量研究后,主要终点仍具有统计学意义(卒中或短暂脑缺血:RR=0.25,95%CI:0.10~0.62,P<0.01;大出血:RR=0.67,95%CI:0.53~0.85,P<0.01)。
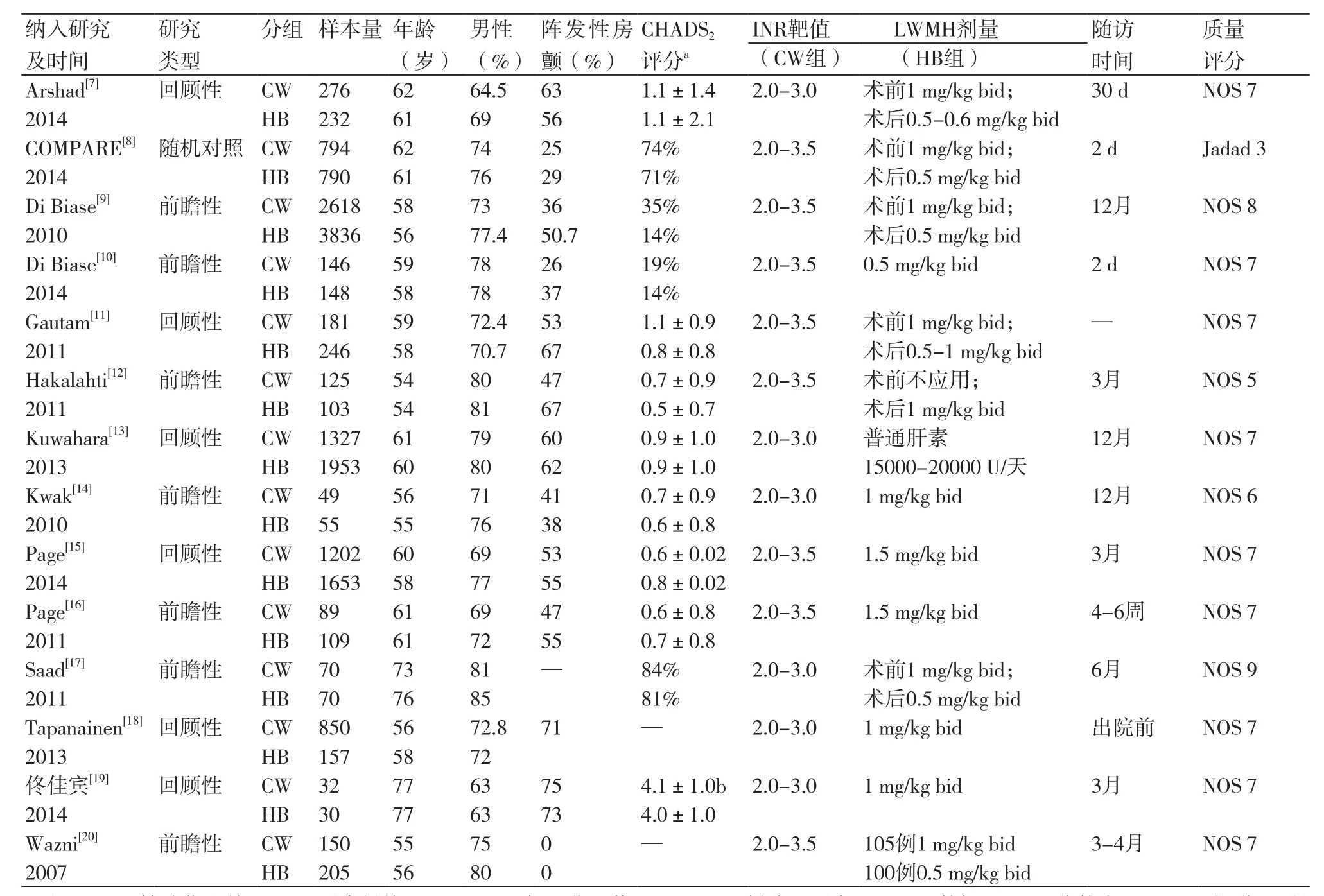
表1 纳入研究基本信息

图2 卒中或短暂脑缺血发作的森林图(CI:置信区间;CW:持续华法林;HB:肝素桥接;RR:风险比)
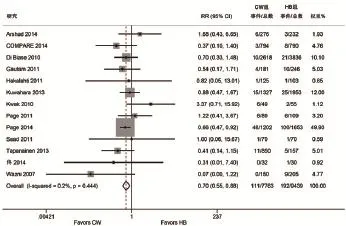
图3 大出血风险的森林图
2.6发表偏倚 因报道小出血事件、短暂脑缺血发作的研究个数较少,故未对其进行发表偏倚检测。对于卒中或短暂脑缺血发作、大出血、卒中等三个指标进行发表偏倚检测,所有漏斗图直观对称,经Egger检验表明均不存在明显的发表偏倚(卒中或短暂性脑缺血:PEgger=0.61;大出血:PEgger=0.96;卒中:PEgger=0.85)。
3 讨论
房颤导管消融围手术期抗凝方案的合理选择对预防其并发症极其重要,本研究采用Meta分析的方法对纳入的14项临床研究进行汇总分析,发现对比HB治疗,CW抗凝方案可减少围手术期卒中或短暂脑缺血事件,同时降低大出血和小出血的风险。Santangeli等[21]的Meta分析也得出类似结果,但未观察到CW治疗能降低大出血风险。其研究中纳入的部分数据是通过与大型队列研究相比较而得出的,并非原始研究直接提供。而我们的Meta分析额外纳入了多项其后进行的CW对比HB的临床试验[7,8,10,13,15,17-19],其结果更为可靠。
以下几点可能解释本研究的结果:①术前停用华法林期间肝素桥接剂量不足,易发生血栓栓塞事件;②LMWH桥接抗凝时INR常比预期高,增加潜在出血风险;③华法林恢复使用的早期存在短暂的高凝状态;④术后LMWH和华法林合用也会增加出血风险。然而,桥接治疗相对较高的大出血风险也可能导致输血或外科止血的概率增加,从而增加血栓栓塞的风险。
尽管在Meta回归分析中,我们发现研究类型是卒中或短暂脑缺血发作的研究间异质性的主要来源。但进一步亚组分析发现该终点在两类研究中均具有统计学意义,证明异质性的存在对研究结果影响较小。各研究间随访时间差异过大,但通过亚组分析发现不同的随访时间对结果并无影响。CHADS2评分可能是一潜在偏倚因素,因相关数据报道不一致,我们无法根据其进行分层分析。但仔细观察发现,CW组整体的CHADS2评分并不低于HB组。此外,通过敏感性分析也未发现单个研究或低质量研究能影响主要终点的Meta分析结果,说明该研究的结论可靠。
华法林是临床上最为常用的口服抗凝药,其半衰期长,符合导管消融围手术期的抗凝要求。口服华法林价格便宜,且避免了低分子肝素皮下注射带来的疼痛和淤血,患者依从性较高。然而,应用华法林需常监测INR值,且易受食物、药物影响,因此新型口服抗凝药如利伐沙班、达比加群酯等药可能在这方面具有一定优势。
本研究存在以下不足:①纳入的研究中绝大多数均为观察性研究,存在潜在的偏倚风险,但本研究的结果和COMPARE随机试验一致;②各研究小出血事件的定义不统一,可能会对结果造成一定的影响;③无法根据消融术式等因素进行分层分析,探究这些因素对结局的影响。
综上所述,本Meta分析结果表明:对于房颤接受导管消融的患者,围手术期采取持续华法林抗凝方案相比肝素桥接能降低血栓栓塞和出血的风险。鉴于本研究的局限性,结论仍需更多高质量的大型临床随机对照试验来证明。
[1] Wright M,Narayan SM. Ablation of atrial fibrillation[J]. Trends Cardiovasc Med,2015,25(5):409-19.
[2] Verma A,Tsang B. The use of anticoagulation during the periprocedure period of atrial fibrillation ablation[J]. Curr Opin Cardiol,2012,27(1):55 -61.
[3] Moher D,Liberati A,Tetzlaff J,et al. Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement[J]. BMJ,2009,339:b2535.
[4] Wells GA,Shea B,O'Connell D,et al. The Newcastle-Ottawa Scale (NOS)for assessing the quality of nonrandomised studies in meta-analyses[J]. 3rd Symposium on Systematic Reviews: Beyond the basics, 2000.
[5] Jadad AR,Moore RA,Carroll D,et al. Assessing the quality of reports of randomized clinical trials: is blinding necessary[J]. Control Clin Trials,1996,17(1):1-12.
[6] Altman DG,Bland JM. Interaction revisited: the difference between two estimates[J]. BMJ,2003,326(7382):219.
[7] Arshad A,Johnson CK,Mittal S,et al. Comparative safety of periablation anticoagulation strategies for atrial fibrillation: data from a large multicenter study[J]. Pacing Clin Electrophysiol, 2014,37(6):665-73.
[8] Di Biase L,Burkhardt JD,Santangeli P,et al. Periprocedural stroke and bleeding complications in patients undergoing catheter ablation of atrial fibrillation with different anticoagulation management: results from the Role of Coumadin in Preventing Thromboembolism in Atrial Fibrillation (AF) Patients Undergoing Catheter Ablation (COMPARE)randomized trial[J]. Circulation, 2014,129(25):2638-44.
[9] Di Biase L,Burkhardt JD,Mohanty P,et al. Periprocedural stroke and management of major bleeding complications in patients undergoing catheter ablation of atrial fibrillation: the impact of periprocedural therapeutic international normalized ratio[J]. Circulation,2010,121(23):2550-6.
[10] Di Biase L,Gaita F,Toso E,et al. Does periprocedural anticoagulation management of atrial fibrillation affect the prevalence of silent thromboembolic lesion detected by diffusion cerebral magnetic resonance imaging in patients undergoing radiofrequency atrial fibrillation ablation with open irrigated catheters? Results from a prospective multicenter study[J]. Heart Rhythm, 2014,11(5):791-8.
[11] Gautam S,John RM,Stevenson WG,et al. Effect of therapeutic INR on activated clotting times, heparin dosage, and bleeding risk during ablation of atrial fibrillation[J]. J Cardiovasc Electrophysiol,2011,22(3):248-54.
[12] Hakalahti A,Uusimaa P,Ylitalo K,et al. Catheter ablation of atrial fibrillation in patients with therapeutic oral anticoagulation treatment[J]. Europace, 2011,13(5):640-5.
[13] Kuwahara T,Takahashi A,Takahashi Y,et al. Prevention of periprocedural ischemic stroke and management of hemorrhagic complications in atrial fibrillation ablation under continuous warfarin administration[J]. J Cardiovasc Electrophysiol, 2013,24(5):510-5.
[14] Kwak JJ,Pak HN,Jang JK,et al. Safety and convenience of continuous warfarin strategy during the periprocedural period in patients who underwent catheter ablation of atrial fibrillation[J]. J Cardiovasc Electrophysiol, 2010,21(6):620-5.
[15] Page SP,Herring N,Hunter RJ,et al. Periprocedural stroke risk in patients undergoing catheter ablation for atrial fibrillation on uninterrupted warfarin[J]. J Cardiovasc Electrophysiol,2014,25(6):585-90.
[16] Page SP,Siddiqui MS,Finlay M,et al. Catheter ablation for atrial fibrillation on uninterrupted warfarin: can it be done without echo guidance?[J]. J Cardiovasc Electrophysiol,2011,22(3):265-70.
[17] Saad EB,Costa IP,Costa RE,et al. Safety of ablation for atrial fibrillation with therapeutic INR: comparison with transition to low-molecularweight heparin[J]. Arq Bras Cardiol,2011,97(4):289-96.
[18] Tapanainen JM,Braunschweig F,Schwieler J,et al. Continuous warfarin therapy is safe and feasible in catheter ablation of atrial fibrillation[J]. Scand Cardiovasc J, 2013,47(2):109-13.
[19] 佟佳宾,施海峰,邹彤,等. 高龄心房颤动患者导管消融围术期不同抗凝方案的对比观[J]. 中国介入心脏病学杂志, 2014,4(22):220-4.
[20] Wazni OM,Beheiry S,Fahmy T,et al. Atrial fibrillation ablation in patients with therapeutic international normalized ratio: comparison of strategies of anticoagulation management in the periprocedural period[J]. Circulation,2007,116(22):2531-4.
[21] Santangeli P,Di Biase L,Horton R,et al. Ablation of atrial fibrillation under therapeutic warfarin reduces periprocedural complications: evidence from a meta-analysis[J]. Circ Arrhythm Electrophysiol,2012,5(2):302-11.
本文编辑:张超,姚雪莉
Meta-analysis of postoperative complications effect comparison between continuous warfarin and heparin bridging after ablation of atrial fibrillation
WU Hui-ting*, QIAN Cheng, DING Jin-ye, WEI Bao-zhu, PI Yang,WANG Yang-gan.*Department of Cardiology, Zhongnan Hospital of Wuhan University, Wuhan, 430071, China.
WANG Yang-gan, E-mail: ygwang2013@163.com
Objective To compare the influence of postoperative complications after ablation of atrial fibrillation between two different anticoagulation strategies: continuous warfarin and heparin bridging. Methods Pubmed, The Cochrane Library, Embase, CBM, CNKI and Wanfang database were systematically searched for eligible studies. We also searched the references of relevant reviews for more trials. Only studies that met our pre-defined included criteria up to 31 June, 2015 were enrolled in our Meta-analysis. Results Fourteen studies,including 13 observational studies and 1 randomized controlled trial, were finally included in our study with a total of 17 496 subjects. There were 7909 patients in continuous warfarin group and 9587 patients in heparin bridging group. Compared to heparin bridging, continuous warfarin was associated with fewer stroke or transient ischemic attacks events [RR=0.29, 95%CI:(0.16,0.69), P《0.01]. For bleeding complications, continuous warfarin administration could reduce the risk of major bleeding [RR=0.15, 95%CI:(0.08, 0.29), P《0.01] and minor bleeding [RR=0.70, 95%CI:(0.55, 0.88), P《0.01]. Conclusion Compared with heparin bridging, postoperative continuous warfarin was associated with reduced risks of thromboembolism and bleeding in ablation of atrial fibrillation.
R541.75
A
1674-4055(2016)05-0520-04
1430071 武汉,武汉大学中南医院心内科
王扬淦,E-mail:ygwang2013@163.com
10.3969/j.issn.1674-4055.2016.05.03

