掺氢对生物燃气燃烧的影响研究*
李 源,李国岫,李洪萌
(北京交通大学机械与电子控制工程学院,北京 100044)
掺氢对生物燃气燃烧的影响研究*
李 源,李国岫†,李洪萌
(北京交通大学机械与电子控制工程学院,北京 100044)
为了研究掺氢对生物燃气燃烧特性的内在影响规律,本文开展了生物燃气掺氢层流燃烧的实验和CHEMKIN仿真研究。实验结果表明,当量比一定时,火焰燃烧速度随着掺氢比的增大而增大;大当量比情况下,随着掺氢比的增大,燃烧速度的增大尤为明显。仿真结果表明,掺氢后H和OH的摩尔分数变化较大。利用反应产物生成速率(ROP)分析法对掺氢燃烧过程的化学反应路径进行分析发现,由于H2浓度对基元反应O + H2= H + OH及OH + H2= H + H2O的影响显著,导致后续关键基元反应中H和OH的生成和消耗情况发生变化,特别是掺氢浓度较大时,将造成H的大量增加,同时OH也有一定增加,从而导致预混燃烧速度的显著增大。
掺氢;生物燃气;定容弹;化学反应路径;基元反应
0 引 言
能源问题是世界各国共同面临的主要问题。由于化石燃料的储藏量有限,预计到二十一世纪中叶地球上的化石燃料将被耗尽[1],届时石油替代燃料如天然气、氢气和生物质燃料等将被广泛使用。因此,很有必要从基础上研究石油替代能源的燃烧特性,其中燃烧速率和燃料的着火性能是两个重要的方面。
生物质能是仅次于煤炭、石油和天然气的第四大能源[2],生物质气化得到的生物质燃气被广泛应用于供热、发电和车用燃气等[3]。目前在生物燃气发动机的研究中,国内外均取得了很大进展[4],但相关研究尚不完善,尤其是需要有针对性地研究生物燃气燃烧速度较慢、热效率低等问题的解决措施。对于燃料燃烧质量较差这一问题,有研究表明掺氢是一项十分有效的措施[5]。李明亮[6]开展了各种工况下不同的低热值气体掺氢燃烧的层流预混实验,结果表明随着掺氢比的增大燃烧更加剧烈,燃烧的稀燃极限随之扩展。张红光等[7]开展了掺氢改善燃料燃烧过程的研究,通过定容燃烧室研究不同工况下甲烷掺氢的燃烧特性试验研究,结果表明掺氢能有效降低甲烷稀燃时的循环变动系数,实现快速稳定燃烧。程昱等[8]从化学反应动力学角度研究了掺氢对C1 ~ C4小分子碳氢燃料燃烧的影响,结果表明H2浓度影响了燃烧过程中H的生成及消耗反应,而由于反应的链式关系同时又对OH等活性基的生成及消耗反应造成了影响,从而导致燃烧速率发生改变。
综上所述,燃烧现象的研究从化学反应动力学角度更能揭示物理事实,而生物质燃气掺氢燃烧的应用迫在眉睫,但关于生物燃气掺氢燃烧的研究较少。因此本文为从化学反应动力学角度探寻掺氢对生物燃气燃烧的内在影响规律,开展了生物燃气掺氢燃烧的实验和仿真研究。
1 实验装置及仿真模型介绍
本文基于定容燃烧弹系统进行了当量比为0.7 ~1.1、掺氢比为0 ~ 0.257情况下的生物燃气的掺氢层流预混燃烧实验,并用高速摄影记录燃烧过程中火焰的发展情况,为消除火焰发展初期点火能量以及后期的压力升高而造成的影响,选取6 ~ 20 mm范围内的图片来测算火焰层流预混燃烧速度,并通过求平均值的方法来减少测量误差。实验压力为1个大气压,本文选取生物燃气的组分构成为常用的CH4∶CO = 6∶4(体积比)。实验装置示意图见图1,整套实验装置由配气系统、光路系统、定容弹燃烧系统和数据采集系统组成。
本文的仿真工作采用 CHEMKIN气相反应模拟软件完成,选用层流预混火焰速度模型进行仿真。

图1 定容燃烧弹实验系统示意图Fig. 1 Experiment system of constant volume combustion bomb
2 实验及仿真结果分析
实验结果见图2,从图中可以看出,当量比(φ)一定时火焰燃烧速度随着掺氢比(Xh)的增大而增大,由于氢气燃烧速度相对生物燃气要快得多,掺混氢气增大了混合气的活性,因而氢气的掺混使得混合气的层流预混燃烧速度加快。
从图2中还可以看出,同一掺氢比下火焰燃烧速度随着当量比的增大而增大,而大当量比情况下随着掺氢比增大,燃烧速度的增幅变大。

图2 燃烧速度随掺氢比变化的实验结果Fig. 2 Experimental burning speed versus Xh
然而实验研究只能看到宏观现象,无法进行详细的化学反应动力学过程研究,本文基于CHEMKIN[9-10]软件,采用四种机理[11-14]对生物燃气掺氢燃烧进行了不同当量比(φ)和掺氢比(Xh)情况下的仿真计算,计算结果与实验数据对比见图3。整体上看,在改变掺氢比和当量比的多种工况下,GRI机理对于实验结果的模拟在趋势和数值上更加接近。当然也存在某些工况下出现较大偏差,这是多方面的原因导致的,如实验测量误差和化学反应机理中的某些反应参数存在一些类似经验性估计的问题等。但综合来看,在一定误差范围内,GRIMech3.0的仿真结果具有较好的准确性和适用性。因此,本文采用该机理进行生物燃气掺氢燃烧的化学动力学仿真研究。
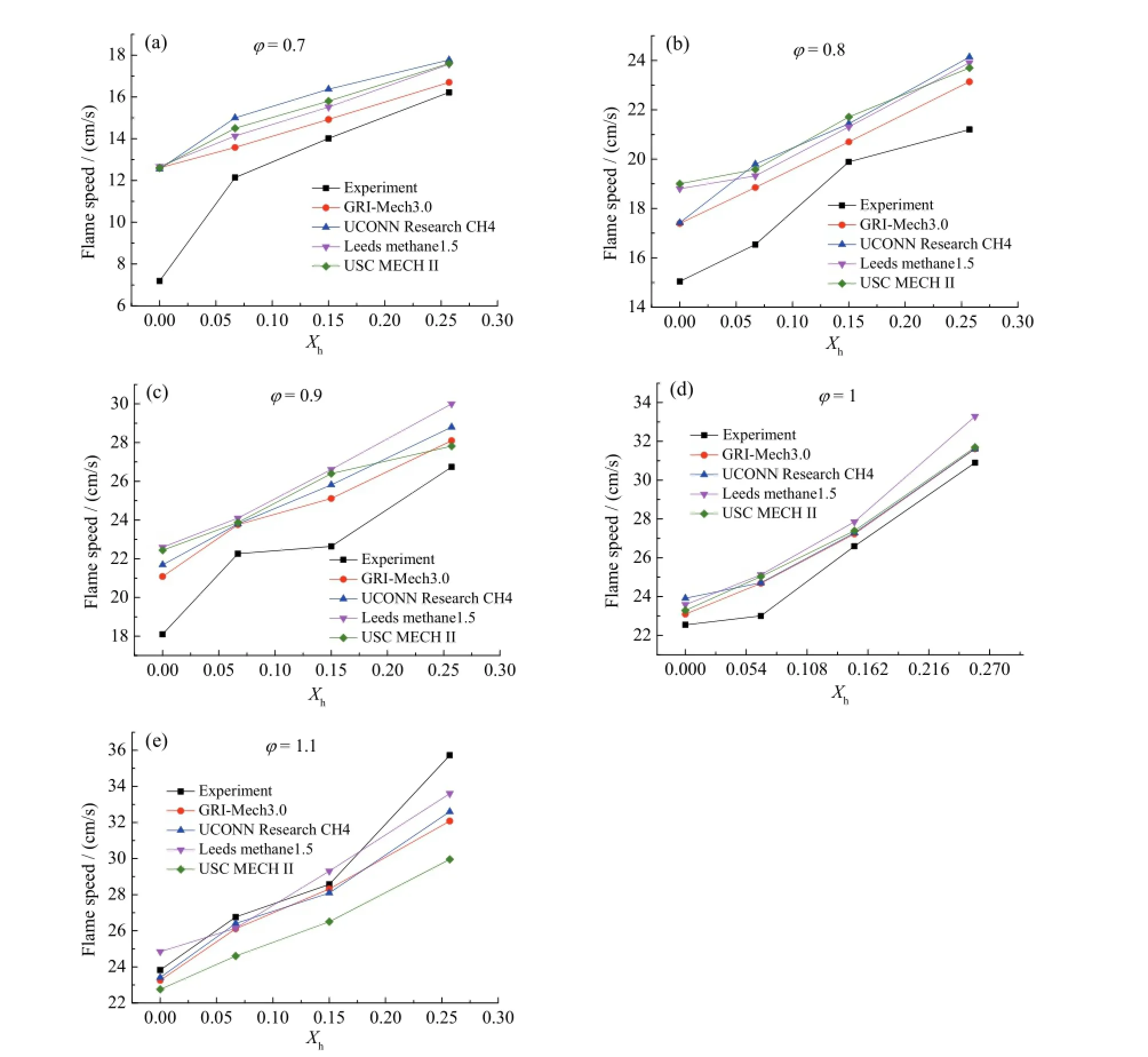
图3 燃烧速度随掺氢量变化仿真结果与实验对比Fig. 3 Comparison of experimental and calculated burning speed versus Xh
图4是当量比为1时,随着掺氢比的变化,火焰结构中关键活性组分变化情况的仿真结果。从图4a中可以看出,不掺氢生物燃气燃烧时,OH的摩尔分数峰值最大,H的摩尔分数峰值比其小很多。随着掺氢量的增大,OH的摩尔分数峰值跟着增大,而H的摩尔分数峰值增大更明显,在掺氢比为0.4时已经稍微超过OH。随着掺氢量增大,O的摩尔分数峰也略微增大,但 CH3的摩尔分数峰几乎不随掺氢量增大而发生变化。
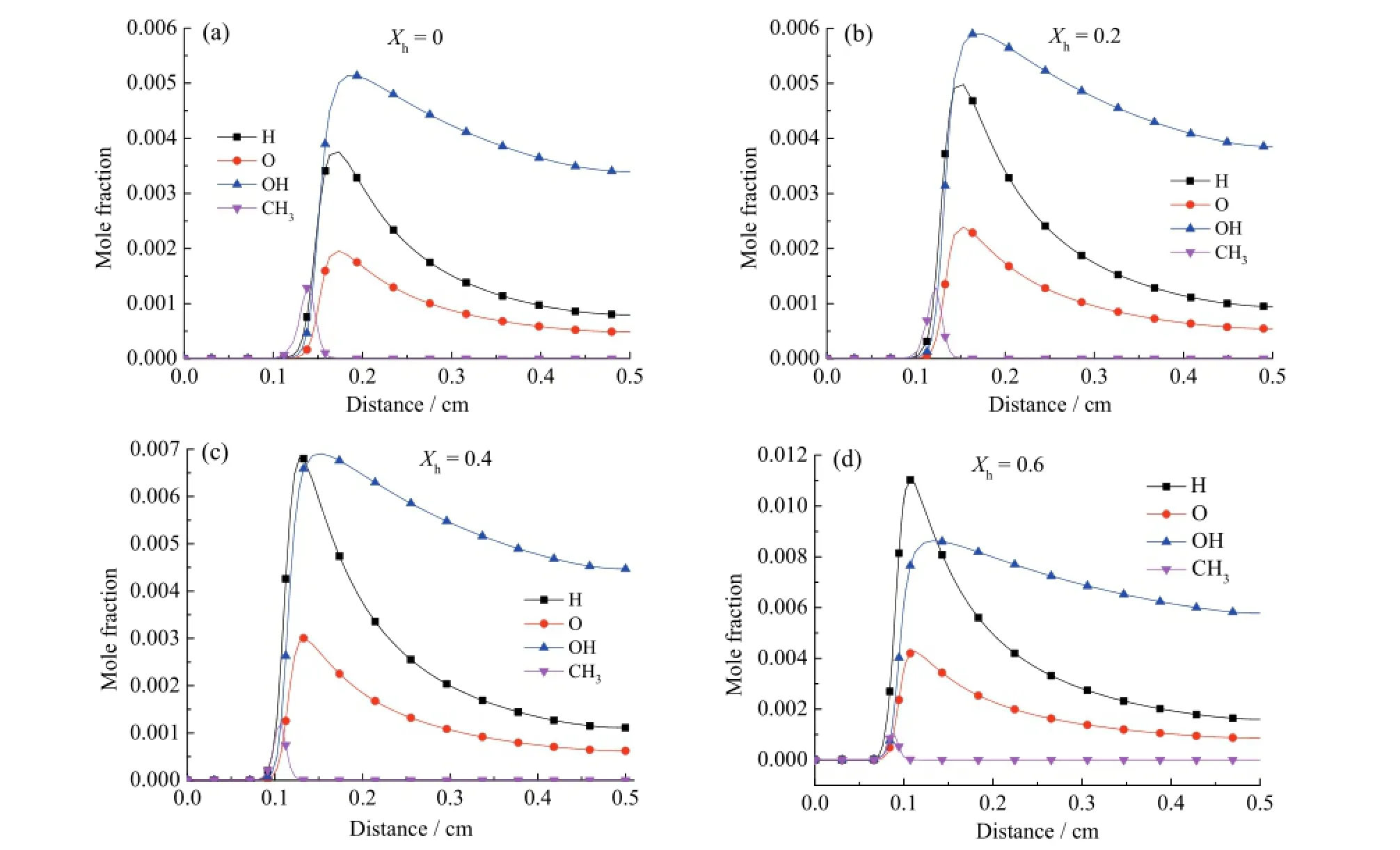
图4 火焰结构中关键活性组分的摩尔分数Fig. 4 The mole fraction of key radicals within flame structure
燃烧速度受活性基含量的影响较大,随着掺氢量增大,上述活性成分摩尔分数的改变影响了火焰的燃烧速度。而H和OH的变化量受掺氢量的影响较大,因此本文通过生成速率分析[15-17],对掺氢生物燃气燃烧过程中H和OH的化学反应路径进行研究。仿真结果表明,H和OH的主要生成及消耗基元反应如下:
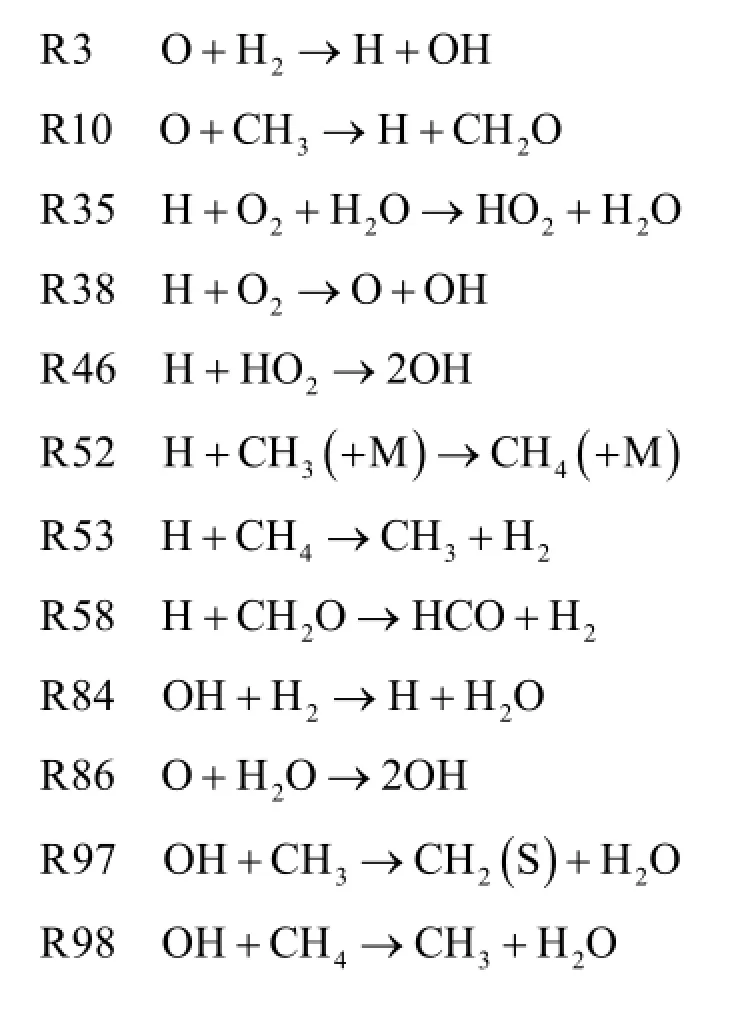
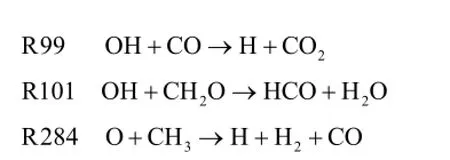
随着掺氢比的变化,主要基元反应的贡献率发生明显变化,图5是φ = 0.7时H和OH生成和消耗速率随掺氢比的变化情况。图中次纵坐标表示以纯生物燃气燃烧为基准 1,随着掺氢比的增大,H和OH总生成(或消耗)速率与基准的比值ν。因而,对某一基元反应,其贡献率与对应的次纵坐标的乘积表示该基元反应对应H和OH的生成(或消耗)速率大小。
从图5a中可以看出,R84和R99作为H的主要生成基元反应,随着掺氢量的增大,表现出相反的变化趋势。不掺氢时,作为中间生成物的CO和H2的浓度相当,而CO中C-O键比H2中H-H键能低,则 OH与CO的反应R99要比OH与H2的反应R84能垒要低,因而R99的贡献率高于R84。但是随着氢气的添加,H2浓度远高于CO浓度,结合质量作用定律可知,对于基元反应R99和R84,反应速率与反应物浓度成正比,因而随着掺氢量的增大,OH与H2的反应速率明显增大,导致R84对H生成的贡献率逐渐高于R99对H的生成贡献率。这同时解释了图5d的两个基元反应对反应物OH消耗贡献率的变化趋势。需要注意的是,虽然R99的贡献率降低,由于H总生成速率显著增大,因而随着掺氢量增大,R99对H的生成速率也在增大。
如图5b和图5c,R38 作为H消耗的最主要消耗路径以及OH的最主要生成路径,与R84互为促进,随着掺氢量增大,虽然贡献率在减小,但均加快了H的消耗及OH的生成速率。
如图5a和图5c,在H和OH主要生成基元反应中,随着掺氢量增大,受氢浓度变化影响较大的基元反应还有R3,作为R3的反应物,O和氢气浓度都随着掺氢量增大而增大,使得R3的反应速率大大增加。另外,从图中可以看出,R3对H和OH的生成贡献率不同,这是由于H和OH的总生成速率不同。
图5a显示,随着掺氢量的增加,R284对H生成的贡献率减小。从火焰结构图4中可以看出,随着掺氢量的增加,O浓度也有一定程度的增加,因而R284的正向反应速率增大,但是由于生成物中H浓度的增大,再加上H2的浓度大大增加,逆向反应的反应速率也在增大,因而R284的反应速率增加量较小,同时由于H的总生成速率的增加量较大,所以R284对H生成的贡献率减小。
如图5b,R35和R46对H消耗的贡献率随掺氢量增加而增大,这是因为R35的生成物HO2是R46的反应物, HO2的积累有利于R46反应,同时R46 对HO2的消耗会加速R35反应,这种链式关系促使H浓度增加时二者对H的消耗速率大大增加。
图5d中,R98为OH消耗的主要基元反应之一,随着掺氢量增加,OH浓度在增加,因而R98对OH的消耗速率增加,但是由于R98的反应能垒比R84 和R99高,因而对OH的消耗反应速率占比减小,导致R98对OH消耗的贡献率减小。R97和R101 对OH消耗的贡献率随掺氢量增加而减小的原因与R98类似。
综上所述,随着掺氢量增大,R84 OH + H2→H + H2O和 R38 H+O2→O+OH的反应速率明显增大,这是H和OH随掺氢量加大而大量积累的主要原因。同时,H和OH的大量积累并不仅仅是由于生成速率增大或者消耗速率减小导致,而是在生成和消耗速率均增大的情况下完成的积累,正是这种现象才导致了火焰燃烧速度的大大加快。

图5 φ = 0.7时H和OH生成和消耗的速率分析Fig. 5 Rate analysis of production and consumption for H and OH, φ = 0.7

图6 φ = 1时H和OH生成和消耗的速率分析Fig. 6 Rate analysis of production and consumption for H and OH, φ = 1

图7 φ = 1.3时H和OH生成和消耗的速率分析Fig. 7 Rate analysis of production and consumption for H and OH, φ = 1.3
图6和图7是当量比改变之后H和OH的生成速率分析结果。从图中可以看出,当量比发生变化后,随着掺氢比的增大,H和OH的总生成和消耗速率依然在增大,且当量比为 1.3时增大幅度更明显。H的最主要生成和消耗路径依旧是受H2浓度影响较大的R84和R38,OH的最主要生成和消耗路径也仍然是R38和R84。
3 结 论
本文对生物燃气掺氢燃烧过程进行了研究,得到如下结论:
(1)实验研究发现,大当量比情况下随着掺氢比增大,燃烧速度的增大尤为明显。
(2)对常用的四种甲烷燃烧机理进行CHEMKIN仿真,其结果与实验数据进行了对比,表明GRI-Mech3.0机理的仿真结果具有较好的准确性和适用性。
(3)基于GRI-Mech3.0机理进行生物燃气掺氢燃烧的化学反应路径分析,发现混合燃气层流预混火焰燃烧速度加快的原因是:随着掺氢量的增大,CH4、H2、H、OH和O等组分的浓度发生变化,从而导致主要基元反应生成及消耗H和OH的速率发生变化。但总体而言,H和OH的总生成和总消耗速率随着掺氢量的增大而增大,也正是由于H和OH的快速生成和消耗,同时导致大量的H和OH等活性基的累积,在很大程度上加快了燃烧速度。而当量比越大这种趋势越明显,因而燃烧速度增幅越大。
[1] 张勇, 黄佐华, 廖世勇, 等. 天然气/氢气燃烧特性研究[J]. 内燃机学报, 2006, 24(3): 200-205. DOI: 10.3321/j.issn:1000-0909.2006.03.002.
[2] 佚名. 生物质能源开发需要提速[J]. 农业工程技术:新能源产业, 2014(8): 14-15.
[3] 马君, 马兴元, 刘琪. 生物质能源的利用与研究进[J].安徽农业科学, 2012, 40(4): 2202-2206. DOI: 10.3969/ j.issn.0517-6611.2012.04.106.
[4] 郑士卓. 低热值气体燃料层流燃烧特性研究[D]. 北京: 北京交通大学, 2009. DOI: 10.7666/d.y1576700.
[5] 汤成龙. 氢气/气体燃料层流燃烧特性及液滴碰撞动力学基础研究[D]. 西安: 西安交通大学, 2011.
[6] 李明亮. 基于定容燃烧弹的低热值气体掺氢火焰特性研究[D]. 北京: 北京交通大学, 2015.
[7] 张红光, 白小磊, 韩雪娇, 等. 甲烷掺混氢气的燃烧特性试验研究[J]. 兵工学报, 2011, 32(2): 230-235.
[8] CHENG Y, TANG C L, HUANG Z H. Kinetic analysis of H2addition effect on the laminar flame parameters of the C1-C4 n-alkane-air mixtures: from one step overall assumption to detailed reaction mechanism[J]. International journal of hydrogen energy, 2015, 40(1): 703-718. DOI: 10.1016/j.ijhydene.2014.11.010.
[9] 翟越. 生物质燃气预混层流火焰传播特性及其不稳定性研究[D]. 北京: 北京交通大学, 2015.
[10] 李星. 甲烷在高温氧化剂中燃烧特性研究[D]. 北京:北京交通大学, 2014.
[11] WANG H, YOU X Q, JOSHI A V, et al. High-temperature combustion reaction model of H2/CO/C1-C4 compounds [EB/OL]. (2007-05). http://ignis.usc.edu/USC_Mech_II.htm.
[12] K. J. Hughes, Turányi T, A. R. Clague , et al. Development and testing of a comprehensive chemical mechanism for the oxidation of methane[J]. International Journal of Chemical Kinetics, 2001, 33(9):513-538.
[13] SMITH G P, GOLDEN D M. GRI-mech version 3.0 [EB/OL]. (1999-07-30). http://combustion.berkeley.edu/gri-mech/index.html
[14] LU T F, LAW C K. A criterion based on computational singular perturbation for the identification of quasi steady state species: a reduced mechanism for methane oxidation with NO chemistry[J]. Combustion and flame,2008, 154(4): 761-774. DOI: 10.1016/j.combustflame. 2008.04.025.
[15] 王泽鑫. CH4在O2/CO2气氛中燃烧机理的研究[D]. 沈阳: 东北大学, 2012.
[16] 谈宁馨, 王静波, 华晓筱, 等. 甲基环己烷的高温燃烧机理及动力学模拟[J]. 高等学校化学学报, 2011,32(8): 1832-1837.
[17] 张云鹏, 钟北京. 正庚烷部分预混对冲火焰中苯环的生成机理[J]. 清华大学学报(自然科学版), 2008, 48(5): 904-908. DOI: 10.3321/j.issn:1000-0054.2008.05.036.
Effect of Hydrogen Addition on Biogas Combustion
LI Yuan, LI Guo-xiu, LI Hong-meng
(School of Mechanical, Electronic and Control Engineering, Beijing Jiaotong University, Beijing 100044, China)
To study the effect of hydrogen addition on biogas combustion, experiment and CHEMKIN simulation of the gas mixture combustion were conducted. The experiment shows that the burning velocity of the gas mixture gets higher with the increase of hydrogen addition at a constant equivalence ratio, and the aggrandizement is more obvious with larger equivalence ratio. The simulation shows that the mole fractions of H and OH grow up with the hydrogen addition. The chemical reaction paths of the mixing hydrogen combustion process were analyzed by rate of production (ROP). The results show that H2affects a lot to the elementary reactions O + H2= H + OH and OH + H2= H + H2O. It changes the formation and consumption of H and OH in subsequent reaction, and the H and OH are rapidly accumulated especially in high percentage of hydrogen addition. The rate of premixed combustion was therefore accelerated obviously.
hydrogen addition; biogas; constant volume bomb; chemical reaction path; elementary reaction
李洪萌(1987-),男,博士研究生,主要从事内燃机燃烧方面的研究。
TK16
A
10.3969/j.issn.2095-560X.2016.03.001
2095-560X(2016)03-0165-07
2016-03-14
2016-06-08
李 源(1992-),男,硕士研究生,主要从事燃烧化学反应动力学研究。
李国岫(1970-),男,博士,教授,主要研究方向包括内燃机燃烧理论与技术、车用发动机电子控制、航天器推进系统、液体燃料雾化机理、流动与燃烧数值模拟。

