在线分光光度法对Fenton降解活性蓝的降解动力学研究
王建旭,张银柯,徐 航
(1.信阳师范学院 化学与化工学院, 河南 信阳 464000;2.河南科技大学 a.数学与统计学院;b.化工与制药学院,河南 洛阳 471023)
0 引言
纺织染料工业在生产过程伴随产生大量含染料废水,如将废水在不经过处理的情况下直接排放到环境中将会产生严重的环境污染[1].活性蓝是含复杂芳香环的有机大分子,结构非常稳定,常规废水处理法难以高效地处理此类染料废水[2].近年来有关染料降解的报道有很多,如:物理吸附法、混凝脱色法、光催化氧化法[3]、Fenton氧化法[4]、生物化学法等.其中Fenton法以其操作方便、运行费中等、降解效率高等优点受到广泛关注,其主要反应如(1)-(10)所示[4].目前关于Fenton氧化方面的实验中取样分析的步骤是在某时刻将反应液取出少量样品用于检测,然后将样品加中止剂终止反应,取上层清液进行测定有机物浓度,这样的操作过程会因操作时间和沉淀过程而引入大量的实验误差.在线分光光度计数瞬时采集Fenton试剂降解活性蓝的浓度随时间的变化,具有快速、准确、简便的特性,不但解决实验误差的问题,而且提高效率,获得大量准确的数据.本工作为Fenton氧化方面提供基础实验数据.
链引发:
Fe2++H2O2→Fe3++·OH+OH-
(1)
链的传递:
Fe3++H2O2→Fe2++H++·OOH
(2)
Fe3++·OOH→Fe2++·OO-+H+
(3)
Fe3++·OO-→Fe2++O2
(4)
·OH+H2O2→·OOH+H2O
(5)
·OH+RH→R·+H2O
(6)
链的终止:
2·OH→H2O2
(7)
·OH+H2O2→·OO-+H2O+H+
(8)
·OOH+·OH→H2O+O2
(9)
·OO-+·OOH→·OOH-+O2
(10)
1 实验部分
1.1 主要试剂和仪器
活性蓝其单体的结构式如图1所示.FeSO4、H2O2(wt30%)、H2SO4等试剂均为分析纯购置于北京化学试剂公司.UV-2102PC紫外-可见光分光光度计(上海UNICO公司),与分光光度计配套的蠕动泵、流动池和计算机,79HW-1型恒温磁力搅拌器(荣华仪器有限公司).
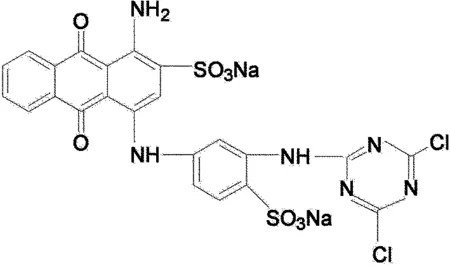
图1 活性蓝的化学结构式Fig. 1 Chemical structure of Reactive Blue
1.2 实验方法
首先将分光光度计的监测波长调节为599 nm,在磁力搅拌下将200 mL活性蓝染料废水加入到250 mL烧杯中,然后滴加一定浓度的FeSO4溶液,调节pH值,等待体系平衡.开启蠕动泵,将染料废水输送到分光光度计内的流动池中带体系平衡后,将H2O2快速加入到溶液中后计时,每2 s检测一个数据点,总检测时间为400 s.
2 结果与讨论
2.1 波长选择
图2为染料、H2SO4、Fe2+、Fe3+和H2O2的紫外可见光谱图,紫外可见光谱在500~700 nm区域内仅有活性蓝有比较强的吸光度,最大吸收峰为599 nm.在599 nm附近其他物质对活性蓝吸光度无干扰,因此实验的操作波长可确定为599 nm.在599 nm处,通过外标法标准曲线实验的测定吸光度(A)与活性蓝浓度(C)的关系为A=0.006 34C-0.011,相关度0.9999.
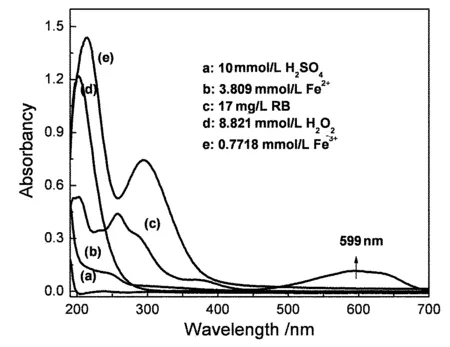
图2 各物质紫外可见光谱比较Fig. 2 UV-Vis spectrum of reactants
2.2 Fe2+初始浓度的影响
图3表示Fe2+初始浓度对活性蓝降解率的影响.随着Fe2+浓度的增加染料去除率也有很大程度的提高,活性蓝降解随时间的变化趋势是反应初期活性蓝快速下降,但经过短短的50 s后,活性蓝下降迅速趋于平坦,从活性蓝的降解曲线可以说明说明反应可能经历了两个过程.
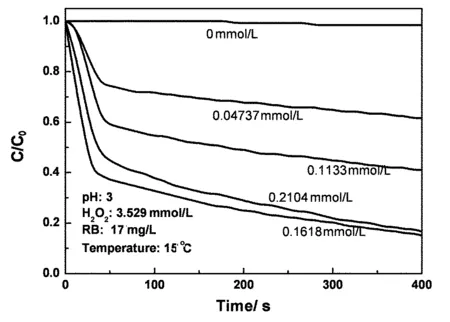
图3 Fe2+初始浓度的影响Fig. 3 Effect of initial Fe2+ concentration
BOSSMANN等[5-6]认为反应初期Fe2+不是单独以离子形态存在于极性的水溶液中,而以水合离子的形态存在,如方程(11)、(12)所示.其中[Fe(OH)(H2O2)(H2O)4]+具有很强的氧化能力,可快速夺走活性蓝分子的一个电子,从而使活性蓝分子因失电子而出现化学结构极度不稳定性,并快速分解达到降解目的,因此Fe2+浓度对前期反应的影响很大.当然四价铁也是一种极其不稳定的物质,无法在溶液中长时间存在,因此,到反应的中后期·OH的氧化作用凸现出来形成支配作用.
[Fe(OH)(H2O)5]++H2O2→
[Fe(OH)(H2O2)(H2O)4]++H2O
(11)
[Fe(OH)(H2O2)(H2O)4]+→[Fe(OH)3(H2O)4]+
(12)
根据文献报道,Fenton氧化符合准一级动力学[7],即:ln(C0/Ct)=kt,其中C0为活性蓝的初始浓度,Ct为反应在t时刻时活性蓝的浓度,k为反应速率常数.从图3全段曲线可以看出,这个过程明显不符合拟一级动力学,但如果按照反应初期和中后期进行分段处理,在反应初期和反应中后期这两个过程均符合准一级动力学,拟合后获得的反应前期降解速率常数k1和反应中后期降解速率常数k2结果如表1所示.从表1中可以看出,k1与k2相差约一个10倍,拟合系数0.98以上.其中在k1对Fe2+初始浓度呈线性关系,拟合结果k1=0.1354[Fe2+]0,R2=0.9917,这种线性关系佐证了反应初期Bossmann的四价铁理论.
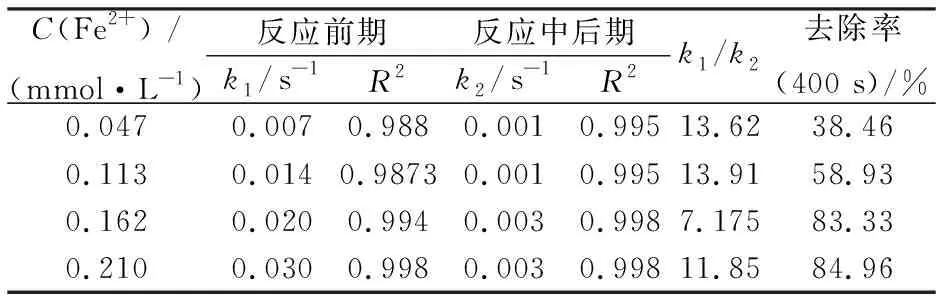
表1 Fe2+初始浓度对降解反应速率的影响Tab. 1 Effect of initial Fe2+ concentration to k by Fenton’s reagent
2.3 H2O2初始浓度的影响
H2O2的初始浓度影响活性蓝降解过程如图4所示.当H2O2的浓度由1.412 mmol/L增至3.529 mmol/L,活性蓝下降的速度有很大程度的提高;当H2O2的浓度超过3.529 mmol/L,活性蓝降解率受到明显抑制.
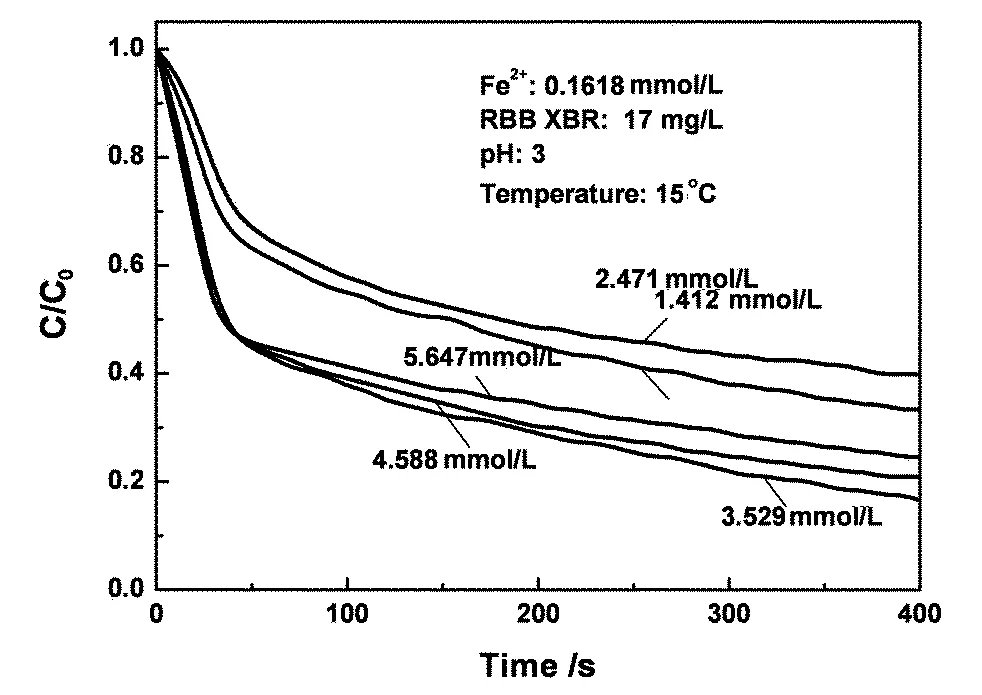
图4 H2O2初始浓度的影响Fig. 4 Effect of initial H2O2 concentration
反应初期(t≤50 s)和反应中后期利用的实验结果利用准一级动力学进行拟合,反应速率见表2.从表2中可以看出拟合系数均超过0.98,说明反应初期和中后期符合准一级动力学,反应初期的速率与反应中后期的速率相差约10倍.当H2O2的浓度超过最佳投加量3.519 mmol/L时,反应初期速率k1改变不明显,也可说明此时H2O2投加量到最佳.当H2O2的投加量过高时, Fe2+可能直接被氧化生成Fe3+,从而降低了活泼的四价铁和·OH的产生率,对活性蓝的降解是不利的.
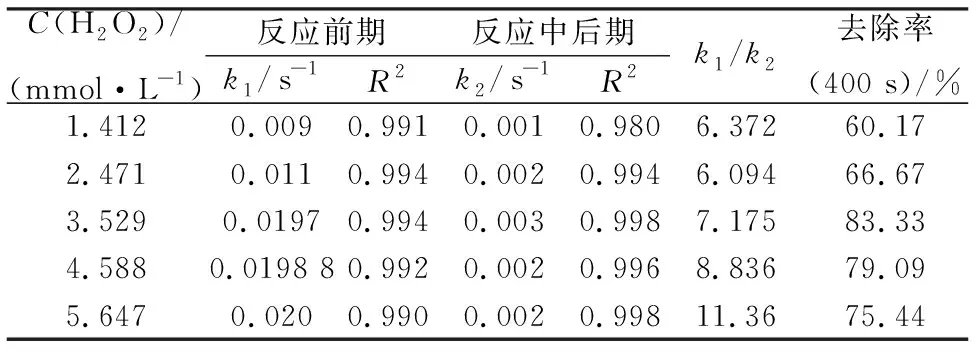
表2 H2O2初始浓度对降解反应速率的影响Tab. 2 Effect of initial H2O2 concentration to k by Fenton's reagent
2.4 活性蓝初始浓度的影响
图5表示活性蓝初始浓度对活性蓝降解曲线,从图5中可以看出,随着活性蓝初始浓度的增加,降解速率和去除率都有一定的下降,原因分析污染物浓度的增加必然会降低处理速率和效率.利用一级动力学进行拟合反应前期和反应中后期的速率,拟合结果如表3所示,从表中可以看出,拟合系数均超过0.98,说明这种拟合是合理的,k1与k2相差约一个数量级,k1和k2均随活性蓝浓度的增加而下降.
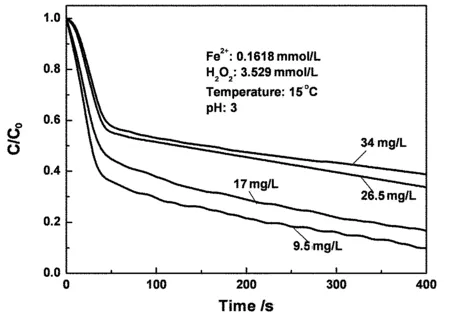
图5 活性蓝初始浓度的影响Fig. 5 Effect of initial RB concentration
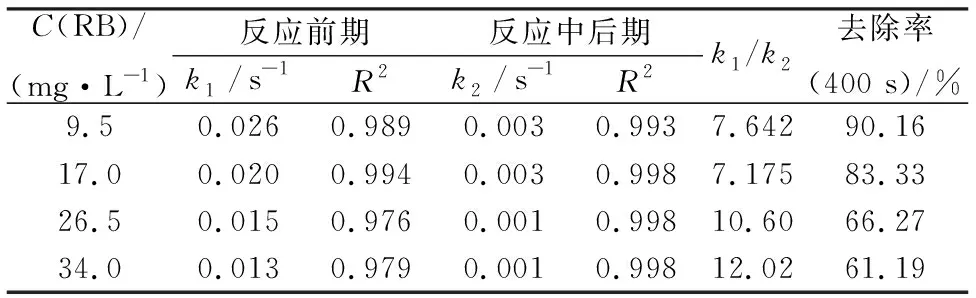
C(RB)/ (mg·L-1)反应前期反应中后期k1 /s-1R2k2 /s-1R2k1/k2去除率(400 s)/%9.50.0260.9890.0030.9937.64290.1617.00.0200.9940.0030.9987.17583.3326.50.0150.9760.0010.99810.6066.2734.00.0130.9790.0010.99812.0261.19
2.5 温度的影响
图6为改变体系温度对活性蓝降解的影响.利用拟一级动力学在反应初期和中后期分别进行拟和,结果如表4所示.结果表明,温度升高可加速k1的提高,但是k2却出现很大程度的下降,因此k1/k2随着温度的升高而大幅度增加,当温度达38 ℃时,两者差100倍.同时,在400 s时刻去除率也有一定程度的下降.总之,升高温度可以加速反应达到平衡的时间.原因分析如下:反应初期为四价铁控制反应,不受·OH的限制,升高温度本身也提高的反应速率;反应中后期为·OH控制反应, H2O2高温易分解,产生的·OH高温下容易发生触灭消亡,造成了反应后期速率常数很小.在反应前期利用阿伦尼乌斯公式( lnk1=Ea/RT+lnA)描述,将 lnk对 -1/T线性拟和,获得反应初期活化能Ea为25.21 kJ/mol.化学反应活化能小于63 kJ/mol时,反应在室温下可反应,因此Fenton处理活性蓝废水在室温下能迅速发生,完全符合实际水处理的要求.
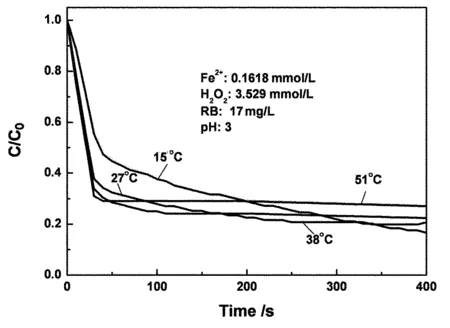
图6 温度的影响Fig. 6 Effect of temperature
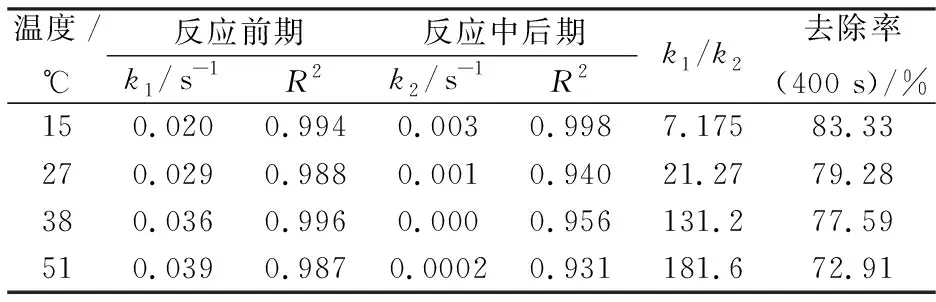
温度/ ℃反应前期反应中后期k1/s-1R2k2/s-1R2k1/k2去除率(400 s)/%150.0200.9940.0030.9987.17583.33270.0290.9880.0010.94021.2779.28380.0360.9960.0000.956131.277.59510.0390.9870.00020.931181.672.91
2.6 pH值的影响
图7为控制pH值为较强酸性(2)、弱酸性(3)和中性(7)条件下活性蓝浓度随时间的变化.从图7中可以看出弱酸性条件下活性蓝去除率最佳;在中性条件下,几乎没有任何的降解效率,而在较强的酸性条件下活性蓝反应速率和去除率与弱酸性条件下比较也有一定的下降.原因分析:与酸性条件比较中性条件不利于H2O2和Fe2+的稳定存在,强酸性溶液中过多的H+会抑制反应(2)的发生,Fe3+还原为Fe2+催化作用受阻.所以本实验控制pH值为3.
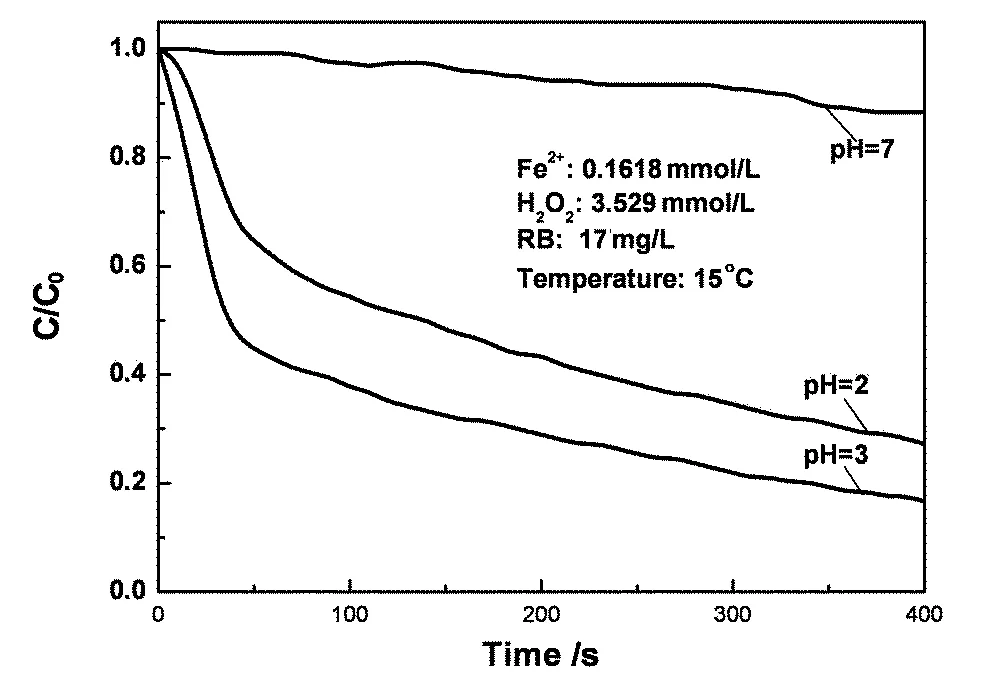
图7 pH的影响Fig. 7 Effect of pH
3 结论
利用在线分光光度法对活性蓝降解过程行动力学分析,将其降解过程分为两个拟一级动力学,反应前期降解速率常数和反应中后期降解速率常数相差约一个数量级.反应前期降解速率常数与Fe2+的初始浓度存在正向线性关系;H2O2浓度和pH值存在最佳值;升高体系温度能够加快反应速率并降低反应平衡的时间.该方法具有快速、准确、简便的特性,不但解决了实验误差的问题,而且提高了工作效率.

