第29届中国化学奥林匹克(决赛)实验试题的设计与解析
查正根 金 谷 兰 泉 黄 微 朱平平
(中国科学技术大学化学实验教学中心,合肥230026)
·竞赛园地·
第29届中国化学奥林匹克(决赛)实验试题的设计与解析
查正根金谷兰泉黄微朱平平*
(中国科学技术大学化学实验教学中心,合肥230026)
摘要:详细介绍和评析了第29届中国化学奥林匹克决赛实验试题;并详细介绍了实验设计思路和筛选过程,给出了评分规则制定的原则。
关键词:中国化学奥林匹克;化学竞赛;实验试题
第29届中国化学奥林匹克(决赛)暨冬令营实验考试于2015年11月29日在中国科学技术大学化学实验教学中心顺利举行。实验试题兼顾了内容的新颖性和综合性,全面考查了营员的基本实验技能和综合分析问题能力。本文是命题小组对本届实验试题的回顾和总结。
1 实验试题:3-苯基丙烯酸的合成及其纯度分析
1.1实验内容简介
Heck反应通常是指在碱性条件以及钯的催化下,不饱和卤代烃和烯烃之间发生的偶联反应。自20世纪70年代初Heck等发现该反应以来,化学家通过对催化剂和反应条件的不断改进使其得到广泛应用[1,2]。该反应已成为构建C―C键的重要方法之一,具有简单、便捷和高效的优势,在天然产物合成、医药以及新型高分子材料制备等领域具有重要的应用价值,Heck因此获得了2010年诺贝尔化学奖[3,4]。
本实验即利用水相Heck反应合成3-苯基丙烯酸,并分析其纯度,主要内容如下。
(1)3-苯基丙烯酸的合成:原位生成催化剂,在其催化作用下,以碘苯和丙烯酸为原料,在水溶液中合成3-苯基丙烯酸。
(2)3-苯基丙烯酸的纯度分析:用酸碱滴定法测定自制3-苯基丙烯酸的纯度。
1.2相关物质的物理化学性质
表1列出了相关物质的物理化学性质。

表1 相关物质的物理化学性质
1.33-苯基丙烯酸的制备
在100 mL圆底烧瓶中加入17 mg醋酸钯(已提供)和38 mg三聚氰胺(已提供),再加入50 mL蒸馏水,室温搅拌6 min。
用注射器分别移取1.7 mL碘苯(需记录,0.015 mol)和1.2 mL丙烯酸(需记录,0.018 mol),加入上述反应瓶中,再缓慢加入3.2 g碳酸钠(已提供),设置搅拌器温度约为220°C,搅拌下(转速1000-1300 r·min-1)回流45 min。移除热源,趁热进行减压过滤(注意:使用棉线手套操作!在布氏漏斗的滤纸上垫一层硅藻土,厚度约1 cm,现场黑板上给出说明)。将滤液转移至250 mL烧杯中,搅拌下滴加约45 mL 1 mol·L-1盐酸,析出白色固体。减压过滤,将烧杯内所生成固体完全转移至布氏漏斗中,并用少量冷水洗涤。收集固体产品于大称量瓶(规格70 mm×35 mm、标注营员号、空称量瓶需称重并记录),置于烘箱中,于110°C下干燥约半小时(需记录干燥起始时间),称重(需记录)并计算收率。产品转移至小称量瓶(规格25 mm×40 mm)中,进行纯度分析。
1.43-苯基丙烯酸的纯度分析
(1)NaOH溶液的标定
采用减量法准确称取0.7-0.9 g二水合草酸,置于250 mL烧杯中,加入约50 mL蒸馏水,搅拌使其溶解,定量转移至250 mL容量瓶中,稀释至刻度,摇匀、备用。
准确移取3份上述标准草酸溶液各25.00 mL,分别置于3个250 mL锥形瓶中,各滴加2滴酚酞指示剂,分别用0.05 mol·L-1NaOH溶液滴定至微红色,30 s不褪色即为滴定终点。各自读取数据,填入实验报告。
(2)3-苯基丙烯酸的纯度分析
采用减量法准确称取3份0.20-0.25 g自制的3-苯基丙烯酸,分别置于3个250 mL锥形瓶中,各加入10 mL无水乙醇,摇动使其溶解,分别缓慢加入10 mL蒸馏水,充分摇匀,各滴加2滴酚酞指示剂,分别用标准0.05 mol·L-1NaOH溶液滴定至终点。各自读取数据,填入实验报告。根据所消耗NaOH溶液的体积,分别计算3-苯基丙烯酸的纯度。
2 命题思路
2.1考查知识点
全国高中学生化学竞赛暨冬令营是全国高中学生最高水平的化学赛事,它与国际化学奥林匹克竞赛接轨,是中国高中学生的化学“全运会”。在第29届中国化学奥林匹克(决赛)的实验试题设计中,命题小组结合2010年诺贝尔化学奖工作以及自身科研成果,将有机化学领域中“C―C键构建”这一热点研究课题转化为考查内容,体现了内容的新颖性。同时在命题过程中又充分考虑了中学化学实验知识点,涉及产品的制备与分析,充分考查了营员在有机化学实验和分析化学实验等方面的基本操作技能,以及综合分析问题的能力,确保了实验内容的完整性。
2.2特色
(1)现代合成方法和经典化学分析相结合
Heck反应是当今合成方法学研究的杰出成果,是构建C―C键的重要方法之一。利用Heck反应合成目标化合物3-苯基丙烯酸(肉桂酸),代替经典合成方法——Perkin反应,体现了现代的合成方法与经典的化学分析相结合的特点。
(2)符合绿色化学的理念
选用新的催化剂体系钯-三聚氰胺配合物催化反应,达到高效催化的目的。以水为反应溶剂,避免了有机溶剂的使用,减少污染。而且目标化合物无毒、无害,常用于制备食品添加剂、香精香料,相对安全。符合现代绿色化学的理念。
(3)全面考查学生综合能力
考查学生综合运用知识和实验技能以及解决错综复杂问题的能力,结果更客观、更准确、更公平。
3 实验筛选与设计
3.1目标化合物和合成方法的选择
为了考查有机合成技能、化学分析能力、以及综合运用知识解决问题的能力,我们首先筛选出一系列目标化合物,例如,3-苯基丙烯酸、4-苯基苯甲酸、N-乙酰基苯丙胺酸(脯氨酸)。最终选择3-苯基丙烯酸作为目标化合物,它既可以用传统的方法合成,也可以用现代的绿色合成方法合成,同时又能满足化学分析方法对分析目标化合物的要求。
3-苯基丙烯酸(肉桂酸)的制备是经典有机化学实验的教学内容[5],通常采用Perkin反应来合成,即:芳香醛和酸酐在碱性催化剂作用下,发生类似羟醛缩合反应,生成α,β-不饱和芳香酸。催化剂通常是相应酸酐的羧酸钾或钠盐,有时也可用碳酸钾或叔胺代替。
根据最新报道[6],钯与配体三聚氰胺形成的配合物能有效地催化均相和非均相Suzuki-Miyaura偶联反应。命题小组通过反复探索和实验,选择原位生成这一配合物作为催化剂,可以在较短的时间内有效地催化碘苯和丙烯酸发生Heck反应,实现肉桂酸的合成。
与Perkin反应相比,Heck反应合成肉桂酸时,以水为溶剂,催化剂容易制备和获得,千分之一的催化量就可得到产物定量转化的效果,反应时间短,无需惰性气体保护,反应条件温和,充分体现了绿色化学理念(表2)。

表2 Perkin反应和Heck反应合成3-苯基丙烯酸比较
在Heck反应的基础研究中,可以采用常见的加热搅拌、微波反应器、超声波反应器,考虑到化学基本操作的普遍性和适用性,在本次实验竞赛中(图1),我们选择带聚四氟乙烯保温套的IKA磁力搅拌器及磨口玻璃仪器组装反应装置来合成目标化合物,实验过程较为安全。

图1 实验考试现场截图
3.2目标化合物纯度分析的方案设计
用差减法准确称量,酚酞作指示剂,进行酸碱滴定分析[7]。
设计产品的纯度分析时,考虑到既能考查学生分析化学的基本操作和数据处理能力,又能对合成的产品纯度做出客观评价。在前期筛选出的几个有机分子中,手性N-乙酰基脯氨酸易溶于水,涉及到有机溶剂水相萃取和有机溶剂的处理,耗时较长,很难在规定的时间内完成,且实验不绿色环保。4-苯基苯甲酸不溶于水,分析实验部分涉及到非水滴定,超出竞赛大纲的范围。而3-苯基丙烯酸的合成和纯度分析实验则能避免上述问题。
3-苯基丙烯酸(pKa=3.89)是一种有机弱酸,设计采用0.05 mol·L-1NaOH溶液滴定。原因是在这种情况下:(1)滴定到化学计量点时pHsp约为8.15左右,表明可用酚酞作指示剂(变色范围在pH 8.0-10.0),酚酞变色敏锐,便于终点的准确判断;(2)分析所需样品质量在0.20-0.25 g范围内,既能达到定量分析称量的误差要求,又能使称量样品质量较少,确保合成产品能满足滴定分析的需要。
但是3-苯基丙烯酸水溶性欠佳,考虑竞赛在冬季进行,若加热溶解,温度不好控制,测定结果就难以保证其准确度;若加入过量NaOH方法溶解,需两种标准溶液,无形中增加了准备的难度和竞赛时间。为此,我们选择在溶解时加入10 mL无水乙醇,保证样品完全溶解,经过较系统的分析实验,我们发现,只要加入乙醇的量不超过样品总体积的75%,滴定结果可控制在定量化学分析误差范围内。
3.3实验思考题设计
实验思考题的设计紧紧围绕实验内容,考查营员对实验内容、特别是实验合成方法的理解。
(1)写出合成3-苯基丙烯酸的反应式,用结构简式表示(3分);
(2)写出三聚氰胺的结构式(1分);
(3)三聚氰胺可以提高催化效率,简述原因(3分);
(4)简述碳酸钠在本反应中的作用(2分);
(5)3-苯基丙烯酸还可通过Perkin反应进行合成,请写出以苯甲醛为原料制备3-苯基丙烯酸的反应式,用结构简式表示(2分)。
4 评分规则的制定
评分规则包含实验操作和实验报告两部分。评分规则制定时考虑如下几个方面:(1)与实验相关的理论及数据处理能力;(2)实验动手能力;(3)实验结果。
4.1实验操作
实验操作为25分:合成和分析部分分别为13分、12分,占实验总分的25%。
实验操作规范是做好实验的基本要求,评分原则是:不规范的实验操作扣分;规范但直接影响实验结果的操作不扣分。如:合成的温度、时间掌握、产品分离时穿滤和产品的干燥程度等未扣分。
评分实行扣分制:若操作未扣分,即得满分;若有扣分,扣除后即为得分(最终操作得分大于0)。两部分评分细则见表3和表4。

表3 3-苯基丙烯酸的合成操作(共13分)评分细则

表4 3-苯基丙烯酸的纯度测定操作(共12分)评分细则
4.2实验报告
实验报告为75分,占实验总分的75%,在评分中实行得分制。其中,合成为43分,包括:实验思考题11分、产率计算式2分、产量30分。分析为32分,包括:NaOH溶液标定8分、纯度分析24分。
合成部分侧重知识点掌握,分析部分则侧重数据处理。实验结果是衡量实验成功与否的最重要依据,故产量和纯度分析分值较高,约占54%,学生只有在产量和纯度都高时才能得高分,片面地追求产量或纯度得不到高分。此外,产量得分大于纯度分值,旨在鼓励学生采用自己合成的目标化合物进行纯度分析,以完成一个完整的实验。
4.2.13-苯基丙烯酸的合成(共43分)
(1)写出合成3-苯基丙烯酸的反应式,用结构简式表示(3分)。
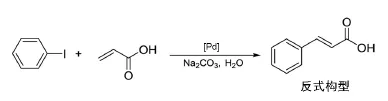
说明:
合成3-苯基丙烯酸的反应中,给出3-苯基丙烯酸,给出反式构型,正确构型得3分;未标明构型者得1分;
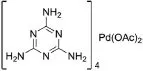
(2)写出三聚氰胺的结构式(1分)。

(3)三聚氰胺可以提高催化效率,简要描述原因(3分)。

说明:
三聚氰胺作为配体,与醋酸钯形成配合物催化剂,增加原位催化剂稳定性(2分)。
提高催化剂分散度,防止团聚,增强活性(1分)。
(4)简述碳酸钠在本反应中的作用(2分)。
Heck反应在碱性条件下进行,加入碳酸钠可以改变反应的pH,提供碱性条件(1分)。
与丙烯酸发生中和反应,以利于反应进行(1分)。
(5)3-苯基丙烯酸还可通过Perkin反应进行合成,请写出以苯甲醛为原料制备3-苯基丙烯酸的反应式,用结构简式表示(2分)。

说明:
反应式正确2分,未给反应条件仅得1分;只写出产物得1分。
(6)写出3-苯基丙烯酸收率的计算式(2分)。
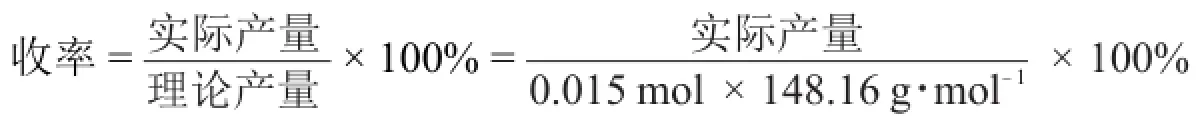
(7)3-苯基丙烯酸(A)的产量(30分)。
表5给出了目标产物3-苯基丙烯酸的质量与得分对应表。
4.2.23-苯基丙烯酸的纯度分析(共32分)
(1)NaOH溶液的标定(8分)。
(a)计算NaOH标准溶液浓度(2分)(每个0.5分)。
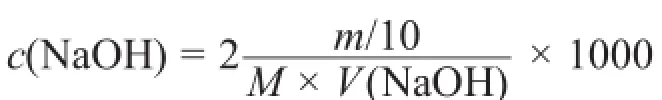
式中m为称量的草酸质量(g);M为二水合草酸的摩尔质量(126.07 g·mol-1);V(NaOH)为滴定消耗的NaOH标准溶液的体积(mL)。
说明:NaOH浓度计算(无正确计算公式不得分,计算结果错误扣0.5分)。
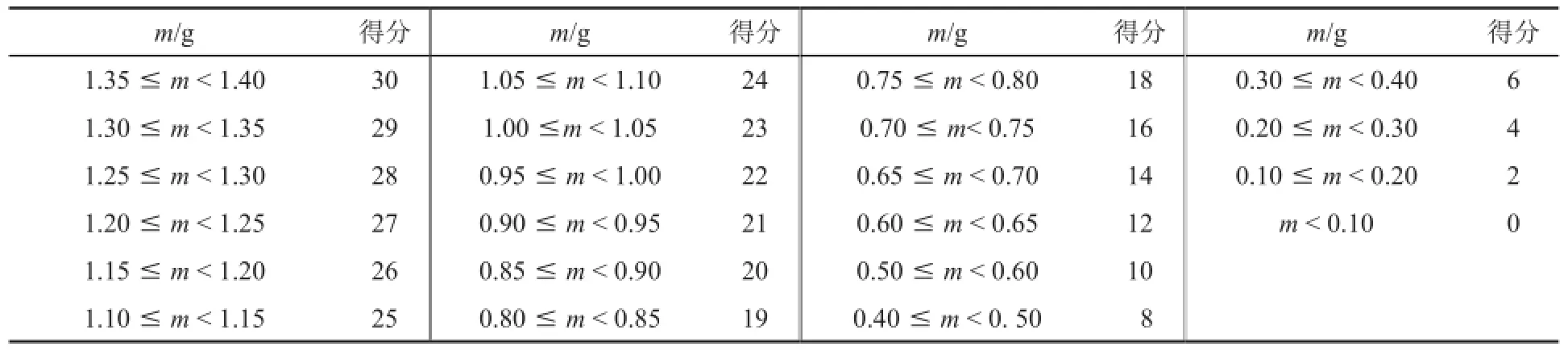
表5 产物质量m与得分对应表
(b)计算测定的相对平均偏差(2分)(每个1分)。

说明:测定的相对平均偏差计算(无正确计算公式不得分,计算结果错误扣0.5分)。
(c)标定精度分值(4分)。
表6给出了相对平均偏差与得分对应表。

表6 相对平均偏差与得分对应表
说明:在NaOH溶液的标定计算中,有效数字错误扣1分(只扣1次)。
(2)3-苯基丙烯酸的纯度分析(24分)。
(a)计算3-苯基丙烯酸的纯度(2分)(每个0.5分)。

式中,m为A的质量(g);M为A的摩尔质量(148.16 g·mol-1);c(NaOH)为NaOH标准溶液的浓度(mol·L-1);V(NaOH)为滴定消耗的NaOH标准溶液的体积(mL);G为称量的A质量。
说明:无正确计算公式不得分,计算结果错误扣0.5分。
(b)测定的相对平均偏差(2分)(每个1分)。
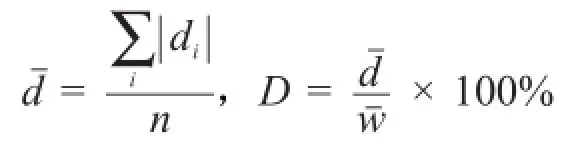
(c)测定精度分值(4分)。详见表6。
(d)纯度分值(16分)。
表7给出了目标产物3-苯基丙烯酸的纯度与得分对应表。
4.3扣分项(从实验总分中扣除)
扣分项包含损坏仪器、索要原料用于重新合成目标化合物、索要目标化合物进行纯度分析实验、废液和固体废渣未按规定倒入指定容器、未经监考教师同意而随意涂改实验数据、因个人操作错误而引起安全事故以及延时扣分。
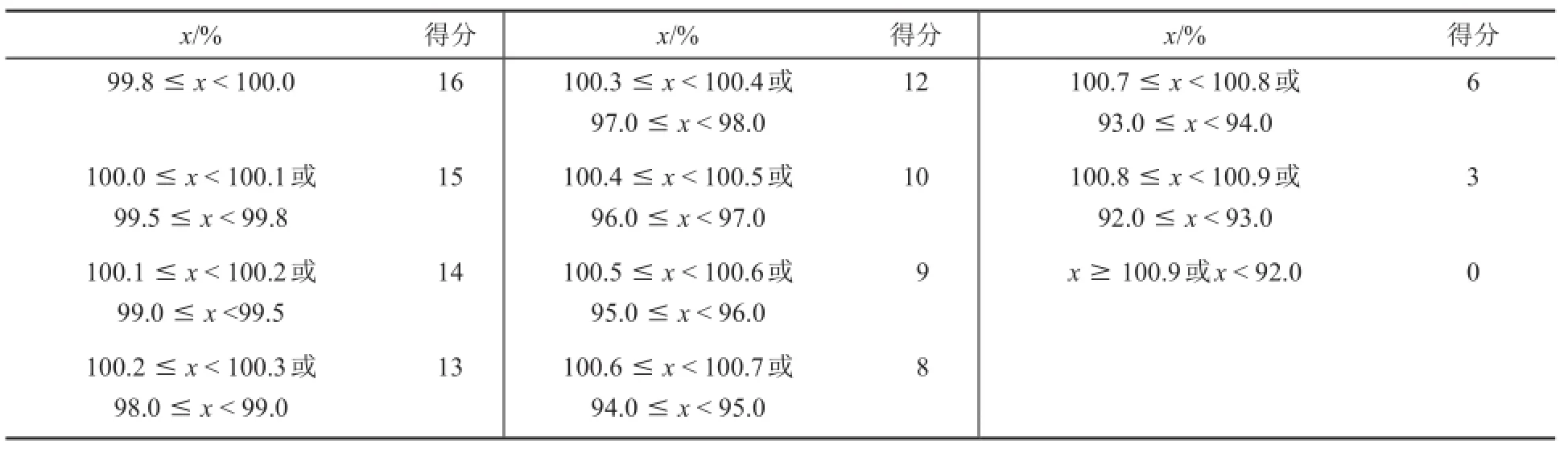
表7 产物纯度x与得分对应表
4.4监考环节
在本次竞赛中,命题小组对一些比赛细节进行了充分考虑,如在产品干燥环节,为了避免考生频繁开关烘箱引起温度波动,从而对干燥效果造成影响,命题组设置了严格的开关烘箱要求,即所有考生将产品放入烘箱时需严格记录时间并经监考老师签字确认,干燥半小时后方可打开烘箱取物。滴定数据和称量数据均须及时记录并经监考教师签名确认。此外,为了避免因考场时钟偏差所带来的考试时间差异,命题组找专人预先调整所有时钟,并在每个考场楼层设置了摇铃,确保时间的一致性。实验考试实行全程监控。这些细节的充分考虑,确保了本次实验考试得以圆满完成。
参考文献
[1]汪志勇,查正根,郑小琦.实用有机化学实验高级教程.北京:高等教育出版社,2016:338-340.
[2]Yang,J.H.;Wang,D.F.;Liu,W.D.;Zhang,X.;Bian,F.L.;Yu,W.Green Chem.2013,15,3429.
[3]Angew.Chem.Int.Edit.2010,49,8300.
[4]Lu,X.;Xiao,B.;Zhang,Z.Q.;Gong,T.J.;Su,W.;Yi,J.;Fu,Y.;Liu,L.Nature Commun.2016,DOI:10.1038/ncomms11129.
[5]王清亷,李瀛,高坤,许鹏飞,曹小平.有机化学实验.第3版.北京:高等教育出版社,2010:306-308.
[6]Edwards,G.A.;Trafford,M.A.;Hamilton,A.E.;Buxton,A.M.;Bardeaux,M.C.;Chalker,J.M.J.Org.Chem.2014,79,2094.
[7]金谷,姚奇志,江万权,胡祥余,李娇.分析化学实验.合肥:中国科学技术大学出版社,2010:122-125.
中图分类号:O6;G64
doi:10.3866/PKU.DXHX201604027
*通讯作者,Email:zhupp@ustc.edu.cn
The Design and Analysis of Experimental Test for the 29th Chinese Chemical Olympiad(Finals)
ZHAZheng-GenJIN GuLAN QuanHUANG WeiZHU Ping-Ping*
(Chemistry Experiment Teaching Center,University of Science and Technology of China,Hefei 230026,P.R.China)
Abstract:The design of experimental test for the 29th Chinese Chemical Olympiad(Finals)was introduced and analyzed.Experimental test,design ideas,the development of experimental selection and evaluation rules were provided.
Key Words:Chinese Chemical Olympiad;Chemistry competition;Experimental test

