钒酸铋黄色颜料的制备
——推荐一个无机化学教学实验
王 周 石建新 彭 敏 赖 瑢 李莲云 陈六平
(中山大学化学与化学工程学院,广州510275)
钒酸铋黄色颜料的制备
——推荐一个无机化学教学实验
王周*石建新彭敏赖瑢李莲云陈六平
(中山大学化学与化学工程学院,广州510275)
摘要:该实验以Bi(NO3)3和NH4VO3为原料,采用液相沉淀法,制备钒酸铋黄色颜料。学生通过控制反应物初始浓度、溶液pH、温度与时间等条件制备分散性良好、颗粒细小、组成均匀的钒酸铋。实验涉及溶液配制、加热搅拌、简易回流、控温、调pH、检验、抽滤、洗涤、干燥等操作。钒酸铋是一种绿色环保的黄色颜料,且具有降解污染物的光催化性能,因此,该实验不仅对于提高学生无机制备实验能力具有很好的教学效果,还在实验教学中渗透了环保理念。
关键词:钒酸铋;黄色颜料;无机化学实验;绿色环保
黄色是一种十分醒目的颜色,人眼只对400-700 nm波长的光敏感,而在波长555 nm处,人眼的感受性最高,它的色调处于黄绿区。因此,凡是需要人们高度注目的地方,如交通标识、出租车、电话亭、起重机械、邮政设施等,一般都涂成醒目、单一的黄色。
无机黄色颜料生产工艺简单,具有优良的热稳定性和耐候性,在颜料领域一直有着十分重要的作
正是在黄国平的引领下,苏印总厂坚持“以诚经营 创新务实”的理念,践行着关乎印刷的传承工作。会议室中陈列的企业近年来收获的诸多成绩,从专利申请证书,国际级、国家级和省级授予奖项,到客户颁发的勋章,体现的恰是以印刷为主题的不断提升。
英语作为一门国际通用语言,使用人数众多,在我国的重要性更是显而易见,从升学、求职、晋升等方面,英语是必备条件之一。关于英语的各类考试种类繁多,少儿英语考试、四、六级大学英语考试、英语专业四级、八级考试、公共英语等级考试(PETS)、商务英语等级考试(BEC)、雅思、托福、GRE等。这在某种程度上扩大了英语的影响力,也导致学生过度崇尚英语、英美国家文化和价值观。
钒酸铋黄色颜料具有无毒、耐候性好、色泽明亮及对环境友好等优良性能[3,4],是一种有着良好应用前景的新型环保颜料,因而可用来代替铬黄和镉黄颜料[5,6],应用于汽车面漆、工业涂料、橡胶制品、塑料制品和印刷油墨的着色等各项性能要求很高的场合[2]。钒酸铋是多晶型化合物,主要有4种不同的晶型:正交晶,系钒铋矿型晶体(Pucherite),属Pnca空间群,是自然界中存在的钒酸铋矿,颜色为棕色;四方晶,系硅酸锆型晶体,属141/amd空间群,为很浅的黄色,不适合作黄色颜料;四方晶,系白钨矿型晶体(Scheelite),属141/a空间群,呈黄色;单斜晶,系β-褐钇铌矿型晶体(Betafergusonite),属12/a空间群,呈黄色[7]。因此,只有单斜晶和白钨矿型四方晶结构的钒酸铋才适合作黄色颜料。
本实验的一个重要目的是锻炼学生控制反应条件的能力,通过有效地控制反应条件,制备出分散性良好、颗粒细小、组成均匀的钒酸铋黄色颜料。钒酸铋黄色颜料的颜色、亮度、着色力等颜料性能随着钒酸铋颗粒的大小而变,颗粒大时产品颜色深、亮度低、着色力低、颜料性能差,所以要控制反应条件使得产品颗粒细小均匀、分散性好,才能得到质量好的黄色颜料。
在大学生四年的钢琴学习中,能够学到非常多的知识,但这些知识如何运用到钢琴教学中,是现如今许多大学生应该考虑的问题。四年所学的钢琴知识,包括弹奏技巧、演奏方式、基本功训练等多种,如若将自己学到的东西在教学中能够很好的展示出来并能够得以运用,那这名学生将会是一位很好的的钢琴教师。但相反,现在多数大学生并不能够将所学到的知识很好的运用到钢琴教学之中。因此,提高大学生对所学知识的掌握能力,并将以转化运用到教学中,是现在多数学习钢琴的大学生应解决的问题。
1385 Application of SF-36 scale in health-related quality of life assessment of naval service personnel
本文介绍的实验是让学生学习和运用液相沉淀法,以Bi(NO3)3和NH4VO3为原料制备钒酸铋黄色颜料,同时学习控制反应物初始浓度、溶液pH、温度与时间等反应条件的方法。
1 实验目的
经过对BIM技术在建筑工程全过程项目管理中的实际应用分析,发现BIM技术在建筑工程全过程项目管理中具有一定的协调性,且这种协调性也多呈现在建筑工程全过程项目管理的多个方面。具体而言,一般情况下,建筑工程在建设的过程中,采用的为分包制的建设与管理方式,这使得建筑工程涉及到的组成单位比较多,很难对建筑工程进行统一化与整体化的信息交流,进而使得建筑工程的协调性比较差。
(2)学习液相沉淀法合成粉体材料的原理。
(1)了解钒酸铋黄色颜料的性质与用途。
(3)学习比较准确地控制反应条件的方法。
(4)学习简易回流操作的应用。
(5)熟悉溶液配制、抽滤、洗涤、干燥等实验操作方法。
2 实验原理
取20 mL Bi(NO3)3溶液于150 mL锥形瓶中,加入2 mL DBS溶液混合均匀。在磁力搅拌与水浴加热的同时,将20 mL NH4VO3溶液滴加到Bi(NO3)3溶液中,用NaOH溶液调节其pH=6(先快速加入5 mL 6 mol·L-1NaOH溶液,后滴加2 mol·L-1NaOH溶液),控制水浴温度约90°C,保温1 h(为减少水分蒸发,可用坩埚盖住锥形瓶口,进行简易回流操作)。此过程中需维持溶液的pH基本恒定,并要检查溶液中是否有Bi3+(Bi3+检查方法:用小漏斗法取上层清液于试管中,加入2滴30%NH4SCN溶液后再滴加0.1 mol·L-1Pb(NO3)2溶液,观察是否有棕色或橙色沉淀生成),若有,则要往锥形瓶中继续滴加NH4VO3溶液至Bi3+完全沉淀为止。
反应方程式:
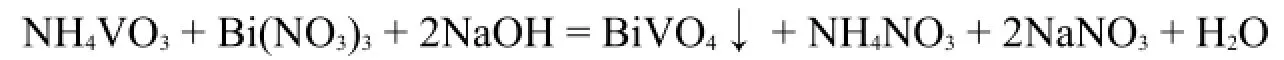
3 仪器和试剂
仪器:电热磁力搅拌器、循环水真空泵、电热鼓风干燥箱。
试剂:1.0 mol·L-1Bi(NO3)3溶液、2 mol·L-1NaOH溶液、6 mol·L-1NaOH溶液、2 mol·L-1HNO3溶液、1%十二烷基苯磺酸钠(DBS)溶液、30%NH4SCN溶液、0.1 mol·L-1Pb(NO3)2溶液、NH4VO3固体、95%乙醇。所有试剂均为AR级。
4 实验步骤
4.1NH4VO3溶液的配制
称取一定量的NH4VO3固体,加入15 mL 2 mol·L-1NaOH溶液,加热溶解完全后,再加水稀释得到1.0 mol·L-1NH4VO3溶液30 mL。
4.2钒酸铋的制备
钒酸铋黄色颜料的合成方法主要有固相煅烧法和水溶液中的化学沉淀法。固相煅烧法是将Bi(Ⅲ)和V(Ⅴ)的氧化物类或热分解能生成相应氧化物的盐类按照一定的组成进行混合,然后置于高温炉中煅烧而制得钒酸铋[2,16]。固相煅烧法所需温度较高(300-1000°C)、反应时间较长、颗粒较大且分布不均匀。液相沉淀法是将一定浓度的Bi(Ⅲ)盐和V(Ⅴ)盐的高纯溶液混合,让其在液相中结晶析出钒酸铋黄色沉淀[2,16]。液相沉淀法克服了固相煅烧法的缺点,反应温度低(100°C以下),反应时间短,反应物混合均匀,可以得到颗粒细小、组成均匀的BiVO4黄色颜料[4]。本实验采用液相沉淀法,通过混合Bi(NO3)3溶液和NH4VO3溶液来制备钒酸铋,该法工艺简单,容易实现工业化生产,但是反应过程中BiVO4粉体容易形成十分有害的团聚体,从而影响颜料的颜色和性能。因此,需控制沉淀的生成条件,如反应物初始浓度、溶液pH、反应温度和反应时间等因素。必要时,可加入少量表面活性剂起分散作用。
反应结束后抽滤,用大量蒸馏水洗涤沉淀至少3次,以洗去杂质离子,再用95%乙醇10 mL洗涤2次。放入105°C的烘箱中烘干,得到松散的钒酸铋黄色颜料。冷却后称重,计算产率。
5讨论
(1)反应条件的控制。
钒酸铋还是一种具有可见光催化性能的新型半导体光催化材料,在可见光辐射下能够降解有机污染物[8,9]、也能分解水制备氢气和氧气[10],因而在解决环境污染与开发新能源等领域具有潜在应用价值。但由于光生电子易与体内空穴复合,量子效率低,对反应物的吸附能力较弱等原因,钒酸铋的光活性不高,离工业化应用仍有较远距离。目前研究者们主要通过金属及非金属掺杂[11,12]、无机化合物复合[13]、合成工艺优化[14]、晶体形貌调控[15]等手段来提高钒酸铋的可见光催化效率。
反应物浓度的影响:由粒子成核理论可知,粒子的形成有晶核的生成与生长两个过程。溶液浓度小,碰撞少,晶核形成慢且数目少,溶质在晶核上不断沉积,晶核不断长大,生成的晶核粒径就比较大;溶液浓度大,物质间碰撞几率大,晶核形成快且数目多。但若反应物初始浓度太大,则生成物量太多,导致溶液搅拌困难,产品容易成团且得到的产品颗粒不均匀。经实验表明,最佳反应物初始浓度为1.0 mol·L-1。
pH的影响:pH会影响晶体的溶解度,使体系中离子平衡发生改变;pH能改变杂质的活度,使杂质活化或钝化;pH还能改变晶面的吸附能力以及晶体的生长速度。pH过低,Bi3+未能完全参加反应而影响产率,而且钒酸铋沉淀易形成团聚体,造成产品颜色暗、成分不均匀;pH过高,会产生过度胶凝,不利于后续的洗涤。经过实验表明,pH为6时,杂质钝化,钒酸铋晶体表面吸附杂质的能力降低,BiVO4晶体的溶解度和晶体生长速度达到最佳,得到的产品不但粒径小,而且颜色鲜艳。
(2)离子检验。
温度的影响:温度低,晶核形成慢且数目少,形成的晶体粒径大;温度高,晶核形成快且数目多,晶核来不及长大,形成的晶体粒径较小。所以要想获得颗粒细小的黄色颜料,就必须严格控制反应温度。水溶液体系最高温度为100°C,若溶液沸腾会造成水分蒸发快,不利于维持溶液浓度、pH等条件的稳定,因此我们将水浴温度设置在90°C,并采用简易回流装置来减少水分蒸发。
反应时间的影响:反应时间短,晶核来不及长大,形成的晶体颗粒较小。但若反应时间太短,则晶核不能很好地生长,形成无定形的有缺陷晶体,影响产物的颜色,且无定形沉淀会造成后续抽滤时发生透滤。但随着反应时间的增长,晶核不断长大,会形成颗粒大的粗晶体,产物颜色和性能变差,质量不好。经过实验表明,反应时间为1 h最合适。
国内互联网期刊出版商家的主要经营模式包括:中心网站包库、镜像站点、(上网卡)流量计费等方式。各互联网出版商也根据自身特色制定出不同的销售推广策略,具体见表5。
选取VXEEM而非VIX(标普500ETF波动率指数)主要有两方面的优势:1)未来原油的新增需求主要来自于新兴市场,新兴市场经济下行影响原油需求预期,VXEEM冲击OVX上行,而VIX受影响相对较小;2)油价受内部因素冲击产生的波动反过来影响新兴市场的通胀预期、经常账户差额和外汇储备,股市、汇率的波动率增加,OVX冲击VXEEM上行,而美国在页岩油气革命后的原油进口依存度减低,且WTI价格低于布伦特油和迪拜油,VIX受油价影响较小。
经过统计学软件分析和处理之后,在膀胱残余尿量方面,组间存在显著差异,统计学意义成立(P<0.05),结果如下表1:
检验Bi3+是否沉淀完全时,不能取上层溶液后直接加检验液,必须经过小漏斗法将悬浮在溶液中的钒酸铋过滤除去,得到清液后再加检验液。因为,若溶液中无Bi3+,那么就会产生白色沉淀,该白色沉淀与溶液中悬浮的钒酸铋混在一起,看起来是橙色,便会误以为Bi3+还未沉淀完全。
用光速来定义“米”,是长度计量科学史上的一次革命,具有非常重要的科学意义。光速作为一个精确的常数,可以提高长度计量的精度。
(3)分离与洗涤。
反应完毕,若直接用循环水真空泵抽滤,由于压差过大且产物颗粒小,在抽滤时容易透滤而造成产物损失,产率降低。建议刚开始抽滤时,先用水抽且调小水抽,让钒酸铋颗粒在滤纸上形成一层孔洞较小的膜,再开大水抽继续抽滤或者用循环水真空泵继续抽滤。
(4)产品的干燥。
沉淀烘干过程中要注意不时翻动沉淀,发现成块状要及时压碎,不然结块现象会造成产物颜色偏深。
6 教学建议
(1)在实验预习阶段,可适当安排学生查阅相关文献资料,了解黄色颜料的研究和发展状况,了解钒酸铋作为一种绿色环保型无机黄色颜料的性能、结构、应用以及合成方法,从而拓展相关的背景知识和激发学生的实验兴趣。要求学生在预习报告中画出实验流程图,让学生熟悉整个实验流程,以便更好地控制实验条件。
(2)本实验内容包括溶液配制、加热搅拌、简易回流、控温、调pH、检验、抽滤、洗涤、干燥等。对于学生的无机化学实验操作和无机制备实验能力的提高具有很好的教学效果。而且钒酸铋是一种新型的绿色环保颜料,具有光催化降解有机污染物和分解水制备氢气和氧气的性能,教师在实验教学中可以渗透环保教育,增强学生的环保意识。
无恒产而有恒心者,惟士为能。若民,则无恒产,因无恒心。苟无恒心,放辟邪侈,无不为已。及陷于罪,然后从而刑之,是罔民也。焉有仁人在位罔民而可为也?是故明君制民之产……然后驱而之善,故民之从之也轻。今也制民之产……此惟救死而恐不赡,奚暇治礼义哉?[4](P211)
(3)根据具体实验教学条件和实验教学学时情况,可以适当添加一些产物表征及性质检测的实验内容。钒酸铋有4种晶型,可以对本实验制备得到的产物进行X射线衍射分析其具体晶型;本实验控制反应条件得到颗粒细小的钒酸铋,可以利用粒度分析仪测试其粒度分布情况。
(4)实验结束后要求学生计算理论产率,并和实际产率对比,分析有差别的原因,锻炼学生讨论实验现象、总结实验经验和教训的能力。
(5)设置一些思考题,让学生课后学习和巩固,培养学生思考和分析问题的能力,并且能够促使学生查找相关资料,拓展知识面。例如:①在反应前加入1%十二烷基苯磺酸钠(DBS)溶液的作用是什么?②NH4VO3溶液滴入Bi(NO3)3溶液后要用NaOH溶液来调节pH,是什么原因造成NH4VO3溶液和Bi(NO3)3溶液的混合溶液呈酸性?③检验Bi3+是否沉淀完全时,有Bi3+和无Bi3+分别是什么现象,为什么?④液相沉淀法制备钒酸铋黄色颜料的影响因素有哪些?它们是如何影响制备产物的性能和产率的?⑤除了作为黄色颜料,钒酸铋还有没有其他有价值的用途?
参考文献
[1]陈荣圻.染料与染色,2014,51(4),1.
[2]唐安平.有色金属,2005,57(11),43.
[3]彭容秋.有色金属提取冶金手册.北京:冶金工业出版社,1992.
[4]张萍,次立杰,张星辰,段书德,许保恩,赵建路.石家庄学院学报,2006,8(11),9.
[5]Liu,J.B.;Wang,H.;Wang,S.;Yan,H.Mater.Sci.Eng.B-Adv.Funct.Solid-State Mater.2003,104(1),36.
[6]Wood,P.;Glasser,F.P.Ceram.Int.2004,30(6),875.
[7]Bayer,A.G.Bismuth Vanadate Pigments:a Process for Their Preparation and Their Use.US Pat.5203917,1993.
[8]Sarkar,S.;Chattopadhyay,K.K.Physica E 2014,58(4),52.
[9]Lai,H.F.;Chen,C.C.;Chang,Y.K.;Lu,C.S.;Wu,R.J.Sep.Purif.Technol.2014,122(3),78.
[10]Harada,H.;Hosoki,C.;Kudo,A.J.Photochem.Photobiol.A-Chem.2001,141(2-3),219.
[11]刘国聪,金真,张喜斌,李险峰,刘鸿.无机材料学报,2013,28(3),287.
[12]Zhao,Z.X.;Dai,H.X.;Deng,J.G.;Liu,Y.X.;Au,Z.T.Chin.J.Catal.2013,34(8),1617.
[13]张鹏,孙振海,耿延玲,匡少平.青岛科技大学学报(自然科学版),2015,36(2),33.
[14]于谦,叶红齐,覃涛,桂珊,马谦,曾凡涛,刘贡钢.应用化工,2014,43(4),600.
[15]杨长秀,王敏,牛超,董占军,王前武,郑浩岩.材料热处理学报,2015,36(4),13.
[16]谭红艳,韩爱军,叶明泉.材料导报,2009,23(5),172.
中图分类号:O61;G64
doi:10.3866/PKU.DXHX201507004
*通讯作者,Email:Wangzh97@mail.sysu.edu.cn用。铬黄和镉黄是当前使用较多的无机黄色颜料,但因含有铅、铬、镉等对人体和环境有害的元素,导致其应用领域受到限制[1]。此外,无机颜料中的氧化铁黄颜色不够鲜亮,钛镍黄和钛铬黄等金红石型混相颜料透明度、着色力和遮盖力较差;有机颜料大多遮盖力、耐候性等性能不理想或者价格相对昂贵[2]。因此,它们都不能作为铬黄和镉黄的理想代用品。
Preparation of Bismuth Vanadate Yellow Pigment: an Inorganic Chemistry Experiment Recommended
WANG Zhou*SHI Jian-XinPENG MinLAI RongLI Lian-YunCHEN Liu-Ping
(School of Chemistry and Chemical Engineering,Sun Yat-sen University,Guangzhou 510275,P.R.China)
Abstract:The preparation of bismuth vanadate yellow pigment by the liquid-phase precipitation method using Bi(NO3)3and NH4VO3as raw materials is recommended as an inorganic chemistry experiment. Students are required to obtain small and uniform BiVO4yellow pigment particles with good dispersity by controlling the initial concentration of reactants,the pH of solution,the reaction temperature and duration. The experimental procedures involve solution preparation,heating,stirring,simple reflux,temperature and pH control,ion test,the suction filtration,washing and drying.Bismuth vanadate not only is a kind of green environmental protection yellow pigment,but also has the photocatalytic performance to degrade pollutants.Therefore,the experiment not only is beneficial to the improvement of students'preparation ability in inorganic chemistry experiment,but also imparts the environmental education in the experimental teaching.
Key Words:Bismuth vanadate;Yellow pigment;Inorganic chemistry experiment;Green environmental protection

