阿奇霉素联合醒脑静序贯治疗大叶性肺炎的疗效
李林,穆秀,王笑一
(1.锦州医科大学附属第一医院 呼吸二科,辽宁 锦州 121001;2.锦州妇婴医院 生殖医学专院,辽宁 锦州 121000)
阿奇霉素联合醒脑静序贯治疗大叶性肺炎的疗效
李林1Δ,穆秀1,王笑一2
(1.锦州医科大学附属第一医院 呼吸二科,辽宁 锦州 121001;2.锦州妇婴医院 生殖医学专院,辽宁 锦州 121000)
目的 阿奇霉素联合醒脑静序贯治疗对大叶性肺炎患者血清高迁移率族蛋白1 (high mobility group box-1 protein, HMGB1)、白介素族及C反应蛋白(CRP)水平的影响。 方法 选取锦州医科大学附属第一医院呼吸科2013年9月~2014年4月大叶性肺炎患者78例,根据随机数字表法随机分为2组:对照组39例,予常规阿奇霉素口服治疗;试验组39例,在常规治疗的基础上加用醒脑静。观察2组患者治疗前后临床疗效、HMGB1、白介素族、CRP、T淋巴细胞亚群以及不良反应。 结果 治疗后与对照组相比,试验组临床总有效率较高(P<0.05)。2组患者血清IL-6、IL-8、IL-10、CD8+、CRP、HMGB1水平降低(P<0.05),CD3+、CD4+及CD4+/CD8+水平较治疗前升高(P<0.05),与试验组相比,血清IL-6、IL-8、IL-10、CD8+、CRP、HMGB1水平较低(P<0.05),CD3+、CD4+及CD4+/CD8+水平较治疗前升高(P<0.05)。2组不良反应相比差异无统计学意义。结论 阿奇霉素联合醒脑静治疗大叶性肺炎的临床疗效确切,可显著降低血清炎症因子水平,调节免疫功能,药物安全性高。
醒脑静;阿奇霉素;大叶性肺炎;白介素;HMGB1
大叶性肺炎又被称为肺炎球菌肺炎,是由肺炎双球菌等细菌感染而导致的在肺部呈大叶性分布的炎症[1]。醒脑静是以中医古方“安宫牛黄丸”基础研发而成的水溶性注射液,具有醒脑开窍、清热解毒、镇痛抑菌、抗炎等功效[2]。阿奇霉素是第二代大环内酯药物,主要用于治疗呼吸道及生殖道感染,是肺炎治疗的首选用药,但由于药物滥用致使机体产生耐药性,药物单独使用已无法满足患者根治疾病的目的。本文系统评价脑静注射液联合阿奇霉素序贯治疗大叶性肺炎的临床疗效及安全性。
1 资料与方法
1.1 一般资料 收集2013年9月~2014年4入住锦州医科大学附属第一医院呼吸科治疗的78例大叶性肺炎患者,男41例,女37例,年龄16~49岁,平均年龄(35.57±4.14)岁。采用随机数字分配法,随机分配为试验组与对照组,其中试验组39例,男20例,女19例,年龄17~49岁,平均年龄(36.04±3.72)岁;对照组39例,男21例,女18例,年龄16~48岁,平均年龄(34.46±3.69)岁。2组患者平均年龄、性别比例差异无统计学意义。
纳入标准:诊断符合《社区获得性肺炎诊断和治疗指南》[3]:①临床表现有发热、咳嗽或气急等呼吸道感染性症状;②肺部听诊闻及呼吸音增粗或湿性罗音;③肺部叩诊可见浊音或实音病灶;④X线或CT等影像检查可见肺叶或肺部节段性大片致密实变影;⑤就诊前未使用抗生素及其他相关性治疗药物。本研究经本市人民医院医学伦理委员会批准。患者签署知情同意书。
排除标准:①不愿参与本研究或不符合纳入标准者;②同时患有其他系统疾病或肺结核等肺部其他干扰疾病者;③患有肝炎、艾滋病或其他传染性较强疾病者;⑤患儿同时有心、肝、肾等器官器质性病变者;⑥入院前2周内曾应用过抗生素或其他治疗性药物者;⑦对本实验所用药物过敏者。
1.2 方法
1.2.1 治疗方法:78例大叶性肺炎患者随机分为对照组与试验组。2组患者均给予入院内抗常规,二级护理,抗炎、退热、止咳、平喘以及雾化等对症治疗。对照组给予阿奇霉素片(规格:每片0.5 g,批号:20130930,海南全星制药有限公司)口服,每次0.5 g,每天1次,用药1~2 d后,改用阿奇霉素口服制剂0.25 g,7 d为1个疗程。试验组缓慢推注10~20 mL0.9%NaCl注射液+注射用酒石酸阿奇霉素20万单位/次,每天2次,0.9%氯化钠注射液100 mL+醒脑静注射液(规格:每支10 mL,批号:20100920,大理药业股份有限公司)20 mL,每天1次,治疗3 d后停用4 d,连续治疗2周。
1.2.2 观察指标
① 疗效评定标准:治疗14 d后,比较2组患者治疗有效率。临床疗效评价标准:痊愈为患者临床症状完全消失,体温恢复正常,血常规和肺部X线检查显示完全正常;显效为患者临床症状基本消失,体温明显下降接近正常水平,血常规和肺部X线检查示明显改善; 有效为患者临床症状有明显改善,体温有所下降,血常规和肺部X线示有所好转;无效为患者临床症状无明显变化甚至出现加重,血常规和肺部X线检查无明显变化或加重。总有效率=[(痊愈+显效例数+有效例数)/本组患者例数]×100%。
② 血清白介素族、HMGB1、CRP以及淋巴细胞亚群水平检测:治疗前后于清晨空腹抽取肘静脉血3 mL,不抗凝,静置后以 2 000 r/min 离心10 min,分离血清置于-70 ℃低温冰箱保存待测。严格按照试剂盒说明书步骤操作,采用武汉博士德生物工程有限公司提供的ELISA试剂盒检测血清中血清白介素族、高迁移率族蛋白1 (high mobility group box-1 protein, HMGB1)及C反应蛋白(CRP)水平;采用流式细胞分析仪测量患者血清中的CD3+、CD4+及CD8+T淋巴细胞亚群浓度水平。

2 结果
2.1 临床疗效比较 治疗后试验组临床总有效率显著高于对照组(χ2=4.523,P=0.033)。见表1。

表1 2组患者临床疗效比较[n(%)]
*P<0.05,与对照组比较,compared with control group
2.2 血清白介素族、HMGB1、CRP水平比较 与治疗前相比,2组患者经治疗后血清IL-6、IL-8、IL-10、CRP、HMGB1水平降低(P<0.05),与试验组相比,血清IL-6、IL-8、IL-10、CRP、HMGB1水平较低(P<0.05)。见表2。
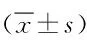
表2 2组患者血清白介素族、HMGB1及CRP水平对比
*P<0.05,与同组治疗前比较,compared with the same group pre-treatment;#P<0.05,与对照组治疗后比较,compared with control group post-treatment
2.3 淋巴细胞亚群水平比较 与治疗前相比,2组患者经治疗后血清CD8+水平降低,CD3+、CD4+及CD4+/CD8+水平较治疗前升高(P<0.05),与对照组相比,试验组血清CD8+水平较低,CD3+、CD4+及CD4+/CD8+水平较治疗前升高(P<0.05)。见表3。
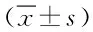
表3 2组患者淋巴细胞亚群水平对比Tab.3 Comparison of lymphocyte subsets levels pre-and post-treatment between two groups(±s)
*P<0.05,与同组治疗前比较,compared with the same group pre-treatment;#P<0.05,与对照组治疗后比较,compared with control group post-treatment
2.4 安全性评价 试验组出现1例恶心呕吐,1例头痛,1例眩晕,总不良反应发生率为8.82%(3/39),对照组出现1例恶心呕吐,2例头痛,1例皮疹,总不良反应发生率为10.26% (4/39),2组不良反应相比,差异无统计学意义。
3 讨论
大叶性肺炎是较为常见的社区获得性肺炎之一,尤其以儿童为高发人群,其临床表现较为复杂多样,以发病急骤、持续性高热、咳铁锈色痰为特征性症状[4]。据现有文献资料研究[5],大叶性肺炎的发病机制目前仍未十分清楚,但多数学者认为炎性因子与细胞免疫在大叶性肺炎形成过程中发挥了重要的作用。肺部受到致病原感染时,机体及病原体本身便会释放相应的毒素刺激肺泡巨噬细胞释放炎性因子,而吸收入血的炎性因子及致病原释放的毒素进一步激活机体单核-巨噬细胞,引起全身炎症反应发生,及时调整患者促炎和抗炎反应的平衡是治疗大叶性肺炎的关键。
醒脑静注射液是由中医古方“安宫牛黄丸”制成,已被临床证实具有清热解毒,凉血活血,开窍醒脑的功效,临床常用于治疗意识障碍或眩晕等[6],醒脑静是由“安宫牛黄丸”的成分为基础研制的的新型药物,其成分以麝香、栀子、牛黄、冰片、郁金等为主,方中牛黄清热解,麝香芳香开窍,兴奋中枢神经系统和呼吸中枢,冰片助麝香以通诸窍,栀子清热解毒、凉血行气,郁金化痰开窍,诸药合用共奏醒脑开窍、清热解毒、镇痛抑菌、抗炎之功效。现代研究已证实,醒脑静具有较好的抗炎、调节机体免疫功能的作用[7],与阿奇霉素的抗炎作用起到协同作用。本研究显示,治疗后与对照组相比,试验组临床总有效率较高(P<0.05),证实阿奇霉素联合醒脑静能有效降低大叶性肺炎的临床疗效显著,药物安全性高。
IL-6是一种多效性细胞因子,也是机体在免疫应答中的重要炎症介质之一[8],能够参与机体多种组织细胞的生长、分化和调节。肺炎患者的血清IL-6升高,可能是由于肺组织受损引起的急性应激反应。IL-8能促进白细胞浸润,产生活性物质,并促进细胞因子的释放失调,导致毛细血管内皮细胞损害,造成血管和神经的损伤,因此在患者肺炎时水平显著升高。IL-10是一种重要的免疫调节细胞因子[9],能够调节细胞的生长以及分化,参与炎性、免疫反应的进行,是目前公认的炎症与免疫抑制因子。上述白介素族具有复杂的生理功能,生物学应用广泛,诱发免疫球蛋白分泌,T细胞的增殖,是临床重要的促炎细胞因子,与呼吸系统疾病、肿瘤以及肾脏疾病等联系广泛。C反应蛋白(C reactive protein,CRP)是一种由肝脏合成特异性以及敏感度较高的急性时相反应蛋白[10],具有免疫调节作用,激活巨噬细胞,激发巨噬细胞吞噬以及降解外来细菌和异物的作用,对其他具有免疫调节功能具有刺激作用[11]。血清CRP的合成迅速,半衰期较短,曾有研究显示,肺炎患者体内血清CRP水平迅速升高并与肺炎的发展呈正比,是临床鉴别炎症感染的重要指标[12]。CD4+是人体免疫系统中十分重要的免疫细胞,能分泌多种细胞因子调节免疫作用,主要表达T(Th)细胞,是TCR识别抗原的受体,参与其信号传导作用,临床对于诊断肺炎的临床疗效以及患者免疫功能具有重要的诊断作用[13]。CD8+T细胞进行抗原提呈,随后T细胞与APC相互接触,表达于CD8分子的T细胞,储存于脾脏、扁桃体以及淋巴结等器官内[14]。大叶性肺炎患者伴随CD4+以及CD8+水平异常[15]。高迁移率族蛋白B1(HMGB1)是一种高度保守的核蛋白,有研究显示,重症肺炎患者HMGB1显著高于正常人[16]。本研究显示,经治疗后,与治疗前相比,2组患者血清IL-6、IL-8、IL-10、CD8+、CRP、HMGB1水平降低(P<0.05),CD3+、CD4+及CD4+/CD8+水平较治疗前升高(P<0.05),与试验组相比,血清IL-6、IL-8、IL-10、CD8+、CRP、HMGB1水平较低(P<0.05),CD3+、CD4+及CD4+/CD8+水平较治疗前较高(P<0.05),证实阿奇霉素联合醒脑静对大叶性肺炎能够降低血清炎症因子水平,调节免疫功能。
本研究通过对本院呼吸科大叶性肺炎患者78例的临床疗效、HMGB1、白介素族、CRP、T淋巴细胞亚群以及不良反应进行研究,证实了阿奇霉素联合醒脑静能有效降低大叶性肺炎的临床疗效确切,可显著降低血清炎症因子水平,调节免疫功能,药物安全性高。在下一步研究中,本课题组将进行药理学方面研究,对本研究做进一步研究。
[1] 郝琴. 儿童大叶性肺炎76例护理体会[J]. 陕西医学杂志, 2013, 42(8):1103.
[2] 孙玉霞, 孔令军. 醒脑静注射液的临床应用研究进展[J]. 中国药业, 2013, 22(A01): 372.
[3] 中华医学会呼吸病学分会. 社区获得性肺炎诊断和治疗指南[J]. 中华结核和呼吸杂志, 2007, 29(4):270-272.
[4] 阮荣林. 纤维支气管镜灌洗治疗儿童大叶性肺炎 70 例疗效观察[J]. 湖北科技学院学报: 医学版, 2014, 28(1): 52-53.
[5] 王颖洁. 儿童肺炎支原体肺炎免疫功能、降钙素原及C-反应蛋白变化及意义[D]. 大连:大连医科大学, 2013.
[6] 过海东, 郝春梅, 邱英茹. 醒脑静注射液临床应用概况[J]. 中国中西医结合急救杂志, 2002(9):60-61.
[7] 范成普, 杜杭根, 田勇. 醒脑静注射液在创伤性脑损伤应用研究进展[J]. 浙江中西医结合杂志, 2015, 25(1): 96-99.
[8] 王立, 陈华, 郑文洁,等. 白细胞介素-6阻滞剂在自身免疫病治疗中的应用进展[J]. 中华风湿病学杂志, 2013, 17(10):699-702.
[9] 冯乐, 赵进良, 周玉麟,等. HCV高危人群血浆IL-10水平及其与F蛋白抗体关系[J]. 中国公共卫生, 2014, 30(8):1080-1081.
[10] 徐爽, 庄金宝, 艾清,等. 快速C反应蛋白联合血常规检测提高儿童上呼吸道感染诊断的临床价值[J]. 中国实验诊断学, 2013, 17(8):1474-1475.
[11] 官建军, 洪永富. 超敏C反应蛋白水平与儿童疾病关系的分析[J]. 上海预防医学, 2013, 25(9):542-543.
[12] 王玉梅, 孙丽娟, 王善菊. 血清PCT和CRP对社区获得性肺炎的诊断价值[J]. 放射免疫学杂志, 2011, 24(4):447-449.
[13] 周凤岩, 乔建国, 何淑云,等. 吉林市HIV-1感染者病毒载量与CD4+T淋巴细胞计数检测研究[J]. 中国实验诊断学, 2014,18(8):1346-1347.
[14] 王鹏鹏, 柴长斌, 汪洋. CD8+T细胞激活和免疫记忆形成的分子调节机制[J]. 中华微生物学和免疫学杂志, 2015, 35(7): 541-545.
[15] 陈正荣, 季伟, 王宇清,等. 肺炎支原体致支气管肺炎和大叶性肺炎患儿的临床及实验室检查特征分析[J]. 临床儿科杂志, 2012, 30(8):744-748.
[16] 陈炎堂,曾勉,黄炎明,等.高迁移率族蛋白B1在重症肺炎患者中的临床研究[J].中华医院感染学杂志,2014,24(6):1558-1560.
(编校:王俨俨)
Efficacy of azithromycin combined with Xingnaojing injection of sequential therapy in lobar pneumonia
LI Lin1Δ, MU Xiu1, WANG Xiao-yi2
(1.Department of Respiratory Medicine, The First Affiliated Hospital of Jinzhou Medical University, Jinzhou 121001,China;2. Center for Reproductive Medicine, Women and Children’s Hospital of Jinzhou, Jinzhou 121000, China)
ObjectiveTo explore the effect of azithromycin combined with Xingnaojing injection of sequential therapy on high mobility group box-1 protein (HMGB1), interleukins and CRP in the treatment of lobar pneumonia .Methods78 patients with lobar pneumonia in department of respiratory medicine of the first affiliated hospital of Jinzhou medical university from September 2013 to April 2014 and were divided into 2 groups according to the random digital table method. 39 cases in the control group were treated with azithromycin. 39 cases in the experimental group were treated with Xingnaojing injection combined with azithromycin of sequential therapy. The efficacy, HMGB1 interleukins, CRP and T lymphocyte subsets and adverse reactions of two groups before and after treatment were compared . ResultsCompared with the control group, the efficacy of experimental group was higher (P<0.05). Compared with pre-treatment, the levels of serum IL-6,IL-8,IL-10,CD8+,CRP and HMGB1 post-treatment in both groups were significantly lower(P<0.05), the CD3+,CD4+and CD4+/CD8+levels in both groups were significantly higher(P<0.05). Compared with control group, the levels of serum IL-6,IL-8,IL-10,CD8+,CRP and HMGB1 post-treatment in experimental group were significantly lower(P<0.05), the CD3+,CD4+and CD4+/CD8+levels in experimental group were significantly higher(P<0.05). There was no significant difference between two groups. ConclusionThe azithromycin combined with Xingnaojing injection has the exact efficacy in the treatment of lobar pneumonia, which could effectively reduce serum inflammatory factors and regulate immune function with high security.
Xingnaojing injection; azithromycin; lobar pneumonia; interleukins; HMGB1
李林,通信作者,女,本科,护师,研究方向:呼吸,E-mail:lilin2016@tom.com。
R563.1+1
A
10.3969/j.issn.1005-1678.2016.05.21

