双硫腙法测定蔬菜中铅残留的研究
徐守霞,王 斌
(1.宿迁高等师范学校生物系,江苏宿迁 223800;2.宿迁学院三系,江苏宿迁 223800)
双硫腙法测定蔬菜中铅残留的研究
徐守霞1,王 斌2
(1.宿迁高等师范学校生物系,江苏宿迁 223800;2.宿迁学院三系,江苏宿迁 223800)
摘要[目的]研究蔬菜中残留二价铅离子的测定,为蔬菜中重金属离子的测定提供参考。 [方法]用双硫腙分光光度法研究了二价铅离子的吸收波长、显色时间、pH以及显色剂的量等对测定蔬菜中铅残留的影响,优化了试验条件。[结果]试验表明,在波长510 nm处、络合显色3 min、pH为8.5等条件下,二价铅离子含量在1~5 μg的范围内与吸光度呈现良好的线性关系,其检出限为2.17×10-6mg/mL。[结论]用双硫腙分光光度法测定二价铅离子可应用于实际蔬菜样品的检测。
关键词双硫腙;分光光度法;二价铅离子
随着近现代工业的发展,铅污染越来越严重。工业废气、废水、汽车尾气,这些不仅污染了水和大气,还会污染土壤,从土壤转移到蔬菜中,会对人类健康造成极大的危害[1-2]。由于铅容易在体内聚集,含量一旦超标就会形成血铅[3-5]。因此,对蔬菜中铅含量的测定具有十分重要的意义。蔬菜中铅离子的测定有荧光光度法[6]、火焰原子吸收法[7]、气相色谱-质谱法[8]等,这些方法有的需要大型仪器、有的试验步骤繁琐。笔者使用铅标准液通过可见光分光光度法,以双硫腙作为显色剂,盐酸羟胺、柠檬酸铵、氰化钾作为掩蔽剂来测定蔬菜中的铅含量,试验结果表明,该方法快速、准确,并能实现实际蔬菜样品的定量测定。
1材料与方法
1.1材料主要仪器:电子秤,722型分光光度计,PHS-3C型精密酸度计。主要试剂:12.5%氨水,盐酸,20%盐酸羟胺,20%柠檬酸铵溶液,10%氰化钾溶液,双硫腙使用液(0.017 8 mg/mL),铅标准溶液。
1.2方法准确取0.3 mL铅标准使用液,移液管移至125 mL分液漏斗中,加硝酸至20 mL,加入1.0 mL盐酸羟胺、5.0 mL柠檬酸铵溶液和2滴酚红指示剂,用氨水调节pH,使溶液呈红色,加入2.0 mL氰化钾溶液摇匀。再加入5.0 mL双硫腙使用液(0.017 8 mg/mL),振荡,静置3 min。溶液分层后,三氯甲烷层经脱脂棉过滤进入10 mm比色皿中,试剂空白作参比溶液,分光光度计波长调至510 nm,测吸光度A。
2结果与分析
2.1波长的选择在125 mL分液漏斗中,加入0.3 mL铅标准使用液和19.80 mL硝酸,再加入1.0 mL盐酸羟胺、2.0 mL柠檬酸铵溶液和2滴酚红指示剂,用氨水调节pH为8.5,溶液呈现红色,之后多加1滴氨水,再加入2.0 mL氰化钾溶液摇匀。然后加入5.0 mL双硫腙使用液(0.017 8 mg/mL),振荡、静置,分层后,三氯甲烷层经脱脂棉过滤进入10 mm比色皿中,分光光度计用相应的试剂空白调节零点,每次改变10 nm波长,测其吸光度。由图1可知,在波长510 nm处,生成的红色络合物吸光度最大,故该试验选取波长为510 nm处作为测定最佳波长。
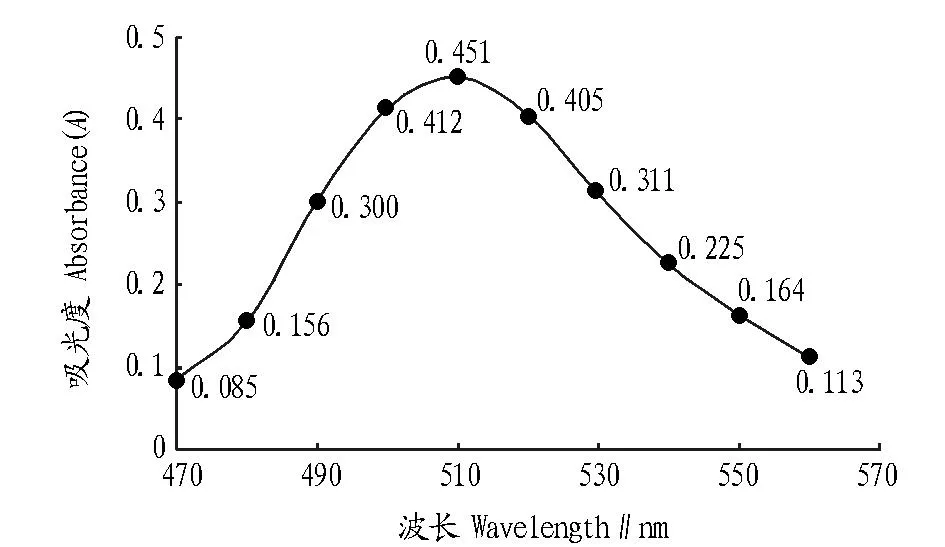
图1 吸光度随吸收波长变化曲线Fig.1 The change curve of absorbance with absorption wavelength
2.2显色时间及络合物的稳定性取0.3 mL铅标准使用液,按上述试验方法配制好溶液使其显色时间分别为1、2、3、5、7、10、20 min,并在波长510 nm处测其吸光度。从图2可知,当显色时间为3 min,吸光度达到顶峰,随着显色时间的继续延长,络合物的吸光度基本不变。故该试验固定显色时间为3 min。同时,将显色后的溶液放置24 h,再测其吸光度,吸光度基本不变,说明该络合物较为稳定。
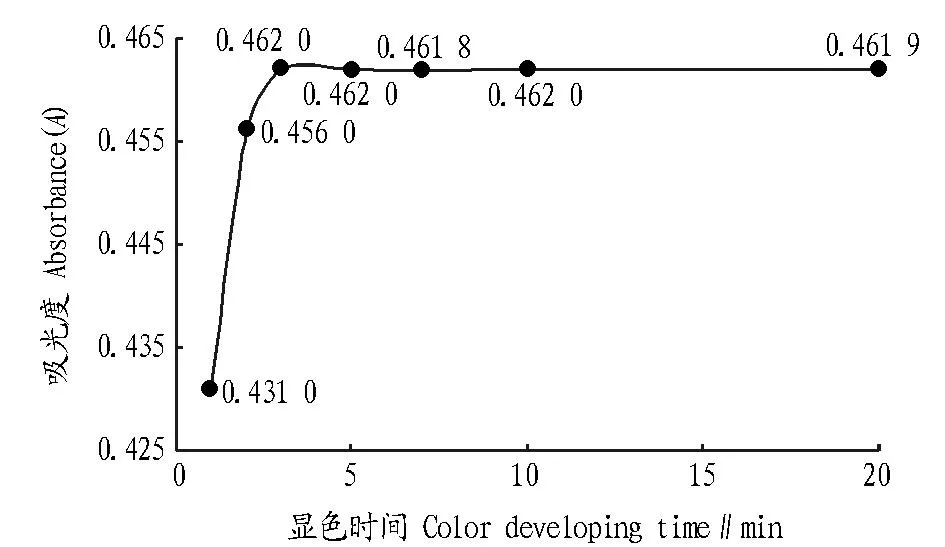
图2 吸光度随显色时间变化曲线Fig.2 The change curve of absorbance with color developing time
2.3酸度的选择分别汲取0.3 mL铅标准使用液,按上述方法生成络合物,用氨水调节其pH,使pH分别为7.0、7.5、8.0、8.5、9.0、9.5、10.0时,测定其吸光度。
由图3可知,当pH由小变大时,吸光度逐渐变大,当pH 8.5时,吸光度达到最大值,当pH偏大时,吸光度又会降低。故试验选择底液pH为8.5作为测定酸度。同时测定时,如果溶液呈酸性,加入氰化钾溶液时,会产生剧毒的氢氰酸,危害试验者的健康。
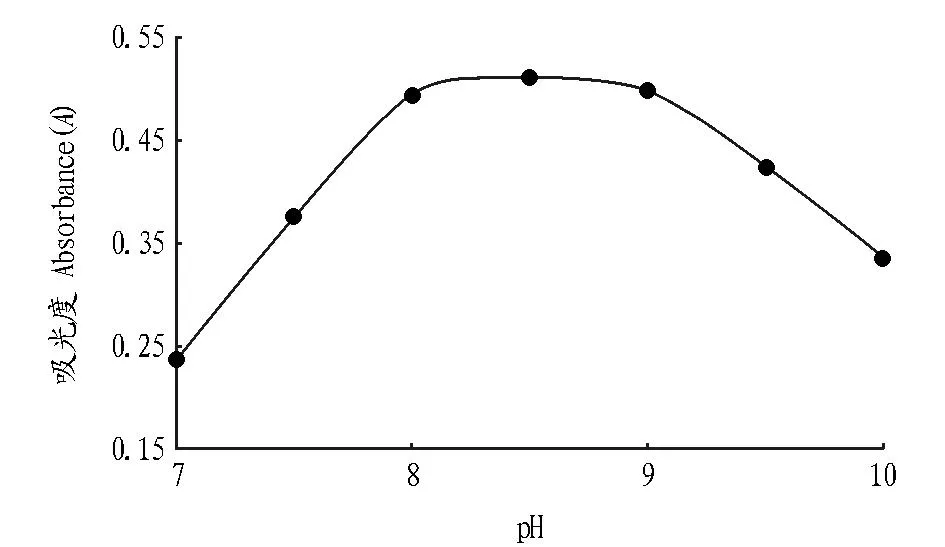
图3 吸光度随底液pH的变化曲线Fig.3 The change curve of the absorbance with the pH of bottom liquid
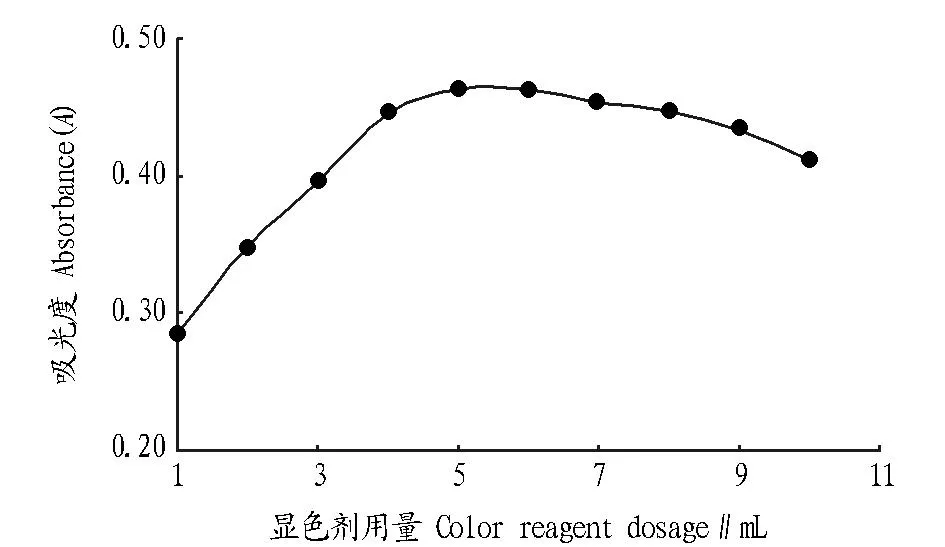
图4 吸光度与显色剂用量的关系Fig.4 Relationship between absorbance and the color reagent dosage
2.4显色剂用量的选择取0.3 mL铅标准使用液,按上述方法生成络合物,氨水调节pH为8.5,分别加入1.0、2.0、3.0、4.0、5.0、6.0、7.0、8.0、9.0、10.0 mL双硫腙使用液,显色3 min,在波长510 nm处测其吸光度。从图4可见,显色剂用量在5.0 mL时,吸光度最大。当显色剂用量过少时,显色不完全,吸光度较低;显色剂用量过多时,会少量稀释溶液的浓度,从而导致吸光度微弱较低。故该试验显色剂的最佳用量为5 mL。2.5标准曲线和检出限分别吸取0.1、0.2、0.3、0.4、0.5 mL铅标准使用液(铅含量相当于1、2、3、4、5 μg)用上述方法处理后,于波长510 nm处测其吸光度。
由图5可知,含铅量在1~5 μg的范围内与吸光度呈现良好的线性关系,线性回归方程为Y=1.419 7X+0.009 9,相关系数为R=0.999 4,其检出限为2.17×10-6mg/mL。
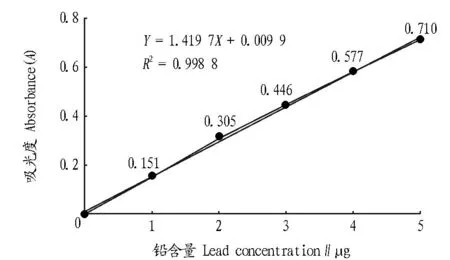
图5 铅的标准曲线Fig.5 Standard curve of divalent lead ion
2.6样品分析
2.6.1样品处理。干法灰化:称取5 g(根据铅含量而定)蔬菜样品于瓷坩埚中,先在电热板上小火炭化至无烟,移入马弗炉中,500 ℃灰化3 h,冷却后加入硝酸使灰分溶解,用50 mL容量瓶定容,摇匀备用。
2.6.2测定。吸取10 mL样品溶液置于分液漏斗中,加蒸馏水直到20 mL,分别加入柠檬酸铵、盐酸羟胺、酚红指示剂、氰化钾、双硫腙在最优条件下于波长510 nm处测吸光度,测得吸光度值之后,与标准曲线对应计算铅含量。
3结论与讨论
该研究通过分光光度法测定了蔬菜中的铅含量,试验表明,在波长510 nm处、络合显色3 min、pH为8.5等条件下,二价铅离子含量在1~5 μg的范围内与吸光度呈现良好的线性关系,其检出限为2.17×10-6mg/mL。基于铅与双硫腙形成的淡红色双硫腙铅络合物的作用,故对铅的检测显示较好的选择性和较高的灵敏度。试验研究了显色剂的选取、用量、显色时间以及酸度等因素,取得了较好的试验结果。此方法检测快速、准确度高,适合低浓度铅含量的检测,可以作为蔬菜中铅离子检测的方法之一。
参考文献
[1] 吴立水.关于双硫腙法测定重金属铅的几点体会[J].海峡预防医学杂志,2002,8(6):55-56.
[2] 宋纪蓉.双硫腙直接光度法测定人发中的铅[J].西北大学学报(自然科学版),1995,25(5):554-556.
[3] 石邦辉,孔祥生,康云华.双硫腙分光光度法测定水中微量铅的改进[J].中华预防医学杂志,2003,37(4):273-275.
[4] 张小军,王成,程军喜,等.双硫腙比色法测定食品中铅含量的影响因素[J].职业与健康,2008,24(17):1782-1783.
[5] 张铁涛,周宁海.双硫腙比色法测定海鱼中的汞含量[J].琼州学院学报,2012,19(2):19-22.
[6] 李瑞琴,于安芬,胡梅.芽菜中铅残留及食用安全性分析[J].北方园艺,2009(2):75-76
[7] 蔡艳荣,孙全敏.大孔树脂富集-火焰原子吸收法测定蔬菜中的铅和镉[J].科学技术与工程,2014,14(4):265-268.
[8] 马智玲,赵文,李凌云,等.气相色谱-三重四极杆串联质谱法快速测定蔬菜水果129种农药的残留量[J].色谱,2013,31(3):228-239.
作者简介徐守霞(1972-),女,江苏宿迁人,副教授,硕士,从事植物生理研究。
收稿日期2016-04-08
中图分类号S 481+.8
文献标识码A
文章编号0517-6611(2016)14-109-02
Detection of Lead Residues in Vegetables by Dithizone Method
XU Shou-xia1, WANG Bin2
(1.Department of Biology, Suqian Higher Normal School, Suqian, Jiangsu 223800; 2. The Third Department of Suqian College, Suqian, Jiangsu 223800)
Abstract[Objective] To detect the divalent lead ion residues in vegetable, and to provide references for the detection of heavy metal ion in vegetable. [Method] Dithizone spectrophotometry method was used to research the influence of the absorption wavelength, color reaction time, pH, color reagent dosage. And the experimental conditions were optimized. [Result] When the divalent lead ion content was in the range of 1 - 5 g, it had good linear relationship with absorbancy under the conditions of 510 nm, 3 min complex coloring time and pH 8.5. The detection limit was 2.17×10-6mg/mL. [Conclusion] Detecting divalent lead ion by dithizone spectrophotometry method can be applied to the determination of actual samples of vegetables.
Key wordsDithizone; Spectrophotometry; Divalent lead ion

