葡萄糖酸钠铁合成工艺优化及表征
马怡璇,王文婷,吴姣娇,潘红春*,刘 红*(西南大学药学院,重庆药物过程与质量控制工程技术研究中心,重庆 400715)
葡萄糖酸钠铁合成工艺优化及表征
马怡璇,王文婷,吴姣娇,潘红春*,刘 红*
(西南大学药学院,重庆药物过程与质量控制工程技术研究中心,重庆400715)
摘 要:通过监测葡萄糖酸钠铁合成反应过程变化,得出pH值对产物的含铁量及产量有显著影响。采用控制反应过程pH值来制备葡萄糖酸钠铁并考察比生成速率、含铁量、产率等参数,筛选出最优的反应工艺条件为控制反应过程pH 11.0反应2 h。结果得最大含铁量为29.9%,产率提升至129.12%,粒径减小了58.77%,反应时间缩短了33.33%。通过工艺结果比较,得出葡萄糖酸钠铁的合成是络合、分离再聚集的过程。表征分析验证了控制pH值条件下生成产物确为葡萄糖酸钠铁复合物,且络合铁特征不变。结果发现控制反应pH值可有效优化葡萄糖酸钠铁的制备工艺,实现高产量和高含铁量的统一,具有较高的应用价值。
关键词:葡萄糖酸钠铁;控制pH值;反应过程;比生成速率;优化
引文格式:
马怡璇, 王文婷, 吴姣娇, 等. 葡萄糖酸钠铁合成工艺优化及表征[J]. 食品科学, 2016, 37(12): 46-51. DOI:10.7506/ spkx1002-6630-201612008. http://www.spkx.net.cn
MA Yixuan, WANG Wenting, WU Jiaojiao, et al. Optimization of synthesis process and characterization of sodium ferric gluconate complex[J]. Food Science, 2016, 37(12): 46-51. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201612008. http://www.spkx.net.cn
缺铁性贫血是世界上常见的营养性疾病之一,长期以来主要以亚铁盐来进行治疗,但亚铁离子化学性质不稳定,易产生内源性自由基造成生物体损伤[1-3]。近年来,糖铁(Ⅲ)复合物作为新型营养型补铁剂的研究层出不穷,其不仅具有较高的络合稳定性,而且无游离铁所致的胃肠道刺激作用和由细胞膜脂质过氧化造成的细胞膜损伤,且当其释放铁之后,其糖配体具有多方面的生物活性[4-7]。相关研究如利用大枣、枸杞、金针菇、二色补血草等提取多糖制备糖铁(Ⅲ)复合物的文献[8-10]屡见报道。葡萄糖酸钠又称D-葡糖酸钠,由于其可调节人体内酸碱平衡,具有恢复神经正常作用,可有效防止低钠综合症的发生[11]。2012年,经我国卫生部许可,列入了新型食品添加剂目录,由于其较好的稳定性和螯合性能、原料来源广泛的特点,备受人们关注,一些新的制备技术与应用层出不穷[12]。
用D-葡糖酸钠作分子外壳有效吸附溶液中的金属铁离子形成稳定的配合物,可制备成葡萄糖酸钠铁口服营养型补铁剂[13-14],其稳定性较高,无毒副作用且工艺操作简便,而分析其动态反应过程是提高产量和优化工艺的关键。提高比生成速率是获得高产量行之有效的方法之一,对生产实践具有很大指导意义[15],本研究运用比生成速率、含铁量以及产率等来分析葡萄糖酸钠铁的络合过程,通过与前期制备工艺进行比较,探讨pH值对葡萄糖酸钠铁制备过程的重要性,并对其动态过程、工艺结果、表征性质等进行研究,进一步优化葡萄糖酸钠铁的制备工艺,提高其含铁量及产量。
1 材料与方法
1.1材料与试剂
D-葡糖酸钠(生物纯)、硅油、三氯化铁、无水碳酸钠、氢氧化钠、硫酸亚铁铵、抗坏血酸、乙酸钠、邻菲罗啉、乙醇、丙酮(均为分析纯)成都市科龙化工试剂厂。
1.2仪器与设备
DF-101s型集热式恒温加热磁力搅拌器郑州科丰仪器设备有限公司;BIOTECH-5JG-9000A 5L全自动发酵控制系统上海保兴生物设备有限公司;UV-1800型紫外-可见分光光度计上海美谱达仪器有限公司;Nano ZS90型马尔文激光粒度仪英国马尔文公司;200F3型差示扫描量热仪德国耐驰公司;IRPrestige-21型傅里叶变换红外光谱仪日本岛津公司;FE-20K实验室pH计、EL104电子天平梅特勒-托利多(上海)有限公司;DZF-6021型真空干燥箱苏州江东精密仪器有限公司;TGL-16M高速台式冷冻离心机长沙湘仪离心机仪器有限公司;78-1磁力加热搅拌器江苏金坛市易晨仪器制造有限公司;LH75G-4型超纯水机重庆浪华仪器设备有限公司。
1.3方法
1.3.1样品制备
1.3.1.1葡萄糖酸钠铁制备工艺
称取10 g D-葡糖酸钠溶于40 mL的超纯水中,室温条件下搅拌加入1.18 mol/L的Na2CO3溶液40 mL,混匀后置于磁力搅拌器上,再缓慢滴加1.25 mol/L的FeCl3溶液60 mL,并用5 mol/L的NaOH溶液调节pH 11.0。混合液于100 ℃油浴条件下回流搅拌反应3 h,过滤并将滤液冷却至室温。加入2倍体积的无水乙醇醇析4 h,4 000 r/min离心10 min,倾去上清液,沉淀真空干燥,得到葡萄糖酸钠铁粗制品[16-17]。10 mL超纯水溶解粗制品,加入2 倍体积的无水乙醇再次醇沉,过滤并收集沉淀物,用10 mL的无水乙醇、丙酮依次洗涤,真空干燥,得到葡萄糖酸钠铁精制品。
1.3.1.2不控制pH值对葡萄糖酸钠铁反应过程的监测
分别于0.5、1、1.5、2、3、4、5、6 h取样,以反应液的pH值和所得样品的含铁量、产率和比生成速率[15]为指标,监测当前工艺条件下葡萄糖酸钠铁6 h的反应过程,通过监测结果来阐明葡萄糖酸钠铁产物的生成规律[18]。
1.3.1.3控制pH值对葡萄糖酸钠铁反应过程的影响
调节140 mL混合液的起始pH 11.0,采用能监测和控制pH值的发酵罐pH值自动控制系统,以5 mol/L的NaOH溶液分别控制反应溶液的pH值为10.5、11.0、11.5,分别于0.5、1、1.5、2、3、4、5、6 h取样,以所得样品的比生成速率、含铁量、产率和反应时间为指标[18-21],考察控制不同pH值反应6 h过程内的产物变化情况,并对最优点进行比较,筛选出最优的反应pH值控制条件。
1.3.1.4不控制pH值与控制pH值(pH 11.0)的对比分析
通过比较6 h内不控制与控制pH值的反应过程,分析不同时间所得产物的粒径和Zeta电位,得出葡萄糖酸钠铁生成变化规律,并通过表征实验比较两种条件下获得的络合产物性质。
1.3.2样品指标测定与表征
1.3.2.1含铁量测定[22]
采用邻菲罗啉分光光度法测定含铁量,在510 nm波长处测定吸光度,根据标准曲线方程Y=0.197 66X+0.010 53(R2= 0.999 5)换算出样品的含铁量。
1.3.2.2产率及比生成速率计算[18-19]

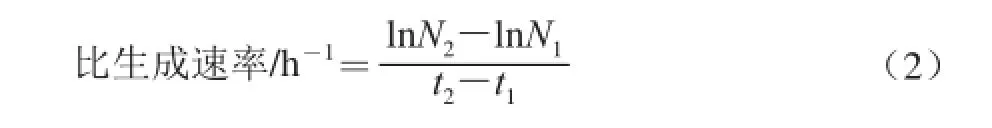
式(2)中:N2为第2次取样时(t2)的葡萄糖酸钠铁质量/g;N1为第1次取样时(t1)的葡萄糖酸钠铁质量/g;t1、t2分别为第1次和第2次取样时间/h。
1.3.2.3粒径及Zeta电位测定
用马尔文激光粒度仪测定葡萄糖酸钠铁的粒径、Zeta电位。
1.3.2.4还原性实验
采用邻菲罗啉比色法[23]对不控制和控制pH值(pH 11.0)条件下所得葡萄糖酸钠铁产物进行还原性实验。精密称取0.1 g样品溶于纯水中,并定容至100 mL容量瓶。分别精密吸取1 mL样品依次移入6 个相同型号的50 mL容量瓶,并调节pH值为3、5、7各两瓶,分别加入5 mL 10 g/L的抗坏血酸溶液和3 mL 1 g/L的邻菲罗啉溶液,加纯水定容并摇匀,37 ℃水浴条件下进行还原反应。以空白试剂为对照,取不同时间点的反应液在510 nm波长处测定吸光度,考察样品5 h内还原性。
1.3.2.5差示扫描量热分析
用差示扫描量热仪对D-葡糖酸钠、三氯化铁、葡萄糖酸钠铁进行差热分析。实验条件为氮气氛,升温速率10 ℃/min,测定量程30~500 ℃。
1.3.2.6红外光谱分析
用傅里叶红外光谱仪测定D-葡糖酸钠、葡萄糖酸钠铁的红外光谱。采用KBr压片,扫描波数范围4 000~400 cm-1。
2 结果与分析
2.1不控制pH值对葡萄糖酸钠铁反应过程的影响

图1 不控制pH值条件下葡萄糖酸钠铁的反应过程变化曲线Fig. 1 Reaction process curves of sodium ferric gluconate complex
反应溶液pH值从起始11.0迅速下降到10.3,0.5 h后呈缓慢下降趋势(图1A)。含铁量随pH值的下降而缓慢增大(图1B),约4 h时达最大值28.20%,然后缓慢减小。产率先随pH值的下降而下降,1.5 h后回升而3 h时又下降。可见整个变化趋势不稳定,铁离子与糖分子处于络合、解离再络合的过程,产率两次降低可能是解离后的糖分子溶于水导致产物产量减少,而随反应时间延长糖分子又聚集,葡萄糖酸钠铁中含糖量增大而使产率虚高,因此无法得到始终均一的稳定络合产物,难以选择工艺最优点。如图1A所示,反应比生成速率在1 h达到-0.271 8 h-1,然后随时间延长比生成速率下降,在1.5~2 h回升并达到最大值0.273 7 h-1后,同图1B出现下降上升的不稳定变化趋势,反应比生成速率偏低,说明随着pH值逐渐降低反应微环境不再稳定。因此,考虑需要控制pH值来维持最大比生成速率,这样可以缩短反应时间,提高反应强度[18]。
2.2控制pH值对葡萄糖酸钠铁反应过程的影响

图2 不同pH值控制条件下比生成速率过程曲线(A)以及pH值对最大比生成速率的影响(B)Fig. 2 Time courses of specific production rate with pH controlled at different levels (A) and effects of pH on maximal specific production rate (B)
如图2A所示,在反应进行前2 h,pH 11.0的比生成速率逐渐增大,高于其他条件下的比生成速率,2 h后比生成速率逐渐下降到稳定状态,提前结束反应进程,而pH值在10.5和11.5的比生成速率呈现上升下降的不规则变化。比较控制不同pH值条件下的最大比生成速率,如图2B所示,随着pH值升高,最大比生成速率迅速增加,pH 11.0时达到最大值0.360 8 h-1,然后随pH值的升高迅速减少,pH 11.5时为0.314 7 h-1。由此可见,控制pH 11.0进行反应可获得最大比生成速率。
选取控制不同pH值条件下反应最大比生成速率为最优点,进行葡萄糖酸钠铁含铁量、产率、反应时间、粒径及Zeta电位5 个参数的对比分析,如表1所示,以不控制pH值为对照,最大比生成速率为0.360 8 h-1时获得最大含铁量和产率,反应时间缩短了33.33%,得出最优的反应工艺条件为控制反应过程pH 11.0反应2 h,此时含铁量可达到最大值29.90%。
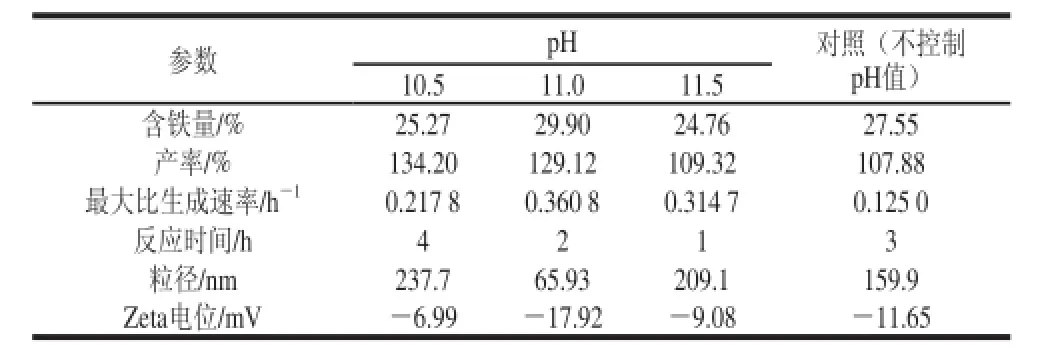
表1 控制不同pH值条件下的最优点结果比较Table 1 Comparison of the best results at different controlled pH values

图3 控制pH值条件下含铁量和产率变化曲线Fig. 3 Curves of iron content and yield with pH control
如图3所示,监测了控制反应过程pH 11.0的产物含铁量和产率的变化曲线,发现含铁量随时间的延长而增大,很快在1 h左右达到最大值,接着随时间延长缓慢下降,而产率近似与含铁量呈反比,可能是由于长时间的反应使糖分子逐渐聚集,葡萄糖酸钠铁中含糖量增大而含铁量降低导致产率虚高[19]。对比不控制pH值所得产物,含铁量最大增加8.53%,产率最大提升19.69%,整个变化趋势相对稳定,无很大波动,说明铁离子与糖的络合程度高,产物分布较为均匀,因此,选择含铁量和产率都较高的控制pH 11.0反应2 h作为工艺最优点是有依据的,可以缩短反应延滞期,减少反应时间,提高产量。
2.3不控制pH值与控制pH值(pH 11.0)的对比分析
2.3.1粒径和Zeta电位随时间变化对比
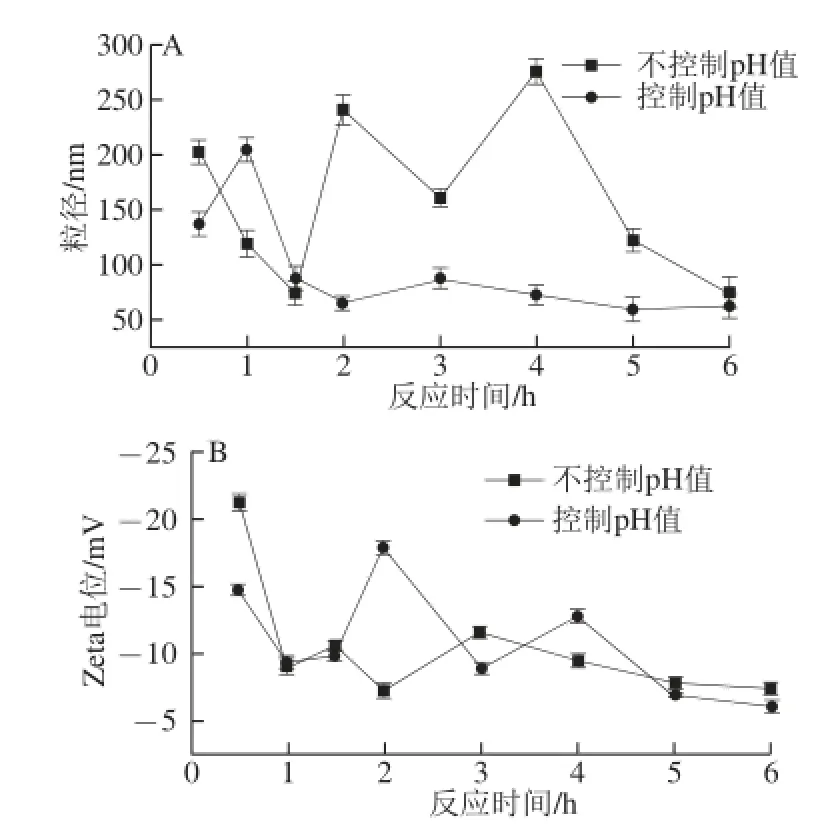
图4 不控制与控制pH值条件下粒径(A)以及Zeta电位(B)的变化Fig. 4 Changes in particle size (A) and Zeta potential (B) without or with pH control
如图4A所示,不控制pH值条件下粒径先随时间的延长而减小,1.5 h时开始增大,2 h后又减小,4 h时达到最大粒径276 nm左右后缓慢下降,发现其变化程度大且粒径都偏大。控制pH值条件下粒径先随时间的延长快速增大,1 h左右粒径达到最大粒径205 nm,然后随时间延长下降并趋于稳定至65 nm左右,发现其变化趋势稳定,并随含铁量的变化而变化,且粒径相对偏小。如图4B所示,不控制pH值条件下Zeta电位先随时间的延长从-21.31 mV迅速下降,1 h后出现上升和下降的不规则变化,3 h达-11.65 mV然后缓慢下降至稳定趋势,发现其变化程度大且数值都偏小。控制pH值条件下Zeta电位也先随时间的延长而下降,1.5 h后回升并在2 h时达到最大值-17.92 mV,然后下降至稳定趋势,说明控制pH值反应体系更加稳定,络合程度较高。
结合表1中最优点所得结果发现,不控制pH值反应中含铁量取最大值时,产率较小,粒径偏大;反之亦然,则很难获得工艺最优点,且整个反应是一个不断变化的过程,络合程度波动大,产物均一性不好,由于pH值不断下降反应很难平稳进行,说明不控制反应pH值对产物结构、生成速率以及反应微环境影响很大,从而影响产物的含铁量及产量,因此,需控制反应过程的pH值。控制pH 11.0反应2 h所得产物的含铁量和产率都较高,而粒子的粒径(65.93 nm)相比减小了58.77%,Zeta电位绝对值最大(17.92 mV),反应体系相对稳定,可选作工艺所需最优点。
综上所述,葡萄糖酸钠铁反应过程是个络合、分离再聚集的过程,随着反应时间的延长,产物含铁量和粒径增大,铁离子与糖分子高度络合,反应体系相对稳定,然后随着长时间反应铁离子发生解离,含铁量下降,随后糖分子开始发生凝聚,使产率虚高,直到最后粒子趋于稳定,整个产物微环境不再变化。
2.3.2还原性实验结果

图5 葡萄糖酸钠铁与抗坏血酸反应体系的吸光度-时间曲线Fig. 5 A-t curves of the reaction system between sodium ferric gluconate complex and vitamin C
由图5可知,控制pH值和不控制pH值所得产物中的铁皆可被还原剂还原,无明显区别,1 h左右几乎可全部溶出,可见其具有良好的溶出还原性能,说明葡萄糖酸钠铁作为口服补铁剂可被食物中的还原性物质(抗坏血酸)将三价铁还原成二价铁后被机体吸收,有较好的生物利用度,且因溶液中无游离的铁离子存在,所以应无明显的消化道刺激作用。
2.3.3差示扫描量热分析
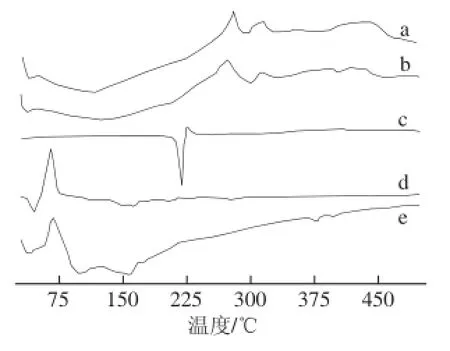
图6 差示扫描量热分析Fig. 6 DSC curves
用差示扫描量热仪分析最优反应工艺条件下的葡萄糖酸钠铁,结果如图6所示,D-葡糖酸钠在214.9 ℃有1个明显的吸热峰,三氯化铁在65 ℃有一个明显的放热峰,三氯化铁和D-葡糖酸钠物理混合也在65 ℃左右有1个明显的放热峰,但在214.9 ℃左右没有吸热峰,可能是由于糖量太少所致。而曲线a、b在270、320 ℃左右皆有2 个新的放热峰,说明形成了新的物质葡萄糖酸钠铁,两者的放热峰峰形较好,产物的热稳定性较高[24],也反映了控制pH值对产物性质没有影响。
2.3.4红外光谱分析
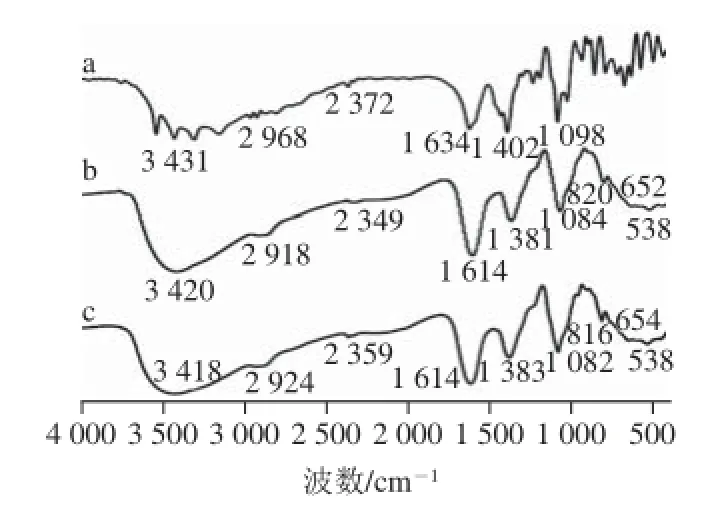
图7 红外光谱图Fig. 7 IR spectra
用红外光谱仪分析最优反应工艺条件下的葡萄糖酸钠铁,如图7所示,各曲线皆含有1 个—OH的伸缩振动吸收峰(3 400 cm-1左右)和H—O—H的变形振动吸收峰(1 640~1 400 cm-1处),铁离子未使D-葡糖酸钠的结构发生明显改变。控制pH值条件下产物的结构特征峰峰值位于820、652、538 cm-1处,不控制pH值条件下产物的结构特征峰峰值位于816、654、538 cm-1处,这与文献[25-26]报道的β-FeOOH的特征吸收峰均位于900~420 cm-1范围内相一致,说明形成了新的物质葡萄糖酸钠铁。而不控制与控制pH值(pH 11.0)条件下产物特征峰的透光率大致相同,表明控制pH值条件对产物络合铁特征无影响。
3 结 论
本实验以D-葡糖酸钠和三氯化铁为原料制备葡萄糖酸钠铁,通过监测不控制pH值与控制pH值对反应过程的影响,阐明葡萄糖酸钠铁产物的生成规律。特别运用比生成速率,结合含铁量和产率得出最优的反应工艺条件为控制反应过程pH 11.0反应2 h,与前期制备工艺相比,含铁量获得最大值29.9%,产率提升至129.12%,粒径减小了58.77%,反应时间缩短了33.33%。通过工艺结果对比和表征分析,得出葡萄糖酸钠铁动态反应是络合、分离再聚集的过程,也验证了控制pH值条件下生成产物确为葡萄糖酸钠铁复合物,稳定性较高且络合铁特征不变。本实验证明了pH值对产物含铁量及产量产生显著影响,控制pH值可有效优化葡萄糖酸钠铁的制备工艺,其也可应用于其他复合铁的制备,具有较高的应用价值,为铁制剂的开发开拓思路。
参考文献:
[1] AUERBACH M, GOODNOUGH L T, SHANDER A. Iron: the new advances in therapy[J]. Best Practice and Research Clinical Anaesthesiology, 2013, 27(1): 131-140. DOI:10.1016/ j.bpa.2012.12.001.
[2] 展筱林, 王凤山, 王京端, 等. 缺铁性贫血治疗药物研究进展[J].齐鲁医学杂志, 2008, 23(5): 467-468; 470. DOI:10.11712/ qlyx200805046.
[3] KOSKENKORVA-FRANK T S, WEISS G, KOPPENOL W H, et al. The complex interplay of iron metabolism, reactive oxygen species, and reactive nitrogen species: insights into the potential of various iron therapies to induce oxidative and nitrosative stress[J]. Free Radical Biology and Medicine, 2013, 65: 1174-1194. DOI:10.1016/ j.freeradbiomed.2013.09.001.
[4] MITSUOKA T. Development of functional foods[J]. Bioscience of Microbiota, Food and Health, 2014, 33(3): 117-128. DOI:10.12938/ bmfh.33.117.
[5] CANCADO R D, MUNOZ M. Intravenous iron therapy: how far have we come?[J]. Revista Brasileira de Hematologia e Hemoterapia, 2011, 33(6): 461-469. DOI:10.5581/1516-8484.20110123.
[6] 汤春妮. 多糖铁复合物的研究进展[J]. 安徽化工, 2012, 38(4): 1-3; 6. DOI:10.3969/j.issn.1008-553X.2012.04.001.
[7] KOWALCZYK M, BANACH M, RYSZ J. Ferumoxytol: a new era of iron deficiency anemia treatment for patients with chronic kidney disease[J]. Journal of Nephrology, 2011, 24(6): 717-722. DOI:10.5301/ jn.5000025.
[8] 赵兵, 徐清海. 枸杞多糖铁(Ⅲ)配合物的合成及理化性质的初步研究[J]. 中成药, 2008, 30(8): 1245-1246. DOI:10.3969/ j.issn.1001-1528.2008.08.054 .
[9] 马利华, 秦卫东, 陈学红, 等. 金针菇多糖-Fe(Ⅱ)螯合物的制备及抗氧化活性[J]. 食品科学, 2010, 31(20): 202-207.
[10] 李琳, 李稳宏, 雒羽, 等. 二色补血草多糖铁(Ⅲ)配合物的制备及理化性质研究[J]. 食品科学, 2012, 33(16): 54-58.
[11] 韩延雷, 范宜晓, 赵晨, 等. 中国葡萄糖酸钠行业市场及发展[J]. 山东食品发酵, 2013(3): 36-39.
[12] 董贞, 张百胜, 典姣姣, 等. 食品级葡萄糖酸钠制备及应用的研究进展[J]. 食品工业, 2014, 35(9): 242-245.
[13] KUDASHEVA D S, LAI J, ULMAN A, et al. Structure of carbohydrate-bound polynuclear iron oxyhydroxide nanoparticles in parenteral formulations[J]. Journal of Inorganic Biochemistry, 2004, 98(11): 1757-1769. DOI:10.1016/j.jinorgbio.2004.06.010.
[14] 毛凯, 马怡璇, 潘红春, 等. 新型静脉补铁剂的研究进展[J]. 中国新药杂志, 2015, 24(6): 659-663.
[15] 唐晓阳, 郭晓滨, 郭丹凤, 等. 高通量快速测定致病性及非致病性副溶血性弧菌最大比生长速率[J]. 微生物学通报, 2013, 40(11): 2138-2144. DOI:10.13344/j.microbiol.china.2013.11.017.
[16] 毛凯, 杨琴, 刘丽, 等. 低聚异麦芽糖铁配合物的制备工艺优化[J]. 食品科学, 2014, 35(22): 22-27. DOI:10.7506/spkx1002-6630-201422005.
[17] 杨树平, 韩立军, 邱燕华, 等. 向日葵茎髓多糖铁配合物的制备工艺[J].食品科学, 2012, 33(20): 61-64.
[18] 曾勇峰. 新型抗菌物质CF66I发酵工艺的优化及动力学的研究[D].大连: 大连理工大学, 2006.
[19] 毛凯, 李丹, 吴姣娇, 等. pH值过程控制优化低聚异麦芽糖铁配合物的制备工艺[J]. 食品科学, 2015, 36(16): 56-60. DOI:10.7506/ spkx1002-6630-201516010.
[20] 翁宋生. L-苏氨酸发酵条件优化及其动力学研究[D]. 福州: 福建师范大学, 2012.
[21] 潘红春, 刘红, 程永刚, 等. 聚乙二醇修饰重组人干扰素ω的过程优化[J]. 化工学报, 2011, 62(10): 2876-2884. DOI:10.3969/ j.issn.0438-1157.2011.10.028.
[22] 李玉贤, 游志恒, 褚意新. 百合多糖铁复合物的合成及其铁含量的测定[J]. 中国实验方剂学杂志, 2010, 16(7): 47-49. DOI:10.3969/ j.issn.1005-9903.2010.07.016.
[23] 李琳, 李稳宏, 雒羽, 等. 二色补血草多糖铁(Ⅲ)配合物的制备及理化性质研究[J]. 食品科学, 2012, 33(16): 54-58.
[24] 张新娜, 孙君社, 王淑豪, 等. 羧甲基壳聚糖亚铁配合物的表征及其对CO的吸附研究[J]. 高校化学工程学报, 2011, 25(1): 91-95.
[25] WEI C, NAN Z. Effects of experimental conditions on onedimensional single-crystal nanostructure of β-FeOOH[J]. Materials Chemistry and Physics, 2011, 127(1/2): 220-226. DOI:10.1016/ j.matchemphys.2011.01.062.
[26] 徐轶群, 杨明, 何成达, 等. 铁的氢氧化合物稳定相α,β-FeOOH的表征及光谱分析[J]. 光谱学与光谱分析, 2013, 33(12): 3330-3333. DOI:10.3964/j.issn.1000-0593(2013)12-3330-04.
Optimization of Synthesis Process and Characterization of Sodium Ferric Gluconate Complex
MA Yixuan, WANG Wenting, WU Jiaojiao, PAN Hongchun*, LIU Hong*
(Chongqing Engineering Research Center for Pharmaceutical Process and Quality Control, College of Pharmaceutical Sciences, Southwest University, Chongqing400715, China)
Abstract:By monitoring the synthetic reaction of sodium ferric gluconate complex, pH value was found to have a significant impact on the iron content and yield of product. Under controlled pH conditions, specific production rate, iron content and yield of sodium ferric gluconate complex were investigated. The maximum iron content of 29.9% and the maximum yield of 129.12% were obtained when the reaction proceeded for 2 h with pH controlled at 11.0. Meanwhile, a 58.77% reduction in the particle size of sodium ferric gluconate complex as well as a 33.33% decrease in reaction time was found compared to that without pH control. Comparative analysis revealed that the synthetic reaction of sodium gluconate iron complex was a process involving complexation, separation and re-aggregation. The results of characterization confirmed the product under controlled pH condition to be sodium ferric gluconate complex with no change in iron-chelating capacity. Therefore, it has been found that pH control provides an effective and applicable approach towards the optimization of the preparation process of sodium ferric gluconate complex for achieving high yield and iron content simultaneously.
Key words:sodium ferric gluconate complex; pH control; reaction process; specific production rate; optimization
收稿日期:2015-10-19
基金项目:重庆市制药过程与质量控制工程技术研究中心能力提升项目(CSTC2012gg-yyjsb10002-33);西南大学博士基金项目(SWU110056;SWU110057)
作者简介:马怡璇(1992—),女,硕士研究生,研究方向为药物新制剂。E-mail:ma_yixuan0108@sina.com
*通信作者:潘红春(1966—),女,教授,博士,研究方向为药物新制剂及其质量。E-mail:panhongchun216@126.com 刘红(1965—),男,教授,博士,研究方向为药物制备过程。E-mail:lhphch@126.com
DOI:10.7506/spkx1002-6630-201612008
中图分类号:R914.1
文献标志码:A
文章编号:1002-6630(2016)12-0046-06

