数学思想在高中化学解题中的应用
熊蕾
新课程标准中,课程目标明确要求重视化学与其他学科之间的联系,能综合运用有关的知识、技能与方法分析和解决一些化学问题。作为理科的化学和数学有着密切的联系,若巧妙利用数学思想来解决一些化学问题,会轻松很多。
一、数列
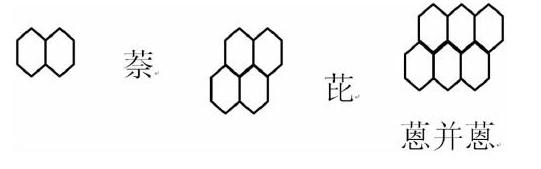
例1:沥青中存在一系列稠环芳香烃
(1)这一系列稠环芳香烃的通式为。
(2)从萘开始,这一系列稠环芳香烃中第25个的分子式为。
(3)随着n值的增大,这一系列稠环芳香烃的含碳量增加,含量以为极限。
解析:(1)首先确定以上三个物质的分子式:C10H8、C16H10、C22H12,再利用数学中等差数列知识:an=a1+(n-1)d,碳原子数an=10+6(n-1)=6n+4,氢原子数an=8+2(n-1)=2n+6,因此,这一系列稠环芳香烃的通式为:C6n+4H2n+6(n>1)。
(2)第25个稠环芳香烃的分子式为:C6×25+4H2×25+6即C154H56。
(3)利用函数法求12(6n+4)/[12(6n+4)+(2n+6)]的最大值(见下文例5)。
二、不等式
不等式法关键是根据题意,挖掘隐含条件,列出不等式。
例2:某CO、C2H4、O2混合气体,平均摩尔质量为30.4,点燃,充分反应后,混合气体中不再有CO、C2H4,试求原混合气体中各气体的体积分数范围(在同温同压下测定)。
解析:首先用“十字交叉法”求出CO、C2H4混合组分与O2的体积比为2 ∶ 3,则原混合气体中ω(O2)=60%;接着,建立不等式求出CO、C2H4的体积分数范围。
设原混合气体5L,则V(O2)=3L,设V(CO)=xL,V(C2H4)=(2-x)L。
x/2+3(2-x)≤3(O2过量),解得1.2L≤x。
又2-x>0,所以1.2L≤x<2L。
即:24%≤ω(CO)<40%,0<ω(C2H4)≤16%。
三、欧拉定律
不同的晶体具有不同的空间结构,多面体的顶点数、面数、棱边数遵循欧拉定律,即顶点数+面数-棱边数=2。
例3:晶体硼的基本结构单元是由硼原子组成的正二十面体的原子晶体,每个面为等边三角形,每个顶点有一个硼原子,请问:这个基本结构单元由个硼原子组成。
解析:根据欧拉定律,列式:硼原子数+20-20×3÷2=2。
即解得硼原子数为12。
四、极值法
例4:已知相对原子质量:Li:6.9,Na:23,K:39,Rb:85。今有某碱金属R及其氧化物R2O组成的混合物10.8g,加足量水充分反应后,溶液经蒸发和干燥得固体16g,据此可金属R是( )
A. Li B. Na C. K D. Rb
解析:设此碱金属的相对原子质量为M,依题意:10.8g混合物由R和R2O组成,采用极端假设法。
假设全是R,则生成的ROH为:10.8g/Mg·mol-1=16g/(M+17)g·mol-1,解得M=35.3。
假设全是R2O,则生成的ROH为:2×10.8g/(2M+16)g·mol-1=16g/(M+17)g·mol-1,解得M=10.7。但10.8g为R和R2O的混合物,所以10.7 五、函数 根据题目涉及的化学反应方程式,建立量的函数表达式解题。 例5:例1第(3)小题,求(6n+4)/[12(6n+4)+(2n+6)]的最大值。 解析:f(n)=12(6n+4)/[12(6n+4)+(2n+6)]=(72n+48)/(74n+64) 当n值为∞时,f(n)有最大值,f(n)max=72/74=97.3%。 六、分析推理 有些计算型选择题看上去数据多、计算繁琐,但可能不需计算,直接利用化学原理进行分析、推理就可解出。关键是认真审题、分析,理清思路,抓住原理,附加简单计算,即可得出正确答案。 例6:锌粉、铝粉、镁粉的混合物44g与一定量质量分数为17.25%的硫酸溶液恰好完全反应,将溶液蒸干,得无水固体140g,则放出的气体在标况下的体积为( ) A. 22.4L B. 33.6L C. 6.72L D. 无法求解 解析:很多学生会考虑设三种金属的物质的量,用方程组求解而误入歧途,最后只能选D。 若从数值特征上把握,从三种金属混合物44g到无水固体140g,增加的恰是SO42-的质量,为96g,即1mol,又知恰好完全反应,则产生的H2也是1mol,所以A项正确。 责任编辑 罗 峰

