氯对饮用水中可同化有机碳的影响
吴炜玮,陈嘉珮,董秉直(.同济大学环境科学与工程学院,上海 200092;2.同济大学长江水环境教育部重点实验室,上海 200092)
氯对饮用水中可同化有机碳的影响
吴炜玮1,陈嘉珮1,董秉直2*(1.同济大学环境科学与工程学院,上海 200092;2.同济大学长江水环境教育部重点实验室,上海 200092)
摘要:通过分析太湖水的分子量分布变化以及亲疏组分,考察氯反应生成AOC的效果和机理.结果表明,弱疏组分的AOC生成量最大,其次为强疏,中亲和带负电亲水的生成量最少.氯主要与小分子的疏水性有机物反应,AOC的生成量最多.通过考察深度处理工艺的有机物分子量以及组分的变化,发现疏水性有机物呈逐渐下降而亲水性组分呈上升的趋势,表明氯化产生的AOC呈减少趋势.小分子的疏水性有机物是主要的氯化AOC的前体物.
关键词:饮用水;可同化有机碳;前体物;氯化
* 责任作者, 教授, dongbingzhi77@126.com
臭氧生物活性炭是目前国内应用最为广泛的深度处理工艺.针对深度处理工艺的效果和机理所开展的大量研究得出的较为一致的结论是,臭氧和氯的氧化均使AOC增加,而生物活性炭可有效去除AOC,因而深度处理工艺可保证出水的生物稳定性[1-4].但是,仍有一些问题尚不清楚.研究表明,活性炭出水经氯消毒,AOC仍然增加[5-6].这表明AOC前体物,即与氧化剂反应产生AOC的有机物仍存在于深度处理的出水中,影响管网的生物稳定性.有研究致力于了解不同的氧化剂产生AOC的作用以及机理[7-8].许多研究表明,氯消毒会明显增加AOC浓度,原水经过预处理、常规处理和深度处理后AOC满足世界卫生组织(WHO)的《饮用水水质准则》(不加氯时AOC<10µg乙酸碳/L),但出水经氯消毒后AOC迅速增加,有的甚至超过原水AOC浓度,使出厂水AOC处于生物稳定性临界区间[9-10].因此,了解氯消毒产生AOC的规律和机理,特别是AOC的前体物,从而降低氯消毒工艺增加的AOC浓度,保障管网的生物稳定性.但是,很少见到有关这方面的报道.
本论文主要以东太湖原水作为研究对象,考察氯与有机物反应的动力学原理、不同工况(反应时间和投加量)对AOC变化的影响以及AOC的前体物.
1 材料与方法
1.1 水质
试验水样取自苏州太湖渔洋山取水口,DOC = 3.065mg/L,UV254= 0.059cm-1,SUVA =1.91L/ (mg·m).
1.2 AOC的测定
AOC的测定采用先后接种法[11-12],测试菌种为荧光假单胞菌(Fluorescent pseudomonads)P17和螺旋菌(spirillum)NOX.试验前先对取样或培养用的器皿按APHA《水和废水检验标准方法》进行无碳化处理,以避免有机碳污染对测定结果产生影响[13].水样经巴氏灭菌并冷却后,按照10000CFU/mL的接种浓度接种P17,在25℃的条件下黑暗静置培养3d后,对水样中的P17进行细菌平板计数.然后水样在70℃的水浴锅中巴氏灭菌30min以杀死水样中的P17,冷却后按照10000CFU/mL的接种浓度接种NOX,在25℃的条件下黑暗静置培养4d后,对水样中的NOX进行细菌平板计数.本研究对P17和NOX的产率系数进行了测定,Y(P17)=4.68×106CFU/µgC, Y(NOX)=1.43×107CFU/µgC.AOC的计算公式如下:

1.3 亲疏水性有机物的分离
水样经0.45µm 滤膜过滤,固相萃取的水样经反渗透浓缩后,用5mol/L的盐酸调节pH至2.0,通过XAD 大孔径吸附树脂(Supelite DAX-8、Amberlite XAD-4)和阴离子交换树脂(Amberlite IRA-958)[14-15].采用0.1mol/L的NaOH洗脱DAX-8树脂和XAD-4树脂,分别得到强疏水性组分(HPO)和弱疏水性组分(TPI),采用0.1mol/L浓度的NaOH和NaCl洗脱IRA-958树脂,得到带负电亲水性组分(C-HPI),未被任何树脂吸附的为中性亲水性组分(N-HPI).回收率均控制在80%~120%.
水样的亲疏水比例如表1所示.

表1 水样亲疏水组分比例(%)Table 1 Hydrophobicity proportion of the water samples (%)
1.4 氯消耗曲线
将原水浓缩亲疏水分离后将各组分DOC调节至10(±0.5)mg/L,pH=7,氯投加量为1.5mg/L(过量).水样采用磁力搅拌器控制转速,先以2500r/ min的转速快速搅拌氧化30s,随后以400r/min的转速缓慢反应.从开始向反应器加入NaClO即开始计时,在t = 0,0.5, 1,1.5,2,3,5,7,10,15,20,30, 60min时,从反应器取样口接取水样,并测定其该时刻的余氯浓度,最后绘制出余氯浓度-时间消耗曲线.
1.5 影响AOC因素的试验
1.5.1 反应时间 准备7个250mL锥形瓶并编号,均加入250mL太湖原水(DOC=3.065mg/L).将锥形瓶放在磁力搅拌器上,转速400r/min.水样中加入1.5mg/LNaClO的同时开始计时,分别在0.5,1,2,5,10,30,60min时向1~7号锥形瓶中依次加入过量Na2S2O3(1:1.2)同时将转速调为2500r/min,迅速混合并终止反应.重复3次,测定AOC.
1.5.2 投加量 按同样方法测定氯投加量为1.5,3.0和4.5mg/L以及反应时间为30min和6h时的AOC.
1.6 亲疏水组分AOC前体物
将原水浓缩亲疏水分离后将各组分DOC调至3.5(±0.5)mg/L,pH=7,氯投加量为1.5mg/L,反应时间为5min和30min.由于XAD-8树脂不能吸附无机盐,巴氏灭菌前需在强疏和弱疏组分中补加矿物盐.
1.7 有机物分子量的测定
采用HPSEC-UV-TOC系统测定分子量分布,并用分峰软件PeakFitv4.12处理凝胶色谱图.大分子的分子量大于10000,中分子的分子量为1000~10000,小分子的分子量小于1000.
2 结果与讨论
2.1 反应时间和投加量的影响
2.1.1 余氯随反应时间的变化 有机物各组分与氯反应的余氯消耗情况如图1所示.由图可知, 在DOC相同的条件下,疏水性组分的余氯减少程度明显高于亲水性组分,表明氯更容易与疏水性组分反应.
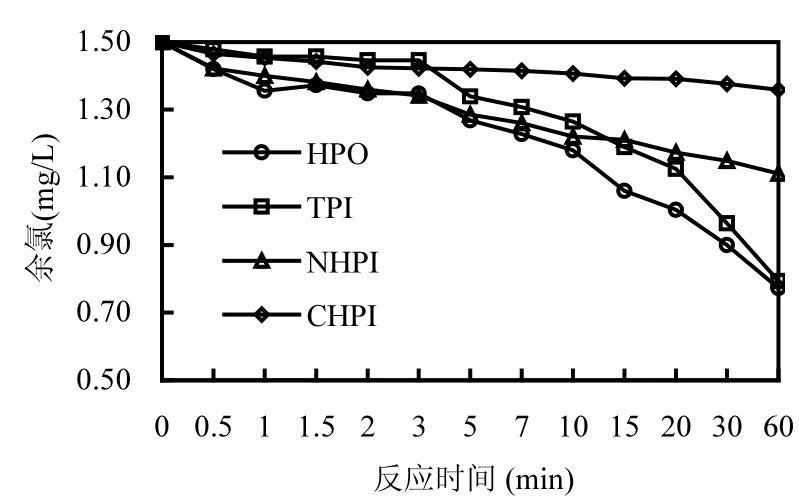
图1 亲疏水组分氯消耗变化Fig.1 Consumption kinetics of chlorine for HPO, TPI, NHPI and CHPI fractionated from the raw water
2.1.2 反应时间对AOC生成和分子量分布的影响 图2为氯反应时间对AOC生成的影响.水样的初始AOC浓度为51µgC/L,其中AOCP17为45µgC/L,占88.7%,AOC-NOX为6µgC/L, 占11.3%.由图2可见,加氯后的AOC生成量随时间逐渐增加,1min时达到67µg/L,随后下降到52µg/L,在5min时又迅速上升最高值,随后缓慢下降.P-17生成量随时间变化与AOC几乎完全一致,而NOX生成量随时间缓慢增加,在5min时达到最高值,而后缓慢下降.研究表明AOC的生成与小分子有机物密切相关[15],我们继而考察氯与原水反应时的有机物分子量变化,如图3所示.反应初始,大分子有机物增加,表明氯将悬浮性有机物转化成溶解性的.氯同时氧化小分子和中分子,导致它们的减少,由于溶解性大分子逐渐增加,而中小分子也逐渐增加,这反映了大分子有机物先转化成中分子继而转化为小分子的过程,小分子的增加导致AOC的增加.当大分子达到最大时,小分子也达到了最大值,不清楚为何此时的AOC会出现小幅下降.随后的小分子和大分子出现下降,但中分子则保持不变,而AOC却达到了最大值,表明大量小分子有机物为AOC的生成提供了充足的来源.而后的大分子下降,小分子有机物也逐渐下降,AOC也逐渐下降.由此可见,小分子有机物是AOC的主要氯化前体物.30min时AOC生成已趋稳定,因此后续试验均采用30min为反应时间.

图2 反应时间对AOC生成量的影响Fig.2 The effect of reaction time on AOC formation
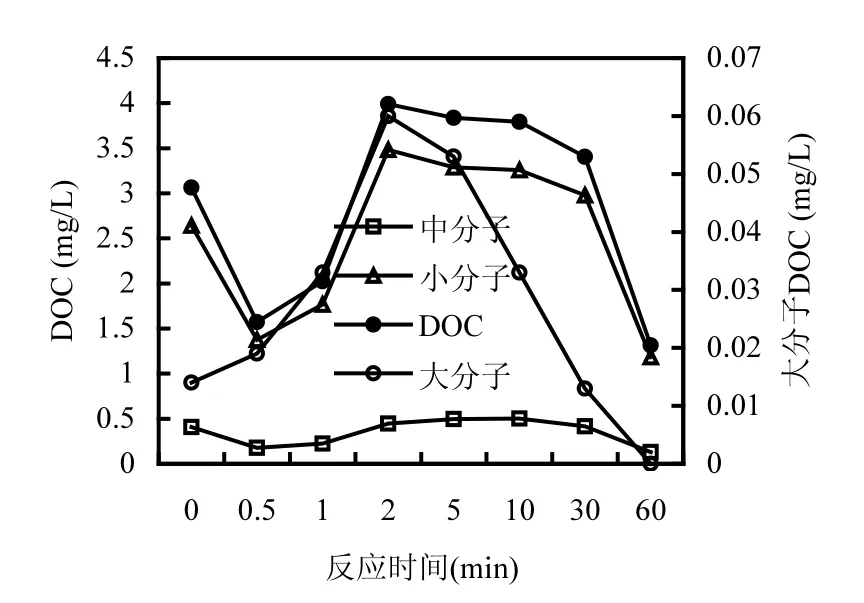
图3 反应时间对分子量分布的影响Fig.3 The effect of reaction time on MWD
2.1.3 投加量对AOC生成的影响 图4为投加量对AOC生成量的影响.水样的初始AOC浓度为55µg/L,其中AOC-P17为45µg/L,占81.9%, AOC-NOX为10µgC/L,占18.1%.由图4可知,投加氯1.5mgCl2/L,反应30min,AOC大幅增加,但投加量的增加对AOC的增加影响甚微.
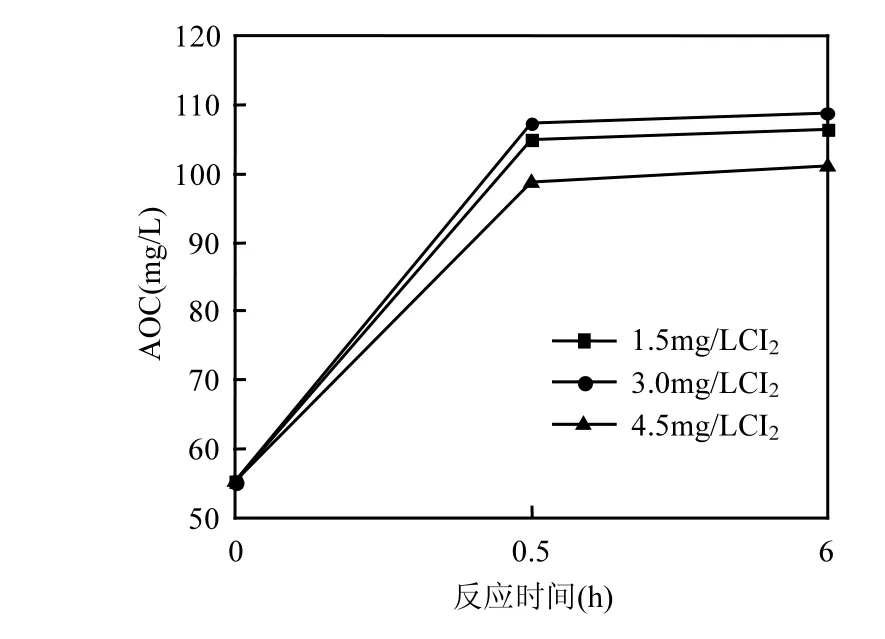
图4 氯投加量对AOC生成量的影响Fig.4 The effect of chlorine dosage on AOC formation
2.2 AOC的前体物
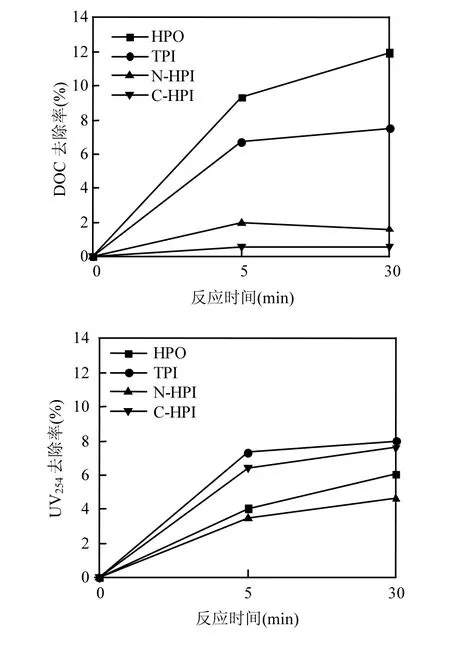
图5 氯对有机物各组分的氧化效果Fig.5 Oxidation of chlorine for HPO, TPI, NHPI and CHPI fractionated from the raw water
2.2.1 氯对亲疏水组分DOC和UV254的降解如图5所示,氯去除强疏的效果最好,其次为弱疏,而中亲和极亲的去除效果最差,30min时,强疏和弱疏组分去除率分别达11.9%和7.5%,而中亲和极亲组分只有1.6%和0.6%,这与图1亲疏水组分氯消耗曲线的结果一致.由DOC变化分析可知氯氧化有机物主要去除的是疏水性组分;UV254去除率大小依次为:弱疏>极亲>强疏>中亲,由于树脂的洗脱,导致极亲组分的离子强度较大,使之疏水化,SUVA值远大于中亲组分,并超过强疏组分,所以UV254去除率相对较高.但是,极亲所含的有机物种类不同于疏水性组分,氯化后的产物多数并不能为微生物所利用,因而AOC的生成量较低.另外,5~30min,除了强疏组分DOC和UV254的去除率还有缓慢上升,其余三个组分已趋于稳定.
2.2.2 氯对亲疏水组分AOC生成量的影响图6是各组分单位DOC加氯后AOC生成量的变化.由图可见,加氯后的AOC生成量增加最多的为TPI,其次为HPO,N-HPI和C-HPI的最少.这说明疏水性组分更易与氯反应.图7为氯与有机物各组分反应30min时的分子量去除情况,可知与氯反应后,小分子的HPO和TPI均有一定程度的下降,这些组分的减少几乎均由小分子所贡献,而小分子的N-HPI和C-HPI反而有所增加,这说明氯主要氧化小分子的疏水性组分.
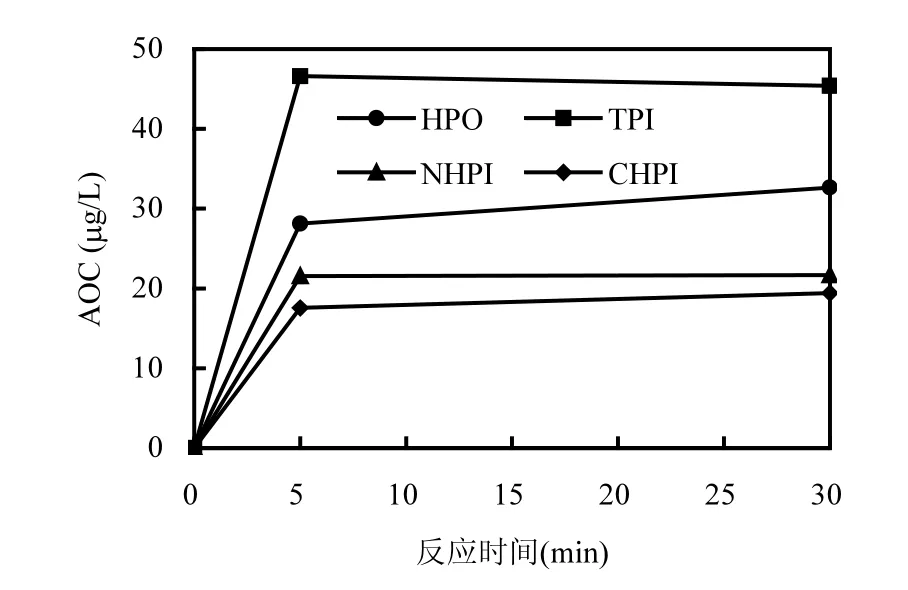
图6 有机物各组分与氯反应产生AOC的效果Fig.6 The effect of chlorine on AOC formation for HPO, TPI, NHPI and CHPI fractionated from the raw water
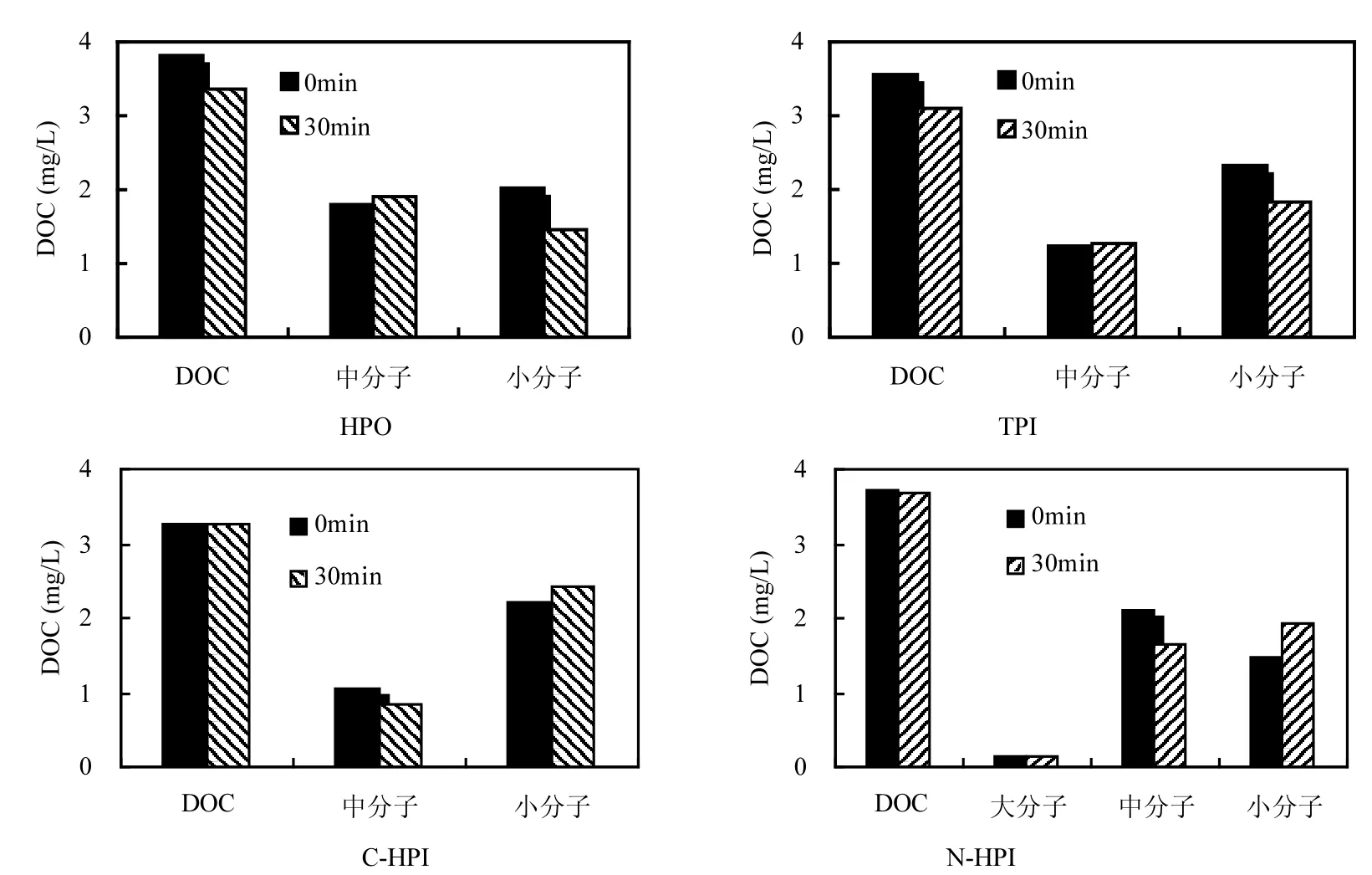
图7 氯对有机物各组分分子量氧化的效果Fig.7 Oxidation of chlorine for MWD in HPO, TPI, NHPI and CHPI fractionated from the raw water
2.3 深度处理工艺的AOC前体物
为了进一步了解加氯对AOC生成的影响,取某水厂(水源与上述小试的相同)各个处理工艺的出水,然后加1.5mg/L的氯,反应30min,分别测定加氯前后的AOC,结果如图8所示.由图8可见,原水加氯后,AOC的增加幅度最多,经预臭氧后,增加幅度下降,在混凝沉淀时,降为最低,而后略微增加.图9表明,HPO和TPI组分随着处理工艺逐渐下降,N-HPI经混凝沉淀后增加,砂滤后进一步增加,经后臭氧后明显下降.图10表明,HPO所占比例在整个处理流程中逐渐下降,而TPI基本保持不变, N-HPI的比例经混凝沉淀后大幅上升,由30%上升到50%,表明混凝可有效去除疏水性有机物,降低AOC前体物的含量,从而减少AOC生成量.有机物组分在处理工艺中的变化与加氯后的AOC增加有密切的关系,进一步说明了HPO和TPI组分为AOC的主要前体物.深度处理过程中的有机物分子量变化如图11所示.由图11可知,原水中的大分子所占比例非常小,中分子占有一定的比例,有机物中主要由小分子构成.随着深度处理的进行,中分子比例逐渐降低而小分子的逐渐上升.
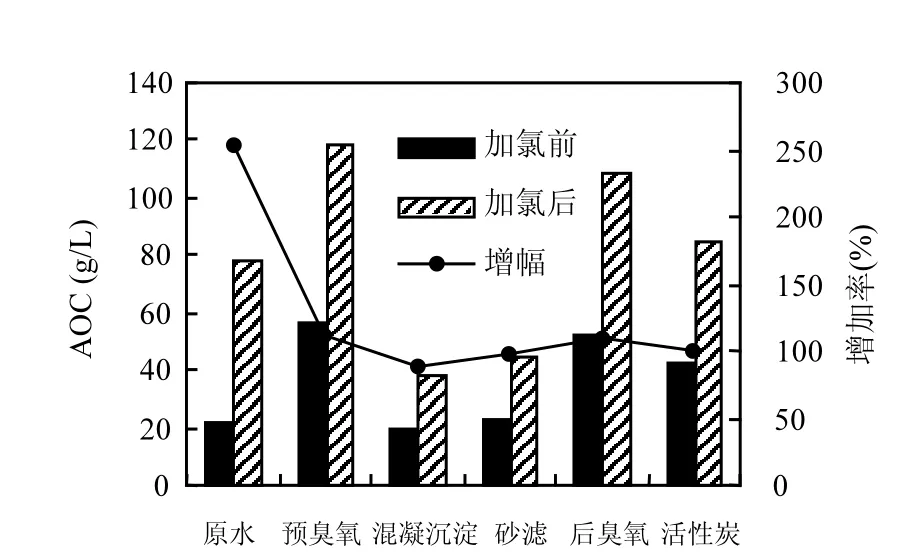
图8 深度处理工艺加氯AOC的变化Fig.8 Formation of AOC during advanced treatment process
提高预臭氧和后臭氧的投加量,虽然可有效去除疏水性有机物,但这些有机物转化成小分子的亲水性有机物,为微生物所利用,从而增加AOC.因此,臭氧的投加量应适当,不可过量投加.混凝可有效去除AOC[14].此外,混凝还可去除疏水性有机物,降低AOC的前体物,从而强化深度处理工艺去除AOC.
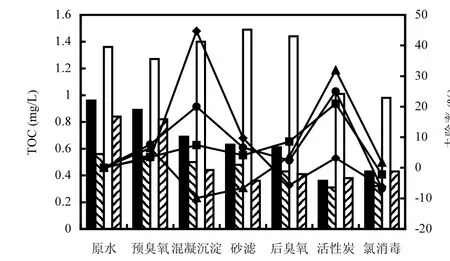
图9 深度处理工艺有机物组分的去除Fig.9 Removal of HPO, TPI, NHPI and CHPI during advanced treatment process
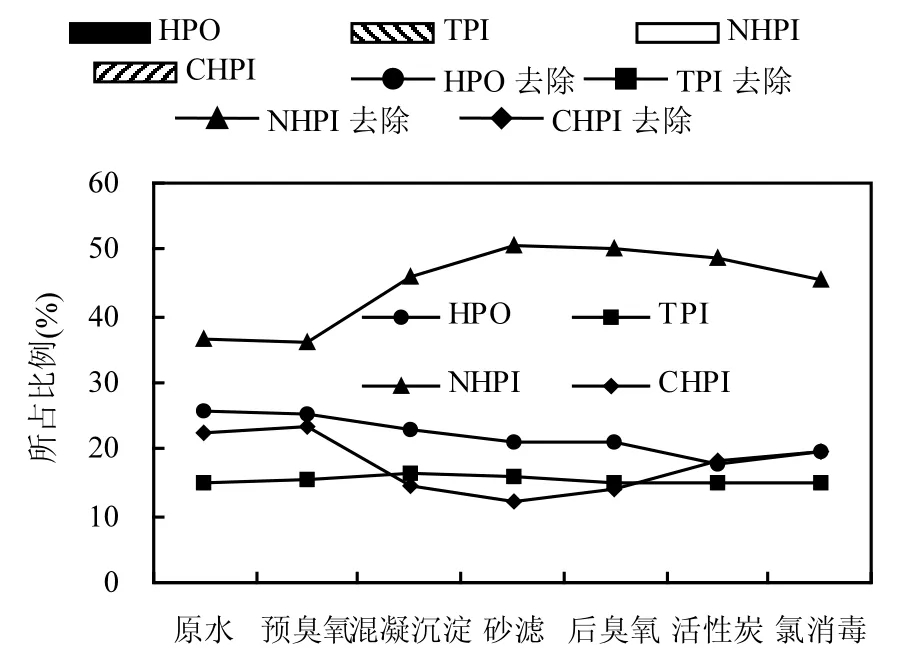
图10 深度处理工艺有机物组分的变化Fig.10 Composition of HPO, TPI, NHPI and CHPI during advanced treatment process
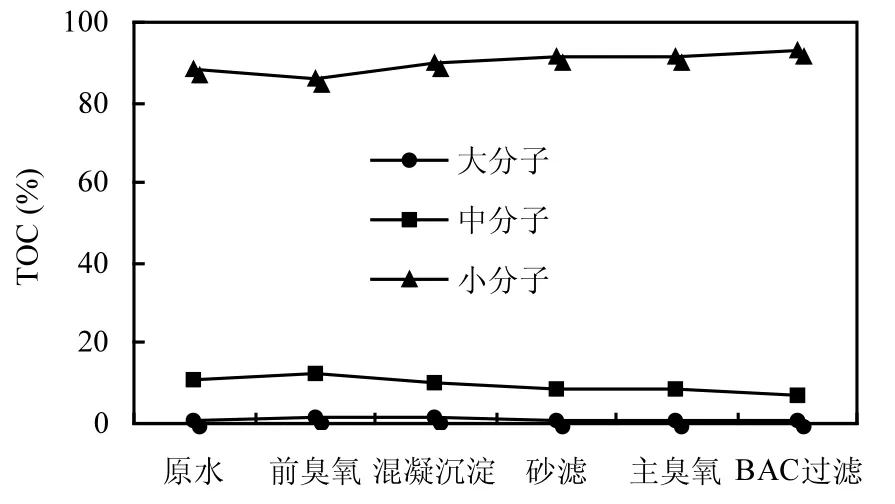
图11 深度处理工艺有机物分子量的变化Fig.11 MDW during advanced treatment process
3 结论
3.1 弱疏组分的AOC生成量最大,其次为强疏,中亲和极亲的生成量最少.
3.2 氯主要与小分子的疏水性有机物反应, AOC的生成量最多.
3.3 在深度处理工艺中,疏水性有机物呈逐渐减少而亲水性组分增加,氯化产生的AOC呈减少趋势.
3.4 小分子的疏水性有机物是主要的氯化AOC的前体物.
参考文献:
[1] 刘文君,吴红伟,张淑琪,等.某市饮用水水质生物稳定性研究[J]. 环境科学, 1999,20(2):34-37.
[2] 吴红伟,刘文君,王占生.臭氧组合工艺去除饮用水源水中有机物的效果 [J]. 环境科学, 2000,21(7):29-33.
[3] 孔令宇,张晓健,王占生.臭氧-生物活性炭组合工艺中最佳臭氧投加剂量的确定 [J]. 环境科学, 2006,27(7):1345-1347.
[4] 鲁 巍,唐 峰,张晓健,等.净水工艺对饮用水生物稳定性控制的研究 [J]. 环境科学, 2005,26(6):71-74.
[5] 王继萍,华 伟,蒋福春,等.臭氧-生物活性炭工艺去除AOC和有机物的效果研究 [J]. 给水排水, 2014,40(2):11-15.
[6] 舒诗湖,严 敏,苏定江,等.臭氧-生物活性炭对有机物分子量分布的影响 [J]. 中国环境科学, 2007,27(5):638-641.
[7] Ramseier M K, Peter A, Traber J, et al. Formation of assimilable organic carbon during oxidation of natural waters with ozone, chlorine, dioxide, chlorine, permanganate and ferrate [J]. Water Research, 2011,45(5):2002-2010.
[8] Lai W L, H H Yeh, I C Tseng. The effect of ozonation and filtration on AOC value of water from eutrophic lake [J]. Ozone-Science & Engineering, 2006,28(1):29-35.
[9] Polanska M, Huysman K, Van Keer C. Investigation of assimilable organic carbon (AOC) in Flemish drinking water [J]. Water Research, 2005,39(11):2259-2266.
[10] Mieettinen I T, Vartiatiainen T, Nissinen T, et al. Microbial growth in drinking waters treated with ozone, ozone hydrogen peroxide or chlorine [J]. Ozone-Science & Engineering, 1998,20(4):303-315.
[11] Paode Rdag. Predicting the formation of aldehydes and BOM [J]. Journal of AWWA, 1997,89(6):79-93.
[12] 刘文君,王亚娟,张丽萍,等.饮用水中可同化有机碳(AOC)的测定方法研究 [J]. 给水排水, 2000.
[13] American Public Health Association. Standard methods for the examination of water and wastewater [S]. Washington DC, 1998.
[14] Jin Wang, Huaqiang Chu, Bingzhi Dong. Multiple views of biological stability and optimized coagulation in the control of biostability in traditional water treatment processes: a pilot test [J]. Desalination and Water Treatment, 2015:1-11.
[15] Hem L J, Efraimsen H. Assimilable organic carbon in molecular weight fractions of natural organic matter [J]. WATER RESEARCH, 2001,35(4):1106-1110.
致谢:本实验的现场采样工作由江苏省苏州市自来水公司工程师们协助完成,在此表示感谢.
Effects of chlorination on assimilable organic carbon in drinking water.
WU Wei-wei1, CHEN Jia-pei1, DONG Bing-zhi2*(1.College of Environmental Science and Engineering, Tongji University, Shanghai 200092, China;2.Key Laboratory of Yangtze River Water Environment, Ministry of Education, Tongji University, Shanghai 200092, China). China Environmental Science, 2016,36(4):1067~1072
Abstract:The formation and mechanism of assimilable organic carbon (AOC) production after chlorination is evaluated through analyzing variation of molecular weight (MW) distribution and hydrophobic/hydrophilic fractions. The experimental results showed that the hydrophobic part of AOC was dominant, followed by transphilic and neutral hydrophilic fractions. The charged hydrophilic fraction was the least. It was found that chlorine reacted mainly with hydrophobic organics with low MW, leading to the most AOC formation. By investigating the variations of organics of MW and fractions through advanced treatment process, it was found that hydrophobic fraction was reduced and hydrophilic fraction was increased gradually, indicating the decrease of AOC formation after chlorination. It can be concluded that hydrophobic organics with low MW is the main precursor of AOC after chlorination.
Key words:assimilable organic carbon (AOC);precursor;chlorine;drinking water
作者简介:吴炜玮(1990-),女,江苏无锡人,硕士,主要从事饮用水深度处理研究.
基金项目:国家水体污染控制与治理科技重大专项
收稿日期:2015-09-10
中图分类号:X524
文献标识码:A
文章编号:1000-6923(2016)04-1067-06

