对氢氧化铁胶体制备要求的检验
吕圣晨
摘 要:制备氢氧化铁胶体是高中生接触到的第一个具有探究性质的实验。本文介绍了如何针对这一实验中所设置的饱和氯化铁溶液等要求,运用控制变量的方法进行实验探究,并依据探究所得到的结论尝试使用稀氢氧化钠溶液与稀氯化铁溶液混合的方法制备氢氧化铁胶体。
关键词:氢氧化铁胶体 丁达尔效应 电解质
化学是一门以实验为基础的科学,所以在任何时候都应该根据实验现象进行理论分析。在进行氢氧化铁胶体制备实验的时候,教材介绍了用饱和氯化铁溶液滴入沸腾蒸馏水的方法,并且在教学和考试中老师们无数次强调了教材中的要点。但在实际教学中,为了节省时间,往往只是用饮水机中的热水进行实验。胶体的本质是一种分散质大小在1~100nm间的分散系,并且能够产生丁达尔效应。本文将从这些要点出发,进行研究和思考。
一、实验探究
1.温度对胶体形成的影响
分别向不同温度的30ml蒸馏水中滴入6滴饱和氯化铁溶液,并静置一天,结果如图1所示。
可以很明显地看到试管中的颜色在60℃以下时不再发生明显变化,而在90℃(北京地区水的沸点达不到100℃)到75℃之间,颜色也没有明显差异。经过激光笔(5mW 红光)检验丁达尔效应,发现水温在80℃以上时形成的光路十分清晰,温度越低丁达尔效应越不明显。
2.氯化铁溶液浓度对胶体形成的影响
分别向30ml沸腾的蒸馏水中逐滴加入6滴不同浓度(5%~45%,每组浓度相差5%)的氯化铁溶液,并静置一天。结果如图2所示。
所有浓度制得的分散系均产生了明显的丁达尔效应。氯化铁溶液浓度在15%以上时溶液颜色无明显变化。
3.电解质对胶体保存的影响
按照教材中所述方法制备氢氧化铁胶体若干,并分别向其中(30ml)加入不同电解质进行实验。实验结果如表1、表2、表3所示。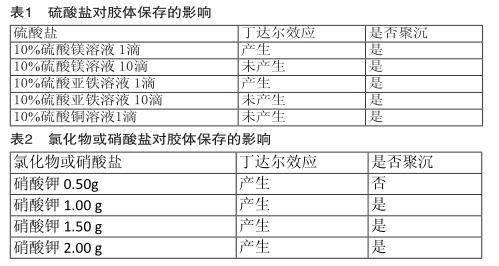

由表1、表2可知,硫酸盐对氢氧化铁胶体聚沉效果比氯化物和硝酸盐好,氯化物和硝酸盐浓度足够时也可以引发氢氧化铁胶体聚沉。这是因为氢氧化铁胶体中胶粒带正电荷,所以硫酸根离子(带两个负电荷)要比氯离子和硝酸根离子(带一个负电荷)对氢氧化铁胶粒的中和能力强。
4.新方法制备氢氧化铁胶体
综合以上探究结果,我们发现,即使在某些条件不符合教材中要求的情况下,依然可以制备氢氧化铁胶体。所以笔者进行了尝试,使用稀氢氧化钠溶液与稀氯化铁溶液混合的方法。
实验中,先向每支试管中加入30ml的蒸馏水,再加入数滴10%氢氧化钠溶液,振荡后加入10%氯化铁溶液,分别在加入后和静置一天后观察现象。实验现象如表3所示。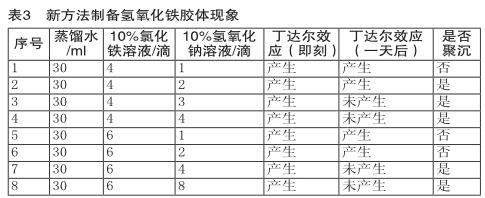
以上现象表明1~2滴10%氢氧化钠溶液与4~6滴10%氯化铁溶液混合,可以制得比较稳定的氢氧化铁胶体。但用该方法制得的氢氧化铁胶体颜色较教材中所述方法浅。综合来说,这种方式不需要较长的时间对液体进行加热,在时间不长的课堂上可以进行多组实验。
二、实验分析及结论
实验表明,氢氧化铁胶体制备要求有一定的伸缩空间,不是一定要按照教材的方法走。尽管这样,教材中的方法仍然是最能揭示胶体性质的方法。并且教材只是介绍了相关的性质及应用,并没有否定其他方法。只是有关这一部分的试题以偏概全,而忽视了胶体的本质。
对于丁达尔效应这一光学现象,应该是多种因素共同作用的结果。尽管实验中产生了丁达尔效应,但可能溶液中还存在大量未反应铁离子,实验中不同浓度的氯化铁溶液制得的氢氧化铁胶体颜色改变不大和实验中分散系颜色较浅都与此有关。
总之,本次实验探究有关氢氧化铁胶体制备实验的相关方面,但还有许多条件需要继续进行探究,比如激光笔的功率、盛放氢氧化铁胶体器皿形状等等。
参考文献:
[1]宋心琦.普通高中课程标准教科书:化学(必修一)[M].北京:人民教育出版社,2007.
[2]朱传征,许海涵.物理化学[M].北京:科学出版社,2002.(作者单位:北京市第二十中学)

