Ca2Co2O5氧化物热电陶瓷材料的制备研究
冷菊 魏贺 程汉池
摘 要:本文通过溶胶-凝胶法和固相合成法两种方法研究Ca2Co2O5氧化物热电陶瓷材料的制备过程。湿法制备前驱体粉,以Ca(NO3)2·4H2O和Co(NO3)2·6H2O为原料,纯净水为溶剂,柠檬酸为络合剂。采用溶胶-凝胶法制备Ca2Co2O5粉末,以CaO和Co3O4为原料,采用固相合成法制备Ca2Co2O5粉末,采用常压烧结的方法,在1000℃、950℃、900℃三种温度下进行烧结,并利用TG-DSC、XRD、SEM等手段对Ca2Co2O5的热分解过程,物相组成和形貌进行表征。结果表明:干粉800℃热处理,湿法950℃烧结时,块体呈现致密的片层结构,相组成成分纯度高[1~3]。
关键词:溶胶凝胶法;固相混合;致密度;Ca2Co2O5粉末
1 引言
随着工业化进程的加快,全球性环境恶化和能源危机正严重威胁着社会的长期稳定发展,人们迫切需要寻找新型绿色能源取代传统化石燃料,热电材料引起了研究者们的广泛关注。热电材料是一种先进的能量转换材料,通过载流子的移动能静态地进行热能与电能的相互转换[4]。利用热电材料制备的发电器、致冷器、传感器等元件具有体积小、重量轻、结构简单、无化学反应、无介质泄漏、无噪音、无磨损、移动方便、使用寿命长等优点,已应用于军事、航天等高科技领域,在废热发电、医学恒温、小功率电源、微型传感等民用领域也有着广泛的应用。Ca-Co-O体系氧化物热电材料由于具有较高的电导率和较大的Seebeck系数,以及使用温度区间广、耐腐蚀、抗氧化、无毒性等特点受到了广泛关注[5]。
制备Ca-Co-O系氧化物陶瓷材料的方法有很多,本文采用溶胶-凝胶法和固相反应法制备出了三种Ca-Co-O体系氧化物热电陶瓷,再利用脉冲激光沉积技术(PLD)选择合适的陶瓷靶材在不同衬底上制备出Ca-Co-O体系氧化物热电薄膜,为Ca-Co-O体系氧化物热电材料的热电性能的提高开辟了一条新的途径。
2 实验材料和实验方法
2.1 实验材料
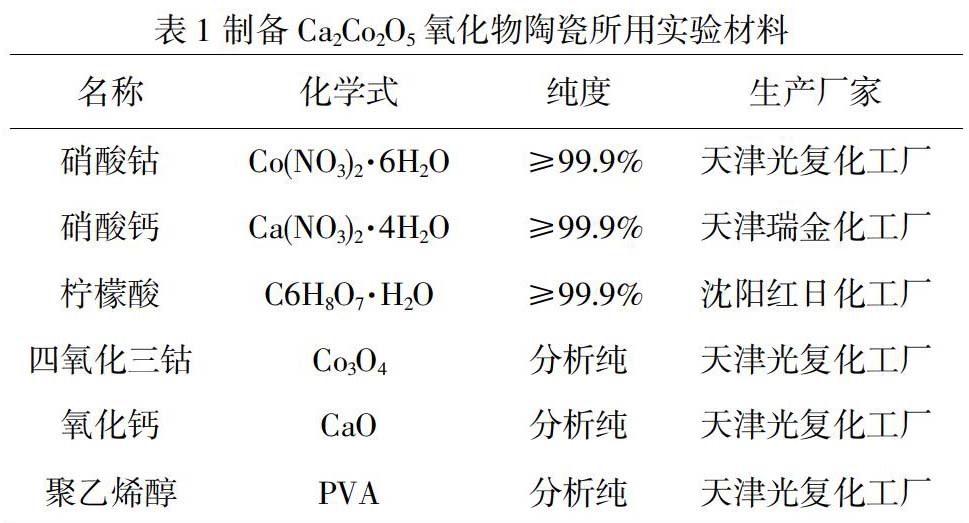
实验选用硝酸钴、硝酸钙、柠檬酸、无水乙醇、四氧化三钴、氧化钙以及聚乙烯醇等试剂为原材料,其纯度及生产厂家如表1所示。
2.2 实验方法
2.2.1 溶胶凝胶法(Sol-Gel)制备Ca2Co2O5氧化物陶瓷
溶胶-凝胶法是一种湿式化学方法。其化学反应通常分为两步:第一步为前驱体反应物的水解过程,形成羟基化合物;第二步是羟基化合物的缩聚过程。经上述水解、缩聚后,得到透明且有一定粘度的溶胶。随着水解缩聚反应的进一步进行,最后生成凝胶。其基本原理如下:
(1) 溶剂化:能电离的前驱物即金属阳离子MZ+(Z为M的价态)吸收水分子形成溶剂单元M(H2O)nZ+,为保持它的配位数而有强烈的释放H+离子的趋势。
M(H2O)nZ+ → M(H2O)n-1(OH)(Z-1)++H+
这时如有其它离子进入就可能产生聚合反应,但反应极为复杂。
(2) 水解反应:非电离式分子前驱物,如金属醇盐M(OR)n(n为金属M的原子价)与水反应:
M(OR)n+XH2O → M(OH)X(OR)n-X+XROH
反应可持续进行,直至生成M(OH)n。
(3) 缩聚反应:
-M-OH+HOM → -M-O-M+ROH
溶胶-凝胶法制备粉体过程是将所需组成的溶剂化前躯体溶剂和水配成混合溶液,经水解、缩聚反应形成透明溶胶,并逐渐凝胶化,在经过干燥,热处理后,即可获得所需粉体材料。由于凝胶中含有大量液相或气孔,使得在热处理过程中不易使粉体颗粒产生严重团聚。同时在制备过程中易控制粉体颗粒尺度,因此用溶胶-凝胶法可制备多种纳米粉体[6-8]。
制备粉体时,采用适当的无机或有机盐配置成溶液,然后加入能使之成核,使溶液凝胶化,控制其凝胶化过程即可制得球形颗粒的凝胶体,经一定温度煅烧分解得到所需的粉体。采用溶胶-凝胶法制得的粉体具有高度的化学组成均匀性、高纯度、超细(凝胶颗粒一般小于0.1 μm)、易烧结等特点。
目前采用此法已制备出种类众多的氧化物粉体和非氧化物粉体。如在900℃将凝胶处理后可获得颗粒度为0.1-0.5 μm的NaZr2P3O12晶相粉体;在1200℃将凝胶处理后可制备出平均粒径为0.4 μm的α-Al2O3粉体;在1350℃将凝胶处理后可形成粒径为0.08~0.15 μm的晶相Al2TiO5粉体;在400℃将凝胶处理后也可形成粒径较小的Na-B-Bi-O粉料,此粉料可熔融形成玻璃,其熔融温度比常规方法低250℃。
溶胶-凝胶法可分为传统胶体型、无机聚合物型(即金属醇盐水解法)和络合物型3种。其中络合物法需要加入络合剂,这是由于一些盐或氧化物不易溶于水,加入有机络合剂可以改变盐或氧化物的溶解度,使之溶解在溶剂中;同时络合剂的加入还能减缓水解的速度,有助于得到均匀透明的凝胶。常用于溶胶-凝胶过程的络合剂有柠檬酸、酒石酸等。本实验采用的络合剂为柠檬酸[9-11]。
首先将硝酸钙和硝酸钴按一定比例(要求金属离子浓度为0.2 mol/L)混合并加入蒸馏水,适当加热下不断搅拌溶解,然后将己称好的柠檬酸(摩尔数为金属离子摩尔数的1.3~1.7倍)缓慢加入到溶液内不停搅拌使其充分反应,并控制溶液的PH值在1~4之间,加热过程中形成了柠檬酸盐,随着反应的进行水分逐渐蒸发,使其缓慢发生水解、缩聚反应,形成具有网络结构的湿凝胶(温度在70~80℃),呈粘稠状,然后转至鼓风干燥箱中烘干8 h,蒸发剩余水分,最后制得紫黑色粉体,在高温下对其进行锻烧,煅烧温度分别为700℃,750℃,800℃(升温速率5℃/min保温4 h),排除胶体中的有机物和硝酸根离子,得到黑色的Ca2Co2O5干凝胶粉末。将干凝胶粉末磨细后压片,然后在900℃、950℃、1000℃下烧结(升温速率为5℃/min且在450℃时保温1 h,在升至最高温度时保温10 h),最终形成结构致密的Ca2Co2O5热电材料[12]。
2.2.2 固相法制备Ca2Co2O5氧化物陶瓷
将原料按照一定的配比混合均匀,湿磨5 h后干燥4 h,制成前躯体粉末。加入少量4%左右PVA溶液作为粘结剂,碾磨混合均匀,过60目筛完成造粒。使用直径为12 mm的不锈钢模具压片,压力选择12 MPa,压片的厚度在1~2 mm。起始升温速度为2℃/min,这一过程中,样品会发生轻微的热膨胀,同时生坯中的水分缓慢挥发。在450℃保温1 h是为了排除干坯中加入的PVA,如果没有此阶段保温,可能会造成排胶不完全或样品开裂。继续升温,在950℃保温10 h,在保温过程中促进晶格完善,晶粒长大,烧结致密,保温完毕后,样品随炉冷却[13,14]。
2.2.3 Ca2Co2O5热电材料的表征
(1) 利用STA409PC差热分析仪对试样干凝胶的热分解过程进行分析;
(2) XRD技术对烧后的粉体及烧结后的块体进行分析:试样的物相分析是在日本理学Rigaku公司生产的D/Max2500型X射线衍射仪上进行的。实验条件为:Cu靶Kα衍射,扫描速度为8o/min,步长为0.02 deg,工作电压和电流分别为40 kV和200 mA;
(3) SEM分析:试样利用日本电子公司的JSM-6460LM扫描电镜观察断口的形貌;
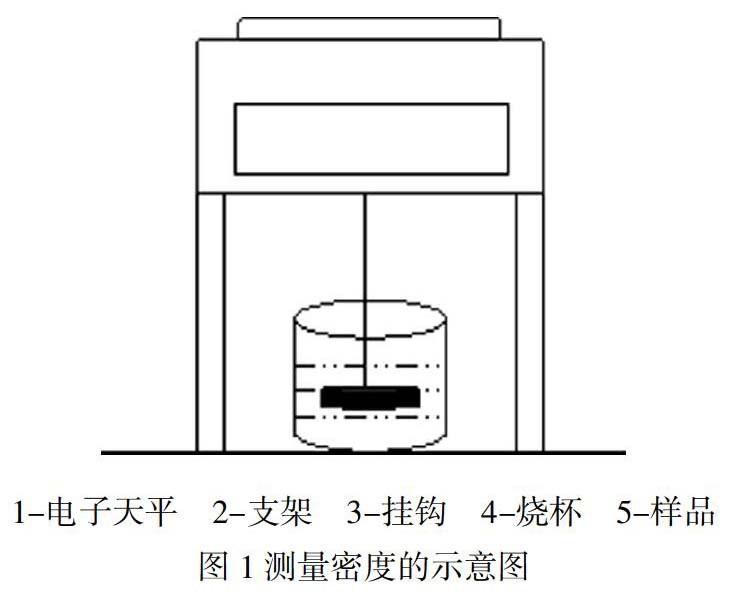
(4) 密度测试:本试验采用阿基米德排水法测定试样的体积密度[17~19]。所用的设备为电子分析天平、小烧杯等。试验装置如图1所示[15]。
具体方法是:在电子分析天平上准确称取样品质量为M空。将盛有水的烧杯放在电子分析天平支架下面,将带有挂钩的小篓挂在电子天平下部,浸入装有水的小杯里,调零。注意水不要盛的太满以至超过天平的最大量程。接着将试样放入小篓中,注意不要让试样接触到烧杯壁。称它在水中的重量为M浮。根据下式计算试样的体积密度D:
D =M空 / M浮
式中,D为试样体积密度;M空为试样在空气中的重量;M浮为试样没入水中后天平显示值。
(5)致密度测试:在电子分析天平上准确称取样品质量为W空。然后将样品全部侵入蒸馏水中,浸泡18 h,将侵满水的试样放在流动的空气中风干,将风干的试样放在电子分析天平上测量质量为W水,根据下式计算式样的致密度σ:
σ=W空/W水
式中,σ是致密度;W空是样品净质量;W水是风干的试样质量[16,17]。
3 结果与讨论
3.1 差热-热重分析(DSC)
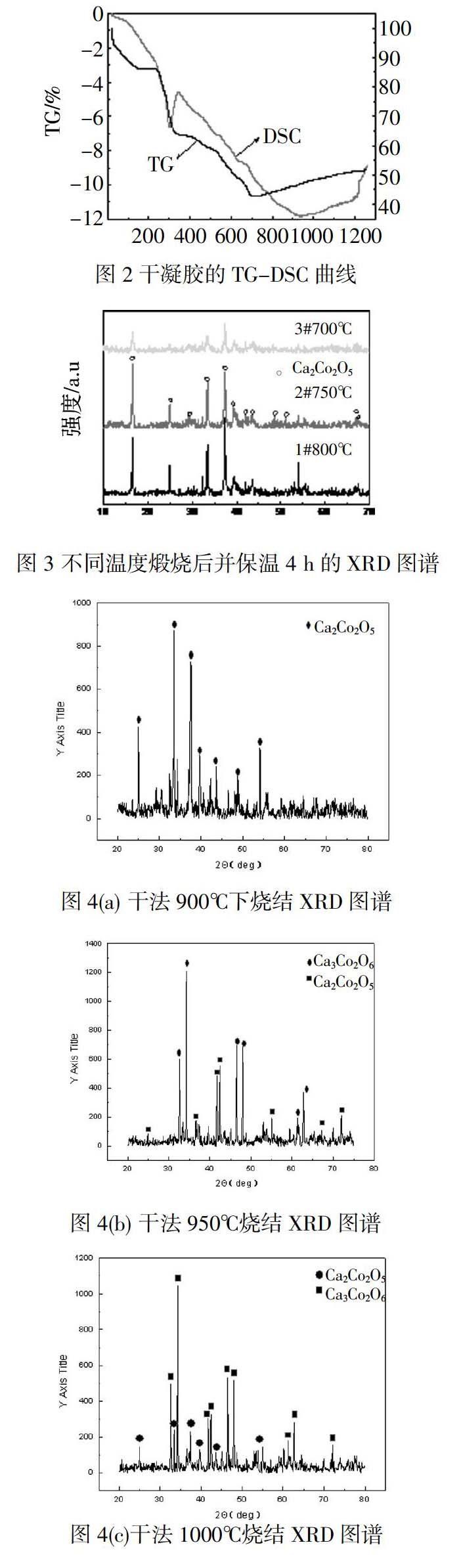
经过差示扫描量热法分析,可以从DSC曲线上峰形面积得到试样的放热量和吸热量。图2为干凝胶的TG-DSC曲线。由图可见,在90℃左右出现了一个微弱的吸热峰,这是残留的水分蒸发的结果。在290℃至550℃之间的放热峰,伴随两次失重,失重达52.8%,这是由于柠檬酸盐分解氧化,生成Co3O4和CaCO3。在680℃左右有个小的吸热峰,这是由于CaCO3分解为CaO,此过程伴随失重7.68%。在910℃的放热过程为CaO与Co3O4晶化最终形成钴酸钙的过程[18]。
3.2 X-射线衍射分析(XRD)
图3为干凝胶粉体在700~800℃各指定温度下常压煅烧并保温4 h后的XRD图谱。在750℃煅烧的产物主要成分为Ca2Co2O5,很少的其他杂相存在。而在700℃和800℃煅烧后的产物出现了Ca3Co4O9的衍射峰,表明在Ca2Co2O5中生成了Ca3Co4O9杂相。由图可见随温度的增加衍射峰强度增强,表明随反应温度升高产物晶化的程度更好。而在750℃下煅烧后可得到较纯的Ca2Co2O5。
图4(a)(b)(c)为干法在900℃、950℃、1000℃下烧结(保温10 h)不同温度热处理(保温4 h)的纯粉所得的块体的XRD图谱。我们可以看到:(1)在900℃、950℃、1000℃下得到的烧结体主要都由Ca2Co2O5和Ca3Co2O6组成,而由900℃到1000℃的对比可知,随着烧结温度的提高,Ca3Co2O6的含量逐渐增高,并在1000℃烧结后在块体中占主要地位。可见烧结温度越高Ca3Co2O6的含量越多,这是由于Ca2Co2O5相随着温度升高不稳定,发生分解转化为Ca3Co2O6相的缘故。所以在常压烧结此材料时温度应控制在900℃以下的某个温度范围内。也可通过改善烧结方法,如采用SPS来提高纯度。(2)此外,从不同热处理条件的粉体烧结情况来看,它们在相同温度下烧结时的XRD图谱大致相同,说明它们都能得到成分基本相同的物质,所以在热处理粉体时,通常在100℃温差范围内都可[19-22]。
图5(a)(b)(c)是用凝胶-溶胶法所制得前驱体粉,在900℃、950℃、1000℃温度制度下烧结(保温10 h)成的块体所呈现的XRD照片,和干法制备相比湿法制得块体中基本上没有杂相出现,而且出现的峰也比较尖锐,密集分布,可见湿法制备的Ca2Co2O5陶瓷成分更加纯净,在图5(b)、5(c)的XRD图谱中,块体样品的(00l) 晶面的衍射峰峰强比非 (00l) 晶面的衍射峰要强得多,表明在 (00l) 方向上存在一定的织构取向[23]。可见提高烧结温度后在950℃、1000℃下的到的XRD图谱主要衍射峰值与Ca2Co2O5一致,说明经提高烧结温度后产品纯度提高。
3.3 扫描电子显微镜(SEM)
图6(a)、(b)、(c)所示分别为溶胶-凝胶方法(sg)制备的粉体在700℃,750℃,800℃煅烧的纯钴酸钙氧化物粉体所得的放大 10000倍的SEM照片。在700℃煅烧的粉体颗粒的片状结构还不十分明显且出现了严重的团聚现象。而在750℃下煅烧的粉体,颗粒尺寸分布得很均匀且可看出颗粒较细,呈片状结构,这种片状结构与Ca2Co2O5的晶体结构生长一致,即CoO2面沿C轴方向与岩盐Ca2CoO3层交替重叠堆砌。在800℃颗粒片状结构不如750℃明显[24]。可见,适当提高煅烧温度有利于Ca2Co2O5晶体的生长。而在750℃时结晶最好,也正与XRD测试结果吻合。图(d)是固相混合法(cs)所得粉体的SEM图片,可见与溶胶-凝胶法相比,颗粒粒度较大且分布不均匀,大小不一,层状结构不明显[25]。

