3,5-二氨基-2,6-二硝基吡嗪-1-氧化物合成及性能
王 帜, 张文全, 王康才, 亓秀娟, 张庆华
(中国工程物理研究院化工材料研究所, 四川 绵阳 621999)
1 引 言
现代武器要求含能材料在具有高能量的同时也必须具有良好的安全性。能量水平高于奥克托今(HMX),而感度与1,3,5-三氨基-2,4,6-三硝基苯(TATB)相当的高能钝感材料一直是人们努力追求的目标[1],这也对新型高能骨架的构建提出了极大的挑战。吡嗪骨架是一种具有巨大研究潜力和应用价值的六元氮杂芳环结构,在生物学、合成化学、药物化学、分析化学、含能材料等领域有着许多前沿性的研究[2-5]。特别在含能材料领域,硝基功能化的氧化吡嗪骨架化合物的合成一直受到广泛关注[6-7]; 由于氧化吡嗪环具有很好的对称性、较高的生成焓、高热稳定性、多样化的化学修饰位点,成为极具潜力的构建高能低感材料的理想骨架之一。
2,6-二氨基-3,5-二硝基吡嗪-1氧化物(LLM-105)是美国利弗莫尔含能材料实验室发展的一种高耐热炸药,其晶体密度高达1.913 g·cm-3, 实验爆速为8560 m·s-1,比冲为2212.68 N·s/kg (7 MPa),能量比TATB高出20%,DSC放热峰值为354 ℃,优于大多数单质炸药,同时对撞击、火花、摩擦、冲击波相对低感,与铜、铝、不锈钢及RDX等相容性良好,在石油射孔弹、传爆药等领域显示出一定的应用前景[8]。中国工程物理研究院化工材料研究所[9],西安近代化学研究所[10]、中北大学[11]、北京理工大学[12]等均对LLM-105的合成及生产工艺等进行了深入研究。鉴于LLM-105的优越性能,开发类似骨架结构且与之性能相近或更优、工艺成本更低,合成路线简洁的新型含能化合物,具有一定的科学意义。
基于此,本研究以2,6-二氯吡嗪为起始原料,经四步反应首次设计合成了一种全新的氧化吡嗪骨架含能化合物,即LLM-105异构体——3,5-二氨基-2,6-二硝基吡嗪-1-氧化物(DDPZO-i),并对其结构进行了表征,初步研究了3,5-二氨基-2,6-二硝基吡嗪-1-氧化物的热性能,对吡嗪骨架的可能氧化机理做出推测,并通过X射线衍射技术确定了DDPZO-i的晶体结构,为进一步开展应用研究奠定基础。
2 实验部分
2.1 试剂与仪器
试剂: 2,6-二氯吡嗪(购于百灵威,纯度99%),市售浓硫酸、30%双氧水、工业发烟硝酸、二氯甲烷、乙酸乙酯、甲醇钠、甲醇、乙腈、氨水等为分析纯,购自成都科龙试剂公司。
仪器: 瑞士Bruker公司600 MHz (Bruker AVANCE 600)核磁共振仪,TMS为内标; 日本Shimadzu 公司LCMS-IT-TOF质谱仪。差示扫描量热仪(瑞士Mettler Toledo公司)。美国Micromeritics公司Micromeritics Accupyc II 1340全自动气体置换法密度仪。美国PerkinElmer Spectrum Two IR傅里叶变换红外光谱仪,溴化钾压片。
2.2 合成路线

Scheme1Synthetic route of DDPZO-i
2.3 实验步骤
2.3.1 3,5-二氯吡嗪-1-氧化物的制备
0 ℃下,将1.5 g (10 mmol) 2,6-二氯吡嗪加入30 mL浓硫酸中搅拌,30 min内缓慢加入11 mmol H2O2溶液(30%),加完后将反应体系升至室温搅拌48 h后,倾入冰中,(4次×50 mL/次)乙酸乙酯萃取、10 mL饱和食盐水洗涤、1.4 g无水硫酸钠干燥、过滤,蒸干溶剂后得到白色固体用甲醇重结晶得到3,5-二氯吡嗪-1-氧化物1.32 g,收率80%。m. p.: 31~33 ℃。1H NMR (600 MHz, DMSO-d6)δ: 8.53 (2H, CH);13C NMR (600 MHz, DMSO-d6)δ: 144.62, 142.46; IR (KBr,ν/cm-1): 3658.71, 2978.94, 2901.25, 1408.22, 1398.77, 1381.72, 1250.20, 1229.64, 1075.18, 1055.08, 1056.51, 893.70。
2.3.2 3,5-二甲氧基吡嗪-1-氧化物的制备
室温下,将0.98 g(18 mmol)甲醇钠溶于15 mL无水甲醇中搅拌,缓慢加入制备得到的3,5-二氯吡嗪-1-氧化物(1.32g,8 mmol),加完后反应体系升温至60 ℃,保持30 min。降至室温后倾入30 g冰中,(4次×50 mL/次)乙酸乙酯萃取、10 mL饱和食盐水洗涤、1.5 g无水硫酸钠干燥、过滤,蒸干溶剂后得到白色固体3,5-二甲氧基吡嗪-1-氧化物1.12 g,收率90%。m.p.: 47~49 ℃。1H NMR (600 MHz, DMSO-d6)δ: 7.78 (2H, CH), 3.96 ( 6H, CH3);13C NMR (600 MHz, DMSO-d6)δ: 158.97, 124.50, 53.56; IR (KBr,ν/cm-1): 3675.15, 3117.93, 2901.10, 2987.70, 1403.97, 1249.97, 1229.95, 1075.24, 1066.07, 1056.75, 891.75。
2.3.3 3,5-二乙氧基-2,6-二硝基吡嗪-1-氧化物的制备
0 ℃下,向7 mL 20%发烟硫酸中加入1.1 g(7 mmol)3,5-二甲氧基吡嗪-1-氧化物,搅拌至完全溶解后,缓慢加入1.5 mL 95%发烟硝酸。加完后反应体系于0 ℃搅拌5 h。倾入冰中,析出黄色固体,过滤、50 mL冰水洗涤、自然干燥后得到黄色固体3,5-二甲氧基-2,6-二硝基吡嗪-1-氧化物1.20 g,收率70%。m.p.: 259~261 ℃。1H NMR (600 MHz, DMSO-d6)δ: 4.15 (6H, CH3);13C NMR (600 MHz, DMSO-d6)δ: 153.15, 134.28, 57.31; IR (KBr,ν/cm-1): 3117.92, 2987.39, 2901.07, 1402.24, 1249.94, 1075.61, 1066.14, 1056.70, 891.75。
2.3.4 3,5-二氨基-2,6-二硝基吡嗪-1-氧化物的制备
室温下将0.5g (2 mmol) 3,5-二甲氧基-2,6-二硝基吡嗪-1-氧化物加入3 mL乙腈中搅拌,加入0.56 g(10 mmol) 浓氨水后升温至60 ℃反应2 h。降至室温后过滤、10 mL乙腈洗涤、自然干燥后得到棕红色固体3,5-二氨基-2,6-二硝基吡嗪-1-氧化物(DDPZO-i) 0.35 g,收率80%。1H NMR (600 MHz, DMSO-d6)δ: 7.92 ( 2H, CH);13C NMR (600 MHz, DMSO-d6)δ: 150.29, 130.33; IR (KBr,ν/cm-1): 3412.89, 3003.26, 2916.54, 1556.2, 1021.6, 1665.40, 1371.90, 1315.20, 1191.55, 1022.93, 826.75, 704.57; ESI-HRMS:m/zcalcd. for cation C4H3N6O5[M-H]-: 215.0170; found: 215.0146; 纯度97%。
3 结果与讨论
3.1 氧化反应机理
由文献[13]可知吡嗪环的氮氧化反应受到环电子云密度与氮原子碱性的综合影响,单氮氧化以及双氮氧化条件稍有变化,则所得氧化产物可能截然不同。对于吸电子基团取代的吡嗪结构来说,进一步的氧化反应则愈发难以实现,需要更加苛刻的反应条件。由于吸电子基团的存在将显著降低芳香二嗪环氮原子碱性,吡嗪环的氮氧化反应因此受到氧化剂酸性以及环电子云密度的影响。当氧化剂酸性不足以使吡嗪氮原子发生质子化(如使用双氧水进行氧化),则二氯吡嗪的氮氧化反应优先发生在碱性最强、空间位阻最小的位点。如果氧化剂的酸性足够强,能够使吡嗪氮原子发生质子化,则氮氧化反应发生在未被质子化的碱性较弱的氮原子上。因此,推测强酸性氧化剂有利于生成1位氧化的2,6-二氯吡嗪,弱酸性氧化剂有利于生成4位氧化的2,6-二氯吡嗪,可能的反应机理如Scheme 2所示。

Scheme2The oxidation of 2,6-dichloropyrazine
3.2 热稳定性
在N2流速为20 mL·min-1,升温速率为10 ℃·min-1,温度范围为40~400 ℃条件下获得了DDPZO-i的DSC曲线(图1)。从图2可以看出,DDPZO-i在215 ℃出现放热峰,当温度低于212 ℃时该物质失重较少,累积失重约为5%; 从212 ℃上升过程中,DDPZO-i快速分解,至220 ℃累积失重约44%。DSC曲线没有明显的吸热峰,表明在整个温度范围内没有熔化过程,大于215 ℃附近出现小的放热峰,可能为第二阶段的分解。TG失重及DSC放热峰值反映了DDPZO-i的固相分解过程。
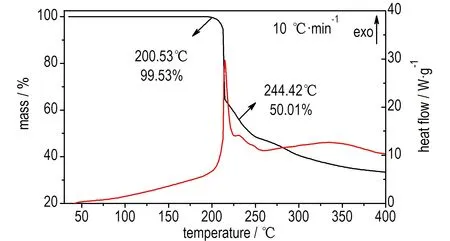
图1DDPZO-i的DSC-TG曲线
Fig.1DSC-TG curve of DDPZO-i
3.3 DDPZO-i的爆速与爆压
采用Gaussain03程序[14],B3LYP/6-331++G(d,p)方法计算DDPZO-i的气相生成焓,根据Politzer经验公式计算升华焓[15],由表1可知,凝聚态的DDPZO-i标准摩尔生成焓为169.4 kJ·mol-1,高于RDX(70.7 kJ·mol-1),远高于LLM-105(-12.0 kJ·mol-1); DDPZO-i的实测密度为1.935 g·cm-3,高于LLM-105(1.913 g·cm-3); 通过Explore5 v6.02软件计算可得爆速为9070 m·s-1,爆压为36.9 GPa,均高于RDX (爆速为8890 m·s-1,爆压为3.7 GPa)。
表1DDPZO-i和一些炸药的爆轰性能
Table1The detonation performances of DDPZO-i and some explosives

explosiver/g·cm-3ΔfHΘ298(s)/kJ·mol⁃1D/m·s-1p/GPaDDPZO⁃i1.935169.4907036.9LLM⁃105[16]1.913-12.0856033.4TNT[16]1.72-65.5737023.5RDX[16]1.81870.7889033.7

3.4 晶体结构
将3,5-二甲氧基吡嗪-1-氧化物溶于乙酸乙酯之中,室温静置1天,自然挥发溶剂,析出无色针状晶体。采用单晶X射线衍射法对析出晶体进行晶体结构测试。图2为3,5-二甲氧基吡嗪-1-氧化物的单晶结构,结果表明该晶体属于三斜晶系,P-1空间群,晶胞参数为a=6.9393(9) Å,b=8.4486(12) Å,c=11.8300(17) Å,α=81.696(3)°,β=86.976(3)°,γ=87.981(3)°。不对称结构单元中包含两个晶体学上独立的3,5-二甲氧基吡嗪-1-氧化物分子。
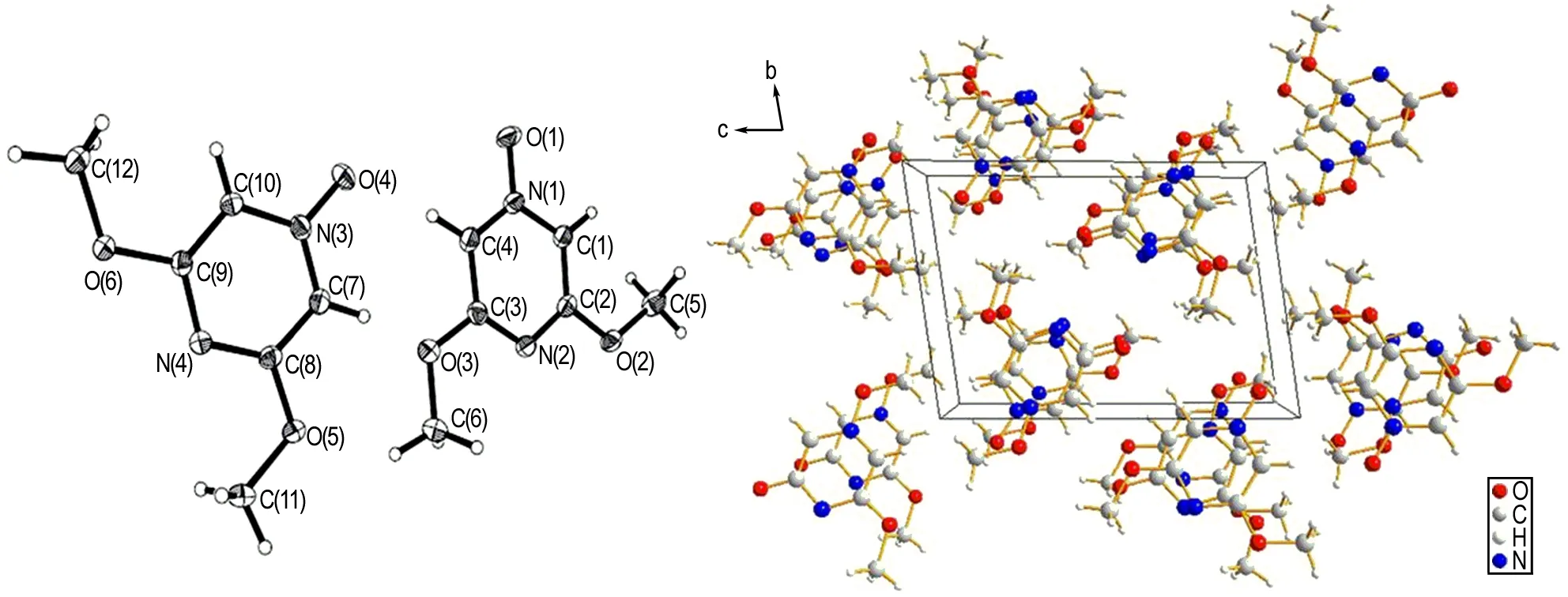
图23,5-二甲氧基吡嗪-1-氧化物的单晶结构
Fig.2Single crystal structure of 3,5-dimethoxypyrazine 1-oxide
将DDPZO-i溶于DMSO中,室温静置7天,析出黄色片状晶体。采用单晶X射线衍射法对所得晶体进行测试。图3为DDPZO-i与DMSO的共晶晶体结构,结果表明该晶体属于单斜晶系,P21/n空间群,晶胞参数为a=4.7716(1) Å,b=25.0711(6) Å,c=10.1631(3) Å,α=90°,β= 99.897(2)°,γ=90°。不对称结构单元中包含一个晶体学上独立的DDPZO-i分子和一个晶体学上独立的DMSO分子,是DDPZO-i与溶剂DMSO的共晶晶体。

图3DDPZO-i与DMSO的共晶晶体结构
Fig.3The eutectic crystal structure of DDPZO-i and DMSO
3.5 DDPZO-i的安全性
将0.1 g的合成产物置于BAM撞击感度测试仪中,使用中物院化材所的BAM撞击感度仪实测撞击感度为5 J,撞击感度数值低于LLM-105,接近RDX,高于CL-20。
4 结 论
(1)合成了新型含能化合物3,5-二氨基-2,6-二硝基吡嗪-1-氧化物(DDPZO-i),反应总收率为40%,并通过X射线晶体衍射、核磁、质谱等确定其结构。
(2)DDPZO-i的实测密度高达1.935 g·cm-3,计算标准生成焓为169.4 kJ·mol-1,优于LLM-105; DDPZO-i计算爆速为9070 m·s-1,爆压为36.9 GPa; 在212 ℃左右开始失重,215 ℃时出现放热峰。
(3)使用中物院化材所BAM撞击感度仪实测撞击感度为5 J,低于LLM-105撞感23 J,接近RDX撞感7 J,高于CL-20的撞感4 J。
可见DDPZO-i是一种具有潜在应用价值的新型单质炸药分子。
参考文献:
[1] 田均均,张庆华,李金山. 含能分子合成最新进展[J]. 含能材料, 2016, 24(1): 1-9.
TIAN Jun-jun, ZHANG Qing-hua, LI Jin-shan. Recent advances
in energetic molecule synthesis[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2016, 24 (1): 1-9.
[2] Schönberger M, Althaus M, Fronius M, et al. Controlling epithelial sodium channels with light using photoswitchable amilorides[J].NatureChemistry. 2014, 6: 712-719.
[3] Miniyar P B, Murumkar P R, Patil P S, et al. Unequivocal role of pyrazine ring in medicinally important compounds: a review[J].Mini-ReviewsinMedicinalChemistry, 2013, 13(11): 1607-1625.
[4] Ferreira S B, Kaiser C R. Pyrazine derivatives: a patent review (2008-present)[J].ExpertOpiniononTherapeuticPatents2012, 22(9): 1033-1051.
[5] Rajput A, Mukherjee R. Coordination chemistry with pyridine/pyrazine amide ligands. Some noteworthy results[J].CoordinationChemistryReviews, 2013, 257(2): 350-368.
[6] Pagoria P F, Gregory S, Alexander R. A review of energetic materials synthesis[J].ThermochimicaActa, 2002, 384(1): 187-204.
[7] Millar R W, Philbin S P, Claridge R P, et al. Studies of novel heterocyclic insensitive high explosive compounds: pyridines, pyrimidines, pyrazines and their bicyclic analogues[J].Propellants,Explosives,Pyrotechnics, 2004, 29(2): 81-92.
[8] Pagoria P F. Synthesis, scale-up, and characterization of 2, 6-diamino-3, 5-dinitropyrazine-1-oxide (LLM-105)[R]. UCRL-JC-117228, 1997.
[9] 李海波, 程碧波, 李洪珍, 等. 2,6-二氨基-3,5-二硝基吡嗪-1-氧化物的合成[J]. 有机化学, 2007, 27(1): 112-115.
LI Hai-bo, CHENG Bi-bo, LI Hong-zhen, et al. Synthesis of 2,6-diamino-3,5-dinitropyrazine-1-oxide[J].ChineseJournalofOrganicChemistry, 2007, 27(1): 112-115.
[10] 邓明哲, 周杰文, 王伯周, 等. LLM-105炸药制备工艺改进[J]. 含能材料, 2013, 21(3): 294-296.
DENG Ming-zhe, ZHOU Jie-wen, WANG Bo-zhou, et al. Preparation improvement of LLM-105 explosive[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2013, 21(3): 294-296.
[11] 郭峰波, 刘玉存, 刘登程, 等. 2,6-二氨基-3,5-二硝基-1-氧吡嗪合成工艺优化 [J].火炸药学报,2006, 29(1): 17-19.
GUO Feng-bo, LIU Yu-cun, LIU Deng-cheng, et al. The synthesis of 2, 6-dianimo-3, 5-dinitropyrazine-1-oxide process improvement [J].ChineseJournalofExplosivesandPropellants, 2006, 21(3): 17-19.
[12] 刘进全, 陈树森, 欧育湘, 等. 1-氧-2,6-二氨基-3,5-二硝基吡嗪(LLM-105)的合成[J].化学通报. 2006, 69(2): 151-153.
LIU Jin-quan, CHEN Shu-sen, OU Yu-xiang, et al. Synthesis of 2, 6-diamino-3, 5-dinitropyrazing-1-oxide (LLM-105)[J].Chemistry, 2006, 69(2): 151-153.
[13] Mixan C E, Pews R G. Selective N-oxidations of chlorinated pyrazines and quinoxalines[J].JournalofOrganicChemistry, 1977, 42(11):1869-1871.
[14] Frisch M J, Trucks G W, Schlegel H B, et al. Gaussian 03, Revision D.01, Gaussian[CP/DK]. Inc., Wallingford CT, 2004.
[15] Politzer P, Murray J S, Grice M E,et al. Calculation of heats of sublimation and solid phase heats of formation[J].MolecularPhysics, 1997, 91(5): 923-928.
[16] 田德余, 赵凤起, 刘剑洪, 编著. 含能材料及相关物手册 [M]. 国防工业出版社. 2011.

