基于模糊C均值法的CTA图像冠状动脉狭窄量化
孙巧榆 杨冠羽 舒华忠
(1东南大学影像科学与技术实验室,南京 210096)(2东南大学中法生物医学信息研究中心,南京 210096)(3淮海工学院电子信息工程系,连云港 222005)
基于模糊C均值法的CTA图像冠状动脉狭窄量化
孙巧榆1,3杨冠羽1,2舒华忠1,2
(1东南大学影像科学与技术实验室,南京210096)
(2东南大学中法生物医学信息研究中心,南京210096)
(3淮海工学院电子信息工程系,连云港222005)
摘要:针对冠状动脉造影图像中由软斑块造成的冠状动脉狭窄,提出了一种基于模糊C均值法的狭窄精确量化方法.首先,在沿冠状动脉中心线的三维数据图上,对专家给定起讫位置的冠状动脉血管片段进行切割和阈值化.其次,利用模糊C均值法分割出血管腔区域,计算血管每个横截面的血管腔面积检测值,通过起讫位置的检测面积拟合得到参考值.然后,通过比较血管横截面面积的检测值和参考值来确定分段中最狭窄的位置及其狭窄比率.最后,利用该方法对13个病人的CTA数据进行了测试,并将测试结果与专家给出的狭窄比率进行比较.结果表明,所提方法能够对CTA中给定起讫位置的冠状动脉血管片段的狭窄区域进行精确量化,狭窄比率的平均绝对差和均方根差分别为2.21%和3.11%.
关键词:模糊C均值;狭窄量化;软斑块;血管分割; CTA
引用本文:孙巧榆,杨冠羽,舒华忠.基于模糊C均值法的CTA图像冠状动脉狭窄量化[J].东南大学学报(自然科学版),2016,46(1) : 30-34.DOI: 10.3969/j.issn.1001-0505.2016.01.006.
冠状动脉疾病(CAD)是全球首要致死原因[1].冠状动脉CT造影(CCTA)作为一种新发展起来的心脏无创成像方法,正越来越多地应用于冠心病的早期诊断中.最新的临床研究表明,冠状动脉CT造影成像是目前无创成像方法中进行冠状动脉易损斑块检测的最为有效的方法[2].但冠状动脉的狭窄等级很大程度上需要依靠心脏病专家通过手工绘制来确定,从而不可避免地造成观测者间差异(inter-observer variability)和观测者自身差异(intra-observer variability).此外,一个冠状动脉CT造影体数据通常包括200幅以上的二维图像,带给医生巨大的读片工作量.因此,临床上需采用自动化系统或算法来提供辅助诊断,以提高工作效率和分割准确性,减少手工标定带来的偏差.
近年来涌现出越来越多关于冠状动脉狭窄的检测和量化的方法.Dey等[3]根据图像灰度信息确定后续分割需要的血管腔、钙化斑块和软斑块等区域的一系列阈值,采用基本的图像处理算法对冠状动脉中的斑块进行量化分析.Kelm等[4]实现了一个基于冠状动脉CT造影图像的血管狭窄检测系统,该系统利用非线性回归算法估计2D血管横截面中的血管半径,并由此确定血管的狭窄位置.Xu等[5]利用模糊距离变换来检测并量化CTA中的冠状动脉狭窄.Shahzad等[6]采用图割法进行管腔分割,根据轮廓直径的估计值和预期值之间的差别来检测并量化狭窄.血管片段的起讫位置是血管狭窄量化的关键因素,然而,上述方法中血管片段的起讫位置是由使用的分割算法来决定的,容易受噪声、血管分叉、伪影等影响而产生估计偏差,导致狭窄量化结果不准确.
本文针对冠状动脉造影图像中由软斑块造成的冠状动脉狭窄,提出了一种基于模糊C均值的狭窄精确量化方法.首先,对专家给定起讫位置的冠状动脉血管片段进行切割和阈值化,然后利用模糊C均值(FCM)法将血管区域分割出来,通过计算血管分段上各横截面中血管面积的参考值和检测值来完成狭窄的量化,为临床诊断提供帮助,避免人工估计的主观误差.
1 方法
本文主要针对给定起讫位置的血管分段分割和狭窄量化.首先,进行切割和阈值化等预处理操作以提高方法的计算效率,利用模糊C均值法对冠状动脉血管片段的管腔进行分割.然后对分割结果进行进一步精细化处理,降低分叉和噪声所带来的干扰.狭窄的量化则通过计算每层血管面积的参考值和检测值来获得.
1.1预处理
采用文献[7]的方法提取冠状动脉中心线.在MeVisLab软件中,沿中心线上的点将CTA中的冠状动脉血管拉直并重建为3D数据.
图1给出了正视角下冠状动脉的长轴图和冠状动脉中间位置(L/2处)的横截面图.长轴图起始于主动脉,其直径从近心端到远心端呈下降趋势.图中,L为冠状动脉的长度; W,H分别为重建后冠状动脉横截面的宽度和高度.由图1(b)可知,血管区域中心与截面图中心贴近,且冠状动脉的直径小于横截面图边长的1/2.因此,可以对图像数据进行切割,如图1(b)中矩形边框所示.切割后的数据量仅为原来的1/4,从而减少了计算时间,并避免了部分周围组织对后续处理的干扰.

图1 冠状动脉的长轴图和横截面图
切割处理可以去掉外围区域中包含的一些与血管区域灰度值接近的周围组织,但仍然有一些离血管较近的组织(如心肌)被保留下来,这些组织会对后续血管的准确分割造成影响.因此,需要对切割后的冠状动脉片段进行阈值化,即
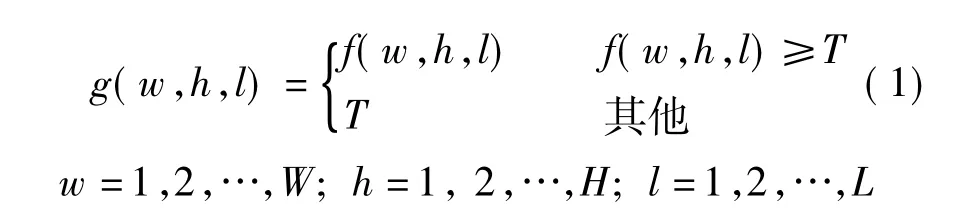
式中,f(w,h,l),g(w,h,l)分别表示坐标为(w,h,l)的体素的初始灰度值和阈值化后的灰度值; T为阈值.
阈值化操作使得目标和背景区域之间的对比度降低,从而减小了非血管组织对于分割结果的干扰,提高了分割准确度.
1.2血管分割
本文采用FCM算法[8]来分离血管腔区域.FCM算法的主要思想是:为一个数据点集合xj∈Rd(j =1,2,…,N)寻找一个分割(c个模糊集群)使得代价函数最小,即
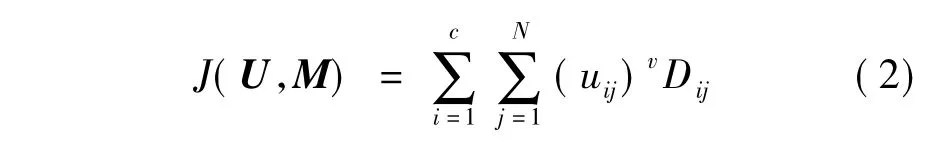
式中,uij∈[0,1]为第j个目标在第i个集群中的隶属度系数; U = (uij)c×N为模糊集群矩阵; M = [m1m2…mc]为集群原型(均值或中心)矩阵; v∈[1,∞)为模糊化参数,一般取v = 2; Dij= Dist(xj,mi)为xj与mi之间的Euclidean距离.
FCM分割算法的具体步骤参见文献[9].本文中,冠状动脉的分割步骤如下:
①令c =2,即输入数据被分为血管区域和背景区域2类,步长变量t =0.随机初始化原型矩阵M.
②若t =0,计算隶属度矩阵U;若t>0,更新U,即
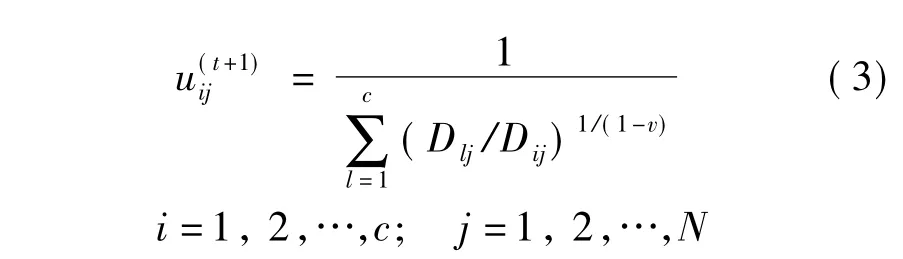
③更新原型矩阵M,即
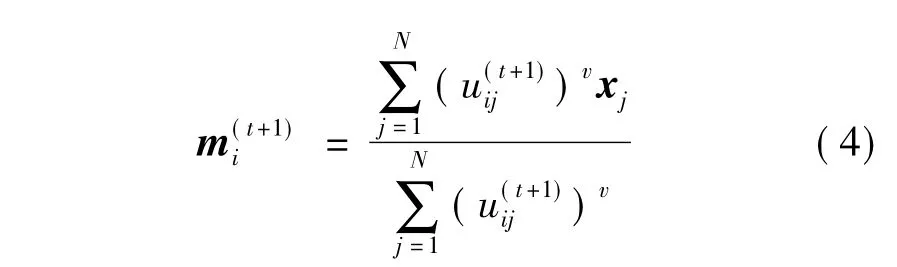

图2 血管分段1的长轴图及部分横截面上的分割结果
图2给出了一个具有明显狭窄的血管分段1及其所在冠状动脉的长轴图.lstart,lend,lsten分别表示专家给出的冠状动脉分段的起始层、终止层和最狭窄处所对应的层序号.
分割算法常常会将分叉血管归为目标区域,若狭窄的位置正好在冠状动脉的分叉处,则会影响狭窄量化的正确性.一般来说,相邻层的血管腔直径是渐变的,因此,可以利用分叉处血管的邻近横截面分割结果来校正分叉处的分割结果.
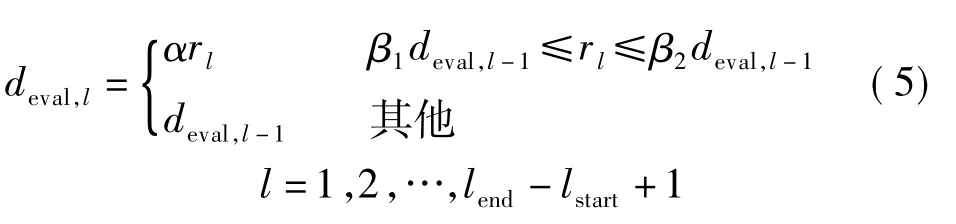
定义一个直径为deval的圆的序列,则第l层血管直径的预测值deval,l为为血管中心点至血管边界处的最短行程长度; rl,θ为θ方向上横截面中心到血管边界处的行程长度,θ=0°,45°,90°,135°; lend-lstart+ 1为血管片段的层数;α>1为乘数因子,用于修正血管中心与横截面图中心的偏差,以确保deval所定义的圆可以覆盖整个血管区域;β1,β2为系数,用于避免出现因噪声或狭窄导致相邻横截面之间变化过大或过小的预测直径.
图3(a)为血管分叉处横截面的初始分割结果;图3(b)中标出了中心点处的4个行程长度.血管的预测直径deval由式(5)得到,并用圆覆盖在分割结果图上,结果见图3(c).精细化后分叉部分被除去,检测出的血管区域更接近于真实的血管区域,结果见图3(d).根据精细化后的分割结果来预测每一层的血管区域面积,误差将显著减小.
式中,rl=
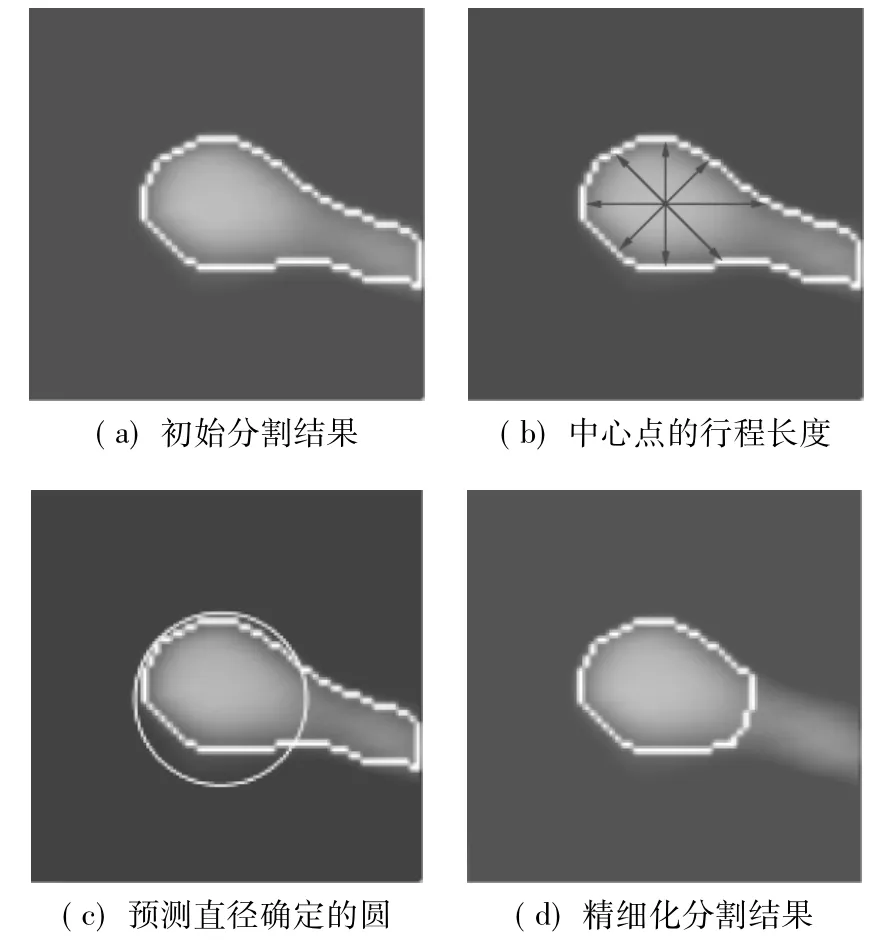
图3 精细化分割结果示例图
1.3狭窄量化
分割后,计算血管片段中每一层血管区域面积的检测值,并且根据起始层和终止层的血管腔面积拟合出血管面积的参考值,然后利用检测值和参考值来定位血管的最狭窄位置及其狭窄比率.
图4给出了血管片段2的狭窄量化示例.图4(b)为图4(a)中血管片段各层的血管面积检测值及参考值的变化曲线.由于冠状动脉血管的横截面面积呈缓慢下降趋势,并且健康血管的横截面积下降趋势更加平滑.因此,可以根据血管片段的起讫层的血管横截面面积来估计整个血管片段上每一层的参考值[10].

图4 冠状动脉血管片段2的狭窄量化示例
第l层横截面上血管的狭窄比率为
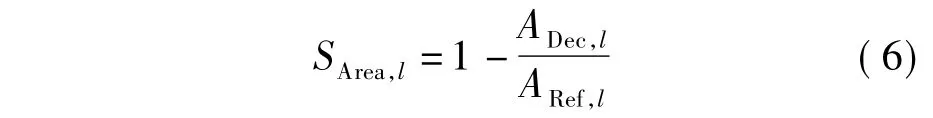
式中,ARef,l和ADec,l分别是第l层横截面上血管面积的参考值和检测值.
整个血管片段的最狭窄比率为
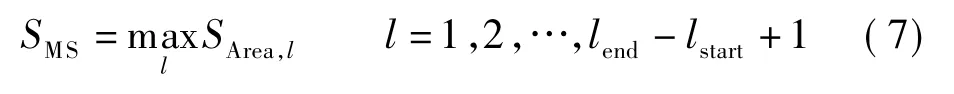
2 实验结果及讨论
本实验中所用的CTA图像数据来自于13个病人,通过Siemens双螺旋64层CT扫描仪获取.其轴位图像的大小为512×512像素,平均轴向分辨率约为0.33 mm,2幅轴向片之间的距离为0.5 mm.放射科专家标记出19处狭窄.专家通过Siemens Syngo CT冠状动脉分析软件来测量狭窄比率.狭窄比率的范围为0~100%,变化步长为5%.令T =1 000,α=1.2,β1=0.8,β2= 1.2.实验在64位台式PC (Intel Core i5 CPU,4G RAM,2.8 GHz)上利用Matlab(R2009a)软件单线程运行.一根长约10 mm的血管片段的运行时间约为12.8 s.
将血管片段k的狭窄量化误差定义为检测出的最狭窄比率SMS,k与专家给出的参考值SMGT,k之间的差值,即
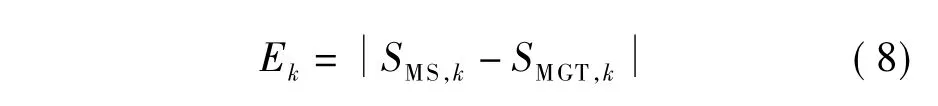
该数据集的狭窄比率的平均绝对差(AAD)和均方根差(RMSD)分别定义为
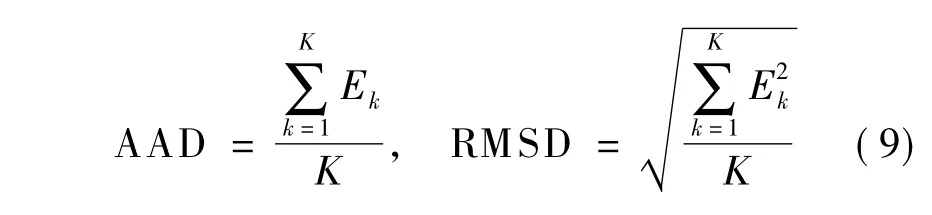
式中,K为测试数据集中狭窄的个数.
为了验证本文方法的有效性,将分割结果与基于高斯混合模型(GMM)的方法以及基于CM的方法[9]的分割结果进行比较,结果见表1.由表可知,本文方法的检测性能最佳,狭窄比率的平均绝对差和均方根差分别为2.21%和3.11%.基于GMM的方法和基于CM的方法的检测性能基本相同,且后者略好,但由于其分割结果具有不确定性,故其性能不够稳定.
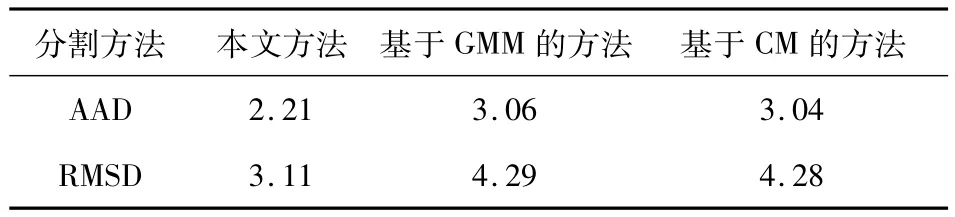
表1 3种方法的性能比较 %
利用本文方法与其他2种方法对血管片段3进行分割,结果对比见图5.血管片段3开始于血管分叉的位置,且血管的最狭窄位置也在附近(见图5(a) ).专家给出的最狭窄比率为20%,利用本文方法、基于GMM的方法和基于CM的方法所得到的狭窄比率则分别为19.77%,31.46%和31.46%.从图5(b)中可以看出,基于GMM的方法和基于CM的方法在血管起始位置处分割出的血管区域偏大,将分支血管部分错分为血管区域,故起始位置处血管面积的检测值偏大,健康血管面积的预测值也偏大,导致计算得到的最狭窄位置的狭窄比率偏大.
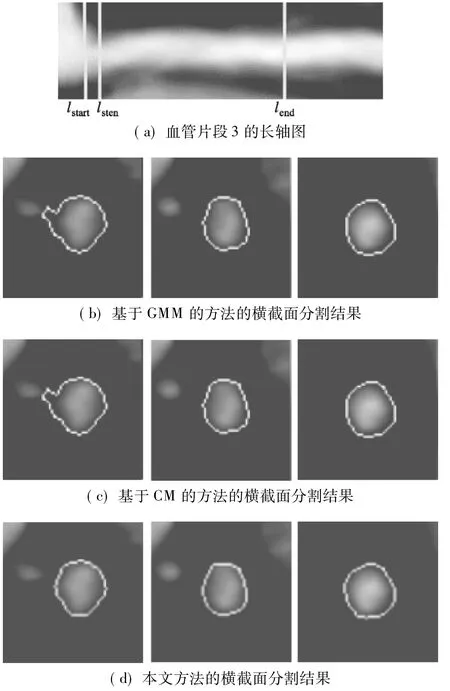
图5 本文方法与其他方法的分割结果比较
本文方法是一个针对CTA数据的冠状动脉狭窄精确量化方法.与其他方法不同,该方法直接对专家定义的血管片段进行狭窄量化,而非根据算法自动检测出的可能包含检测偏差的血管片段.利用本文方法得到的实验结果与专家给出的参考值吻合较好,故该方法可为放射科或心脏科医生提供精确的狭窄等级估计.
本实验所针对的血管分段主要是冠状动脉的近段和中段.鉴于部分容积效应,本文方法针对远段血管的可行性还有待验证.此外,本实验所用数据集仅包含了13个病人的19段血管,未来需要在更多的数据集上验证本文方法的有效性.由于X射线血管造影术和内血管超声(IVUS)常被用作临床狭窄量化的精确参考,下一步还可利用这些仪器对本文方法进行验证,以进一步提高精确性.
3 结论
冠状动脉的管腔分割是CAD计算机辅助诊断的关键技术之一.随着64层CT的广泛使用,CTA中冠状动脉管腔和斑块的分割方法成为研究焦点.本文提出了一个精确的CTA图像冠状动脉狭窄量化方法.首先,经过一些必要的预处理后,利用FCM算法来判别血管片段的血管区域与背景区域;其次,对分割结果进行精细化处理;然后,逐层比较血管横截面面积的参考值和检测值,以确定最狭窄位置及狭窄比率;最后,在包含13个病人的CTA数据集上进行测试,验证了本文方法对冠状动脉狭窄量化的有效性.
参考文献(References)
[1]Mackay J,Mensah G A,Mendis S,et al.The atlas of heart disease and stroke[M].Geneva,Switzerland: World Health Organization,2004: 5-6.
[2]Vancraeynest D,Pasquet A,Roelants V,et al.Imaging the vulnerable plaque[J].J Am Coll Cardiol,2011,57 (20) : 1961-1979.DOI:10.1016/j.jacc.2011.02.018.
[3]Dey D,Cheng V Y,Slomka P J,et al.Automated 3-dimensional quantification of noncalcified and calcified coronary plaque from coronary CT angiography [J].J Cardiovasc Comput Tomogr,2009,3(6) : 372 -382.DOI: 10.1016/j.jcct.2009.09.004.
[4]Kelm B,Mittal S,Zheng Y,et al.Detection,grading and classification of coronary stenoses in computed tomography angiography[C]/ /International Conference on Medical Image Computing and Computer-assisted Intervention.Toronto,Canada,2011: 25-32.
[5]Xu Y,Liang G,Hu G,et al.Quantification of coronary arterial stenoses in CTA using fuzzy distance transform [J].Comput Med Imaging Graph,2012,36(1) : 11-24.DOI:10.1016/j.compmedimag.2011.03.004.
[6]Shahzad R,Kiri爧li H,Metz C,et al.Automatic segmentation,detection and quantification of coronary artery stenoses on CTA[J].Int J Cardiovasc Imaging,2013,29(8) : 1847-1859.DOI:10.1007/s10554-013-0271 -1.
[7]Yang G,Kitslaar P,Frenay M,et al.Automatic centerline extraction of coronary arteries in coronary computed tomographic angiography[J].Int J Cardiovasc Imaging,2012,28(4) : 921-933.DOI:10.1007/s10554-011-9894-2.
[8]Dunn J C.A fuzzy relative of the ISODATA process and its use in detecting compact well-separated clusters[J].Journal of Cybernetics,1973,3(3) : 32-57.DOI: 10.1080/01969727308546046.
[9]Xu R,Wunsch DⅡ.Survey of clustering algorithms [J].IEEE Transactions on Neural Networks,2005,16 (3) : 645-678.DOI: 10.1109/TNN.2005.845141.
[10]Broersen A,Kitslaar P,Frenay M,et al.French Coast: Fast,robust extraction for the nice challenge on coronary artery segmentation of the tree[C]/ /MICCAI Workshop 3D Cardiovascular Imaging: a MICCAI segmentation challenge.Nice,France,2012: 1-8.
Stenosis quantification of coronary artery CTA images based on fuzzy C-means algorithm
Sun Qiaoyu1,3Yang Guanyu1,2Shu Huazhong1,2
(1Laboratory of Image Science and Technology,Southeast University,Nanjing 210096,China)
(2Centre de Recherche en Information Bimédicale Sino-Français,Southeast University,Nanjing 210096,China)
(3Department of Electric Information Engineering,Huaihai Institute of Technology,Lianyungang 222005,China)
Abstract:As for coronary artery stenosis caused by soft plaques in coronary artery angiography images,an accurate stenosis quantification method based on the fuzzy C-means algorithm is proposed.First,the segment of the coronary artery with starting and ending positions defined by experts is cropped and thresholded on the three-dimensional data along the centerline.Secondly,the fuzzy C-means algorithm is applied to separate the region of vessel lumen from other tissues.The detected value of the vessel lumen area in each slice is computed and the reference value is fitted by the detection area between the starting and ending positions.Then,the location and the ratio of the most stenosis are determined by comparing the detected value with the reference value of the vessel area.Finally,the proposed method is tested on clinical computed tomography angiography (CTA) datasets of thirteen patients and the detection results are compared with the stenosis ratios defined by experts.The experimental results indicate that the proposed method can accurately quantify the stenosis of the coronary artery segment with given starting and ending positions in CTA.The absolute average difference and the root mean squared difference of the stenosis ratios are 2.21% and 3.11%,respectively.
Key words:fuzzy C-means; stenosis quantification; soft plaque; vascular segmentation; computed tomography angiography(CTA)
基金项目:国家自然科学基金资助项目(61271312,81101104)、江苏省自然科学基金资助项目(BK2012743)、江苏省“六大人才高峰”资助项目(2012 DZXX-031)、江苏省“333高层次人才培养工程”资助项目(BRA2015288)、江苏省博士后科学研究基金资助项目(1302018C).
收稿日期:2015-09-24.
作者简介:孙巧榆(1973—),女,博士,副教授;杨冠羽(联系人),男,博士,副教授,yang.list@ seu.edu.cn.
DOI:10.3969/j.issn.1001-0505.2016.01.006
中图分类号:TP301.5
文献标志码:A
文章编号:1001-0505(2016) 01-0030-05

