太湖沉积物中重金属的垂向分布特征及迁移转化
杨 陈,王沛芳*,刘佳佳,王 超,侯 俊,钱 进
(1.河海大学浅水湖泊综合治理与资源开发教育部重点实验室,南京210098;2.河海大学环境学院,南京210098)
太湖沉积物中重金属的垂向分布特征及迁移转化
杨陈1,2,王沛芳1,2*,刘佳佳1,2,王超1,2,侯俊1,2,钱进1,2
(1.河海大学浅水湖泊综合治理与资源开发教育部重点实验室,南京210098;2.河海大学环境学院,南京210098)
摘要:为了解太湖沉积物中重金属污染的变化特征和迁移规律,选取太湖柱状沉积物为研究对象,测定Cd、Pb、Cu、Cr 4种重金属的总量及赋存形态,分析重金属在垂向上的分布状况及污染程度。结果表明,金属Cd、Pb、Cu、Cr的含量随着深度的增加而降低,并在1950年和1980年出现拐点,其中1980年污染最为严重;湖区分布特征表现为西北部梅梁湾、竺山湾和贡湖湾的重金属污染最为严重,湖心次之;重金属的赋存形态均以残渣态为主,Cd、Pb、Cu、Cr的残渣态分别占59.74%、81.67%、77.81%、97.56%,除残渣态外,Cd 和Cu的可交换态含量较高,分别占15.81%、13.62%,而Pb的铁锰化物结合态所占比例较高,平均为11.36%。通过计算淋失比可知,重金属在上层沉积物中的迁移率较高,而下层沉积物中的重金属较稳定,迁移性较弱;分析重金属的形态迁移可知,表层沉积物中重金属的可交换态较多,由细颗粒物质等吸附直接沉淀在表层沉积物中,随着泥沙的运动逐渐向下迁移;随着沉积物中铁锰化物的积累、AVS(酸可挥发性硫化物)积累等环境条件的变化,可交换态向铁锰化物结合态、有机物及硫化物结合态转化。
关键词:太湖;柱状沉积物;重金属;垂向分布;迁移转化
杨陈,王沛芳,刘佳佳,等.太湖沉积物中重金属的垂向分布特征及迁移转化[J].农业环境科学学报, 2016, 35(3):548-557.
YANG Chen, WANG Pei-fang, LIU Jia-jia, et al. Vertical distribution and migration of heavy metals in sediment cores of Taihu Lake[J]. Journal of Agro-Environment Science, 2016, 35(3): 548-557.
太湖位于长江中下游,是中国第三大淡水湖泊,随着流域周边经济发展以及人口增长,污染状况愈加明显,其中重金属因其持久性、生物毒性和生物积累作用[1],给生态系统和人类健康带来巨大的威胁。水生系统中,超过90%的重金属与悬浮颗粒物和沉积物有关[2],沉积物作为水生生态系统中重金属的主要储存库和来源,在运输和储存潜在有毒重金属的过程中扮演着重要的角色[3]。在工业发展和城市化的进程中,不同历史时期人类活动对湖泊沉积物重金属的污染具有显著影响[4]。自20世纪80年代以来,太湖沉积物中人为活动导致的重金属含量逐年增加[5],竺山湾和梅梁湾尤为严重[6]。而近年来,重金属已经严重威胁到太湖水体中的水生植物和水生动物。虽然对沉积物中重金属污染的研究很多,但是关于沉积物重金属在垂向上的迁移转化研究还很少。调查沉积物柱状样中重金属含量的历史变化有助于我们认识湖泊重金属的演化历史,研究重金属在沉积物中的迁移规律对治理沉积物的重金属污染和预测将来环境演化趋势具有一定的指导作用。
本文测定了太湖全湖区柱状沉积物中的重金属含量,结合沉积速率,反演了不同历史时期重金属的污染水平,以便了解沉积物中重金属的垂向分布特征和污染情况,分析重金属在沉积物中的迁移性,并研究重金属赋存形态的分布来探讨重金属在垂向上的迁移转化规律,旨在为太湖重金属污染治理提供理论依据。
1 材料与方法
1.1沉积物样品的采集
为了解重金属的垂向分布,利用柱状采样器,于2010年4月在太湖上采集沉积物样品,采样点按地理位置和沿岸特征划分为8个湖区,如图1所示。现场采用GPS导航定位,采得的柱状样长度20 cm左右,现场按2 cm切割。现场采用活塞式柱状采样器,取样时将采样器平放在地面上,活塞推杆慢慢将泥样推出,尽量保持泥样的形状,快速测量并进行切割,泥样用干净的聚氯乙烯密封袋密封保存,迅速带回实验室,于-80℃冰箱内冷冻干燥,研磨至100目,放入干燥自封袋中保存备用。
1.2沉积物样品的分析方法
1.2.1沉积物重金属总量分析
取0.2 g待测样品于聚四氟乙烯消解罐中,加入6 mL HNO3,静置30 min后依次加入4 mL HF和1 mL H2O2,在Berghof -MWS-3+微波消解系统中消解,冷却后全量转移至聚四氟乙烯坩埚中,加入0.5 mL HClO4,于红外电热板上加热(340℃)至近干,加1 mL (1+1)HNO3微热溶解残渣,冷却后利用纯水定容至25 mL,上清液移至10 mL离心管中备测。消解过程同时做空白样和平行样的实验,所有的玻璃仪器和聚四氟乙烯坩埚在使用前均用10%的硝酸溶液浸泡,然后用纯水冲洗干净。
1.2.2沉积物中不同赋存形态重金属的提取方法
对于沉积物中重金属赋存形态的提取方法有Tessier的“五步连续提取法”[7]、Forstner的“连续提取法”[8]以及BCR提取方法[9]。鉴于BCR方法具有窜相效应较低、步骤相对简便等优点,故采用改进的BCR连续提取法提取沉积物中不同形态的重金属。
1.3分析方法
所有提取液中的重金属含量采用ICP-MS(Agilent 7700)分析。
1.4数据处理
利用SPSS 21对各层重金属含量进行相关性分析。相关性分析是指对两个或多个具备相关性的变量元素进行分析,从而衡量两个变量因素的相关密切程度。采用Origin 2015对处理结果进行绘图。
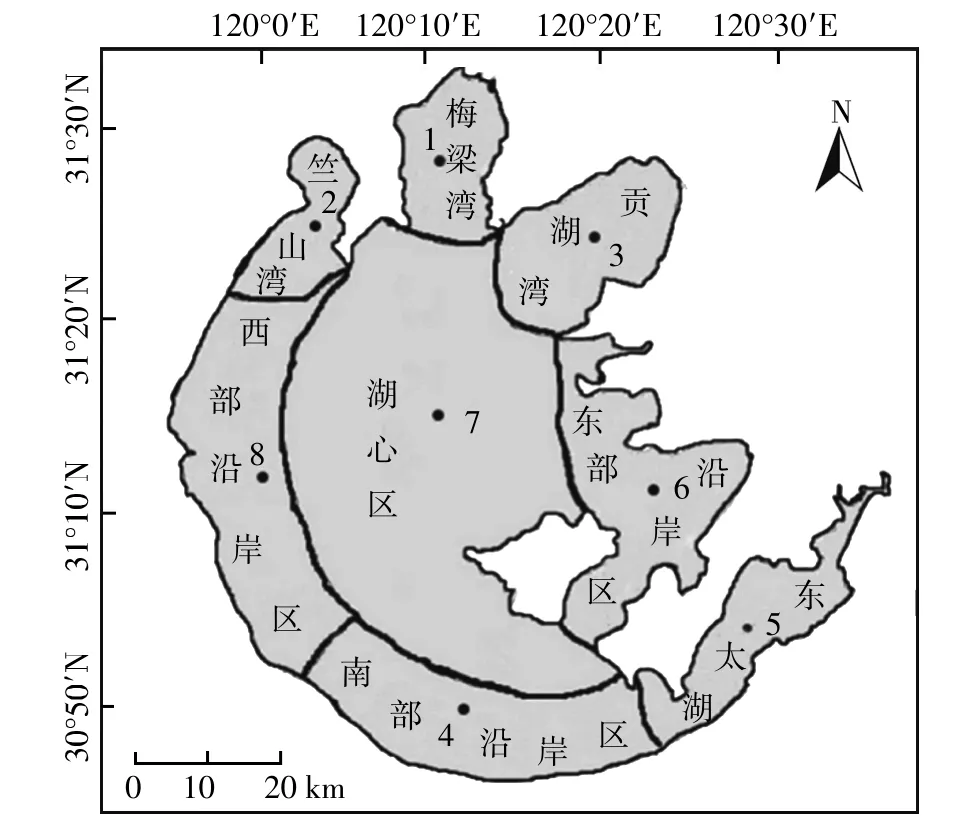
图1 太湖湖区划分及采样点Figure 1 Regions and sampling sites of Lake Taihu
2 结果与讨论
2.1沉积物重金属垂向分布特征及污染特征
2.1.1重金属总量的垂向分布
太湖全湖区表层沉积物中Cd、Pb、Cu和Cr总量的均值分别为1.97、46.5、40.0、86.8 mg·kg-1,是太湖流域土壤背景值的7.88、2.49、2.2和1.12倍,Cd的含量远大于太湖土壤背景值,Cr的含量与太湖流域土壤背景值相近,和之前的研究结果[10]类似。从图2中可以看出,Cd、Pb、Cu和Cr的总量都随着沉积深度的增加而下降,且在深度为12 cm和6 cm处出现较大的拐点,根据太湖沉积物的沉积速率0.2 cm·a-1[11],12 cm和6 cm分别对应1950年和1980年,分别是太湖流域周边经济发展的初期和高峰期。6 cm处Cd、Pb、Cu和Cr的含量分别为1.42、39.2、31.2、81.0 mg·kg-1,是背景值的5.68、2.10、1.72、1.05倍;12 cm处的金属含量分别为0.64、26.2、18.7、74.2 mg·kg-1,是背景值的2.56、1.4、1.03、0.96倍。
Cd和Pb在梅梁湾和竺山湾表现出相似的变化趋势,相对于其他点位来说这两种金属的含量较高,且在6 cm处有大幅度的增加,梅梁湾处Pb的含量比竺山湾处高;Cu和Cr在梅梁湾的6 cm处出现很大的拐点,即1980年时梅梁湾的底泥中沉积了大量的Cu和Cr,梅梁湾处的Cr含量是全湖区最高的;竺山湾处的Cu和Cr在1980年时也出现较大幅度的增加。贡湖湾的Cd和Pb在1980年大幅度增长后一直居高不下,Cu的含量在1980年前后有较大的增长,之后变化不大;Cr在1950年出现小拐点后一直在快速增长,表层浓度达到86.1 mg·kg-1,是背景值的1.09倍。南部沿岸区各金属浓度的变化趋势类似,在1980年时有大幅度增加,之后变动很小。
在各湖区中,东太湖和东部沿岸区的各重金属含量较低,除Cd在1950—1980年间有较大增长外,其他金属变化幅度不大,一直处于上升的状态。湖心区的Pb和西部沿岸区的Cd污染很严重,于太湖土壤背景值而言,分别超标95.3%、311%,湖心区的Cu和Cr的含量也很高,分别为34.1、87.1 mg·kg-1,表层沉积物中Cr的含量达到109 mg·kg-1,仅次于梅梁湾;西部沿岸区的Cu在1950—1980年间增幅明显,而Cr 在1980年出现拐点,之后一直小幅增长。
Cd的污染在各个湖区都很严重,其中梅梁湾、竺山湾和湖心处污染尤为严重,而贡湖湾在近年来的污染较为突出,甚至在表层沉积物中已经出现偏重污染;Pb在西部和南部沿岸处和湖心的污染较严重;Cu在梅梁湾、竺山湾和湖心处含量较高;Cr在各个湖区都是轻度污染,但在梅梁湾和湖心处Cr的浓度明显比其他湖区的浓度高很多。
西北部湖区的污染比较严重,可能是由于梅梁湾和竺山湾位于太湖的入湖口,接纳来自周边城市的生活污水、工业废水以及农业灌溉等,无锡和常州的加工和制造业发达,化工、纺织业等产生的污水未经妥善处理直接排入太湖中,工业废水中重金属含量高,而农业污水中包含农药、化肥等。因此,来水成分众多,来源复杂,且易沉积,导致西北部湖区的重金属污染问题十分突出,一直以来都受到政府和专家的高度重视[12]。而东太湖的重金属污染较轻,可能是因为东太湖位于出水口,水体中携带的污染物质较少,且东太湖是草型湖区,沉水植物较多,可以吸附大量的重金属,导致底泥中的重金属含量较少。
对重金属进行相关性分析可知,在全湖区Cd和Pb表现出显著的正相关性(r=0.82,P<0.05),尤其是梅梁湾、竺山湾和贡湖湾的相关系数达到0.98(P<0.05),说明这两种金属具有相似的污染源和污染程度。Cd和Pb主要来自电镀等工业,而离北部湖湾最近的无锡和常州地区的电镀、机械制造和冶炼等工业发达,其产生的重金属污染能够经直湖港和梁溪河排入太湖[13],在入湖口的位置累积,使得污染持续严重。Zhang等[14]也证明武进港是梅梁湾污染的重要输入源。Cu和Cr的相关系数也很高,可能是因为两者的污染程度较轻,且与Cd、Pb的污染源不同[15]。
2.1.2沉积物重金属的赋存形态
对各湖区重金属赋存形态的垂向分布进行分析,结果如图3所示。四种金属均以残渣态为主,平均分别占59.7%、81.7%、77.8%、97.6%。Cd的可交换态和铁锰化物结合态所占比例较多,分别占15.8%、16.6%;Pb的铁锰化物结合态所占比例较高,Cu的可交换态占13.6%,Cr的残渣态占了绝大部分,所占比例在95%以上。
在不同湖区中,不同重金属赋存形态的分布也不同。梅梁湾和竺山湾中Cd的可交换态和铁锰化物结合态所占比例较高,可交换态在梅梁湾和竺山湾中的比例分别为3.4%~21.1%、18.6%~24.9%,铁锰化物结合态的比例分别为15.3%~28.9%、19.0%~23.2%;Pb的赋存形态在各湖区的分布类似,湖心区Pb的铁锰化物结合态所占比例最高,在8.04%~23.8%之间;Cu的可交换态较多,在各湖区中,又以竺山湾和东太湖为多,分别为19.9%~36.0%、25.6%~27.2%;各湖区中Cr的残渣态占了绝大部分,可提取态含量极少,可利用率很低。
2.2重金属的迁移与转化
2.2.1重金属的迁移率

图2 各湖区重金属总量垂向分布图Figure 2 Vertical distribution of heavy metals in sediments

续图2 各湖区重金属总量垂向分布图Continued figure 2 Vertical distribution of heavy metals in sediments
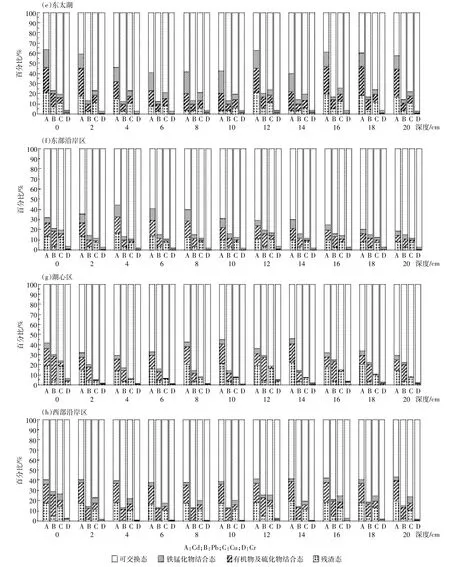
续图3 重金属赋存形态垂向分布图Continued figure 3 Vertical distribution of heavy metal fractions in sediments
为了解重金属在垂向上的迁移规律,需要分析柱状样中重金属的含量变化。重金属在土壤中的迁移率也称为淋失比率,可用来比较重金属在土壤中的迁移特征,本文以淋失比率来分析重金属在沉积物中的迁移特性。李亮亮等[16]提出了改进后的淋失比率计算公式如下:
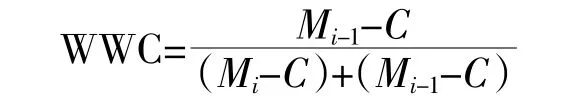
式中:WWC为i层某元素的迁移率;Mi-1为i-1层中某元素的含量,mg·kg-1;Mi为i层中某元素的含量,mg·kg-1;C为当地土壤背景值,mg·kg-1。
计算结果表明,梅梁湾和竺山湾在12 cm处的迁移率开始上升,且Cd和Pb的迁移率较高,Cd在梅梁湾和竺山湾的迁移率分别达到0.488、0.495,Pb为0.479、0.489;12 cm以下Cd和Pb的迁移率在0.20左右,而12 cm以上Cd和Pb的迁移率都快速上涨,表明上层沉积物中重金属的活性比下层的高很多。贡湖湾从4 cm处开始重金属的迁移率出现大幅度的增长,Cd、Pb和Cu的迁移率从0.367、0.317、0.198增长到0.443、0.489、0.494,而Cr的迁移率变化很小。东太湖和东部沿岸区Cd和Cu分别是从4 cm和6 cm处迁移率上升,Cr的迁移率在垂向上变化不大。西部沿岸区和南部沿岸区Cd都是从10 cm处迁移率增长,活性增加,Cu是从6 cm开始活跃。湖心区Cd、Pb和Cu的迁移率都是从12 cm处开始增长,其后也都处于增长中,直至表层。通过分析柱状沉积物各层间重金属含量的相关性也发现各湖区表层沉积物(0~2 cm)与2~6 cm层间存在显著的正相关性(r=0.979,P<0.05),而表层与8 cm处的正相关性开始降低(r= 0.886,P<0.01),也表明沉积物上层之间的活跃性很高,下层间的迁移率则显著下降。
2.2.2不同形态的重金属迁移性
不同形态的重金属的迁移和转化与沉积物自身特性和沉积环境密切相关。重金属通过吸附、离子交换、沉淀和络合等不同的方式与沉积物中的微粒结合在一起[17],形成不同形态的重金属。而不同形态的重金属浓度可以给重金属的释放潜力、毒性和迁移性等提供很多信息[18]。可交换态在酸性条件下,易被重新释放;铁锰化物结合态在氧化还原电位下降或缺氧时易被还原;有机物及硫化物结合态相对较稳定,在强氧化条件下才会被释放;残渣态性质非常稳定,对重金属的迁移和生物的毒性不大,所以一般认为对环境是安全的[19]。一般将可交换态、铁锰化物结合态、有机物及硫化物结合态称为可提取态,通过研究可提取态的分布可以分析重金属的迁移规律。
从图2的形态分布结果发现,四种金属的可提取态中,Cd的可交换态和铁锰化物结合态含量较高,因此Cd的活性很强,很容易迁移;Pb则是铁锰化物结合态的浓度高,在缺氧或氧化还原电位下降时,就会重新释放,但近年来的污染趋势有所缓解;Cu的可交换态含量较高,铁锰化物结合态和有机物及硫化物结合态所占比例差不多,因此Cu的迁移性也很强;Cr的可提取态所占比例极少,迁移性很弱,对生物的毒性也很低。梅梁湾和竺山湾位于入湖口位置,表层沉积物中可交换态含量明显较高,可能是由于表层沉积物与水相互动频繁,水相中的金属离子与碳酸盐等结合随即沉淀下来;贡湖湾中Cd和Cu的增加都集中在上几层沉积物中,表明重金属污染发生在近些年,Pb的铁锰化物结合态在10 cm处(1960年)有明显的增长;南部沿岸区和西部沿岸区中,Cd、Pb和Cu的可交换态在1950年后的沉积物中有较明显聚集,而Pb的铁锰化物结合态在亚表层的聚集现象明显,含铅汽油被认为是环境中Pb的主要来源,而最上面一层的Pb有下降趋势是由于中国自1990年代以来含铅汽油的禁止使用[20],东太湖及东部沿岸区中,Cd、Pb和Cu在上层沉积物中有机物及硫化物结合态含量较高,但与下层沉积物中的含量差异不大;湖心区中Cd和Cu的可交换态在1950年左右开始大幅增加,最表层和亚表层中的含量达到峰值。
人为输入会影响沉积物中的金属元素迁移,除了污染,沉积物本身的特性如粒径大小、有机碳、AVS(酸挥发性硫化物)等对沉积物中重金属的分布和迁移也有很大的影响[20]。如图4所示,细颗粒即微粒从水相中吸附金属离子形成可交换态沉淀到沉积物表层中,从而在环境条件(如含氧量等)变化时,可转化成铁锰化物结合态,上层沉积物中有机质含量较高,有机物及硫化物结合态含量亦较高,而下层沉积物处于厌氧环境下,AVS等因素使得有机物及硫化物结合态含量没有减少。
细颗粒沉积物可以很好地结合重金属,高浓度的细颗粒物会降低许多金属的溶解性和毒性[21],因为细颗粒沉积物中拥有更多的颗粒有机碳,它对金属的亲和力很高,且颗粒物数量相同时,细颗粒沉积物拥有更大的比表面积,有更大的空间吸附重金属[22]。因此,细颗粒沉积物中重金属浓度很高。也有很多研究表明[23],粒径小于63 μm的细颗粒是吸附和运输金属最重要的途径,因为他们有更大的表面积和特殊的地球化学组成,细颗粒从水相中吸附活性金属,然后沉淀在表层沉积物中[24]。与下层的细颗粒相比,沉积物上层的细颗粒与水体接触更多,能从水体中吸附更多的重金属,因此上层沉积物吸附的重金属较多。铁锰化物主要在好氧沉积物中积累,其巨大的表面积,使其在吸附金属铁、铬、锰、镍和TOC上贡献很大[25],铁锰化物结合态在上层沉积物中聚集较为明显。有机质是不同资源的衍生品,如植物、动物的碎屑及其粪便,甚至是进入地下水生系统的人造有机材料。中等分子量的有机质可以溶解金属配位体形成可溶性复合物,高分子量的有机质可以减少金属的可用性[23]。东太湖为草型湖泊,水生植物较多,有机质含量也相对偏高,所以有机物及硫化物结合态含量相对较高;沉积物中上层有机质含量高,下层有机质含量低。因此,有机物及硫化物结合态在上层沉积物中的含量高,但与下层间的差距不大。可能是因为下层沉积物中与AVS结合的重金属较多,在厌氧沉积物中,硫酸盐在硫酸盐还原菌作用下形成AVS,反应过程可表示如下:
SO2-4+8e-+8H+→S2-+4H2O
有二价Fe离子存在时,反应如下:
Fe2++SO2-4+8H++8e-→FeS(s)+4H2O
AVS与金属离子结合的化学基础是FeS与二价金属离子生成不溶性金属硫化物[27]。
Me2++FeS(s)→MeS(s)+Fe2+
基于此反应机理,Zn、Cu等二价离子生成铜蓝(CuS)、闪锌矿(ZnS),AVS的浓度随着深度的增加而增加[27],下层沉积物中高浓度AVS足以绑定金属阳离子,从而降低金属离子对生物的毒性[28];而表层沉积物中AVS的浓度较低,是由于表层沉积物中的生物扰动以及从表层水中渗透的氧气,给硫化物创造了有氧环境,又因FeS在热力学上的不稳定,所以在有氧条件下,AVS结合重金属的能力变成一个可有可无的变量[29]。因此,上层沉积物中的有机物及硫化物结合态向下迁移比较明显(图4)。
综上,由于沉积物粒径、有机质、AVS等环境原因,表层沉积物中可交换态含量高,上层沉积物中铁锰化物结合态含量比下层中高,而上层沉积物中有机质含量较高,下层沉积物中有AVS的积累,并与重金属结合,使得有机物及硫化物结合态的含量没有随着有机质的减少而降低,所以有机物及硫化物结合态在上下层间的差距不大。人为输入的污水中所含的金属等从水相中沉淀在表层沉积物中,此时以可交换态为主,随着铁锰化物在沉积物中的累积,金属向铁锰化物结合态转化,随着泥沙运动等,金属继续下沉,而下层沉积物中的AVS含量增加,AVS绑定金属离子形成不溶性的金属硫化物,重金属也随之稳定下来,迁移性随之减弱。
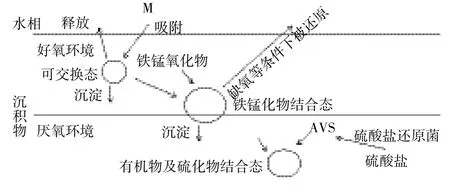
图4 重金属可提取态迁移示意图Figure 4 Diagram for transformation of heavy metal fractions in sediments
3 结论
(1)太湖沉积物中重金属含量在垂向上随深度的增加而降低,在1950年和1980年处出现拐点,且1980年的污染最为严重;空间分布上,西北部的梅梁湾、竺山湾和贡湖湾的污染最为严重,湖心次之。
(2)四种金属在赋存形态上都以残渣态为主,除残渣态外,Cd和Cu的可交换态含量较高,Pb的铁锰化物结合态所占比例较高,Cr的残渣态占绝大部分,比例达到95%左右。
(3)重金属在上层沉积物中(0~12 cm)迁移率较高,下层沉积物中的重金属较为稳定,迁移率不高。
(4)重金属在表层沉积物中可交换态所占比例居多,随着深度的增加向铁锰化物结合态、有机物及硫化物结合态转化。
参考文献:
[1]王立硕,毕见霖,王馨慧,等.非常规水源补给城市河流表层沉积物重金属污染及风险评价[J].环境科学学报, 2015, 35(3):903-910. WANG Li-shuo, BI Jian-lin, WANG Xin-hui, et al. Characteristics and ecological risk assessment of heavy metal pollution in unconventional supply urban river[J]. Acta Scientiae Circumstantiae, 2015, 35(3):903-910.
[2] Zahra A, Hashmi M Z, Malik R N, et al. Enrichment and geo-accumulation of heavy metals and risk assessment of sediments of the Kurang Nallah—feeding tributary of the Rawal Lake Reservoir, Pakistan[J]. Science of the Total Environment, 2014, 470:925-933.
[3] Superville P J, Prygiel E, Magnier A, et al. Daily variations of Zn and Pb concentrations in the Deûle River in relation to the resuspension of heavily polluted sediments[J]. Science of the Total Environment, 2014, 470:600-607.
[4] Bing H, Wu Y, Liu E, et al. Assessment of heavy metal enrichment andits human impact in lacustrine sediments from four lakes in the mid-low reaches of the Yangtze River, China[J]. Journal of Environmental Sciences, 2013, 25(7):1300-1309.
[5] Liu E F, Birch G F, Shen J, et al. Comprehensive evaluation of heavy metal contamination in surface and core sediments of Taihu Lake, the third largest freshwater lake in China[J]. Environmental Earth Sciences, 2012, 67(1):39-51.
[6]郑乐平,刘玉梅,钱显文,等.太湖、巢湖沉积物中重金属污染的总量特征及其区域性差异[J].环境化学, 2009, 28(6):883-888. ZHENG Le-ping, LIU Yu-mei, QIAN Xian-wen, et al. The Characteristics and regional differences of heavy matal contents in the sediments of Taihu Lake and Chaohu Lake[J]. Environmental Chemistry, 2009, 28(6):883-888.
[7] Tessier A, Campbell P G C, Bisson M. Sequential extraction procedure for the speciation of particulate trace metals[J]. Analytical Chemistry, 1979, 51(7):844-851.
[8] Forstner U. Metal pollution in aquatic environment[M]. Second Edition. Berlin:Springer, Verlag, 1981:128-132.
[9] Rauret G, Lopez-Sanchez J F, Sahuquillo A, et al. Improvement of the BCR three step sequential extraction procedure prior to the certification of new sediment and soil reference materials[J]. Journal of Environmental Monitoring, 1999, 1(1):57-61.
[10]秦延文,张雷,郑丙辉,等.太湖表层沉积物重金属赋存形态分析及污染特征[J].环境科学, 2012, 33(12):4291-4299. QIN Yan-wen, ZHANG Lei, ZHENG Bing-hui, et al. Speciation and pollution characteristics of heavy metal in the sediment of Taihu Lake [J]. Environmental Science, 2012, 33(12):4291-4299.
[11]成杭新,赵传冬,庄广民,等.太湖流域土壤重金属元素污染历史的重建:以Pb, Cd为例[J].地学前缘, 2008, 15(5):167-178. CHENG Hang-xin, ZHAO Chuan-dong, ZHUANG Guang-min, et al. Reconstruction of the regional soil pollution history by heavy metals in Taihu Lake drainage area:Taking Pb and Cd as examples[J]. Earth Science Frontiers, 2008, 15(5);167-178.
[12]陈春霄,姜霞,战玉柱,等.太湖表层沉积物中重金属形态分布及其潜在生态风险分析[J].中国环境科学, 2011, 31(11):1842-1848. CHEN Chun-xiao, JIANG Xia, ZHAN Yu-zhu, et al. Speciation distribution and potential ecological risk assessment of heavy matals in sediment of Taihu Lake[J]. China Environmental Science, 2011, 31(11):1842-1848.
[13] Qu W C, Mike D, Wang S M. Multivariate analysis of heavy metal and nutrient concentrations in sediments of Taihu Lake, China[J]. Hydrobiologia, 2001, 450:83-91.
[14] Zhang R, Jiang D, Zhang L, et al. Distribution of nutrients, heavy metals, and PAHs affected by sediment dredging in the Wujin'gang River basin flowing into Meiliang Bay of Lake Taihu[J]. Environmental Science and Pollution Research, 2014, 21(3):2141-2153.
[15]王小雷,杨浩,顾祝军,等.抚仙湖沉积物重金属垂向分布及潜在生态风险评价[J].地球与环境, 2014, 42(6):764-772. WANG Xiao-lei, YANG Hao, GU Zhu-jun, et al. Vertical distribution and potential ecological risk assessment of heavy matals in sediment cores of Lake Fuxian[J]. Earth and Environment, 2014, 42(6):764-772.
[16]李亮亮,张大庚,依艳丽,等.葫芦岛市连山区、龙港区土壤重金属垂直分布与迁移特征[J].安徽农业科学, 2007, 35(13):3916-3918. LI Liang-liang, ZHANG Da-geng, YI Yan-li, et al. Vertical distribution and immigrant character of heavy metals in soil in Lianshan and Longgang districts of Huludao City[J]. Journal of Anhui Agricultural Science, 2007, 35(13):3916-3918.
[17] Kabata-Pendias A. Trace elements in soils and plants[M]. Boca Raton: CRC Press, 2010.
[18] Usero J, Gamero M, Morillo J, et al. Comparative study of three sequential extraction procedures for metals in marine sediments[J]. Environment International, 1998, 24(4):487-496.
[19] Fernández E, Jiménez R, Lallena A M, et al. Evaluation of the BCR sequential extraction procedure applied for two unpolluted Spanish soils [J]. Environmental Pollution, 2004, 131(3):355-364.
[20] Zhou G, Sun B, Zeng D, et al. Vertical distribution of trace elements in the sediment cores from major rivers in east China and its implication on geochemical background and anthropogenic effects[J]. Journal of Geochemical Exploration, 2014, 139:53-67.
[21] Strom D, Simpson S L, Batley G E, et al. The influence of sediment particle size and organic carbon on toxicity of copper to benthic invertebrates in oxic/suboxic surface sediments[J]. Environmental Toxicology and Chemistry, 2011, 30(7):1599-1610.
[22] Guven D E, Akinci G. Effect of sediment size on bioleaching of heavy metals from contaminated sediments of Izmir Inner Bay[J]. Journal of Environmental Sciences, 2013, 25(9):1784-1794.
[23] Fernandes L, Nayak G N, Ilangovan D, et al. Accumulation of sediment, organic matter and trace metals with space and time, in a creek along Mumbai coast, India[J]. Estuarine, Coastal and Shelf Science, 2011, 91 (3):388-399.
[24] Zhang C, Yu Z, Zeng G, et al. Effects of sediment geochemical properties on heavy metal bioavailability[J]. Environment international, 2014, 73:270-281.
[25] Sutherland T F, Petersen S A, Levings C D, et al. Distinguishing between natural and aquaculture-derived sediment concentrations of heavy metals in the Broughton Archipelago, British Columbia[J]. Marine Pollution Bulletin, 2007, 54(9):1451-1460.
[26] Hernández-Crespo C, Martín M, Ferrís M, et al. Measurement of acid volatile sulphide and simultaneously extracted metals in sediment from Lake Albufera(Valencia, Spain)[J]. Soil and Sediment Contamination:An International Journal, 2012, 21(2):176-191.
[27] Chen F, Yang Y, Zhang D, et al. Heavy metals associated with reduced sulfur in sediments from different deposition environments in the Pearl River estuary, China[J]. Environmental Geochemistry and Health, 2006, 28(3):265-272.
[28] Nizoli E C, Luiz-Silva W. Seasonal AVS-SEM relationship in sediments and potential bioavailability of metals in industrialized estuary, southeastern Brazil[J]. Environmental Geochemistry and Health, 2012, 34(2):263-272.
[29] Burton E D, Bush R T, Sullivan L A. Acid-volatile sulfide oxidation in coastal flood plain drains:Iron-sulfur cycling and effects on water quality[J]. Environmental Science & Technology, 2006, 40(4):1217-1222.
Vertical distribution and migration of heavy metals in sediment cores of Taihu Lake
YANG Chen1,2, WANG Pei-fang1,2*, LIU Jia-jia1,2, WANG Chao1,2, HOU Jun1,2, QIAN Jin1,2
(1.Key Laboratory of Integrated Regulation and Resources Development on Shallow Lakes, Ministry of Education, Hohai University, Nanjing 210098, China; 2.College of Environment, Hohai University, Nanjing 210098, China)
Abstract:Studying the distribution of heavy metals in sediment profiles is of great significance for understanding the pollution history and migration of heavy metals in lake sediments. Here we collected sediment cores from Taihu Lake, and determined total content and fractions of Cd, Pb, Cu, and Cr. The total content of Cd, Pb, Cu, and Cr decreased with increasing depth, with the turning points appeared in 1950 and 1980, especially in 1980. Meiliang bay, Zhushan bay and Gonghu bay suffered from very severe pollution, followed by the central area. The residual fraction of the metals was dominant. The average values of residual Cd, Pb, Cu, and Cr accounted for 59.74%, 81.67%, 77.81% and 59.74% of their total, respectively. The exchangeable Cd and Cu fractions were respectively 15.81% and 13.62%, while the proportion of iron and manganese oxides bound Pb was 11.36%. Migration rates of heavy metals in the upper sediments were higher, whereas the heavy metals in bottom sediments were relatively stable and poorly mobile. Calculation of the form migration of heavy metals showed that exchangeable metals were higher in the surface sediments as they were adsorbed on fine particulate matter, settled directly in the surface sediments and moved downward along with the sediment movements. At deeper sediments where iron and manganese oxides and AVS(Acid Volatile Sulfide)accumulated, the exchangeable metals were transferred into iron and manganese oxides bound, organic matter and sulphide bound fractions.
Keywords:Taihu Lake; sediment cores; heavy metals; vertical distribution; migration
*通信作者:王沛芳E-mail:pfwang2005@hhu.edu.cn
作者简介:杨陈(1990—),女,江苏大丰人,硕士研究生,从事水资源生态修复。E-mail:ychhu1990@sina.com
基金项目:国家自然科学基金面上项目(51479065);国家重大水专项课题(2012ZX07101-008)
收稿日期:2015-09-28
中图分类号:X524
文献标志码:A
文章编号:1672-2043(2016)03-0548-10
doi:10.11654/jaes.2016.03.019

