骨刺胶囊HPLC指纹图谱
汪艳平, 戴德雄, 谢媛媛, 王义明*, 李 嬛, 罗国安
(1.江西中医药大学,江西南昌330004;2.清华大学化学系,北京100084;3.浙江维康药业有限公司,浙江杭州310012;4.南京中医药大学,江苏南京210023)
骨刺胶囊HPLC指纹图谱
汪艳平1,2, 戴德雄3, 谢媛媛2*, 王义明1,2*, 李 嬛4, 罗国安1,2
(1.江西中医药大学,江西南昌330004;2.清华大学化学系,北京100084;3.浙江维康药业有限公司,浙江杭州310012;4.南京中医药大学,江苏南京210023)
摘要:目的 建立骨刺胶囊(昆布、骨碎补、白芍、党参等)指纹图谱,并结合质谱信息鉴定特征峰的化学结构信息。方法 骨刺胶囊75%甲醇提取液的分析采用Phenomenex Luna C18柱(4.6 mm×250 mm,5 μm);流动相为乙腈-20 mmo1/L甲酸铵水溶液体系;体积流量为1.0 m L/min,梯度洗脱;检测波长为254 nm。采用飞行时间质谱(TOFMS)结合离子阱多级质谱(Ion-trap/MSn),鉴定骨刺胶囊指纹图谱中特征峰的结构,正、负两种离子模式扫描。结果 骨刺胶囊HPLC-MS指认21个共有峰,表征昆布、白芍、杜仲、党参、马钱子、鸡血藤、骨碎补、延胡索和桂枝等9味药材的特征成分。以绿原酸为参照物峰,12批样品的相似度在0.821~0.945之间。结论 该方法显示,骨刺胶囊主要化学成分相似,质量较稳定。
关键词:骨刺胶囊;指纹图谱;高效液相色谱;飞行时间质谱;离子阱多级质谱
王义明(1945—),女,教授,研究方向为中药质量控制。Te1:(010)62781688,E-mai1:wangyim@mai1.tsinghua.edu.cn
骨刺胶囊由昆布、骨碎补、白芍、党参、马钱子粉、鸡血藤、桂枝、延胡索、杜仲、牡蛎(煅)等组成,具有散风邪、祛寒湿、舒筋活血、通络止痛的功效,用于颈椎、胸椎、腰椎、跟骨等骨关节增生性疾病,对风湿性、类风湿性关节炎有一定疗效[1-2]。在国家食品药品监督管理总局官方网站上检索,发现目前全国共有3家骨刺胶囊生产企业,此外市场上还有处方组成不同、药品名称相同或相似的中成药。为避免原料来源、生产工艺等众多因素影响骨刺胶囊药品质量的一致性和稳定性,正本清源,保障其临床合理、安全、有效应用,亟需“合理、全面、可行”的骨刺胶囊质量控制标准。
罗国安教授[3-4]等提出的多维多息指纹图谱,运用液相色谱-质谱联用、气相色谱-质谱联用等色谱和光谱手段的联用技术,综合色谱的成分分离、分析和光谱的结构鉴定,获取多维指纹图谱,体现分析对象的整体成分信息、结构信息和中药指标成分的定量信息,系统、完整地实现中药复方制剂化学特征整体性和特征性的综合分析。可弥补目前大多数中药指纹图谱研究采用单一分析仪器获取(如HPLC-UV等),难以充分刻画中药复方制剂整体化学特征的缺陷。
本实验针对骨刺胶囊复方体系,采用HPLCDAD-MS联用技术建立其多维指纹图谱,指认了21个共有峰,从整体上更全面系统地反映骨刺胶囊内在化学信息。同时,采用飞行时间质谱(TOF/MS)与离子阱质谱(Ion-trap/MSn)信息组合分析策略鉴定了骨刺胶囊指纹图谱中21个共有峰的化学结构信息,为实现其全面质量控制奠定了基础。
1 仪器与试药
1.1 仪器 Agi1ent 1200 Series高效液相色谱仪(配有在线脱气机G1322A,低压二元梯度泵G1312A,自动进样器G1329A,柱温箱G1316A,二极管阵列检测器G1315D,Chemstation化学工作站)、Agi1ent1200 LC/MSD TOF/MS高效液相色谱-飞行时间质谱联用仪(配有二元梯度泵G1312A,二极管阵列检测器G1315D,电喷雾离子源)、Agi1ent1100 series LC/MSD Trap MSn高效液相色谱-离子阱质谱联用仪(配有二元梯度泵G1312A,二极管阵列检测器G1328A,电喷雾离子源)(Agi1ent,USA);Buchi Rotavapar R-200旋转蒸发仪(瑞士Buchi公司);SHB-III循环水式多用真空泵(郑州长城科工贸有限公司);DLSB-10L/10低温冷却液循环泵及HH-S型水浴锅(巩义市予华仪器有限责任公司);RQ-250B型超声波清洗器(昆山市超声仪器有限公司);高速台式离心机(Hettich Zentrifugen);QL-901涡旋振荡器(海门市其林贝尔仪器制造有限公司);Mi11i-Q Synthesis超纯水纯化系统(Mi11ipore,USA);0.45 μm滤膜(天津津腾实验设备有限公司)。
1.2 试剂与样品 绿原酸对照品(中国药品生物制品检定所,纯度≥98%,含有量测定用)。甲醇(分析纯,北京化工厂);乙腈(色谱纯,Merck KGaA);甲酸(分析纯,北京现代东方精细化学品有限公司);Mi11i-Q超纯水(自制);甲酸铵(纯度99%,A1fa Aesar);
骨刺胶囊共12批,其中批号为20130205、20130207、20130301、20130302、20130306、20130401、20140306、20140307、20140308和20140405等10批骨刺胶囊由浙江维康药业有限公司提供;批号为130102、130104者购于北京金象大药房,为陕西康惠制药股份有限公司产品。
2 方法与结果
2.1 色谱条件 Phenomenex Luna C18色谱柱(4.6 mm×250 mm,5 μm);流动相A为20 mmo1/L甲酸铵水溶液(含0.2%甲酸),流动相B为乙腈,梯度洗脱(0~80 min,1%~22% B;80~105 min,22%~35% B;105~115 min,35%~95% B);体积流量1.0 mL/min;柱温45℃;进样量10 μL。2.2 质谱条件[5]
2.2.1 飞行时间质谱 电喷雾离子源(ESI);正、负两种离子模式采集数据;干燥气温度为350℃;干燥气体积流量为9.0 L/min;雾化气压为35 psi(1 psi=6.895 kPa);质量扫描范围为m/z 50~2 200;毛细管电压在正、负模式下均为3 500 V;碎裂电压175 V;Skimmer电压60 V;八级杆DC1电压-38.0 V;八级杆射频电压250 V;采用分流比设置,分流比为1∶3。试验数据采用Ana1yst QS软件处理。
2.2.2 离子阱质谱 电喷雾离子源(ESI);正、负两种离子模式采集数据;自动二级碎片分析;干燥气体积流量为9.0 L/min;干燥气温度为350℃;雾化气压力为35 psi;毛细管电压在正、负模式下均为3 500 V;质量扫描范围为m/z50~2 200;ICC目标参数为30 000,累积时间为200 ms;采用分流比设置,分流比为1∶3。试验数据采用Agi1ent化学工作站Rev.A.09.01软件处理。
2.3 对照品溶液的制备 取绿原酸对照品1.0 mg,精密称定,置于10 mL量瓶中,用75%甲醇溶液溶解定容,配制成质量浓度为0.1 mg/mL的绿原酸对照品溶液。
2.4 供试品溶液的制备 取骨刺胶囊50粒,剥去胶囊壳,将胶囊内粉末充分混合。取粉末0.5 g,精密称定,置于10 m L具塞离心管中,加入75%甲醇溶液10 mL,涡旋2 min后室温下超声处理30 min(40 kHz、500 W),4 500 r/min离心15 min,过滤,滤液用75%甲醇溶液定容至10 mL量瓶中,摇匀,0.45 μm微孔滤膜滤过,作为供试品溶液。
2.5 方法学考察
2.5.1 精密度试验 取同一批号(批号20130401)的骨刺胶囊供试品溶液,在“2.1”项色谱条件下连续进样测定6次,计算21个共有峰的相对保留时间和相对峰面积,考察它们的一致性。结果表明,色谱图中各共有峰相对保留时间的RSD为0.15%~1.2%,相对峰面积的RSD为0.35%~4.1%,表明仪器精密度良好。
2.5.2 重复性试验 取同一批号(批号20130401)骨刺胶囊0.5 g,按“2.4”项下方法重复制备6份供试品溶液,在“2.1”项色谱条件下进样测定6次,计算21个共有峰的相对保留时间和相对峰面积。结果表明,色谱图中各共有峰相对保留时间的RSD为0.10%~0.66%,相对峰面积的RSD为0.70%~5.2%,表明该方法重复性良好。
2.5.3 稳定性试验 取同一批号(批号20130401)的骨刺胶囊供试品溶液,室温下放置,在“2.1”项色谱条件下分别于0、2、4、8、12、24 h进样测定,计算各色谱峰的相对保留时间和相对峰面积。结果表明,各共有峰相对保留时间的RSD为0.15 %~1.1%,相对峰面积的RSD为0.65%~4.6%,表明供试品溶液在24 h内保持稳定。
2.6 测定方法 取不同批次骨刺胶囊0.5 g,按“2.4”项下方法制备供试品溶液,将对照品溶液和供试品溶液各进样10 μL,记录色谱图,见图1。

图1 骨刺胶囊的HPLC指纹图谱Fig.1 HPLC fingerprints of Guci Capsules
2.7 骨刺胶囊化学成分分析 由于骨刺胶囊化合物种类较多,质谱分析采用正、负离子两种扫描模式。同时,根据文献建立骨刺胶囊组方药材的化学成分质谱信息库[6-20],采用TOF/MS获取化合物精确分子量信息,Ion-trap/MSn获取化合物多级质谱碎裂信息,结合色谱保留行为、DAD提供的紫外吸收光谱图等解析鉴定了骨刺胶囊指纹图谱中主要化学成分的结构信息,结果见图2及表1。
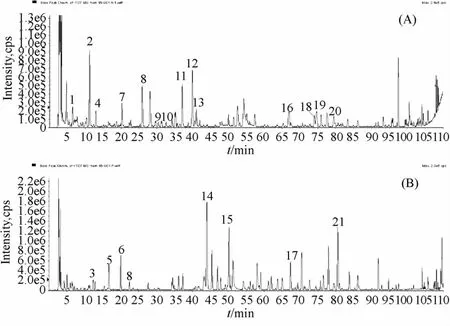
(A)负离子模式 (B)正离子模式(A)negative ion mode (B)positive ioncurrentmode图2 骨刺胶囊HPLC TOF/MS总离子流图(TIC)Fig.2 HPLC TOF/MS total ion current(TIC)chromatogram s of Guci Capsules
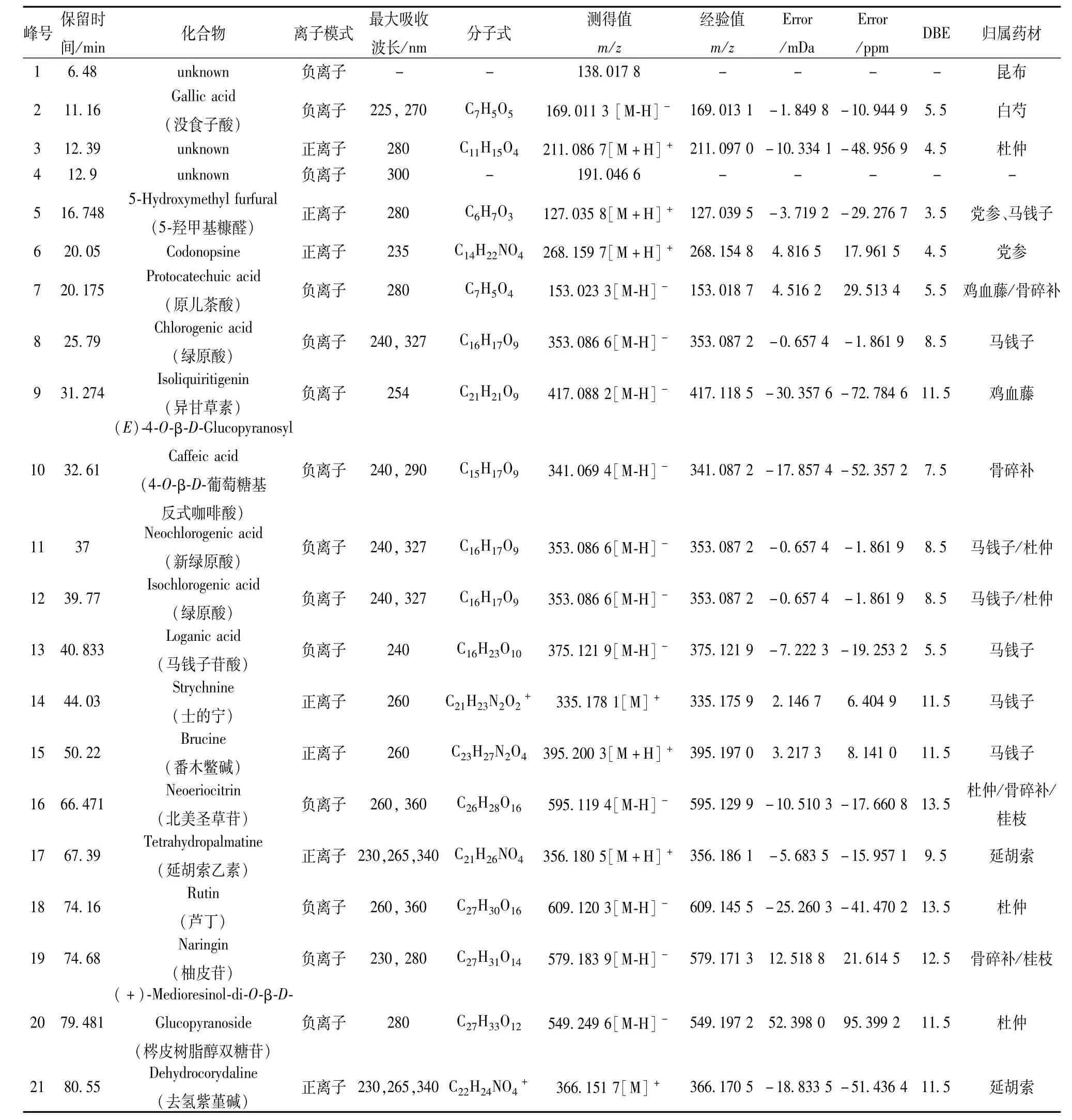
表1 骨刺胶囊化学成分的鉴定Tab.1 Identification of chem ical constituents in Guci Capsules
2.8 骨刺胶囊指纹图谱的建立与分析
2.8.1 参照色谱峰的选择 骨刺胶囊由15味中药材组成,含有机酸、生物碱、黄酮类、环烯醚萜苷、皂苷、多糖等多种成分。经色谱峰的光谱分析及与对照品保留时间比较,图1(254 nm)所示指纹图谱中11号峰(保留时间约为37 min)为绿原酸,其分离度好、保留时间居中,因此作为骨刺胶囊指纹图谱的参照色谱峰。
2.8.2 指纹图谱分析 本实验共分析测定了来源于2个生产厂家的12个批次骨刺胶囊供试品的指纹图谱,共标定了21个共有峰,见图1 (254 nm)。采用国家药典委员会《中药色谱指纹图谱相似度评价系统2009A版》生成骨刺胶囊对照指纹图谱,计算12批样品指纹图谱与对照指纹图谱的相似度,结果见表2。12批骨刺胶囊指纹图谱相似度在0.821~0.945之间,表明不同生产厂家、不同批次骨刺胶囊主要化学成分相似,该制剂质量较稳定。

表2 12批骨刺胶囊HPLC指纹图谱相似度Tab.2 Sim ilarities of fingerprints for 12 batches of Guci Capsules
3 讨论
3.1 提取溶剂和方法的考察 供试品溶液应充分反映样本的基本特性,保证待测样品所含特性的完整性,保证样品物质信息不减失、不转化。实验考察了水、25%甲醇、50%甲醇、75%甲醇、纯甲醇提取样品后的指纹图谱情况,发现75%甲醇提取样品的指纹图谱色谱峰个数较多,且整体图形中各峰峰面积大小相对均匀,故提取溶媒选择75%甲醇。对超声和加热回流2种不同提取方法进行比较,两种提取液中色谱峰个数及峰面积相差不大,但超声方法较简便快捷,故选择超声提取方式。同时,对提取溶剂用量(10、20和40 mL),提取时间(30、60和90 min)以及提取次数进行考察,以10 mL(20倍用量)、超声提取30 min为最优提取条件。考虑到本研究提取料液比小,会出现提取溶剂不能渗透骨刺胶囊粉末团,造成溶剂和粉末的混合不均匀而影响提取效果的情况,比较了涡旋后超声提取30 min和未涡旋直接超声30 min的提取效果,结果表明涡旋2 min后超声30 min较直接超声30 min提取效率高。综上所述,最终确定了“2.4”项下供试品溶液的制备方法。
3.2 色谱条件的选择 其由15味中药材组成,含有机酸、生物碱、黄酮类、环烯醚萜苷、皂苷、多糖等多种成分,其供试液中酸性成分与碱性成分,极性和非极性成分并存,增加了指纹图谱分析的难度。在流动相选择上,本实验分析测试了中性的乙腈-水体系,结果色谱峰拖尾较为严重,为改善拖尾问题,抑制有机酸类成分的水解,在水相中加入适量的甲酸,拖尾问题改善,但基线不平稳。推测可能由生物碱类成分引起,随后在流动相中加入三乙胺,其碱性较强,用磷酸调节pH至6.0,分离效果有所改善。考虑到磷酸不能进入质谱分析,之后比较了甲酸铵-甲酸缓冲盐体系和三乙胺-磷酸缓冲盐体系,结果表明,在水相中加入一定浓度甲酸-甲酸铵可以得到的色谱图分离度较好,基线平稳;有机相考察了甲醇和乙腈,选择乙腈作为有机相,分离效果优于甲醇。最终,选择了乙腈-20 mmo1/L甲酸铵水溶液(含0.2%甲酸)流动相体系。利用HPLC/DAD对骨刺胶囊样品进行紫外全波长扫描,色谱峰整体在190~350 nm波长范围内吸收较强,其中254 nm下色谱峰数最多,可最大化地反应指纹有效信息,故选择254 nm为骨刺胶囊综合质量控制的指纹图谱检测波长。同时,对体积流量(0.8、1.0、1.2 mL/min)、柱温(25、30、35、40、45℃)和进样量(5、10、15、20 μL)进行了考察,最后确定了“2.1”项下色谱方法。
3.3 指纹图谱的建立 本研究采用HPLC-TOF/MS 及HPLC-ion-trap/MSn两种质谱信息组合分析的策略,对骨刺胶囊中的化学成分进行了快速鉴别,共解析鉴定了其色谱图中75个化学成分的结构信息,分别归属于昆布、白芍、杜仲、党参、马钱子、鸡血藤、骨碎补、附片、川乌、草乌、威灵仙、延胡索、三七和桂枝等14味药材(数据未提供)。除牡蛎中主要成分为蛋白质和碳酸钙等,难于采用高效液相色谱-质谱联用鉴定其主要成分外,通过正、负离子扫描获取总离子流图中其他来源药材的成分均指认其结构,可基本表征骨刺胶囊化学物质基础及其质量。但是,“可行性”在指纹图谱用于中药质量控制也是一个不可忽略的因素,虽然质谱分析得到的骨刺胶囊正、负离子总离子流图可全息表征骨刺胶囊中所有植物来源药材中特征有机小分子化合物,但个别成分含有量很低,在液相色谱图上属于微量或痕量成分,难于采用以表征“整体性”和“特征性”的指纹图谱控制其质量。同时,考虑到目前液相质谱联用仪对实验环境要求严格,在生产企业和基层药检单位普及度不高等诸多因素,本实验最终选择建立骨刺胶囊的高效液相色谱指纹图谱,指认21个共有峰,表征昆布、白芍、杜仲、党参、马钱子、鸡血藤、骨碎补、延胡索和桂枝等9味药材的特征成分。此外,来源于三七药材中的人参皂苷类成分的紫外吸收光谱属末端吸收,且含有量较低,在检测波长为205 nm时,被基线所掩盖;而来源于附片等药材中生物碱类成分由于含有量低,尽管其在正离子模式下具有较高的检测灵敏度,但在色谱指纹图谱中未能表征,后续研究中考虑通过优化样品前处理方法,针对上述成分建立专属性强的定性定量分析方法。此外,本研究为骨刺胶囊多波长多指标成分定量指纹图谱的建立提供了研究基础,以期从整体表征与局部特征相结合实现其质量全面管理控制。
参考文献:
[1] 王彧丽,戴德雄,朱 莹.高效液相色谱法测定骨刺胶囊中士的宁[J].中草药,2006,41(9):1482-1483.
[2] 姚灵凤.骨刺胶囊抗炎镇痛作用的实验研究[J].中国民康医学,2011,23(3):309-310.
[3] 罗国安,王义明,曹 进.多维多息特征谱及其应用[J].中成药,2000,22(6):395-397.
[4] 罗国安,梁琼麟,王义明.中药指纹图谱-质量控制与新药研发[M].北京:化学工业出版社,2009.
[5] 夏 菁,谢媛媛,张宗璇,等.骨通贴膏指纹图谱及化学成分研究[J].中成药,2014,36(3):572-576.
[6] He JY,Ma N,Zhu S,et al.The genus Codonopsis(Campanu1aceae):a review of phytochemistry,bioactivity and qua1ity contro1[J].JNat Med,2015,69:1-21.
[7] Li S L,Song JZ,Franky F K Choi,et al.Chemica1profi1ing of Radix Paeoniae eva1uated by u1tra-performance 1iquid chromatography/photo-diode-array/quadrupo1e time-of-f1ight mass spectrometry[J].J Pharm Biomed Anal,2009,49(2):253-266.
[8] Ma X Q,A1exander K M L,Chi L C,et al.UHPLC UHD Q-TOF MS/MS ana1ysis of the impactof su1fur fumigation on the chemica1profi1e of Codonopsis Radix(Dangshen)[J].Analyst,2014,139(2):505-516.
[9] 王振中,李家春,窦 霞,等.液相色谱-质谱联用法对桂枝茯苓胶囊指纹图谱中特征峰的鉴定[J].南京中医药大学学报,2009,25(3):194-196.
[10] He X R,Wang JH,LiM X,etal.Eucommia ulmoides O1iv. ethnopharmaco1ogy,phytochemistry and pharmaco1ogy of an important traditiona1Chinese medicine[J].J Ethnopharmacol,2014,151(1):78-92.
[11] 何 峰,王永林,郑 林,等.UPLC-PDA-ESI-MS分析杜仲中化学成分[J].中国实验方剂学杂志,2014,20(3):59-62.
[12] Zhou H B,Wang C Y,Qi Y,et al.Rapid qua1ity assessment of Radix Aconiti Preparata using directana1ysis in rea1timemass spectrometry[J].Anal Chim Acta,2012,752:69-77.
[13] Yang Y,Yin X J,Guo H M,et al.Identification and comparative ana1ysis of the major chemica1 constituents in the extracts of sing1e fuziherb and fuzi-gancao herb-pair by UFLC-IT-TOF/ MS[J].Chin JNat Med,2014,12(7):542-553.
[14] Xiao S,Yu R R,Ai N,et al.Rapid screening natura1-origin 1ipase inhibitors from hypo1ipidemic decoctions by u1trafi1tration combined with 1iquid chromatography-mass spectrometry[J].J Pharm Biomed Anal,2015,104:67-74.
[15] Zhang Y,Guo L,Duan L,et al.Simu1taneous determination of16 pheno1ic constituents in SpatholobiCaulis by high performance 1iquid chromatography/e1ectrospray ionization trip1e quadrupo1emass spectrometry[J].JPharm Biomed.Anal,2015,102:110-118.
[16] Wu W,Qiao C F,Liang Z T,et al.A1ka1oid profi1ing in crude and processed Strychnosnux-vomica seedsbymatrix-assisted 1aser desorption/ionization-time of f1ightmass spectrometry [J].JPharm Biomed Anal,2007,45(3):430-436.
[17] Xie Y Y,Luo D,Cheng Y J,etal.Steaming-induced chemica1 transformationsand ho1istic qua1ity assessmentof red ginseng derived from Panax ginseng bymeans of HPLC-ESI-MS/MSn—based mu1ticomponent quantification fingerprint[J].J Agric Food Chem,2012,60(7):8213-8224.
[18] Wang Y,Kong L,Hu L H,et al.Bio1ogica1 fingerprinting ana1ysis of the traditiona1Chinese prescription Longdan Xiegan Decoction by on/off-1ine comprehensive two-dimensiona1 biochromatography[J].J Chromatogr B,2007,860(2):185-194.
[19] Cheng Z H,Guo Y L,Wang H Y,et al.Qua1itative and quantitative ana1ysis of quaternary ammonium a1ka1oids from Rhizoma Corydalis bymatrix-assisted 1aser desorption/ionization Fourier transform mass spectrometry coup1ed with a se1ective precipitation reaction using Reinecke sa1t[J].Anal Chim Acta,2006,555(2):269-277.
[20] Sun M Q,Liu JX,Lin C R,et al.A1ka1oid profi1ing of the traditiona1Chinesemedicine Rhizoma corydalis using high performance 1iquid chromatography-tandem quadrupo1e time-off1ightmass spectrometry[J].Acta Pharm Sin,2014,4(3):208-216.
[成分分析]
HPLC fingerprint of Guci Capsules
WANG Yan-ping1,2, DAIDe-xiong3, XIE Yuan-yuan2*, WANG Yi-ming1,2*, LIHuan4, LUOGuo-an1,2
(1.Jiangxi University of Traditional Chinese Medicine,Nanchang 33OOO4,China;2.Department of Chemistry,Tsinghua University,Beijing 1OOO84,China;3.Zhejiang Wecome Pharmaceutical Co.,Ltd.,Hangzhou 31OO12,China;4.Nanjing University of Chinese Medicine,Nanjing 21OO23,China)
ABSTRACT:AIM To estab1ish a fingerprint for ana1yzing GuciCapsu1es(Laminariae thallus eck1oniae tha11us,Drynariae Rhizoma,Paeoniae Radix a1ba,Codonopsis Radix,etc.)by HPLC,as we11 as a combinative LC/MS method for the identification of components in Guci Capsu1es.M ETHODS The ana1ysis of 75% methano1ic extract of GuciCapsu1eswas carried outon Phenomenex Luna C18co1umn(4.6 mm×250 mm,5 μm),with acetonitri1e-20 mmo1/L ammonium formate so1ution as themobi1e phase in a gradient e1ution manner at 1 mL/min for f1ow rate and 254 nm for detection wave1ength.A combination of time-of-f1ightmass spectrometer(TOF-MS)and ion trap tandem mass spectrometer(ion Trap-MSn)was app1ied for the identification of characteristic peaks under positive and negative ion modes.RESULTS Twenty-one common peaks,representing L.thallus eck1oniae tha1-1us,P.Radix a1ba,E.Cortex their,C.Radix,S.Semen,S.Caulis,D.Rhizoma,C.Rhizoma and C.Ramulus,were obtained from HPLC chromatograms of Guci Capsu1es.The simi1arities of the twe1ve batches of samp1es with the referentia1ch1orogenic acid peak ranged from 0.821 to 0.945.CONCLUSION Thismethod can show the simi1ar chemica1 constituents and stab1e qua1ity of Guci Capsu1es.
KEY WORDS:Guci Capsu1es;fingerprint;high performance 1iquid chromatography(HPLC);time-of-f1ight mass spectrometer(TOF-MS);ion trap tandem mass spectrometer(Ion-trap/MSn)
*通信作者:谢媛媛(1980—),女(满族),博士,高级工程师,研究方向为中药质量控制。Te1:(010)62772264,E-mai1:yuanyuan8078@gmai1.com
作者简介:汪艳平(1987—),女,硕士生,研究方向为中药质量控制。Te1:(010)62772265,E-mai1:wangyanpingdy@163.com
基金项目:国家“重大新药创制”科技重大专项(2014ZX09304307-001-010)
收稿日期:2015-06-08
doi:10.3969/j.issn.1001-1528.2016.01.021
中图分类号:R927.2
文献标志码:A
文章编号:1001-1528(2016)01-0098-06

