CFP10/ESAT6融合蛋白-ELISPOT在肺结核病中的诊断价值
王金湖,杨剑虹,李晓红,曹季军,潘晓园
(太仓市第一人民医院检验科,江苏太仓 215400)
·临床研究·
CFP10/ESAT6融合蛋白-ELISPOT在肺结核病中的诊断价值
王金湖,杨剑虹,李晓红,曹季军,潘晓园
(太仓市第一人民医院检验科,江苏太仓 215400)
摘要:目的探讨CFP10/ESAT6融合蛋白-酶联免疫斑点试验(ELISPOT)和结核菌素试验(PPD试验)在肺结核病中的诊断价值。 方法应用ELISPOT和PPD试验检测30例结核患者、54例非结核患者和37例健康者,比较两者的诊断价值。结果国产试剂盒CFP10/ESAT6融合蛋白-ELISPOT检测30例结核患者、54例非结核患者和37例健康者的阳性率分别为70.0%、18.5%和13.5%,PPD试验检测的阳性率分别为60.0%、29.6%和29.7%。在30例结核患者中ELISPOT和PPD试验的灵敏度分别为70.0%和60.0%。在54例非结核组和37个健康组中ELISPOT和PPD试验的特异性分别为83.5%和70.3%。结论国产试剂盒CFP10/ESAT6融合蛋白-ELISPOT在肺结核的诊断中具有高灵敏度和特异性。
关键词:CFP10/ESAT6融合蛋白;酶联免疫斑点法(ELISPOT);PPD试验;肺结核病
目前结核病仍是全球性面临的传染性疾病之一,WHO公布的2010年全球新增TB达到880万[1],而国内有5.5亿人受结核分枝杆菌感染,其中4 500万为活动性结核[2]。结核菌素试验(PPD试验)一直被用于结核感染和活动性结核诊断的体内免疫试验,但由于PPD是多种抗原的混合物,受到非结核分枝杆菌和卡介苗及机体内免疫因素的影响,导致PPD试验诊断结核感染的特异性和灵敏度较差。
酶联免疫斑点试验(ELISPOT)通过特异的相对分子质量6×103的早期分泌性抗原靶ESAT-6和培养滤液蛋白CFP10体外刺激T淋巴细胞分泌γ干扰素,由于其特异性和灵敏度高得到广泛应用[3-5]。本研究选用新的国产试剂盒基因工程重组CFP10/ESAT6融合蛋白作为刺激剂,检测健康人群、非结核病患者和确诊结核患者,回顾性分析ELISPOT在肺结核病诊断中的应用价值。
1资料与方法
1.1一般资料2014年12月至2015年3月,选取太仓第一人民医院收治的45例疑似结核病患者、120例非结核患者及30例体检人群,所有受试者同时进行国产试剂盒CFP10/ESAT6融合蛋白ELISPOT和PPD试验,对所有受试者的临床诊断、PPD试验及ELISPOT检测结果行回顾性分析。所有病例均为初治病例,无人类免疫陷缺病毒合并感染,结核病依据中华医学会结核病学分会制定的肺结核病诊断和治疗指南进行诊断。
1.2方法ELISPOT:使用新鲜肝素锂或枸橼酸钠抗凝的真空采血管无菌抽取受试者外周静脉血4~5 mL,颠倒使抗凝液和血液混匀待用。按(2~3)∶1的比例将抗凝血缓缓加入到含淋巴细胞分层液的灭菌离心管中,在室温下1 000 r/min离心20 min,形成分界面。吸取淋巴细胞层至灭菌离心管中,加入250 μL无血清培养基重悬细胞,取10 μL细胞悬液加入40 μL 0.4%台盼蓝,混匀后取10 μL台盼蓝混合细胞液,在显微镜下计数,然后用无血清培养基配制浓度为2.5×106个/mL 的细胞悬液待用。取出结核感染T细胞检测国产试剂盒反应板条、特异性刺激抗原、阳性对照刺激物平衡至室温,每孔加入100 μL配制好的细胞悬液。将反应板放入培养箱,37 ℃、5% CO2培养18~20 h。将反应板取出,洗涤液洗板后每孔中加入100 μL标记抗体工作液,置37 ℃孵育1 h。再次洗涤液洗板后,每孔加入平衡至室温的显色液50 μL,置37 ℃闭光显色15 min至斑点大小肉眼清晰可见。
当阴性孔斑点数小于13个,检测孔斑点数减去阴性对照孔斑点数大于或等于16个,可判断所检测标本为阳性;当阴性对照孔斑点数大于或等于13个且小于或等于20个,检测孔斑点数为阴性对照孔2倍,可判断所检测标本为阳性。
PPD试验:选择患者前臂屈侧上1/3与中1/3交界处为注射部位,皮内注射0.1 mL结核菌素纯蛋白衍生物,72 h后观察结果,测量硬结直径,若硬结直径大于或等于5 mm,判定为阳性。
1.3统计学处理使用SPSS18.0统计软件进行统计学分析。计数资料以率表示,进行χ2检验,检验两种诊断方法的吻合程度运用K检验。P<0.05为差异有统计学意义。
2结果
2.1临床诊断回顾性病例分析受试者诊断结果。结核病组:男23例,女7例,平均年龄(55.2±23.5)岁,其中肺结核21例,结核性腹膜炎3例,结核性胸膜炎5例,淋巴结核1例。非结核组:男28例,女26例,平均年龄(57.9±20.6)岁,其中肺炎19例,支气管哮喘10例,慢性阻塞性肺病9例,呼吸衰竭5例,糖尿病5例,帕金森氏病3例,肺恶性肿瘤3例。健康组:男20例,女17例,平均年龄(59.2±18.1)岁。
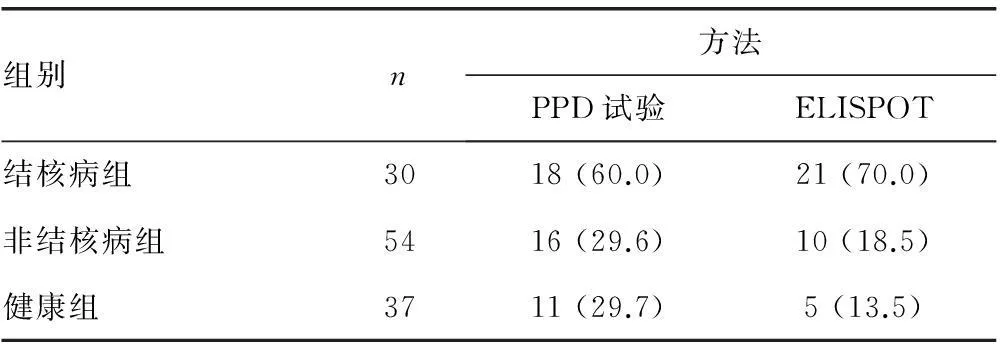
表1 ELISPOT与PPD试验检测阳性结果[n(%)]

表2 结核病组ELISPOT与PPD试验检测结果比较(n)
2.2ELISPOT与PPD试验灵敏度、特异性、诊断价值比较结果ELISPOT检测30例结核病患者、54例非结核病患者和37例健康者的阳性率分别为70.0%、18.5%和13.5%,PPD试验检测的阳性率分别为60.0%、29.6%和29.7%(表1)。3组阳性率经χ2检验,差异有统计学意义(χ2=8.8,P<0.05)。将30例结核病患者的ELISPOT与PPD试验检测结果进行四格表χ2检验,两组检测结果差异无统计学意义(χ2=0.44,P>0.05,见表2)。将54例非结核病患者和37例健康者的ELISPOT与PPD试验检测结果进行四格表χ2检验,两组检测结果差异有统计学意义(χ2=4.53,P<0.05,见表3)。

表3 非结核病组及健康组ELISPOT与PPD试验
3讨论
γ干扰素释放分析试验是近十年来体外免疫试验在结核病诊断领域的成功应用[3-5]。而本研究选用的国产试剂,其选用的结核分枝杆菌特异性刺激抗原为基因工程重组CFP10/ESAT-6融合抗原。Wu[6]等评估了CFP10/ESAT-6融合抗原的ELISPOT试验对结核病患者和健康人群的诊断价值,其特异性为95.5%,肺结核敏感性为60.8%,肺外结核敏感性为33.3%。
本研究结合CFP10/ESAT-6融合抗原的ELISPOT和PPD试验,对121例受试者进行比较性分析显示。临床回顾性分析,121例受试者包括30例结核病患者、54例非结核病患者和37例健康者。本研究结核病组中ELISPOT和PPD试验的阳性率分别为70.0%和60.0%,两者比较差异无统计学意义(P>0.05)。而非结核病组和健康组中ELISPOT和PPD试验的特异性分别为83.5%和70.3%,两者比较差异有统计学意义(P<0.05)。说明CFP10/ESAT-6融合抗原的ELISPOT对结核病的诊断具有更高的临床价值,尤其是在排除诊断方面。
有报道指出,进口的Oxford T细胞斑点试验(T-SPOT)的灵敏度和特异性分别为90%和77%[7]。本研究CFP10/ESAT-6融合抗原的ELISPOT检验特异性(83.5%)高于进口的T-SPOT(77%),这可能与ELISPOT阈值的设置提高有密切关系,其特异性得到明显上升,可区分潜伏性结核分枝杆菌感染[6]。
综上所述,在肺结核诊断中,CFP10/ESAT-6融合抗原的ELISPOT灵敏度明显高于传统的PPD试验,且特异性更高,更快速,可以进行高通量筛选。因此,CFP10/ESAT-6融合抗原的ELISPOT是良好的辅助诊断结核病的方法,值得推广应用。
参考文献
[1]WHO.Global tuberculosis control[M/OL].Geneva,Switzerland:WHO.2011-10-04[2015-11-10],http://www.who.int/tb/publications/global_report/2011/gtbr11_full.pdf.
[2]Duanmu H.Report on the 4th national epidemiological sampling survey of tuberculosis[J].Chin J Tuberc Respir Dis,2002,25(1):3-7.
[3]Kim CH,Kim JY,Hwang YI,et al.Interferon-γ enzyme-linked immunospot assay in patients with tuberculosis and healthy adults[J].Tuberc Respir Dis,2014,76(1):23-29.
[4]O'Shea MK,Fletcher TE,Beeching NJ,et al.Tuberculin skin testing and treatment modulates interferon-gamma release assay results for latent tuberculosis in migrants[J].PLoS One,2014,9:e97366.
[5]Vassilopoulos D,Tsikrika S,Hatzara C,et al.Comparison of two gamma interferon release assays and tuberculin skin testing for tuberculosis screening in a cohort of patients with rheumatic diseases starting anti-tumor necrosis factor therapy[J].Clin Vaccine Immunol,2011,18(20):2102-2108.
[6]Wu X,Li Q,Liang Y,et al.Clinical Evaluation of a Homemade Enzyme-Linked Immunospot Assay for the Diagnosis of Active Tuberculosis in China[J].Mol Biotechnol,2011,47(1):18-25.
[7]Keyser E,Keyser F,and Baets F.Tuberculin skin test versus interferon-gamma release assays for the diagnosis of tuberculosis infection[J].Acta Clin Belg,2014,69(3):358-366.
(收稿日期:2015-01-28)
DOI:10.3969/j.issn.1673-4130.2016.01.055
文献标识码:A
文章编号:1673-4130(2016)01-0116-02

