第48届国际化学奥林匹克实验试题
江万权朱平平王颖霞裴坚,*
(1中国科学技术大学化学与材料科学学院,合肥230026;2北京大学化学与分子工程学院,北京100871)
第48届国际化学奥林匹克实验试题
江万权1朱平平1王颖霞2裴坚2,*
(1中国科学技术大学化学与材料科学学院,合肥230026;2北京大学化学与分子工程学院,北京100871)
第I部分
注意事项
只有在发出“START”命令后,才可以开始实验。实验考试包括两大部分,第I部分(实验1)需100分钟,第I部分实验结束后,必须离开实验室30分钟。
实验试题第I部分(实验1)包括试题5页、答题纸4页。
遵守预备题中告知的安全规则。若违反规则,只给一次警告;若再次违反,将被取消参赛资格。
在实验室始终穿着实验服并佩戴防护镜。需要时向监考老师索要大小合适的手套。
只能使用提供的笔、记号笔以及计算器。不要用记号笔在纸上书写,记号笔只用于在玻璃或者塑料物品上做记号。
确认每一页答题纸上都有你的参赛号。
解答必须写在答题纸上指定的答题框内。写在其他任何地方的解答不予评判。可以在试题的背面打草稿。
实验室中你无法使用水池。提供给你的实验物品足够使用。只有少数器皿需要重复使用。利用合适的溶剂小心洗涤这些器皿,洗涤液倒入废液容器中。需要的时候利用试管刷。蒸馏水和纸巾自由使用。
废液须倒入标有“Liquid waste Test 1”的容器中。垃圾(纸巾、塑料,等等)勿放入此容器,而应投入实验室的废物筐中。
所提供的化学品和实验器皿预计无须添加或者替换。仅在整个实验开始时允许提出添加或者更换,之后每替换一件,将在实验考试的40分中扣去1分。
若有安全的问题,或者需要饮水、去洗手间,举手示意。
完成这一部分的实验后,将答题纸放入所提供的信封中,不要封口,置于台面上。不能再次接触这一部分的答卷。
当发出“STOP”命令后,必须立刻停止实验工作。拖延将可能导致取消你的实验考试。在监考人允许之前不能离开你的位置。你可以保留实验试题。
为了澄清问题,可向监考人要求英文原版试卷。
实验器皿清单

物品(Item)放在公用台上,用于所有实验乳胶手套(Latex gloves),有不同尺寸,选取适合你的尺寸所有实验的通用物品,放在你的实验台面上试管架(60孔),Test tube rack(60 holes)纸巾(可以索取),Paper tissue(can ask for extra)防涂擦记号笔,Permanent marker 20 cm玻璃棒,Glass stirring rod,20 cm直径3.5 cm的塑料漏斗,Polypropylene funnel,diam.3.5 cm软质塑料杯,Soft plastic cup硬质塑料杯,Strong plastic cup实验用品,放在你实验台面上的软质塑料杯中塑料试管用盖子,Caps for polystyrene test tubes实验1用品,放在你的实验台面上离心管架(21孔),Rack for centrifuge tubes(21 holes)带盖的、标有“Liquid waste Test 1”的废液容器,Container with a screw cap for waste,1 dm3,labeled“Test 1”封口袋中的滤纸,Paper filters in zip-bag实验1用品,放在你实验台面上的硬质塑料杯中塑料滴管,Pasteur pipettes实验1用品,放在你台面上的试管架(60孔)中10 cm3塑料试管,Polystyrene test tubes,10 cm3数量(Quantity)-1 5 1 1 1 3 1 2 2 1 1 5 2 0 35
化学品(Chemicals)
实验1
10种不同化合物的水溶液两两混合(每种化合物均用到且只用一次),配得5个未知液,并分别编号。这10种化合物分别为:AgNO3,Al2(SO4)3,Ba(NO3)2,Fe(NO3)3,KI,KIO3,Na2CO3,Na2SO3,MgCl2,NH3。
实验室提供HNO3溶液、NaOH溶液、己烷和上述10种纯化合物的溶液。
利用所提供的空试管以及任何液体(包括未知液),鉴定未知样品中的化合物。所提供的漏斗和滤纸可用于分离。
鉴定未知液1-5中所含的化合物。
在答题纸上写出每种化合物所在溶液的编号。对于未知液中每种化合物所发生的反应,写出两种化学反应现象,这些现象均采用相应的代码(从列表中选择一种或者一种以上)表示,写出可以解释与观察到的现象对应的离子方程式并配平。这两种现象中至少有一种必须是从未知液中鉴定该化合物的特征反应。
注意:当发出STOP信号后,将标有参赛号的盛有未知液的离心管用盖子盖紧,置于试管架上。
第II部分
注意事项
在实验之前你有15分钟的读题时间。只有在发出“START”命令后,才可以开始阅读。
遵守预备题中告知的安全规则。若违反规则,只给一次警告;若再次违反,将被取消参赛资格。在实验室始终穿着实验服并佩戴防护镜。需要时可以向监考老师索要大小合适的手套。
只能使用提供的笔、记号笔和计算器。不要用记号笔在纸上书写,记号笔只用于在玻璃或者塑料物品上做记号。
确认每一页答题纸上都有你的参赛号。
解答必须写在答题纸上指定的答题框内。写在其他任何地方的解答不予评判。可以用试题的背面打草稿。
你无法使用实验室的水池。提供给你的实验物品足够使用。只有少数器皿需要重复使用。利用合适的溶剂小心洗涤这些器皿,洗涤液倒入废液容器中。需要的时候可以使用试管刷。蒸馏水和纸巾自由使用。
废液须倒入标有“Liquid waste Test 2&3”的容器中。垃圾(纸巾、塑料,等等)勿放入此容器,而应投入实验室的废物筐中。
所提供的化学品和实验器皿预计无须添加或者替换。仅在整个实验开始时允许提出添加或者更换,之后每替换一件,将在实验考试的40分中扣去1分。
有关于安全的问题,或者需要饮水、去洗手间,举手示意。
完成这一部分的实验后,将答卷纸放入所提供的信封中,不要封口,置于台面上。
当发出“STOP”命令后,立刻停止实验工作。拖延将导致取消你的实验考试。在监考人允许之前不能离开你的位置。你可以保留实验试题。
为了澄清问题,可向监考人要求英文原版试卷。
第II部分实验特别提示
第II部分(实验2和3)时间为200分钟。
第II部分从实验2开始。当你做好开始实验3的准备后,告知监考老师,你将拿到实验3的化学药品和实验器皿。实验2的试剂同时将被收走。
第II部分(实验2和3)包括实验试题10页,答题纸6页。
需要点燃酒精灯时,告知监考老师。只能加热玻璃试管。加热结束后,盖上盖子以熄灭酒精灯。
实验器皿清单
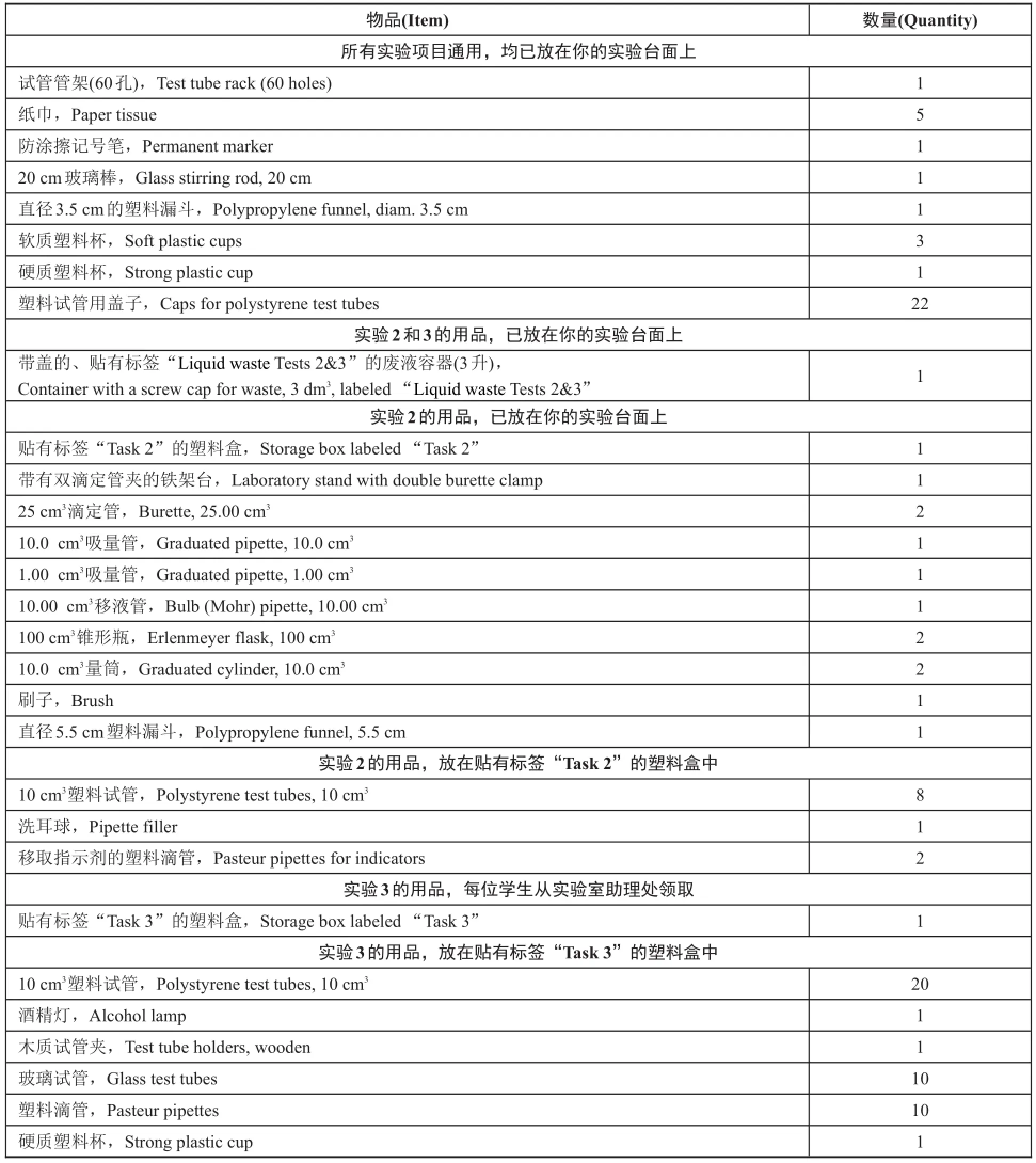
物品(Item)所有实验项目通用,均已放在你的实验台面上试管管架(60孔),Test tube rack(60 holes)纸巾,Paper tissue防涂擦记号笔,Permanent marker 20 cm玻璃棒,Glass stirring rod,20 cm直径3.5 cm的塑料漏斗,Polypropylene funnel,diam.3.5 cm软质塑料杯,Soft plastic cups硬质塑料杯,Strong plastic cup塑料试管用盖子,Caps for polystyrene test tubes实验2和3的用品,已放在你的实验台面上带盖的、贴有标签“Liquid waste Tests 2&3”的废液容器(3升),Container with a screw cap for waste,3 dm3,labeled“Liquid waste Tests 2&3”实验2的用品,已放在你的实验台面上贴有标签“Task 2”的塑料盒,Storage box labeled“Task 2”带有双滴定管夹的铁架台,Laboratory stand with double burette clamp 25 cm3滴定管,Burette,25.00 cm310.0 cm3吸量管,Graduated pipette,10.0 cm31.00 cm3吸量管,Graduated pipette,1.00 cm310.00 cm3移液管,Bulb(Mohr)pipette,10.00 cm3100 cm3锥形瓶,Erlenmeyer flask,100 cm310.0 cm3量筒,Graduated cylinder,10.0 cm3刷子,Brush直径5.5 cm塑料漏斗,Polypropylene funnel,5.5 cm实验2的用品,放在贴有标签“Task 2”的塑料盒中10 cm3塑料试管,Polystyrene test tubes,10 cm3洗耳球,Pipette filler移取指示剂的塑料滴管,Pasteur pipettes for indicators实验3的用品,每位学生从实验室助理处领取贴有标签“Task 3”的塑料盒,Storage box labeled“Task 3”实验3的用品,放在贴有标签“Task 3”的塑料盒中10 cm3塑料试管,Polystyrene test tubes,10 cm3酒精灯,Alcohol lamp木质试管夹,Test tube holders,wooden玻璃试管,Glass test tubes塑料滴管,Pasteur pipettes硬质塑料杯,Strong plastic cup数量(Quantity) 1 5 1 1 1 3 1 2 2 1 1 1 2 1 1 1 2 2 1 1 8 1 2 1 2 0 1 1 1 0 10 1
化学品(Chemicals)

*在完成实验1后,剩余的HNO3。

实验2
矿泉水中氟离子和氯离子含量测定
格鲁吉亚出产世界闻名的优质矿泉水,其中不少甚至可治疗某些疾病。生产商必须严格控制水中的各种离子含量,氟离子和氯离子是其中最重要的两种。
目视比色法测定氟离子浓度
氟离子与锆(IV)可以生成更稳定的无色络合物。氟离子存在时可使锆(IV)-茜素红S络合物颜色减褪,据此可测定氟离子的浓度。试剂混合约20分钟后,该褪色反应达到平衡。目视比色法测定是将氟离子样品溶液的颜色与氟离子标准溶液进行比较以确定氟离子的浓度。
从样品瓶中准确移取9.0 cm3矿泉水(mineral water)置于标有“X”的塑料试管中。
配制系列氟离子标准溶液,其浓度分别为:0.0,1.0,2.0,3.5,5.0,6.5,8.0 (mg∙dm-3)。溶液体积均以9.0 cm3计,计算所需浓度为9.0 mg∙dm-3的氟离子标准溶液的体积。
用1.0 cm3和10.0 cm3吸量管分别移取一定量的氟离子标准溶液,加入试管中,在每支试管中各加入1.0 cm3的锆(IV)-茜素红S指示剂,用蒸馏水将系列标准溶液体积调至试管10.0 cm3刻度处(刻度线如图中箭头所示)。
2.1.1 记录所用氟离子溶液的体积。
混匀试管中的溶液,置于试管架上至少20分钟。

2.1.2 比较样品和标准溶液的颜色,由上向下,由前向后仔细观察,选出浓度与水样氟离子最接近的标准氟离子溶液。
注意:实验考试完成后,由监考教师拍照放置所有试管的试管架。
莫尔法(Mohr method)标定硝酸银浓度
用移液管准确移取0.0500 mol∙dm-3NaCl标准溶液10.0 cm3,放入锥形瓶中,加入约20 cm3蒸馏水、10滴10%K2CrO4溶液。
在滴定管中加入硝酸银溶液。用AgNO3滴定锥形瓶中的物质,并剧烈摇动,有沉淀形成。接近终点时,缓慢滴加滴定剂并剧烈摇动锥形瓶。在浅黄色悬浮液中,随着滴定剂加入,体系颜色发生些微可见的变化且不消失,即为终点。记录终点读数。需要时可以重复滴定。
2.2.1 在答题纸上记录滴定体积。
2.2.2 写出NaCl与AgNO3滴定的化学反应式,写出指示终点的反应式。
2.2.3 根据滴定结果计算AgNO3溶液的浓度。
2.2.4 莫尔法滴定必须在中性介质中进行,分别写出pH值偏低或偏高时发生的干扰反应的方程式。
福尔哈德法(Volhard method)测定氯离子浓度
用蒸馏水洗涤移液管。锥形瓶先用少量氨水(实验1剩余的)除去银盐沉淀,再用蒸馏水洗涤干净。(如果实验1用完了所有的氨水,可以向监考老师索取,不扣分。)
用移液管移取10.0 cm3矿泉水样品于锥形瓶中,用量筒量取2 mol∙dm-3HNO3溶液5 cm3。用滴定管加入AgNO3溶液20.00 cm3,混合均匀,形成悬浮液。用塑料滴管加入约2 cm3指示剂(Fe3+)溶液。
在第二支滴定管中加入NH4SCN标准溶液(准确浓度见标签)。用NH4SCN滴定上述悬浮液,并剧烈摇动锥形瓶。当加入一滴滴定剂后有淡褐色产生且充分混合后体系颜色仍然稳定存在,即为终点。记录终点读数。需要时可以重复滴定。
注意:在溶液中,SCN-能置换AgCl沉淀中的Cl-
。如果滴定太慢或有中断,则褐色会随着时间而消失,从而导致滴定剂过量消耗。因此接近终点时,应匀速缓慢加入滴定剂,并持续摇动锥形瓶使悬浮液保持白色。一旦出现淡褐色即为终点。
2.3.1 在答题纸上记录滴定体积。
2.3.2 写出用NH4SCN返滴定的反应方程式,写出指示终点的反应方程式,均配平。
2.3.3 根据你测定的结果计算水样中氯离子浓度(单位:mg∙dm-3)。
2.3.4 如果样品中除Cl-离子外,还存在Br-
、I-和F-
离子,请问哪种或哪些离子对福尔哈德法测定结果有影响?
2.3.5 欲在其他卤素离子存在时测定Cl-离子含量,分析人员在样品中加入碘酸钾和硫酸并煮沸溶液。然后将此溶液与亚磷酸(H3PO3)共沸,使碘酸根转化为碘单质,以除去过量的碘酸根。此处理可以消除哪些阴离子的干扰?写出这些离子与碘酸盐反应的方程式。
实验3
香料和香精化合物的鉴定
来格鲁吉亚旅游的游客都喜欢感受当地特色,其中最重要的当属品尝当地美食。美味的肉食、新鲜的蔬菜、水果以及家酿的果酱等等。怎样才能使真正的美食家们满意呢?当然是独特的香料和香精。
你有8个未知有机化合物(编号分别为1-8)。这些化合物都是商用的香料或香精。所有这些化合物均是纯净的。它们的结构式在以下化合物A-M中。

所有这些未知有机化合物均易溶于乙醚,不溶于NaOH和HCl水溶液。除了未知化合物6微溶于水(3.5 g∙dm-3)外,其他7个化合物均不溶于水。
3.1 按以下描述的实验方法鉴定化合物1-8。每一个反应现象用一个罗马数字代表。选择正确的罗马数字(一个或一个以上)将相应的实验结果填写在对应的方框中。使用+和-符号表明阳性(反应)或阴性(不反应)。
3.2 基于以上所给的化合物性质以及实验结果判断这些未知化合物的结构。在相应的框中写出你所判断的这些化合物的结构代码(从A-M中选择)。
实验步骤
KMnO4实验(Baeyer实验)
在每一个塑料试管中加入约1 cm395%乙醇和1滴未知有机化合物,再加入1滴KMnO4溶液,振荡混合溶液,振荡后能使KMnO4溶液马上褪色的反应定为阳性。
3.3 写出A-M中的一个化合物能进行Baeyer反应的方程式。
硝酸铈(IV)实验
在每一个玻璃试管中加入2滴Ce(IV)试剂和2滴乙腈(acetonitrile)后,接着再加入2滴未知物(滴加的次序非常重要!)。振荡混合溶液,混合溶液的颜色能迅速从黄色转化为橙红色,就定为阳性反应。
说明1:每一个试管只做一个反应。如果你需要洗试管,务必仔细选择合适的溶剂。为了防止气味从试管中逸出,在完成反应后用绿色试管盖子将试管盖上。
说明2:为了合理解释实验现象,推荐做空白实验(无未知物)和对照实验(乙醇)。
说明3:Ce(IV)离子可以与醇形成配合物,起初其颜色比较明亮;与一级醇或二级醇形成的这个配合物可以进一步反应(15秒至1小时),此明亮的颜色最终会褪去。
2,4-二硝基苯肼(2,4-DNPH)实验
在每一个塑料试管中加入1 cm395%乙醇和仅1滴未知物,再加入1 cm3的DNPH试剂,振荡试管后,放置1-2分钟,若观测到黄色至橙红色沉淀生成,检测即为阳性。
3.4 写出A-M中的一个化合物能与2,4-DNPH反应的方程式。羟胺铁盐实验
请监考老师帮你点燃酒精灯。在玻璃试管中将1 cm3的0.5 mol∙dm-3的羟胺盐酸盐乙醇溶液与5滴6 mol∙dm-3的NaOH水溶液混合,再加入1滴未知物,利用酒精灯将混合液加热至沸腾,加热时缓慢晃动试管,以免溶液喷出。稍冷后,加入2 cm3的1 mol∙dm-3的HCl水溶液,再加入1滴2.5%的FeCl3溶液,如溶液颜色变为品红色,则为阳性反应。实验结束后,将酒精灯盖盖上。
说明1:在此实验中只能使用玻璃试管。在加热时,使用试管夹。如果你需要洗试管,使用合适的溶剂。为了防止气味逸出,在完成反应后用绿色试管盖子将试管盖上。
说明2:Fe(III)离子能与酰基羟胺(R-CO-NHOH)形成有色的1:1配合物。
3.5 写出A-M中的一个化合物能进行羟胺铁盐反应的方程式。
注意:在实验停止信号STOP发出后,将取用未知样品的注射器装上原来的针头,放入硬质塑料杯中,将杯子放在实验桌上。
*通讯作者,Email:jianpei@pku.edu.cn
10.3866/PKU.DXHX201608024
www.dxhx.pku.edu.cn

