含银废电子浆料中银的浸出和除杂工艺条件研究
王玲玲,陈 晨,朱炳龙,童 霏,周全法
(江苏理工学院,江苏 常州 213001)
含银废电子浆料中银的浸出和除杂工艺条件研究
王玲玲,陈 晨,朱炳龙,童 霏,周全法*
(江苏理工学院,江苏 常州 213001)
用硝酸作为浸出剂,通过正交试悚考察了各工艺条件对含银电子废料中的银的浸出效率的影响。结果表明,硝酸浓度和浸出温度是影响浸出效率的主要因素;在硝酸浓度为 8 mol/L、搅拌速度为100 r/min、浸出温度和时间分别为80℃和80 min的最佳条件下,浸出效率可达88%以上。控制温度为70℃,以NaOH溶液调节浸出液至近中性(pH=6.0),共存杂质Cu、Fe、Pb、Ni和Bi的一次去除率达到80%以上,可得到较纯净的硝酸银溶液。
银;浸出;除杂;含银废电子浆料
银是电子工业中用量最大和应用最为广泛的贵金属。将一定颗粒度的超细或片状银粉、氧化银、硝酸银等含银化合物,与助熔剂、溶剂、黏合剂和功能助剂等进行机械混合,可以得到具有特定电性能和涂布性能的电子浆料[1]。通过丝网印刷、光刻等工艺可以将含银电子浆料按照一定的形状或线路均匀涂覆到基底材料表面,然后以加热或烧结方式使金属银按照预定的线路与基底材料结合,形成特定的导电层,广泛应用于电容器、电位器、电阻器、压电陶瓷等材料的生产过程[2-3]。
在制浆、涂布、烧结以及相关含银材料的使用过程中,会产生一定量的含银废浆料、抹布、压电陶瓷废片等各类含银废料。对其进行回收和深加工,可有效降低相关电子产品的白银消耗和生产成本,同时也能够减少或避免由含银废料所产生的环境危害。从含银废料中回收利用银等有价金属的方法很多[4-8],火法、湿法和生物方法分别用于不同形态和成分的含银废料中银的再生利用[9-13]。
本文以含银报废电子浆料为原料,考察硝酸浸出银的工艺条件影响,并采用NaOH进行去除金属杂质的实验,尝试建立有效的银回收方法。
1 实验部分
1.1 原料、试剂和仪器设备
原料:废银浆料。来源于江苏某压电陶瓷生产企业,废料形态为粘稠状报废银浆、固化状报废银浆、涂银废抹布等。
试剂:硝酸、氢氧化钠、硝酸铜、硝酸铁、硝酸铅、硝酸镍、硝酸铋、硝酸银、硫氰酸铵、硫酸铁铵等化学试剂均为分析纯。
仪器设备:Optima 2100 DV 型光谱仪,DF-II数显集热式磁力搅拌器,HH-6数显恒温水浴锅,电子天平,电热鼓风干燥箱,箱式电阻炉等。
1.2 试验方法
将废银浆料于600℃灼烧2 h,经冷却、粉碎、过筛、混合后得到均匀的粉料,于110℃恒温干燥1 h后冷却并密封避光保存,得到预处理后的废料(下称废银粉)。废银粉、浸出液和产品中的银含量采用佛尔哈德法测定,其他金属离子含量用ICP-AES法测定[14]。
取废银粉 100 g(准确至 0.0001 g)于圆底烧瓶中,加一定浓度的硝酸并在一定温度的水浴中加热溶解,冷却至室温,过滤除去不溶性物质,得到酸浸液。考察硝酸浓度、时间、温度、搅拌速度等因素对浸出效果的影响。
以NaOH溶液调节酸浸液的pH值,经充分搅拌和沉淀后过滤除杂。考察酸浸液的pH值和温度对杂质金属离子浓度的影响。
2 结果与讨论
2.1 硝酸浓度对浸出效率的影响
称取废银粉(各约100 g) 8份,加入足量浓度分别为15.30、7.65、5.10、3.83、3.06、2.55、2.19和0.00 mol/L的硝酸溶液,于75℃和150 r/min搅拌速度下浸出80 min。以浸出液中银含量与废银粉质量的比值(下称浸出效率,%)衡量浸出效果。所得结果如图1所示。
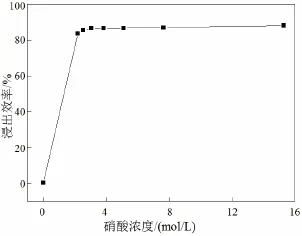
图1 硝酸浓度对浸出效果的影响Fig.1 Effect of nitric acid concentrations on leaching rate of silver
由图1可知,除蒸馏水以外,废银粉在不同浓度的硝酸溶液中于75℃浸出80 min,浸出效率均在80 g/100 g以上。综合考虑浸出速度和降低硝酸消耗等因素,选择8 mol/L的硝酸作为浸出用酸。
2.2 浸出时间对浸出效率的影响
称取废银粉(各约100 g) 6份,分别加入足量8 mol/L硝酸溶液,于75℃和150 r/min搅拌速度下分别浸出 20、40、60、80、90、100 min。浸出效率如图2所示。
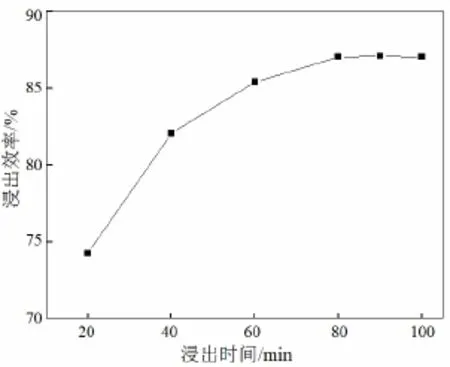
图2 浸出时间对浸出效果的影响Fig.2 Effect of the leaching time on the leaching rate of silver
由图2可见,废银粉于75℃在8 mol/L硝酸溶液中溶解浸出,浸出效率随时间增加而增加,并在浸出时间达到80 min后基本稳定。综合考虑浸出能耗和效率等因素,本实验选择浸出时间为80 min。
2.3 浸出温度对浸出效率的影响
称取废银粉(各约100 g) 8份,加入足量8 mol/L硝酸溶液,分别于25、35、45、55、65、75、85、95℃和150 r/min搅拌速度下浸出80 min。浸出效率如图3所示。
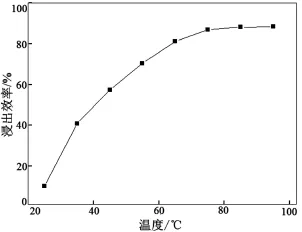
图3 浸出温度对浸出效果的影响Fig.3 Effect of leaching temperature on leaching rate of silver
由图3可见,废银粉在8 mol/L硝酸溶液中溶解浸出80 min,浸出效率随着温度的上升而升高。温度低于40℃时,反应速度很慢,85℃达到最高。综合考虑浸出速度、能耗和挥发量等因素。本实验选择浸出温度为85℃。
2.4 搅拌速度对浸出效率的影响
称取4份废银粉(各约100 g),于75℃在8 mol/L硝酸溶液中浸出80 min。浸出效率与磁力搅拌速度的关系如图4所示。
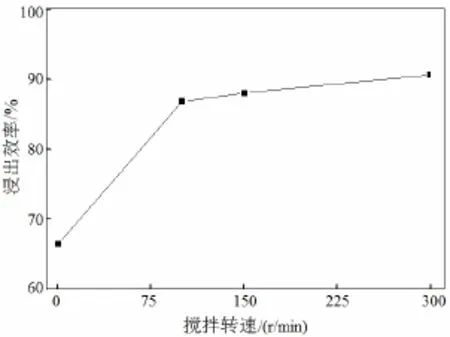
图4 搅拌速度对浸出效果的影响Fig.4 Effect of the stirring speed on the leaching rate of silver
由于废银粉颗粒的密度远大于硝酸溶液密度,为了促使废银粉颗粒能够在反应体系中长时间悬浮,增加与硝酸溶液的接触面积和接触时间,废银粉浸出过程中必须施加一定速度的搅拌。从图4可见,废银粉于75℃在8 mol/L硝酸溶液中浸出80 min,浸出效率随搅拌速度的增加而增加。综合考虑能耗和搅拌安全性等因素,本实验选择搅拌速度为300 r/min。
2.5 浸出条件的正交实验分析
针对硝酸浓度、时间、温度和搅拌速度对浸出效率的影响结果,设计了4因子4水平的正交实验,16次实验的结果如表1所示,显著性水平分析如表2所示。
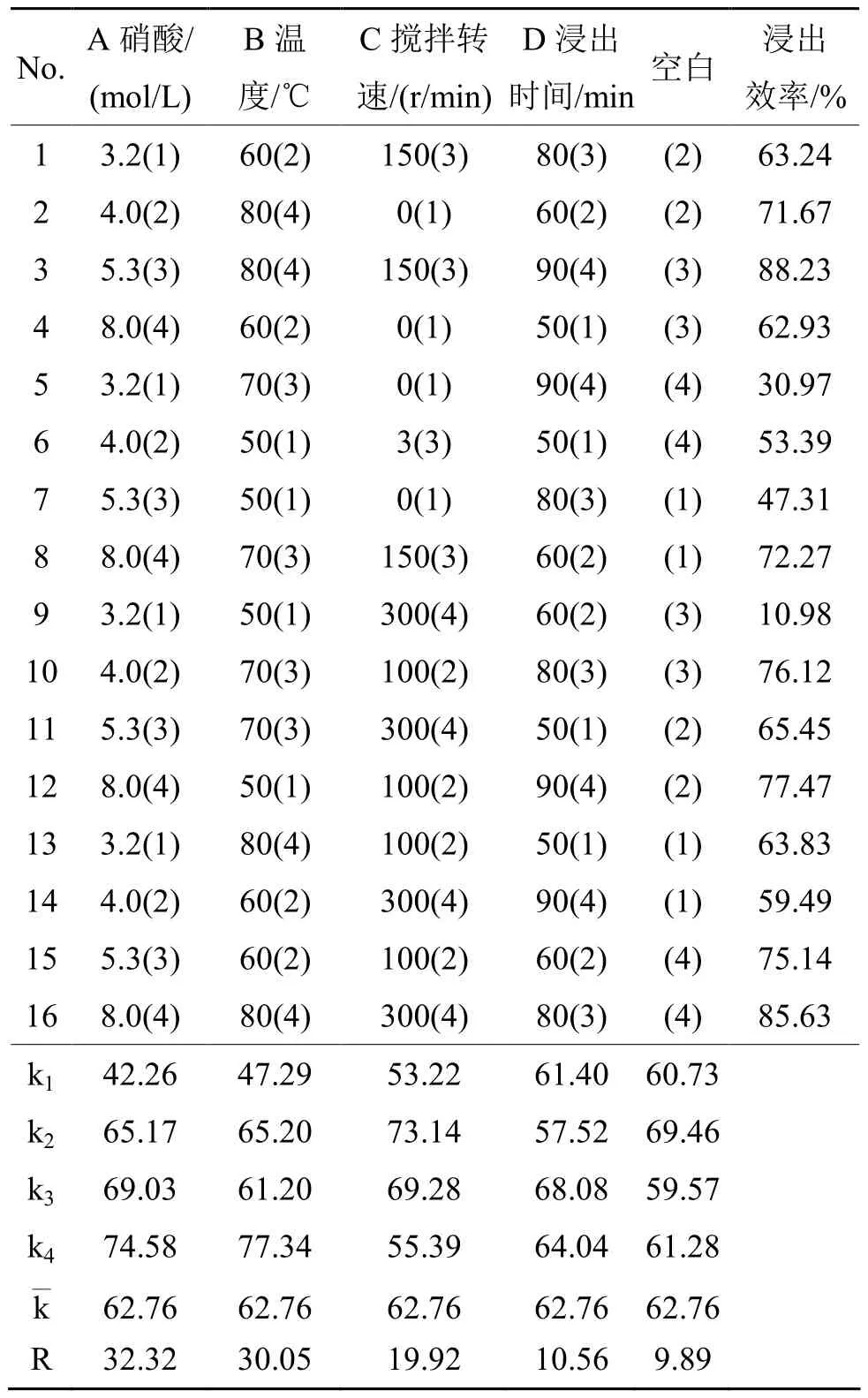
表1 正交实验的条件和结果Tab.1 The condition and results of orthodoxy experiment
由表1直观分析可知,最佳合成条件是硝酸浓度8.0 mol/L、温度80℃、搅拌速度100 r/min、时间80 min。各因素对银浸出效率的影响顺序是硝酸浓度>温度>搅拌速度>时间。
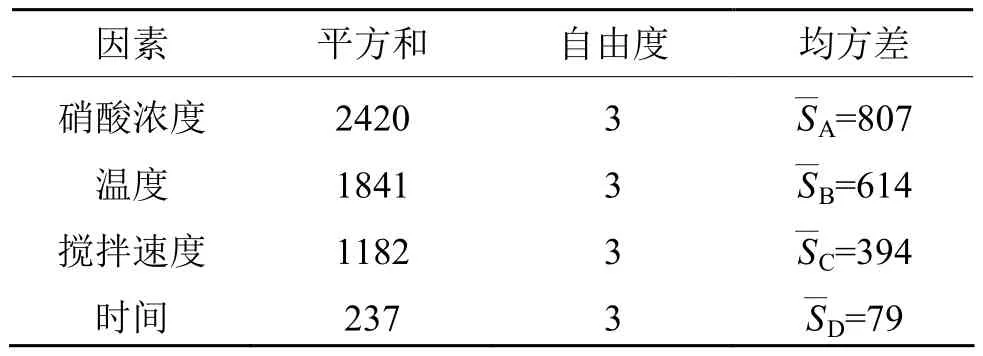
表2 显著性水平分析Tab.2 The analysis of notability level
2.6 pH值对浸出液除杂效果的影响
在最优水平的浸出实验条下对废银粉进行加热浸出,并控制浸出液中银离子浓度维持在1 mol/L。向浸出液中滴加1 mol/L的NaOH溶液,调节pH值,沉淀杂质离子,用ICP-AES法测定除杂前后溶液中杂质离子的浓度,结果见表3。
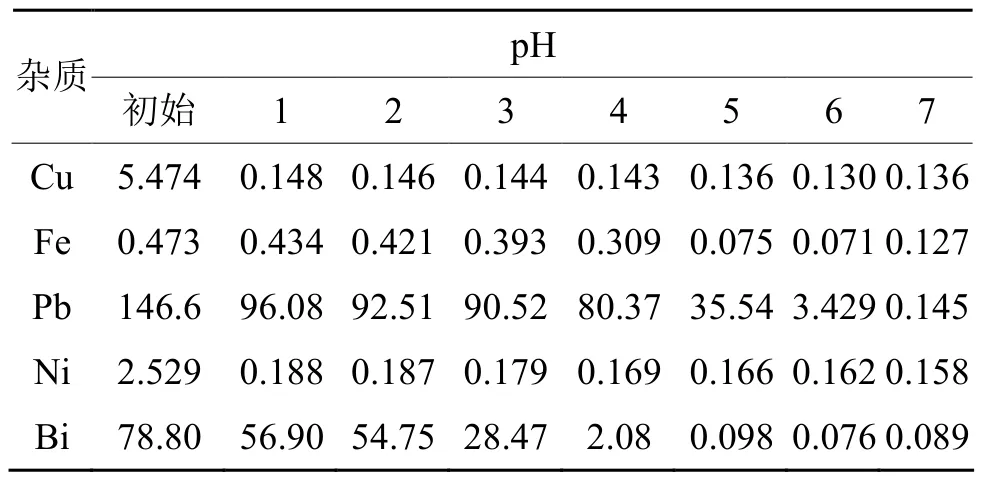
表3 不同pH值下硝酸银溶液中杂质离子的浓度Tab.3 The concentrations of impurity ions in silver nitrate solution at different pH values /10-6
通过各杂质离子的浓度与初始浓度计算杂质去除率,如图5所示。
由图5可见,反应混合物中杂质离子去除率随溶液pH值的升高而不断降低。理论上,Cu、Fe、Pb、Ni和Bi等离子形成氢氧化物而完全沉淀的pH值分别是6.67、3.17、7.88、9.15和5.53,但是本实验浸出液的pH值达到1.0时,铜和镍离子的去除率已达到90%以上,当溶液pH值达到6.0以上时,Fe、Pb、Bi离子的去除率均可达到85%以上。在酸性条件下上述金属离子能够从溶液中沉淀下来的原因在于,浓度相对较高的氢氧根离子遇到浓度很高的银离子时能够瞬间形成呈胶态、表面积大并容易吸附其他金属离子的氢氧化银絮状沉淀,氢氧化银沉淀在酸性条件下因不稳定而分解,被吸附在其中的杂质金属离子被释放,如此反复。被释放的杂质金属离子因扩散速度较低的原因,在NaOH溶液滴入的局部区域浓度增高,从而使杂质金属离子在尚未达到完全沉淀pH值前形成沉淀。当溶液pH值达到杂质金属离子完全沉淀所需的pH值时,沉淀形成的颗粒更大,分离更完全。
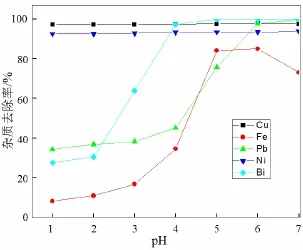
图5 杂质离子去除率与pH值的关系曲线Fig.5 The relation curve between the removal rate of impurity ion and pH value
2.7 温度对浸出液除杂效果的影响
在最优水平的浸出实验条下对废银粉进行加热浸出,并控制浸出液中银离子浓度维持在1 mol/L。向浸出液中滴加1 mol/L的NaOH溶液,调节pH值约为6.0。分别考察浸出液温度为30、50、70、90、100℃时的除杂效果,用ICP-AES法测定除杂前后溶液中杂质离子的浓度,计算杂质离子的去除率,结果如图6所示。
由图6可以看出,杂质金属离子的去除率随浸出液温度的升高,呈现先增大后减小的趋势。尽管Cu、Fe、Pb、Ni和Bi的离子去除率的变化幅度有所不同,但其变化趋势一样,且最高去除率的温度点相同,均在浸出液温度为70℃时有最好的除杂效果。除杂过程是放热反应,从理论上看,温度升高不利于除杂过程,但由于在浸出液除杂过程中产生了大量不稳定的氢氧化银沉淀,氢氧化银对杂质离子有化学吸附作用,在初始阶段提高温度,可以提供化学吸附的活化能,有利于激活吸附反应,从而有利于除杂过程的进行。
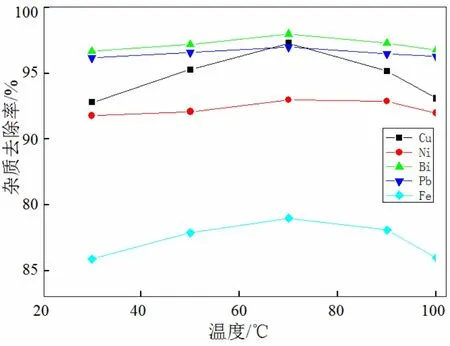
图6 杂质离子去除率与温度的关系曲线Fig.6 The relation curve between the removal rate of impurity ion and temperature
3 结论
以硝酸为浸出剂,探讨了酸浓度、浸出时间、浸出温度和搅拌速度对经过预处理的废银浆料的浸出效率。正交试验结果表明,硝酸浓度和浸出温度是影响浸出效率的主要因素,各因素对银浸出效率的影响顺序是硝酸浓度>温度>搅拌速度>时间。最佳浸出条件为硝酸浓度 8 mol/L、搅拌速度 100 r/min、浸出温度和时间分别为80℃和80 min,浸出效率可达88%以上。在使用NaOH溶液对浸出液进行除杂时,由于浸出液中的银离子能够瞬间形成胶态、表面积大且易吸附其他金属离子的氢氧化银絮状沉淀,并在酸性条件下因不稳定而分解,释放被吸附的杂质金属离子,反复多次,因被释放的杂质金属离子扩散速度较低而使其在尚未达到完全沉淀pH值前形成沉淀。在70℃和pH为6.0时,共存杂质Cu、Fe、Pb、Ni和Bi的一次去除率达到80%以上。本方法具有浸出效率高、操作简便、除杂效果好的特点,有一定的应用前景。
[1] 史泰冈, 祁红璋, 严彪. 电子浆料材料的研究进展及其在印刷电路板方面的应用[J]. 上海有色金属, 2012, 33(3): 145-147. SHI T G, QI H Z, YAN B. Research progress of electronic paste and its application in printed circle board industry[J]. Shanghai nonferrous metals, 2012, 33(3): 145-147.
[2] 赵雪, 邱平达, 姜海静, 等. 超级电容器电极材料研究最新进展[J]. 电子元件与材料, 2015, 34(1): 1-8. ZHAO X, QIU P D, JIANG H J, et al. Latest research progress of electrode materials for supercapacitor[J]. Electronic components and materials, 2015, 34(1): 1-8.
[3] 黄晓梅, 李国斌, 胡亮, 等. 银的提取研究进展及前景展望[J]. 稀有金属, 2015, 39(3): 268-275. HUANG X M, LI G B, HU L, et al. Research progress and prospect of extracting silver[J]. Chinese journal of rare metals, 2015, 39(3): 268-275.
[4] 周全法, 周品, 王玲玲. 贵金属深加工及其应用[M].北京: 化学工业出版社, 2015.
[5] 江成军, 张振忠, 赵芳霞, 等. 化学还原法回收含银电镀废液中的银[J]. 化工环保, 2010, 30(1): 69-71. JIANG C J, ZHANG Z Z, ZHAO F X, et al. Recovery of silver from silver-containing electroplating effluent by chemical reduction method[J]. Environmental protection of chemical industry, 2010, 30(1): 69-71.
[6] 赵飞, 韩守礼, 贺小塘, 等. 用银废料生产试剂级硝酸银的工艺[J]. 贵金属, 2014, 31(4): 20-23. ZHAO F, HAN S L, HE X T, et al. A process for production of reagent-level silver nitrate from silver-containing scrap[J]. Precious metals, 2014, 31(4): 20-23.
[7] 孙蓉, 刘君玉, 庄志红, 等. PDP废电子浆料中银的回收及其含量分析[J]. 西南科技大学学报, 2012, 27(1): 25-28. SUN R, LIU J Y, ZHUANG Z H, et al. The recycle Ag and analyse its content from wasted PDP electronic pastes[J]. Journal of Southwest University of Science and Technology, 2012, 27(1): 25-28.
[8] 肖臻, 徐本军, 黄彩娟, 等. 从含银废渣中提取银的工艺研究进展[J]. 湿法冶金, 2011, 30(3): 194-196. XIAO Z, XU B J, HUANG C J, et al. Research advances on extraction process of silver from silver-containing slag[J]. Hydrometallurgy of China, 2011, 30(3): 194-196.
[9] AHN J W, CHUNG D W, LEE K W, et al. Nitric acid leaching of base metals from waste PDP electrode scrap and recovery of ruthenium content from leached residues[J]. Materials transactions, 2011, 52(5): 1063-1069.
[10] ALVARADO-MACIAS G, FUENTES-ACEITUNO J C, NAVA-ALONSO F. Silver leaching with the thiosulfate-nitrite-sulfite-copper alternative system[J]. Hydrometallurgy, 2015, 152: 120-128.
【】【】
[11] GAO Y X, ZHOU Y, WANG H T, et al. Simultaneous silver recovery and cyanide removal from electroplating wastewater by pulse current electrolysis using static cylinder electrodes[J]. Industrial & engineering chemistry research, 2013, 52: 5871-5879
[12] KOWALSKA S, LUKOMSKA A, LOS P, et al. Potential-controlled electrolysis as an effective method of selective silver electrowinning from complex matrix leaching solutions of copper concentrate[J]. International journal of electrochemical, 2015, 10: 1186-1198.
[13] KHALEGHI A, GHADER S, AFZALI D. Ag recovery from copper anode slime by acid leaching at atmospheric pressure to synthesize silver nanoparticles[J]. International journal of mining science and technology, 2014, 24: 251-257.
[14] 王琪, 周全法, 尚通明. 贵金属深加工实用分析技术[M]. 化学工业出版, 2011: 182.
Conditions of Leaching and Purifying Process for Recycling Silver from Waste Silver-Bearing Electronic Paste
WANG Lingling, CHEN Chen, ZHU Binglong, TONG Fei, ZHOU Quanfa*
(Jiangsu University of Technology, Changzhou 213001, Jiangsu, China)
The leaching rate of silver from the waste silver-bearing electronic paste using nitric acid as the leaching agent was investigated by the orthogonal test. Experimental results show that the concentration of nitric acid and leaching temperature are the main factors affecting the leaching rate. A high leaching rate of 88% was realized when the leaching was carried out in 8 mol/L nitric acid solution for 80 min at 80℃ with a stirring speed of 100 rpm. More than 80% of Cu, Fe, Pb, Ni and Bi ions co-existing in the lixivium could be removed at 70℃ by adjusting the pH value of the lixivium to 6.
silver; leaching; purifying; waste silver-bearing electronic paste
TF832
A
1004-0676(2016)04-0053-05
2015-11-13
国家科技支撑计划项目(项目号2014BAC03B06,废旧电子元器件中稀贵金属和热塑性塑料高值化清洁利用关键技术及示范);江苏省科技支撑计划项目(项目号BE2012645,废电路板器分离与高值资源选择性富集技术研究)。
王玲玲,女,硕士,研究方向:电子废弃物资源综合利用。E-mail:silence0609@foxmail.com
*通讯作者:周全法,男,博士,教授,研究方向:贵金属深加工工程和电子废弃物资源循环利用。E-mail:labzqf@jsut.edu.cn

